Панавир® в комплексной профилактике реактивации герпесвирусных инфекций у детей с рецидивирующими инфекциями органов респираторного тракта
DOI: 10.32364/2587-6821-2022-6-11-618-625
Введение: актуальность разработки терапевтических методов профилактики реактивации герпесвирусных инфекций (ГВИ) у детей обусловлена высокой частотой реактивации через 3–6 мес. после проведения клинически успешного курса противовирусной терапии манифестных форм с применением препаратов прямого противовирусного действия.
Цель исследования: анализ клинической и вирусологической эффективности комплексной терапии с включением спрея Панавир® Инлайт в профилактике ОРИ у детей на фоне реактивации ГВИ. Материал и методы: в ходе наблюдательной программы было обследовано 76 пациентов, из них 35 (46,1%) девочек и 41 (53,9%) мальчик, в возрасте от 0 до 14 лет, медиана возраста составила 5 (IQR 2–8) лет. Срок наблюдения — 3 мес. Основную группу составили 49 детей, которые получали Панавир® Инлайт спрей в составе комплексной терапии, группу сравнения — 27 детей, не получавших данный спрей. Схема применения Панавир® Инлайт спрей — по 1–2 впрыска в горло после еды, 3 курса по 14 дней с перерывами по 14 дней. Всем пациентам проводилось в динамике комплексное клинико-лабораторное обследование. Диагностика ГВИ осуществлялась серологическими методами, а также методом ПЦР. Изучался уровень вирусной нагрузки ДНК вируса герпеса человека (ВГЧ) 6А/В, цитомегаловируса, вируса Эпштейна — Барр в материале мазков из ротоглотки на фоне проводимой терапии.
Результаты исследования: исчезновение или уменьшение жалоб (ежемесячные ОРИ, субфебрилитет, длительная заложенность носа и др.) было зафиксировано у 38 (77,6%) пациентов основной группы и 15 (55,6%) детей в группе сравнения. На момент начала терапии у всех пациентов сравниваемых групп наблюдалось выделение ДНК одного или нескольких герпесвирусов в материале мазка из ротоглотки. После окончания курса терапии ДНК вирусов в ротоглотке не обнаруживались у 37 (75,5%) пациентов основной группы и у 16 (59,3%) пациентов группы сравнения. Медиана вирусной нагрузки ВГЧ-6А/В в ротоглотке снизилась с 645,0 (IQR 399,00–1600,00) копий/мл до 399,00 (IQR 0,00–775,00) копий/мл. По данным комплексного обследования зафиксировано уменьшение активности ГВИ у 27 (55,1%) пациентов, получавших Панавир® Инлайт спрей, и у 10 (37,0%) пациентов группы сравнения. На фоне проводимой терапии реактивация ГВИ достоверно реже была зафиксирована в основной группе — у 3 (6,1%) пациентов, чем в группе сравнения — у 10 (37,0%) пациентов (р<0,001).
Заключение: применение спрея Панавир® Инлайт в комплексной профилактике реактивации ГВИ у детей с рекуррентными респираторными инфекциями способствует нормализации самочувствия и сохранению латентных форм ГВИ после курса терапии с применением препаратов прямого противовирусного действия. У пациентов, применявших Панавир® Инлайт спрей, зарегистрировано уменьшение вирусной нагрузки ДНК герпесвирусов в материале мазков из ротоглотки, наиболее выраженное в отношении ВГЧ-6А/В.
Ключевые слова: дети, рекуррентные инфекции органов респираторного тракта, герпесвирусные инфекции, Панавир Инлайт спрей.
Для цитирования: Мелехина Е.В., Музыка А.Д., Солдатова Е.Ю., Шалбарова Т.В. Панавир® в комплексной профилактике реактивации герпесвирусных инфекций у детей с рецидивирующими инфекциями органов респираторного тракта. РМЖ. Медицинское обозрение. 2022;6(11):618-625. DOI: 10.32364/2587-6821-2022-6-11-618-625.
Введение
Важным вопросом наблюдения пациентов с рецидивирующими инфекциями органов респираторного тракта являются вопросы профилактики реактивации герпесвирусных инфекций (ГВИ) с применением топических препаратов, имеющих доказанный высокий профиль безопасности.
Большинство эпизодов острых респираторных инфекций (ОРИ), возникающих у детей, имеют вирусное происхождение [1]. В литературе представлены данные о роли реактивации ГВИ у детей с рекуррентными ОРИ [2, 3] и о необходимости обследования детей с рецидивирующими ОРИ на ГВИ [4].
Проведенные нами ранее исследования показали, что среди детей с активной ГВИ (вирус герпеса человека (ВГЧ) 6А/В, вирус Эпштейна — Барр (ВЭБ), цитомегаловирус (ЦМВ), вирус простого герпеса 1-го типа (ВПГ-1)) через 3 мес. наблюдения от начала противовирусной терапии (ПВТ) у 89 (84%) пациентов был получен положительный клинический эффект (уменьшение количества ОРИ — у 20 детей, отсутствие ОРИ в течение 3 мес. — у 69 детей). Инфекция, вызванная ВГЧ-6А/В, установлена у 35% пациентов, ВЭБ — у 12%, ВПГ-1 — у 9%, ЦМВ — у 3%. ГВИ сочетанной этиологии имели место у 41% пациентов, из них наиболее часто выявлялось сочетание ВГЧ-6А/В + ВЭБ — у 23%, реже ВГЧ-6А/В + ВПГ-1 — у 9%, ВГЧ-6А/В + ВЭБ + ВПГ-1 — у 5%, ВГЧ-6А/В + ЦМВ — у 2%, ВГЧ-6А/В + ВЭБ + ЦМВ — у 2%.
После проведения курса ПВТ снижение активности ГВИ зафиксировано у 79 (76%) пациентов (у 59 из них после терапии были диагностированы латентные формы ГВИ, у 20 пациентов с ГВИ сочетанной этиологии латентной стала одна из ГВИ). То есть динамика лабораторных показателей несколько запаздывала по сравнению с купированием клинических проявлений заболевания (рис. 1) [5].
![Рис. 1. Эффективность проводимой терапии на первом этапе исследования [5] Fig. 1. Efficacy of the administered therapy during the first stage of the trial [5] Рис. 1. Эффективность проводимой терапии на первом этапе исследования [5] Fig. 1. Efficacy of the administered therapy during the first stage of the trial [5]](/upload/medialibrary/167/618-1.png)
Через 3 мес. после окончания ПВТ с использованием препаратов инозина пранобекс, ацикловир, валацикловир был проведен анализ динамики частоты эпизодов ОРИ за период, прошедший с начала наблюдения. На момент начала наблюдения 77% детей после курса ПВТ препаратами прямого противовирусного действия за предыдущие 3 мес. не болели ОРИ ни разу, 23% детей болели 1–2 раза в месяц с повышением температуры более 38 °С, получали только местную терапию (т. е. заболевание протекало легче, чем до терапии). У детей, которые не получали профилактику реактивации ГВИ, через 3 мес. наблюдалось улучшение в 11% случаев, отсутствие динамики — в 44%, ухудшение — в 44%, а через 6 мес. реактивация имела место у 100% обследованных. Отсутствие профилактики реактивации инфекции ВГЧ-6А/В у детей с рецидивирующими ОРИ и положительной динамикой клинико-лабораторных показателей после курса ПВТ ведет к возникновению реактивации в 100% через 6 мес. Этот факт объясняет необходимость клинико-лабораторного контроля состояния детей, перенесших клини-чески манифестные формы ГВИ минимум в течение 6 мес. [5].
Панавир® — линейка российских противовирусных препаратов растительного происхождения с широким спектром антивирусного действия. Панавир® является биологически активным полисахаридом, который получен из растения Solanum tuberosum (паслен клубненосный). Действующим веществом препарата являются высокомолекулярные полисахаридные частицы. S. Stobun et al. [6] показали, что противовоспалительная активность препарата Панавир® в 4–8 раз усиливает секрецию АТФ и фактора ингибирования миграции макрофагов клетками HL-60. Данный эффект опосредован активным фагоцитозом частиц Панавира клетками.
Российскими исследователями была продемонстрирована эффективность и безопасность Панавир® (суппозитории ректальные) у детей с ОРИ и гриппом. В группе пациентов, которые получали Панавир®, быстрее наступало выздоровление, нормализация температуры, купирование интоксикации и катаральных явлений. В соответствии с данными анкетирования по Интегральной шкале оценки удовлетворенности результатами лечения (Integrative Medicine. Patient Satisfaction, IMPSS) полная удовлетворенность результатами лечения родителями/усыновителями пациентов отмечалась в 80% случаев в группе Панавира и в 25% случаев в группе плацебо [7]. Ранее В.И. Кузнецов и соавт. [8] провели оценку эффективности Панавира в профилактике и лечении ОРИ у взрослых. Авторы показали, что применение спрея Панавир® Инлайт приводило к сокращению продолжительности заболевания в среднем на 3,35 дня, уменьшению продолжительности лихорадки, катаральных явлений и выраженности головной боли, кашля, озноба, насморка, слабости. При назначении средства с профилактической целью имело место положительное влияние на показатели иммунитета. Эффективность спрея Панавир® Инлайт при комплексном лечении гриппа и ОРИ у взрослых пациентов инфекционного стационара изучалась Л.И. Ткаченко и соавт. [9]. Использование спрея Панавир® Инлайт способствовало купированию катаральных проявлений: боли и першения в горле и гиперемии ротоглотки, оказывало положительное влияние на местный иммунитет (sIgA), сокращало продолжительность пребывания в стационаре.
Таким образом, показана эффективность при ОРИ спрея Панавир® Инлайт у взрослых, а также ректальных суппозиториев Панавир® Инлайт у детей. Исследований эффективности применения спрея Панавир® Инлайт у детей с ГВИ ранее не проводилось.
Цель настоящего исследования: анализ клинической и вирусологической эффективности комплексной терапии с включением спрея Панавир® Инлайт в профилактике ОРИ у детей на фоне реактивации ГВИ.
Материал и методы
В наблюдательную программу включались дети в возрасте от 1 до 12 лет до начала применения препаратов прямого противовирусного действия с жалобами на ежемесячные ОРИ в течение последних 3 мес. либо с подтвержденной реактивацией ГВИ, а также пациенты с сохраняющимся выделением ДНК герпесвирусов из ротоглотки или ротоглотки и крови после окончания курса ПВТ. Критериями исключения были: возраст менее 1 года и старше 12 лет; отсутствие ежемесячных ОРИ; отсутствие подтвержденной реактивации ГВИ до начала противовирусного лечения либо отсутствие выделения ДНК герпесвирусов из ротоглотки или ротоглотки и крови после окончания курса ПВТ с применением препаратов прямого противовирусного действия; наличие первичных иммунодефицитных состояний.
Наблюдение осуществлялось в течение 3 мес. Всем пациентам проводилось в динамике комплексное клинико-лабораторное обследование. Диагностика ГВИ осуществлялась серологическими методами, а также методом ПЦР. Методом ПЦР с гибридизационно-флуоресцентной детекцией результатов анализа в режиме реального времени в образцах периферической крови, мазках из ротоглотки выявляли и количественно определяли ДНК ЦМВ, ВГЧ-6А/В, ВЭБ. ПЦР-исследование проводили при помощи наборов реагентов, разработанных в ФБУН ЦНИИ Эпидемиологии Роспотребнадзора. Методом ИФА определяли вирус-специфические Ig М и G к белкам ВПГ-1, ВЭБ, ЦМВ, ВГЧ-6А/В.
Всего было обследовано 76 пациентов в возрасте от 0 до 14 лет, медиана возраста составила 5 (IQR 2-8) лет: 35 (46,1%) девочек и 41 (53,9%) мальчик.
Общая характеристика пациентов представлена в таблице 1.
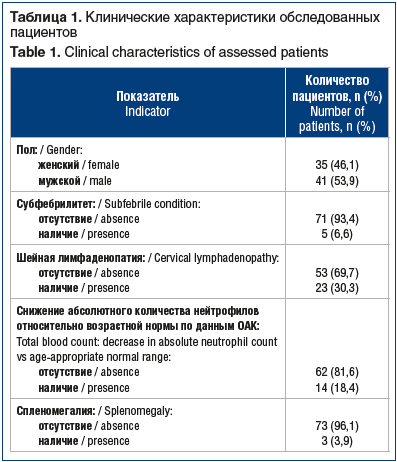
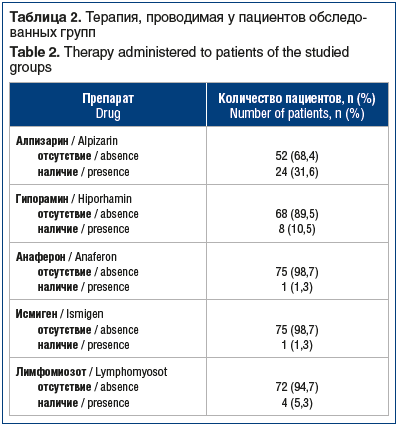
Основную группу составили 49 детей, которые получали Панавир® Инлайт спрей в составе комплексной терапии, в группу сравнения включены 27 детей. Схема приема — по 1–2 впрыска в горло после еды на 14 дней, 14 дней перерыв, затем 14 дней повторить (всего 3 курса). Группы были сопоставимы по возрасту полу, основным характеристикам, а также сопутствующей терапии (табл. 2).
Критериями эффективности (табл. 3), которые оценивались у пациентов, были: клиническая эффективность, оценка уровня выделения ДНК герпесвирусов количественно и качественно в ротоглотке до и после терапии спреем Панавир® Инлайт, вирусологическая эффективность на основании комплексного обследования с применением прямых и непрямых методов диагностики, как суммарная, так и по нескольким вирусам отдельно (ВЭБ, ЦМВ, ВГЧ-6А/В).

Статистический анализ проводился с использованием программы StatTech v. 2.8.8 (разработчик — ООО «Статтех», Россия). Количественные показатели описывались как средние значения (M) и стандартные отклонения (SD) с указанием границ 95% доверительного интервала (95% ДИ) (при нормальном распределении) или как медианы (Me) и межквартильные диапазоны (IQR) (при распределении, отличном от нормального). Категориальные данные описывались с указанием абсолютных значений и процентных долей. Сравнение двух независимых групп по количественному показателю, имеющему нормальное распределение, выполнялось с помощью t-критерия Стьюдента, если распределение отличалось от нормального — с помощью U-критерия Манна — Уитни. Сравнение процентных долей при анализе четырехпольных таблиц сопряженности выполнялось с помощью критерия хи-квадрат Пирсона, точного критерия Фишера. Сравнение процентных долей при анализе многопольных таблиц сопряженности выполнялось с помощью критерия хи-квадрат Пирсона.
Результаты исследования
При включении в наблюдательную программу все пациенты предъявляли жалобы на ежемесячные ОРИ, субфебрилитет, длительную заложенность носа и др. После лечения исчезновение или уменьшение жалоб было зафиксировано у 38 (77,6%) пациентов основной группы и 15 (55,6%) детей в группе сравнения, активные жалобы сохранялись у 11 (22,4%) и 12 (44,4%) пациентов соответственно (р=0,046).
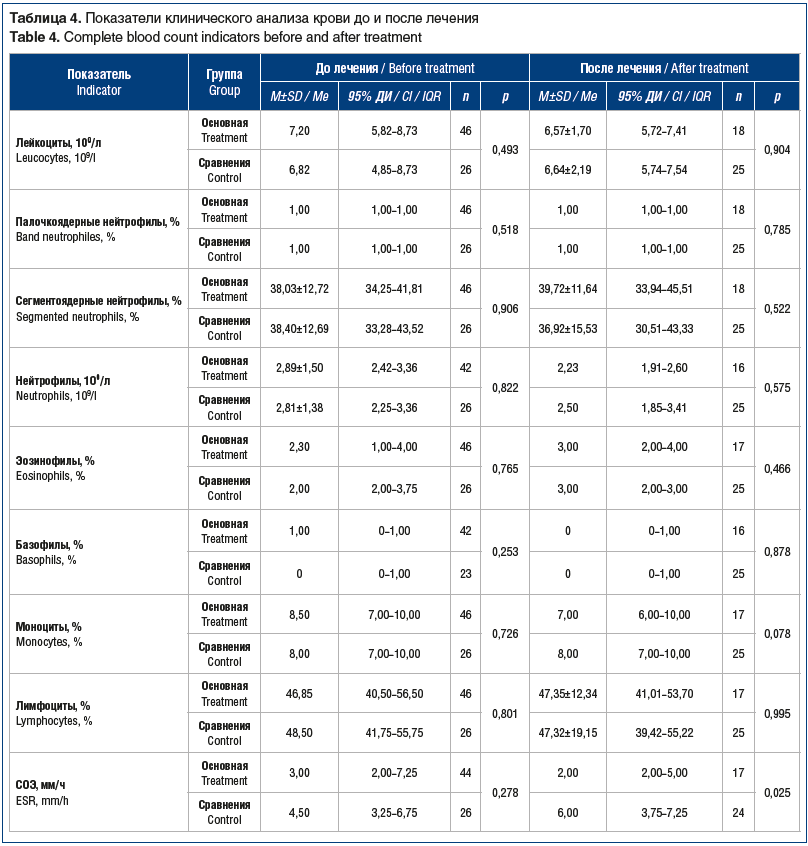
Показатели клинического анализа крови до начала лечения были сопоставимы в сравниваемых группах. После лечения у пациентов группы сравнения достоверно чаще отмечалось повышение СОЭ, а также наблюдался моноцитоз, что, вероятно, связано с реактивацией ГВИ (табл. 4).
Таким образом, назначение спрея Панавир® Инлайт у детей с рецидивирующими ОРИ после проведения основного курса терапии препаратами с прямым противовирусным действием способствовало уменьшению жалоб и нормализации самочувствия в 77,6% случаев (в 1,5 раза чаще, чем в группе сравнения), тогда как в группе сравнения у 11 (40,7%) детей сохранялись жалобы, у 1 (3,7%) наблюдалось появление новых жалоб.
Таким образом, при включении пациентов в исследование показатели клинического анализа крови были сопоставимы в сравниваемых группах. Анализ динамики показателей до и после терапии в обеих группах не выявил достоверных различий. Однако после лечения у пациентов группы сравнения повышение СОЭ и моноцитоз после лечения регистрировались чаще, чем у пациентов основной группы.
На момент начала терапии у всех пациентов сравниваемых групп наблюдалось выделение одного или нескольких герпесвирусов в материале из ротоглотки. В этиологической структуре вирусовыделения в ротоглотке преобладал ВГЧ-6А/В — у 64 (82%) пациентов (из них у 39 (61%) в моноварианте), ВЭБ — у 26 (39%) (из них у 6 (23%) в моноварианте), ЦМВ — у 12 (16%) (из них у 5 (41%) в моноварианте).
При анализе выделения вирусов в материале из ротоглотки у пациентов основной группы было установлено, что после лечения ДНК вирусов в ротоглотке не обнаруживалась у 37 (75,5%) детей, 1 вирус выделен у 10 (20,4%) детей, 2 вируса — у 2 (4,1%).
В группе сравнения количество пациентов с отсутствием выделения вирусов из ротоглотки после лечения составило 16 (59,3%), 1 вирус обнаружен у 10 (37,0%) пациентов, 2 вируса — у 1 (3,7%) обследованного (р<0,001) (табл. 5).
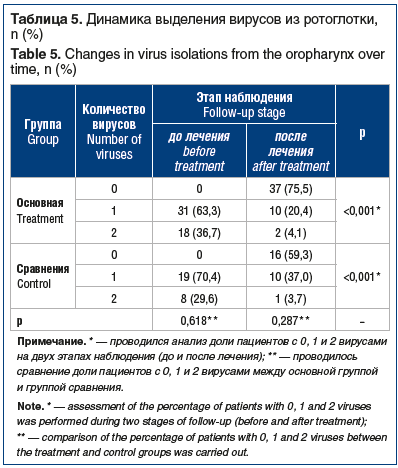
Проведен анализ выделения каждого из исследуемых вирусов по результатам ПЦР-исследования качественным и количественным методом. ДНК ВГЧ-6А/В в основной группе до лечения обнаруживалась у 40 (81,6%) пациентов, после лечения — у 10 (20,4%) пациентов, в группе сравнения — у 24 (88,9%) и 10 (37,0%) соответственно. При анализе связанных совокупностей установлено снижение доли пациентов с выделением ВГЧ-6А/В в каждой из групп (р<0,001). При анализе доли пациентов с выделением ДНК ВГЧ-6А/В в ротоглотке после лечения показано, что ВГЧ-6А/В чаще выделяется у пациентов группы сравнения — 10 (37%) против 10 (20,4%) пациентов, получавших Панавир® Инлайт спрей (р=0,173).
При анализе результатов количественного исследования у пациентов основной группы установлено, что медиана вирусной нагрузки ВГЧ-6А/В в ротоглотке до лечения составила 645,0 (IQR 399,00–1600,00) копий/мл, а после лечения — 399,00 (IQR 0,00–775,00) копий/мл, (р=0,084).
В основной группе ДНК ВЭБ до лечения обнаруживалась у 19 (38,8%) пациентов, после лечения — у 1 (2,0%) пациента, снижение доли пациентов с выделением вируса было статистически значимым (р<0,001); в группе сравнения — у 7 (25,9%) и 1 (3,7%) соответственно (р=0,034).
Выделение ЦМВ из материала ротоглотки у обследованных пациентов наблюдалось реже, чем ВЭБ и ВГЧ-6А/В. Тем не менее была установлена тенденция к снижению доли детей, у которых обнаруживался вирус после лечения: в основной группе — с 8 (16,3%) до 3 (6,1%) после лечения (р=0,059), в группе сравнения — с 6 (22,2%) до 1 (3,7%).
Таким образом, Панавир® Инлайт спрей в комплексной профилактике реактивации приводит к уменьшению выделения ДНК ВЭБ, ЦМВ и ВГЧ-6А/В из ротоглотки. Наиболее выраженный эффект получен в отношении ВГЧ-6А/В.
На момент включения в исследование анти-ВПГ-1, -2 и анти-ЦМВ IgM у пациентов сравниваемых групп отсутствовали. Анти-ВГЧ-6А/В IgM в основной группе до лечения выявлялись у 1 пациента, анти-VCA ВЭБ IgM выявлены у 2 детей в основной группе и у 1 ребенка в группе сравнения до терапии. После лечения IgM к анализируемым герпесвирусам отсутствовали у всех пациентов обеих групп. Медиана анти-ВГЧ-6А/В IgG в основной группе до лечения составила 630,00 (IQR 190,00–1200,00), после лечения — 0 (IQR 0,00–350,00) (р=0,008).
Было установлено, что подключение к комплексной терапии спрея Панавир® Инлайт не оказывало влияния на уровень анти-ВПГ-1, -2, анти-ВЭБ, анти-ЦМВ IgG, в то время как наблюдалось снижение уровня анти-ВГЧ-6А/В IgG в основной группе в динамике.
На основании оценки данных комплексного обследования пациентов до начала терапии и после нее была установлена стадия ГВИ. Активными формами инфекции считали реактивацию ГВИ, проявляющуюся лабораторно наличием анти-ГВИ IgM, ДНК и/или антигенов вируса в крови. К неактивным формам инфекции относили выявление анти-ГВИ IgG в крови и/или ДНК ГВИ в ротоглотке.
Изменение стадии ГВИ до и после терапии фиксировали для каждого вида ГВИ и суммарно: как «лучше» (переход в неактивную стадию), «хуже» (переход в активную стадию), «без изменения» (сохранение той же стадии).
Полученные данные представлены на рисунке 2.
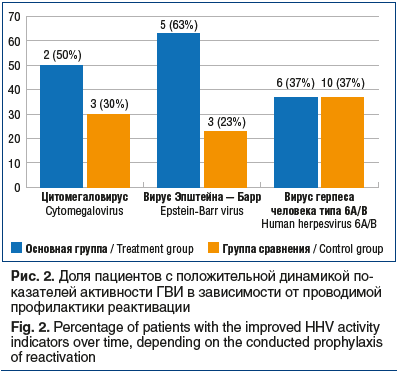
Важно отметить, что в обеих группах были пациенты, у которых отмечена отрицательная динамика активности инфекции, вызванной ВГЧ-6А/В. В группе сравнения такие наблюдения преобладали по сравнению с основной группой: 14 (28,5%) против 5 (18,8%), р>0,05.
Итоговое изменение активности ГВИ на фоне проводимой терапии оценивали на основании уменьшения лабораторной активности инфекции в случае моно-ГВИ и по уменьшению активности хотя бы одной из ГВИ.
Результаты представлены на рисунке 3.
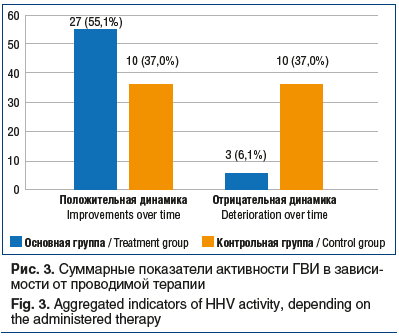
Отрицательная динамика лабораторных показателей, отражающих суммарную активность ГВИ, наблюдалась у пациентов, которые не получали Панавир® Инлайт спрей, — 37%, что достоверно выше, чем в группе детей, которые получали Панавир® Инлайт спрей, — 6,1% (р<0,001).
Обсуждение
Герпесвирусные инфекции являются первично-хроническими плейотропными инфекциями, снижающими иммунную реактивность макроорганизма. Инфицирование происходит преимущественно в детском возрасте, а лабораторные маркеры инфекции сохраняются в течение всей жизни.
Рекуррентные респираторные инфекции представляют собой социально значимые состояния в педиатрической практике и в ряде случаев связаны с реактивацией ГВИ [10, 11].
Проведение курсов ПВТ показало свою эффективность [4], однако длительность курсов ограничена в связи с возможностью развития побочных эффектов. С учетом высокого процента реактивации ГВИ через 3 и 6 мес. после окончания ПВТ встает вопрос о необходимости проведения безопасной профилактики реактивации ГВИ с помощью, например, спрея Панавир® Инлайт.
Выделение ДНК герпесвирусов в материале мазков из ротоглотки является распространенным лабораторным маркером ГВИ и не всегда коррелирует с клиническими проявлениями инфекционного процесса [12]. Однако именно этот показатель наиболее часто и длительно сохраняется после купирования проявлений заболевания и исчезновения ДНК и/или антигенов герпесвирусов из крови.
Учитывая вышесказанное, мы применили спрей растительного происхождения Панавир® Инлайт, имеющий противовирусную активность (в том числе и в отношении герпесвирусов), в комплексной профилактике реактивации ЦМВ, ВЭБ, ВГЧ-6А/В. Группу сравнения составили пациенты, сопоставимые с опытной группой по возрастными и гендерным характеристикам, а также по этиологической структуре выявленных у них ГВИ, не получавшие Панавир® Инлайт спрей в комплексной профилактике.
Нами оценивалось клиническое состояние пациентов по динамике жалоб, активность ГВИ на основании комплексного обследования, включавшего прямые и непрямые методы диагностики. Вирусная нагрузка ДНК герпесвирусов в материале мазков из ротоглотки до и после терапии в обеих группах определялась качественными и количественными методами ПЦР.
Заключение
Показано, что применение спрея Панавир® Инлайт в комплексной профилактике реактивации ГВИ у детей с рецидивирующими ОРИ приводит к клиническому улучшению состояния в 77,6% случаев против 55,6% случаев в группе сравнения. Назначение данного спрея пациентам, у которых выделяется ДНК герпесвирусов в ротоглотке, приводит к уменьшению вирусной нагрузки вдвое в этом локусе. Наибольший эффект получен в отношении инфекции, вызванной ВГЧ-6А/В. По данным комплексного обследования, применение спрея Панавир® Инлайт достоверно чаще приводило к переходу ГВИ в латентное состояние и поддерживало ГВИ в длительном латентном состоянии после курса ПВТ с применением препаратов прямого противовирусного действия. Полученные в ходе исследования результаты позволяют рекомендовать Панавир® Инлайт спрей в комплексной терапии ГВИ пациентам старше 1 года с выделением ДНК герпесвирусов в материале мазков из ротоглотки.
Сведения об авторах:
Мелехина Елена Валериевна — д.м.н., доцент по специальности «педиатрия», в.н.с. клинического отдела инфекционной патологии ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; врач-педиатр инфекционного отделения ГАУЗ МО «Химкинская ОБ»; 141407, Россия, г. Химки, Куркинское шоссе, д. 11; ORCID iD 0000-0002-9238-9302.
Музыка Анна Драгиевна — к.м.н., с.н.с. клинического отдела инфекционной патологии ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORСID iD 0000-0002-2269-2533.
Солдатова Евгения Юрьевна — м.н.с. клинического отдела инфекционной патологии ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0002-0683-8010.
Шалбарова Татьяна Васильевна — лаборант-исследователь клинического отдела инфекционной патологии ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0003-3659-3592.
Контактная информация: Мелехина Елена Валерьевна, e-mail: e.melekhina@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 23.08.2022.
Поступила после рецензирования 15.09.2022.
Принята в печать 10.10.2022
About the authors:
Elena V. Melekhina — Dr. Sc. (Med.), associate professor in pediatrics, leading researcher of the Clinical Department of Infectious Diseases, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being; 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; pediatrician of the Infectious Diseases Department, Khimki
Regional Hospital; 11, Kurkinskoe road, Khimki, 141407, Russian Federation; ORCID iD 0000-0002-9238-9302.
Anna D. Muzyka — C. Sc. (Med.), senior researcher of the Clinical Department of Infectious Diseases, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being; 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; ORСID iD 0000-0002-2269-2533.
Evgeniya Yu. Soldatova — junior researcher of the Clinical Department of Infectious Diseases, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being; 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; ORCID iD 0000-0002-0683-8010.
Tatyana V. Shalbarova — researcher technician of the Clinical Department of Infectious Diseases, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being; 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; ORCID iD 0000-0003-3659-3592.
Contact information: Elena V. Melekhina, e-mail: e.melekhina@mail.ru.
Financial Disclosure: no authors have a financial or property
interest in any material or method mentioned.
There is no conflict of interests.
Received 23.08.2022.
Revised 15.09.2022.
Accepted 10.10.2022.
2. Боковой А.Г., Егоров А.И. Герпесвирусные инфекции у детей и родителей: учебное пособие для врачей педиатров, инфекционистов, иммунологов. Хабаровск: Полиграф — Партнер; 2016.
3. Романцов М.Г., Ершов Ф.И. Часто болеющие дети. Современная фармакотерапия: Руководство для врачей. М.: ГЭОТАР-Медиа; 2009.
4. Лысенкова М.Ю., Каражас Н.В., Мелехина Е.В. и др. Герпесвирусные инфекции у детей с рецидивирующими респираторными заболеваниями. Детские инфекции. 2018;17(2):17–20. DOI: 10.22627/2072-8107-2018-17-2-17-21.
5. Мелехина Е.В. Инфекция, вызванная HUMAN BETAHERPESVIRUS 6A/B, у детей: клинико-патогенетические аспекты, диагностика и терапия: автореф. дисс. … д-ра мед. наук. М., 2019.
6. Stovbun S.V., Kalinina T.S., Zlenko D.V. et al. Antiviral potential of plant polysaccharide nanoparticles actuating non-specific immunity. Int J Biol Macromol. 2021;182:743–749. DOI: 10.1016/j.ijbiomac.2021.03.135.
7. Лукашова Л.В., Афанасьева О.И., Портнягина Е.В. и др. Лечение гриппа и других острых респираторных вирусных инфекций у детей: результаты многоцентрового двойного слепого плацебо-контролируемого рандомизированного сравнительного клинического исследования. Российский вестник перинатологии и педиатрии. 2021;66(1):131–139. DOI: 10.21508/1027-4065-2021-66-1-131-139.
8. Кузнецов В.И., Вялов С.С. Острые респираторные вирусные инфекции: как лечить и предупреждать эффективно? Поликлиника. 2009;5:85–88.
9. Ткаченко Л.И., Ртищева Л.В., Дохов М.Б. и др. Новые возможности повышения эффективности терапии гриппа и острых респираторных вирусных инфекций. Профилактическая медицина. 2018;21(5):113–116. DOI: 10.17116/profmed201821051113.
10. Schaad U.B., Esposito S., Razi C.H. Diagnosis and Management of Recurrent Respiratory Tract Infections in Children: A Practical Guide. Arch Pediatr Infect Dis. 2016;4(1):e31039. DOI: 10.5812/pedinfect.31039.
11. Chiappini E., Santamaria F., Marseglia G.L. et al. Prevention of recurrent respiratory infections: Inter-society Consensus. Ital J Pediatr. 2021;47(1):211. DOI: 10.1186/s13052-021-01150-0.
12. Пермякова А.В., Дерюшева А.Ю. Заболеваемость, вызванная Human Herpesvirus, у детей дошкольного возраста: проблемы и решения. Детские инфекции. 2020;4(73):50–53. DOI: 10.22627/2072-8107-2020-19-4-50-53.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.