Антибактериальная терапия респираторных инфекций сегодня: остались ли надежды?
В настоящее время мировая общественность озабочена повсеместным ростом резистентности клинически значимой патогенной микрофлоры и отсутствием революционных открытий в сфере создания новых групп антибактериальных средств. Рост антибиотикорезистентности происходит на фоне дефицита новых системных антибактериальных препаратов. В последние десятилетия разработка антибиотиков существенно замедлилась, многие фармацевтические компании прекратили работу в этой области по причине сложности проведения клинических исследований и ограниченной экономической привлекательности разработки новых антибиотиков.
Несмотря на то, что и в мире, и в России наблюдается рост устойчивости респираторных патогенов к антибиотикам многих фармакологических групп, амоксициллин/клавуланат по-прежнему сохраняет высокую антибактериальную активность в отношении всех основных возбудителей респираторных инфекций. Амоксициллин/клавуланат рекомендован для лечения инфекций нижних дыхательных путей у взрослых и детей, включен в национальные клинические рекомендации по лечению внебольничной пневмонии и хронической обструктивной болезни легких: для приема внутрь на амбулаторном этапе лечения, для парентерального введения в условиях стационара. Одним из факторов успешного применения амоксициллина/клавуланата является наличие различных лекарственных форм для энтерального и парентерального введения, в т. ч. растворимых форм, которые улучшают фармакокинетику и повышают безопасность препарата.
Ключевые слова: респираторные инфекции, лечение, эффективность, безопасность, амоксициллин/клавуланат,Амоксиклав.
Для цитирования: Визель А.А., Визель И.Ю. Антибактериальная терапия респираторных инфекций сегодня: остались ли надежды? РМЖ. Медицинское обозрение. 2019;3(9(I)):29-33.
A.A. Vizel, I.Yu. Vizel
Kazan State Medical University
Nowadays, the world community is concerned about the widespread increase in the resistance of clinically significant pathogenic microflora and the lack of revolutionary discoveries in creating new groups of antibacterial agents. The increase in antibiotic resistance occurs in the setting of new systemic antibacterial drugs deficiency. In recent decades, antibiotics development has slowed significantly С many pharmaceutical companies have stopped working in this area due to the clinical trials complexity and limited economic attractiveness of developing new antibiotics. Despite the fact that there is an increase in respiratory pathogens resistance to antibiotics of many pharmacological groups (both in the world and in Russia), amoxicillin/clavulanate still retains high antibacterial activity against all the respiratory infections main pathogens. Amoxicillin/clavulanate is recommended for lower respiratory tract infections treatment in adults and children and included in the national clinical guidelines for the treatment of community-acquired pneumonia and chronic obstructive pulmonary disease: for oral administration С at the outpatient treatment stage, for parenteral administration С in a clinical setting. One of the factors for the successful amoxicillin/clavulanate application is the presence of various dosage forms for enteral and parenteral administration, including soluble forms that improve pharmacokinetics and increase drug safety.
Keywords: respiratory infections, treatment, efficacy, safety, amoxicillin/clavulanate, Amoksiklav.
For citation: Vizel A.A., Vizel I.Yu. Modern antibacterial therapy of respiratory infections: is there any hope? RMJ. Medical Review. 2019;9(I):29-33.
Статья посвящена вопросам антибактериальной терапии респираторных инфекций с учетом проблемы антибиотикорезистентности
Актуальность
Представления человечества и медицинской науки о лечении инфекционной патологии нижних дыхательных путей претерпели разительные изменения за последнее столетие: от фатального ожидания "кризиса" в лечении крупозной пневмонии, преодоление которого обеспечивало обоснованную надежду врачу и пациенту на благополучный исход, от ослепляющего оптимизма и надежд на всесилие антибиотиков, которые могли бы даже упразднить гнойную хирургию, до современного состояния озабоченности повсеместным ростом резистентности клинически значимой патогенной микрофлоры и отсутствием революционных открытий в сфере создания новых групп антибактериальных средств. Рост антибиотикорезистентности происходит на фоне дефицита новых системных антибактериальных препаратов: рынок антибиотиков, несмотря на высокую неудовлетворенную потребность, остается непривлекательным для инвестиций. Можно констатировать, что в последние десятилетия разработка антибиотиков существенно замедлилась, многие фармацевтические компании прекратили работу в этой области по причине сложности проведения клинических исследований и ограниченной экономической привлекательности разработки новых антибиотиков. В связи с этим, по данным на 2013 г., в США была поставлена задача разработать 10 новых, безопасных
и эффективных антибиотиков к 2020 г., этот проект Американского общества инфекционных болезней (Infectious Diseases Society of America С IDSA) был назван "Инициатива 10x20" [1]. Возможно, этот проект изменит ситуацию. Пока же основными задачами становятся сохранение эффективности существующих препаратов и замедление развития резистентности к ним патогенной микрофлоры.
Оценка устойчивости респираторной микрофлоры к антибиотикам не может не вызывать тревоги. В международном исследовании D.J. Biedenbach et al., проведенном в пяти странах (Аргентина, Мексика, Венесуэла, Россия, Филиппины), изучалась чувствительность возбудителей внебольничных инфекций к различным классам антибиотиков по критериям EUCAST (European Committee on Antimicrobial Susceptibility Testing - Европейский комитет по определению чувствительности к антимикробным препаратам) и CLSI (Clinical and Laboratory Standards Institution - Институт клинических и лабораторных стандартов) [2].
Результаты исследования подтвердили устойчивую тенденцию последних лет - повсеместное снижение чувствительности пневмококков к макролидам. Так, в России к кларитромицину и по критериям CLSI, и по критериям EUCAST уровень резистентности выделенных штаммов пневмококка составил 43,2%; к азитромицину по критериям CLSI резистентными были 43,2% штаммов пневмококка; по критериям EUCAST С 43,9% штаммов [2].
В этом же исследовании показано, что сохраняется высокая чувствительность к амоксициллину/клавуланату и пневмококков (в Аргентине С 100%, в России С 83,8%), и гемофильной палочки (в Аргентине С 90%, в Мексике, России, на Филиппинах С 100%) (по критериям CLSI).
В Республике Татарстан был проведен ряд ретроспективных исследований причин летальных исходов больных внебольничной пневмонией (ВП), в которых была отмечена высокая эффективность препаратов аминопенициллинового ряда, а среди больных с благоприятным исходом пневмонии достоверно выше была частота применения аминопенициллинов, особенно С амоксициллина/клавуланата [3, 4]. По данным сайта https://www.antibiotic.ru/, чувствительность к аминопенициллинам и ингибитор-защищенным аминопенициллинам в последние годы остается высокой, тогда как многие макролиды и фторхинолоны снижают свою активность in vitro [5].
Эффективность и безопасность амоксициллина/клавуланата подтверждены результатами многих исследований и многолетним практическим опытом использования препарата в клинической практике.
Амоксициллин/клавуланат активен в отношении основных возбудителей пневмонии и хронической обструктивной болезни легких (ХОБЛ): Streptococcus pneumoniae, Haemophilus influenzae, Staphylococcus aureus, Klebsiella pneumoniae [6].
Амоксициллин/клавуланат обладает высокой биодоступностью (90%) при приеме внутрь, создает высокие концентрации в легких и плевральной жидкости, быстро проникает в мокроту и накапливается в слизистой оболочке бронхов, создавая концентрации, значительно превышающие минимальные подавляющие концентрации чувствительных микроорганизмов, включая продуцирующие β-лактамазу штаммы H. influenzae и Moraxella catarrhalis [7].
Амоксициллин/клавуланат имеет хороший профиль безопасности. Согласно результатам многочисленных клинических исследований амоксициллин/клавуланат отличается хорошей переносимостью, нежелательные явления при применении антибиотика развиваются относительно редко, в большинстве случаев являются дозозависимыми, носят транзиторный характер и не требуют отмены препарата [8].
Широкий спектр антимикробной активности, привлекательная фармакокинетика и приемлемый профиль безопасности позволили амоксициллину/клавуланату стать одним из наиболее популярных антибактериальных препаратов, применяемых в лечении большого числа инфекционных заболеваний.
Так, в Испании наиболее часто применяемыми антибиотиками при ВП были амоксициллин/клавуланат (30,7%) и левофлоксацин (30,4%) [9]. В Кабардино-Балкарии был проведен опрос врачей по предпочтениям в назначении препаратов. Наиболее часто назначаемым антибиотиком при лечении ВП был амоксициллин/клавуланат, основными критериями выбора врачей были эффективность и безопасность [10]. Фармакоэкономический анализ продаж антибиотиков для системного применения на фармацевтическом рынке г. Хабаровска показал, что амоксициллин/клавуланат входит в перечень лидирующих препаратов [11].
К числу основных показаний для назначения антибиотика относятся ВП и инфекционное обострение ХОБЛ.
Внебольничная пневмония
Амоксициллин/клавуланат занимает одно из ведущих мест в лечении ВП [12, 13].
Отечественные авторы показали клинические и экономические преимущества ступенчатой терапии амоксициллином/клавуланатом при пневмонии [14].
Часто начальная терапия проводится препаратами нескольких классов, и предельно важной становится тактика последующего снижения антибактериальной нагрузки. Испанские исследователи показали, что при ВП деэскалация антибиотиков может быть сужена до пенициллина, амоксициллина или амоксициллина/клавуланата в течение первых 72 ч после поступления. Было показано, что переход на эти антибиотики не оказывал негативного влияния на исходы ВП даже у больных с бактериемией, тяжелым течением пневмонии и при клинической нестабильности [15].
При анализе ведения 1290 больных с ВП в Испании в 2000Р2013 гг. было отмечено, что чаще всего в виде стартовой терапии были назначены амоксициллин/клавуланат (30,7%) и левофлоксацин (30,4%). При оказании первичной помощи частота этих назначений была 38% и 26% соответственно, а при оказании неотложной помощи препараты менялись местами: левофлоксацин С 35%, а амоксициллин/клавуланат С 25% [9].
В Университетской больнице Кокоди в Кот-д’Ивуаре было проведено ретроспективное исследование 62 пациентов с ВП, госпитализированных с 1 декабря 2008 г. по 30 ноября 2010 г. Наиболее часто были назначены амоксициллин/клавуланат (42,27%), нетилмицин (34,5%) и ципрофлоксацин (6%). Врачи назначали амоксициллин/клавуланат с нетилмицином в 80,64% случаев, а монотерапия антибиотиками составляла 14,52% назначений. Авторы отметили, что уровень соответствия локальным клиническим рекомендациям составлял всего 3,6% [16].
Исследование, проведенное во Франции, свидетельствует о значимости применения амоксициллина/клавуланата в отделениях интенсивной терапии, где встречаются носители Enterobacteriaceae, которая вырабатывает бета-лактамазы расширенного спектра. Мультивариантный анализ показал, что колонизация Enterobacter spp. или Klebsiella pneumoniae является независимым фактором развития пневмонии, вызванной возбудителями, вырабатывающими бета-лактамазы расширенного спектра, а применение амоксициллина/клавуланата в течение более 2 дней пребывания в отделении интенсивной терапии оказывало достоверное протективное действие [17].
В России в настоящее время при выборе антибиотика следует руководствоваться клиническими рекомендациями, разработанными экспертами Российского респираторного общества (РРО) и Межрегиональной ассоциации по клинической микробиологии и антимикробной химиотерапии (МАКМАХ), опубликованными на сайте Российского респираторного общества и на сайте www.antibiotic.ru [12].
Амоксициллин/клавуланат является препаратом выбора у амбулаторных больных ВП с сопутствующими заболеваниями (ХОБЛ, сахарный диабет, хроническая сердечная недостаточность, хроническая болезнь почек со снижением скорости клубочковой фильтрации, цирроз печени, алкоголизм, наркомания, истощение), и/или принимавших за последние 3 мес. антибиотики в течение і2 последовательных дней, и/или имеющих иные факторы риска инфицирования редкими и/или полирезистентными возбудителями (табл. 1) [12].

Амоксициллин/клавуланат является препаратом выбора у госпитализированных больных с нетяжелой ВП, без сопутствующих заболеваний и факторов риска инфицирования редкими и/или полирезистентными возбудителями, а также у пациентов, имеющих сопутствующие заболевания и факторы риска инфицирования редкими и/или полирезистентными возбудителями (табл. 2) [12].
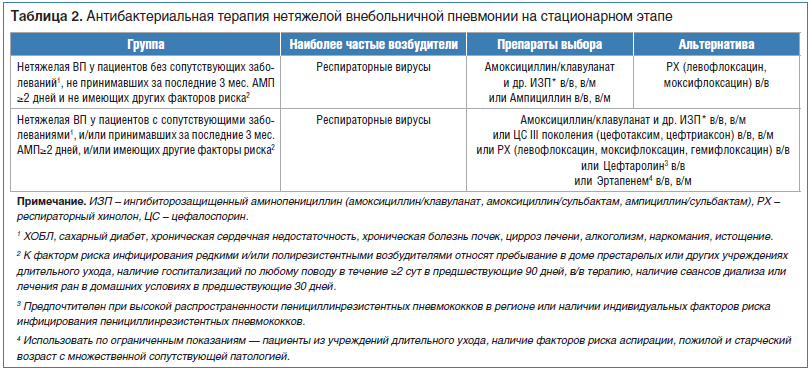
Амоксициллин/клавуланат является препаратом выбора при лечении больных тяжелой ВП на стационарном этапе без факторов риска инфицирования P. aeruginosa и аспирации и у пациентов с подтвержденной/предполагаемой аспирацией (табл. 3) [12].
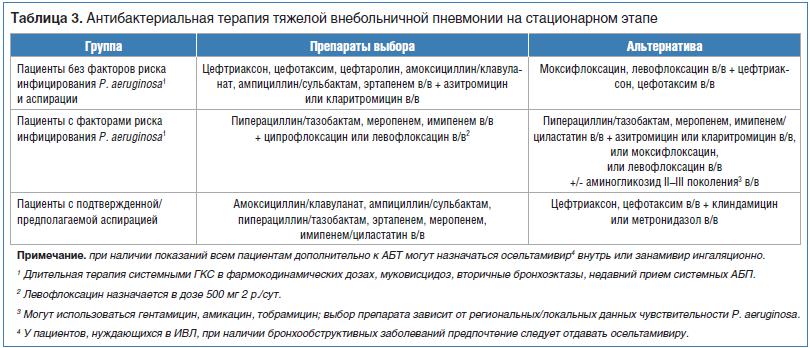
Амоксициллин/клавуланат у госпитализированных пациентов с ВП рекомендовано использовать в соответствии с принципами ступенчатой терапии: вначале внутривенное введение, в дальнейшем по мере клинической стабилизации -перевод пациента на пероральные формы.
Хроническая обструктивная болезнь легких
О влиянии амоксициллина/клавуланата на обострения ХОБЛ свидетельствуют многие публикации. Так, в Германии в плацебо-контролируемом исследовании 353 больных ХОБЛ было показано, что при назначении этого антибиотика время до следующего обострения составляло 233 дня, а в группе плацебо - 160 дней [18].
Однако, в отличие от пневмонии, значимость применения амоксициллина/клавуланата при обострении ХОБЛ не столь однозначна, особенно у амбулаторных больных с промежуточной вероятностью бактериальной инфекции. В Нидерландах у ограниченной группы из 35 пациентов с обострениями ХОБЛ без пневмонии у получавших преднизолон в сочетании с амоксициллином/клавуланатом и в сочетании с плацебо не было достоверных различий во времени от начала лечения обострения до его разрешения [19]. Работа была опубликована 5 лет тому назад. В настоящее время для трактовки таких результатов необходимо было бы разделить больных по уровню эозинофилов в крови, а также более строго доказывать бактериальную природу обострений.
Те же авторы год спустя опубликовали результаты обследования 25 пациентов, госпитализированных по поводу обострения ХОБЛ, у которых на 3-й день лечения определяли активность бета-лактамазы в мокроте и амоксициллина как в мокроте, так и в сыворотке. Они отметили, что у получавших амоксициллин/клавуланат при обострении ХОБЛ активность бета-лактамазы в мокроте не различалась у пациентов с концентрацией амоксициллина в мокроте ниже и выше минимальной ингибирующей концентрации (МИК90). Кроме того, у большинства пациентов концентрация амоксициллина в мокроте была ниже МИК90, на основании чего авторы призывали более тщательно изучать и оптимизировать применение антибиотиков при обострениях ХОБЛ [20]. Там же, в Нидерландах, проблему недостаточной концентрации амоксициллина/клавуланата в мокроте у больных ХОБЛ предложили решить посредством небулизации этого препарата в дозе от 50:10 до 300:60 мг амоксициллина/клавулановой кислоты, а безопасность оценивали по спирометрии до и после вдыхания. 17 пациентов прошли в общей сложности 100 ингаляций амоксициллина/клавуланата. Клинически значимых уменьшений объема форсированного выдоха за 1 с (ОФВ1) отмечено не было. Концентрация этого антибиотика в мокроте значительно превысила МИК90, что позволило авторам сделать заключение о перспективности его небулизации как у стабильных пациентов с ХОБЛ, так и у пациентов с тяжелым обострением [21].
Клинические рекомендации, разработанные экспертами РРО, содержат алгоритм эмпирической антибактериальной терапии инфекционного обострения ХОБЛ с учетом известных факторов риска неблагоприятного исхода и наиболее вероятными возбудителями [22].
В соответствии с национальными клиническими рекомендациями амоксициллин/клавуланат является препаратом выбора при лечении инфекционного обострения у всех пациентов с тяжелым течением ХОБЛ и у пациентов с факторами риска неблагоприятного исхода при легком и среднетяжелом течении ХОБЛ (табл. 4) [22].
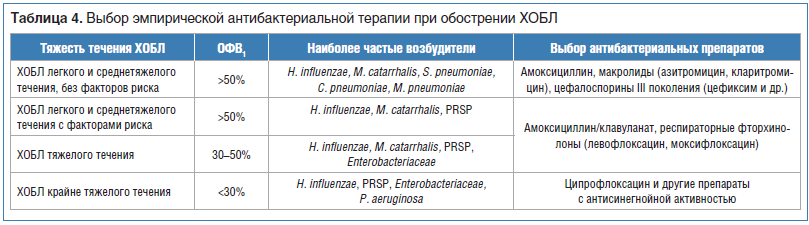
Заключение
Амоксициллин/клавуланат (Амоксиклав®) С комбинированный бета-лактамный антибиотик, который в условиях роста антибиотикорезистентности сохраняет свою клиническую значимость благодаря доказанной in vitro
респираторных патогенов, наличию удобных лекарственных форм для амбулаторного и
стационарного лечения и хорошей переносимости препарата. .
2. Biedenbach D.J., Badal R.E., Huang M.Y. et al. In vitro activity of oral antimicrobial agents against pathogens associated with community-acquired upper respiratory tract and urinary tract infections: a five country surveillance study. Infect. Dis. Ther. 2016;5(2):139–153. DOI: 10.1007/s40121-016-0112-3.
3. Шаймуратов Р.И., Лысенко Г.В., Визель А.А. Структурный анализ состояния пациентов, поступивших в стационары Республики Татарстан, со смертельным исходом от внебольничной пневмонии в 2012 году. Вестник современной клинической медицины. 2013;6(4):25–29. [Shaimuratov R.I., Lysenko G.V., Vizel A.A. Structural analysis of the condition of patients admitted to hospitals of the Republic of Tatarstan, with a fatal outcome from community-acquired pneumonia in 2012. Bulletin of modern clinical medicine. 2013;6(4):25–29 (in Russ.)].
4. Визель А.А., Лысенко Г.В. Особенности ведения больных внебольничной пневмонией в Республике Татарстан. Фарматека. 2014;15(288):31–34. [Vizel A.A., Lysenko G.V. Features of the management of patients with community-acquired pneumonia in the Republic of Tatarstan. Farmateka. 2014;15(288):31–34 (in Russ.)].
5. Кузьменков А.Ю., Трушин И.В., Авраменко А.А. и др. AMRmap: Интернет-платформа мониторинга антибиотикорезистентности. Клиническая микробиология и антимикробная химиотерапия. 2017;19(2):84–90. [Kuzmenkov A. Yu., Trushin I.V., Avramenko A.A., et al. AMRmap: Internet platform for monitoring antibiotic resistance. Clinical Microbiology and Antimicrobial Chemotherapy. 2017; 19 (2): 84–90. (in Russ.)].
6. Chambers H. Other beta-lactam antibiotics. In: Mandell G.L., Bennet J.E., Dolin R., editors. Principles and Practice of Infectious Diseases. Churchill Livingstone, 6th edition, 2004.
7. Bush K. Other b-lactam antibiotics. In: Finch R.G., Greenwood D., Norrby S.R., Whitley R.J., editors. Antibiotic and Chemotherapy. Anti-infective agent and their use in therapy. Churchill Livingstone, 8th edition. 2003.
8. Neu H.C., Wilson A.P.R., Gruneberg RN. Amoxycillin/clavulanic acid: a review of its efficacy in over 38,500 patients from 1979 to 1992. J Chemother. 1993;5:67–93.
9. Pérez-Deago B., Alonso-Porcel C., Elvira-Menendez C. et al. Epidemiology and management of community acquired pneumonia: more than 10 years experience. Semergen. 2018;44(6):389–394. DOI: 10.1016/j.semerg.2018.01.008.
10. Умирова А.А., Кабакова Т.И., Аджиенко В.Л. Оценка врачебных предпочтений при выборе лекарственных препаратов для лечения внебольничной пневмонии на примере Кабардино-Балкарской Республики. Современные проблемы науки и образования. 2015;2(2):514. [Umirova A.A., Kabakova T.I., Adzhienko V.L. Evaluation of medical preferences when choosing drugs for the treatment of community-acquired pneumonia on the example of the Kabardino-Balkarian Republic. Modern problems of science and education. 2015;2(2):514 (in Russ.)].
11. Волкова Ю.С., Слободенюк Е.В. Антимикробные препараты для системного применения на фармацевтическом рынке г. Хабаровска: фармакоэкономический анализ. Тихоокеанский медицинский журнал. 2014;2(56):35–37. [Volkova Yu.S., Slobodenyuk E.V. Antimicrobial drugs for systemic use in the pharmaceutical market in Khabarovsk: pharmacoeconomic analysis. Pacific Medical Journal. 2014;2(56):35–37 (in Russ.)].
12. Клинические рекомендации (проект). Внебольничная пневмония. РРО. МАКМАХ. (Электронный ресурс). URL: http://spulmo.ru/obrazovatelnye-resursy/federalnye-klinicheskie-rekomendatsii/. Дата обращения: 25.07.2019 [Clinical recommendations (draft). Community-acquired pneumonia. RRO. MAX. (Electronic resource). URL: http://spulmo.ru/obrazovatelnye-resursy/federalnye-klinicheskie-rekomendatsii/. Access date: 25.07.2019 (in Russ.)].
13. Синопальников А.И. Антибиотики и внебольничные инфекции нижних дыхательных путей. Кому? Какой? Фарматека. 2019;5:47–60. [Sinopalnikov A.I. Antibiotics and community-acquired infections of the lower respiratory tract. To whom? Which one? Farmateka. 2019;5:47–60 (in Russ.)].
14. Ленкова Н.И., Евдокимова С.А., Демченкова Е.Ю. Амоксиклав при лечении бронхолегочных инфекций. РМЖ. 2005;5:264–266 [Lenkova N.I., Evdokimova S.A., Demchenkova E. Yu. Amoxiclav in the treatment of bronchopulmonary infections. RMJ. 2005;5:264–266 (in Russ.)].
15. Viasus D., Simonetti A.F., Garcia-Vidal C. et al. Impact of antibiotic de-escalation on clinical outcomes in community-acquired pneumococcal pneumonia. J. Antimicrob. Chemother. 2017;72(2):547–553. DOI: 10.1093/jac/dkw441.
16. Kouakou-Siransy G., Horo K., Effo E. et al. Pharmacotherapeutic aspect of antibiotic therapy during acute community-acquired pneumonia in adults at the University Hospital of Cocody (Abidjan). Int. J. Clin. Pharmacol. Ther. 2015;53(11):940–946. DOI: 10.5414/CP202349.
17. Razazi K., Mekontso Dessap A., Carteaux G. et al. Frequency, associated factors and outcome of multi-drug-resistant intensive care unit-acquired pneumonia among patients colonized with extended-spectrum β-lactamase-producing Enterobacteriaceae. Ann. Intensive Care. 2017;7(1):61. DOI: 10.1186/s13613-017-283-284.
18. Steurer J. Positive effect of amoxicillin/clavulanic acid for exacerbations of mild to moderate COPD. Praxis (Bern 1994). 2013;102(5):301–302. DOI: 10.1024/1661-8157/a001195.
19. Brusse-Keizer M., VanderValk P., Hendrix R. et al. Necessity of amoxicillin clavulanic acid in addition to prednisolone in mild-to-moderate COPD exacerbations. BMJ Open Respir Res. 2014;1(1): e000052. DOI: 10.1136/bmjresp-2014-000052.
20. Brusse-Keizer M., VanderValk P., van der Zanden R.W. et al. Amoxicillin concentrations in relation to beta-lactamase activity in sputum during exacerbations of chronic obstructive pulmonary disease. Int. J. Chron. Obstruct. Pulmon. Dis. 2015;10:455–461. DOI: 10.2147/COPD.S70355.
21. Nijdam L.C., Assink M.D., Kuijvenhoven J.C. et al. Safety and tolerability of nebulized amoxicillin-clavulanic acid in patients with COPD (STONAC 1 and STONAC 2). COPD. 2016;13(4):448–454. DOI: 10.3109/15412555.2015.1107893.
22. Хроническая обструктивная болезнь легких. РРО. (Электронный ресурс). URL: http://spulmo.ru/upload/federal_klinicheskie_rekomendaciy_hobl.pdf. Дата обращения: 20.07.2019. [Chronic obstructive pulmonary disease. RRO. (Electronic resource). URL: http://spulmo.ru/upload/federal_klinicheskie_rekomendaciy_hobl.pdf. Access date: 07.25.2019 (in Russ.)].

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
