Особенности использования экстрактов Serenoa repens при долговременной терапии доброкачественной гиперплазии предстательной железы
DOI: 10.32364/2587-6821-2020-4-2-122-127
Статья посвящена механизмам действия и клинической эффективности гексановых экстрактов плодов Serenoa repens в лечении и профилактике развития доброкачественной гиперплазии предстательной железы (ДГПЖ), назначаемых в течение длительного времени, — т. е. тем аспектам терапии ДГПЖ, включая профилактику, которые остаются дискутабельными. Феномен нонреспондеров, которые не отвечают на проводимую терапию или отказываются от нее, также остается открытым. Описаны наиболее часто встречающиеся ярко выраженные побочные эффекты и остальные факторы, являющиеся причиной отказа пациентов от назначаемой терапии. Упомянуты основные патогенетические механизмы ДГПЖ. Подробно рассмотрены факторы прогрессии ДГПЖ и возможности действия гексановых экстрактов плодов S. repens на симптомы нижних мочевыводящих путей (СНМП). Наиболее ярко выраженные эффекты наблюдаются у препаратов, содержащих наибольшую концентрацию жирных кислот, каковым является препарат Пермиксон. Проведена оценка основных клинических плацебо-контролируемых исследований препарата Пермиксон, и показана его эффективность в контроле СНМП и прогрессии ДГПЖ у пациентов с невыраженной симптоматикой ДГПЖ, на начальных стадиях аденомы, при неярких проявлениях заболевания, при появлении признаков сопутствующего простатита, а также у лиц, считающих обязательным сохранение половой функции.
Ключевые слова: симптомы нижних мочевых путей, доброкачественная гиперплазия предстательной железы, гексановый экстракт плодов Serenoa repens, Пермиксон.
Для цитирования: Охоботов Д.А., Козлова П.С. Особенности использования экстрактов Serenoa repens при долговременной терапии доброкачественной гиперплазии предстательной железы. РМЖ. Медицинское обозрение. 2020;4(2):122-127. DOI: 10.32364/2587-6821-2020-4-2-122-127.
Введение
При назначении терапии аденомы предстательной железы (ПЖ) у пациентов с симптомами нижних мочевыводящих путей (СНМП) на фоне доброкачественной гиперплазии предстательной железы (ДГПЖ) выделяются несколько краткосрочных и долгосрочных целей. К краткосрочным относятся устранение СНМП, улучшение скорости мочеиспускания, а также улучшение качества жизни. Долгосрочными целями являются стойкое улучшение симптоматики, профилактика прогрессирования заболевания, поддержание достигнутой скорости мочеиспускания, уменьшение объема ПЖ и, конечно же, снижение риска возникновения острой задержки мочи и необходимости оперативного вмешательства [1, 2].
Разработанные схемы консервативного лечения ДГПЖ достаточно хорошо изучены, возможные побочные эффекты проанализированы, тем не менее некоторые аспекты терапии, например профилактика, остаются дискутабельными. Феномен нон-респондеров, которые не отвечают на проводимую терапию или отказываются от нее, также остается открытым. Чаще всего эти пациенты прекращают принимать препараты ввиду ярко выраженных побочных эффектов, недостаточной эффективности, а также невозможности применения данных групп препаратов из-за их приема по поводу других сопутствующих заболеваний. Наиболее часто возникновение побочных эффектов связано с действием α-адреноблокаторов, особенно у пациентов с отягощенным соматическим статусом. Так, например, при лечении гипертонической болезни тамсулозин усиливает эффект гипотензивной терапии и провоцирует ортостатические коллапсы. В сочетании комплексной терапии с ингибиторами фосфодиэстеразы также возможно возникновение ортостатической гипотензии. Известным побочным действием α-адреноблокаторов является нарушение сексуальной функции в виде ретроградной эякуляции, что вносит существенный дискомфорт в жизнь многих пациентов [3]. Нежелательные эффекты свойственны и второй, наиболее известной группе препаратов — ингибиторам 5α-редуктазы, которые чаще всего влияют на сексуальную функцию, снижая либидо, вызывая эректильную дисфункцию (ЭД) и, реже, нарушения эякуляции или уменьшение объема спермы [4–6].
Патогенетические механизмы ДГПЖ
На данный момент существует несколько теорий патогенеза ДГПЖ: увеличение активности фермента 5α-редуктазы [7, 8]; дефицит тестостерона и дисбаланс соотношения «тестостерон/эстрогены» [9]; влияние гормонов и факторов роста, усиливающие пролиферацию клеток, в частности инсулина и инсулиноподобного фактора роста [10–13]; хроническое нарушение кровоснабжения ПЖ [14]; дефицит витамина D и нарушение его антипролиферативной регуляции апоптоза и ангиогенеза [15]; нарушенный уровень гормонов щитовидной железы [16]; мужской гипогонадизм [17, 18].
Процесс инициации и прогрессии пролиферативной активности ткани ПЖ может сильно усугубляться под действием некоторых сопутствующих заболеваний, таких как ожирение, инсулинорезистентность, сахарный диабет 2 типа, метаболический синдром [19].
Cопутствующие ДГПЖ ирритативные нарушения мочеиспускания связывают с андрогенным дефицитом и хронической ишемией тазовых органов [20].
Воздействие на различные звенья патогенеза составляет основу успешной медикаментозной терапии. Важной задачей профилактической терапии ДГПЖ являются предотвращение прогрессии роста аденомы, развития острой задержки мочи и воспалительных изменений в ПЖ. Выделяют несколько маркеров риска прогрессии ДГПЖ: возраст старше 50 лет, тяжесть СНМП, снижение скорости мочеиспускания (Qmax), объем ПЖ (>30 мл), уровень простат-специфического антигена (ПСА) >1,5 нг/мл. К возникновению СНМП приводят несколько патофизиологических факторов: трофический, гормональный, рецепторный, сосудистый, иммунный, воспалительный, уродинамический, а также фактор повышенной активности вегетативной нервной системы [21–23].
Говоря о трофическом факторе прогрессии, считают, что при обнаружении пролиферативных центров I, II, III стадии пролиферативной активности консервативная терапия ингибиторами 5α-редуктазы будет эффективна, т. к. сохраняется субстрат для действия этой группы препарата, но при этом высок риск рецидива после трансуретральной резекции, а при выявлении IV и V стадии следует отдать предпочтение оперативному вмешательству, т. к. при нем расширяется просвет уретры и резецируется большое количество перерастянутых атрофичных ацинусов в сохраняемой части железы [24].
Немаловажным фактором прогрессирования ДГПЖ является постоянное активное влияние андрогенов на ее функциональную ткань. Постоянная стимуляция андрогеновых рецепторов при прогрессии ДГПЖ необходима для роста и функции ткани ПЖ, путем трансактивации домена, который закодирован в первом экзоне гена АР (Xq 11–12) [25–27]. При исследовании полиморфизма генов, кодирующих 5α-редуктазу 2 типа (SRD 5A1 и SRD 5 A2), было установлено, что имеется тесная взаимосвязь между выраженностью полиморфизма генов, объемом ДГПЖ, эффективностью проводимой антиандрогенной терапии и концентрацией половых гормонов и их метаболитов [28, 29]. Известно, что α1-адренорецепторы непосредственно принимают участие в процессе действия внутриклеточных эффекторов, которые влияют на объем и тонус гладкомышечных элементов ПЖ, что объясняет явный результат их активации [30].
Особенностью иммунных факторов прогрессии заболевания является то, что они формируют порочный круг. Происходит активация иммунных клеток, которые продуцируют и выбрасывают в кровь провоспалительные цитокины, что приводит к увеличению воспалительных клеток. Воспалительная реакция ведет к повреждению эпителиальных и стромальных клеток, а затем к их пролиферации и чрезмерному производству внеклеточного матрикса, результатом которого становится запуск аутоиммунных процессов. Клинически это проявляется кальцификацией с обструкцией ацинусов, что помогает в диагностике при подозрении на воспаление ПЖ [31].
Терапия ДГПЖ
При ДГПЖ без ЭД наиболее эффективным вариантом лечения является комбинация α1-адреноблокатора и ингибитора 5α-редуктазы. При ДГПЖ с ЭД двух- и трехкомпонентная комбинация с включением ингибитора фосфодиэстеразы-5 обеспечивает существенное улучшение эректильной функции и СНМП, обусловленных ДГПЖ. Показано, что многокомпонентные схемы терапии не сопровождаются значимым увеличением частоты побочных реакций [32].
Среди средств, используемых для лечения ДГПЖ, препараты растительного происхождения занимают особое место. В наши дни активно исследуются средства на основе растительных экстрактов, которые считаются более щадящими и безопасными для применения у некоторых групп пациентов, вынужденных получать консервативную терапию в течение длительного времени. Наиболее известными такими препаратами являются экстракты Cucurbita pepo (семена тыквы), Hypoxis rooperi (южноафриканская звездная трава), Pygeum africanum (кора африканской сливы), Secale cereale (ржаная пыльца) и Serenoa repens (вееролистная пальма). Из вышеупомянутых растительных препаратов гексановый экстракт
S. repens оценивают как лекарственный препарат с признанной эффективностью и безопасностью [33].
Выделяют несколько возможных механизмов действия гексановых экстрактов S. repens, которые могут обусловливать применение данных лекарственных средств в лечении ДГПЖ. Они ингибируют синтез простагландинов в ПЖ; снижают секрецию глобулина, связывающего половой гормон в печени; обладают цитотоксическим влиянием на клетки ПЖ; оказывают блокирующее действие на андрогеновые рецепторы; ингибируют пролиферацию простатического эпителия, индуцированного факторами роста, а также уменьшают активность 5α-редуктазы [34]. Считается, что гексановые экстракты S. repens ингибируют синтез простагландинов и лейкотриенов за счет блокады каскада арахидоновой кислоты, снижают экспрессию различных генов, участвующих в воспалительном процессе, стимулируют экспрессию противовоспалительных факторов, уменьшают количество иммунных клеток (B-лимфоцитов и т. д.) и концентрацию интерлейкина1β, фактора некроза опухоли α. Гексановые экстракты S. repens оказывают действие не только на активность 5α-редуктазы, но и на различные фазы метаболизма андрогенов и тормозят связывание дигидротестостерона с андрогеновыми рецепторами, что объясняет его антиэстрогенный эффект, который, кроме того, еще обусловлен уменьшением количества эстрогеновых рецепторов в ПЖ и снижением стимуляции пролактином гиперпластических процессов [35].
Экстракт S. repens обладает свойствами блокатора α1-адренорецептора. Антихолинергические средства широко используются для лечения гиперактивного мочевого пузыря; следовательно, ингибирование мускариновых рецепторов может быть новым фармакологическим действием экстрактов на нижние мочевые пути для облегчения раздражающих и обструктивных симптомов дизурии при ДГПЖ и СНМП [36].
Клиническая эффективность препаратов S. repens базируется на процентном содержании свободных жирных кислот. Препаратом, содержащим наибольшее количество свободных жирных кислот, является гексановый экстракт
S. repens — Пермиксон («Пьер Фабр Медикамент Продакшн», Франция) (табл. 1) [37].
![Таблица 1. Эквивалентное содержание свободных жирных кислот в препаратах S. repens [37] Table 1. Equivalent content of free fatty acids in the agents with S. repens extracts [37] Таблица 1. Эквивалентное содержание свободных жирных кислот в препаратах S. repens [37] Table 1. Equivalent content of free fatty acids in the agents with S. repens extracts [37]](/upload/medialibrary/db8/122-1.png)
При этом доказана селективность его действия на клетки ПЖ [38]. Эксперимент in vivo показал, что Пермиксон является эффективным двойным ингибитором активности изофермента 5α-редуктазы в ПЖ. В отличие от других ингибиторов 5α-редуктазы Пермиксон индуцирует этот эффект, не оказывая влияния на способность клеток секретировать сывороточный ПСА, что позволяет продолжать использовать этот лабораторный показатель для онкоскрининга [39].
Опыты in vitro продемонстрировали, что почти все гены, связанные с воспалением, были экспрессированы на изначальном уровне в культивируемых клетках in vitro и первичных культурах (интерлейкин 6, CCL-5, CCL-2, циклооксигеназа 2 и индуцируемая NO-синтаза), а затем подавлены воздействием препарата Пермиксон, что подтверждает важное для клиницистов противовоспалительное действие [40, 41].
Было проведено большое количество краткосрочных и долговременных клинических исследований, изучавших точки действия препарата Пермиксон на разные элементы патогенеза ДГПЖ. В одном из долговременных клинических испытаний было задействовано 97 пациентов, которым проводили терапию препаратом Пермиксон (320 мг/день) или плацебо в течение 6 мес. В ходе исследования было показано, что в основной группе средняя выраженность воспаления и агрессивности достоверно снизилась с 1,55 на исходном уровне соответственно до 0,79 (р=0,001) и 0,87 (р=0,001) при последующей биопсии. В контрольной группе в среднем воспаление оценивалось в 1,44 балла при первой биопсии и 1,23 балла — при второй. Средняя оценка агрессивности составила 1,09 и 0,89 соответственно. Статистическая значимость не была обнаружена (р=0,09 и р=0,74). Среднее снижение всех показателей воспаления было статистически выше у пациентов, принимающих Пермиксон, по сравнению с контрольной группой. Иммуногистохимическое окрашивание показало значительное изменение экспрессии исследуемых антител у пациентов, которым проводили терапию препаратом Пермиксон, по сравнению с первой биопсией. В группе плацебо при второй биопсии не было обнаружено существенных
отличий [42].
В другом наблюдении, в ходе полугодового двойного слепого рандомизированного исследования эквивалентности, сравнивали эффект препарата Пермиксон
(320 м/день) с эффектом ингибитора 5α-редуктазы (финастерид, 5 мг/день) у 1098 мужчин с умеренной ДГПЖ с использованием шкалы IPSS (International Prostate Symptom Score — Международная шкала оценки простатических симптомов) в качестве основного оценочного критерия. Оба препарата снизили показатель IPSS (-37% и -39% соответственно), субъективно улучшили качество жизни (на 38 и 41%) и увеличили пиковую скорость потока мочи (+25% и +30%; р=0,035). Финастерид заметно уменьшил объем ПЖ (-18%) и уровень ПСА в сыворотке (-41%); а Пермиксон улучшил симптомы с небольшим влиянием на объем (-6%) и без изменений уровня ПСА. В отношении препарата Пермиксон не было зафиксировано выраженных побочных эффектов [43].
Целью двойного слепого рандомизированного исследования F. Debruyne (2002) было оценить эквивалентную эффективность тамсулозина и препарата Пермиксон (n=704, IPSS>10) в течение года. При этом показатели анкет IPSS, QoL (Quality of Life — качество жизни) и Qmax при урофлоуметрии оценивали на исходном уровне и в течение 1 года. Объем ПЖ и ПСА измеряли в начале и в конце терапии. Анализ полученных результатов был выполнен для 542 пациентов (тамсулозин: n=273; Пермиксон: n=269). Через 12 мес. IPSS снизился на 4,4 балла в каждой группе, и никаких различий не наблюдалось ни в улучшении раздражающих, ни в улучшении обструктивных симптомов. Увеличение Qmax было одинаковым в обеих группах лечения (тамсулозин: +1,9 мл/с; Пермиксон: +1,8 мл/с). ПСА оставался стабильным, в то время как объем ПЖ немного уменьшился у пациентов, получавших Пермиксон. Это исследование продемонстрировало, что Пермиксон и тамсулозин эквивалентны при лечении СНМП у мужчин с ДГПЖ при долговременной терапии в течение года [44].
Подобное исследование (n=124, IPSS≥10) (2004) подтвердило эквивалентную эффективность препарата Пермиксон и тамсулозина. Через 12 мес. общий IPSS снизился на 7,8 у пациентов, принимавших Пермиксон, и на 5,8 (р=0,051) у принимавших тамсулозин; симптомы раздражения значительно улучшились (р=0,049): -2,9 против -1,9 с в пользу препарата Пермиксон уже через 3 мес., и эффект сохранялся до конца исследования (p=0,03) [45].
Долгосрочное исследование Y.A. Pytel et al. (2002) оценивало эффективность и переносимость препарата Пермиксон (320 мг/день) в течение 2 лет (n=155). В сроки 6, 12, 18 и 24 мес. оценивались состояние по шкале IPSS, качество жизни и половая функция, а также уродинамические и биологические показатели. IPSS и качество жизни значительно улучшались с каждым разом по сравнению с исходным уровнем. В конце лечения было отмечено значительное улучшение Qmax по сравнению с началом исследования. Размер ПЖ уменьшился. Сексуальная функция оставалась стабильной в течение первого года лечения и значительно улучшилась (р=0,001) в течение второго года. Уровень ПСА не менялся. Улучшение показателей эффективности началось через 6 мес. и сохранялось до 24 мес. Эти данные демонстрируют долгосрочную эффективность и переносимость препарата Пермиксон и подтверждают целесообразность его использования при неосложненной симптоматической ДГПЖ (табл. 2) [46].
Заключение
Подводя итоги множества проведенных исследований, следует упомянуть о метаанализе Vela-Navarrete, проведенном в 2018 г. и содержащем подробный обзор рандомизированных контролируемых исследований, в которых сообщается об эффективности и безопасности препарата Пермиксон. Анализ опирается на 27 исследований (с общим числом пациентов 5800), при этом 15 из них были клиническими рандомизированными и 12 — обсервационными. Основными критериями, представлявшими интерес, были СНМП. По результатам, представленным в данном обзоре, Пермиксон оказался значительно эффективнее, чем плацебо, для уменьшения проявления никтурии (взвешенная разность средних (ВРС) 0,64; 95% доверительный интервал (ДИ) -0,98– -0,31; p<0,001). По данным опросника IPSS, эффективность препарата Пермиксон была сопоставима с эффективностью тамсулозина (ВРС 0,57; 95% ДИ -0,27–1,42; p=0,18) и финастерида (ВРС 0,46; 95% ДИ -0,41–1,34; p=0,3). Отмечено увеличение Qmax, причем показатели урофлоуметрии указывают на бóльшую эффективность гексанового экстракта S. repens, чем плацебо (ВРС 2,75; 95% ДИ 0,57–4,93; p=0,01). Отмечен также сопоставимый эффект Пермиксона с тамсулозином (ВРС -0,02; 95% ДИ -0,71–0,66; p=0,95). При этом наблюдалось уменьшение объема ПЖ [47].
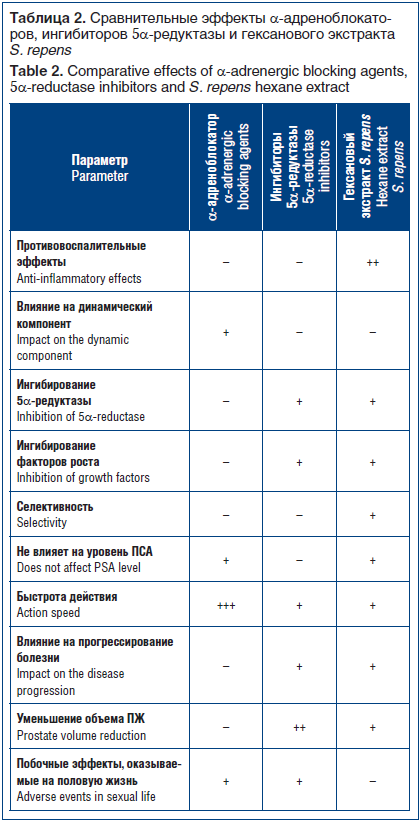
Сравнительные эффекты α-адреноблокаторов, ингибиторов 5α-редуктазы и гексанового экстракта S. repens указаны в таблице 2. Таким образом, α-адреноблокаторы наиболее быстро действуют на уменьшение СНМП, т. е. активно влияют на динамический компонент, а также начинают действовать быстрее других препаратов. Ингибиторы 5α-редуктазы наиболее выраженно уменьшают объем ПЖ. Гексановый экстракт S. repens, в отличие от α-адреноблокаторов и ингибиторов 5α-редуктазы, обладает выраженным противовоспалительным эффектом, селективностью, не влияет на уровень ПСА (как и α-адреноблокаторы), уменьшает прогрессирование ДГПЖ (в одинаковой степени с ингибиторами 5α-редуктазы), объем ПЖ (в меньшей степени, чем ингибиторы 5α-редуктазы) [48],
а также, и это является его большим преимуществом, не вызывает нарушений сексуальной функции мужчин, которые наблюдаются при применении других групп лекарственных средств.
Следовательно, препараты экстракта S. repens целесообразно применять у больных с невыраженной симптоматикой ДГПЖ, на начальных стадиях аденомы, при неярких проявлениях заболевания, при появлении признаков сопутствующего простатита, а также у лиц, считающих обязательным сохранение половой функции. Главной целью долговременной терапии данным препаратом является предотвращение возникновения осложнений, таких как острая задержка мочи и обострение хронического простатита.
Благодарность
Авторы и редакция благодарят компанию «Пьер Фабр Медикамент» за предоставление полных текстов иностранных статей, необходимых для подготовки данной публикации.
Acknowledgement
The authors and Editorial Board are grateful to Pierre Fabre Medication for providing full-text foreign articles required to write the review.
Сведения об авторах:
1,2Охоботов Дмитрий Александрович — к.м.н., врач-уролог, андролог, репродуктолог, старший преподаватель, заведующий учебной частью кафедры урологии и андрологии, факультет фундаментальной медицины, ORCID iD 0000-0002-6768-9004;
1Козлова Полина Сергеевна — студентка 5-го курса факультета фундаментальной медицины, ORCID iD 0000-0001-5346-3285.
1МГУ имени М.В. Ломоносова. 119991, Россия, г. Москва, Ленинские горы, д. 1.
2МНОЦ МГУ имени М.В. Ломоносова. 119192, Россия, г. Москва, Ломоносовский просп., д. 27, корп. 10.
Контактная информация: Охоботов Дмитрий Александрович, e-mail: 14072003m@gmail.com. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 20.11.2019.
About the authors:
1,2Dmitriy A. Okhobotov — MD, PhD, urologist, andrologist, reproductive endocrinologist, Senior Lecturer, Head of the Department of Urology and Andrology, Faculty of Fundamental Medicine, ORCID iD 0000-0002-6768-9004;
1Polina S. Kozlova — 5 year student of Faculty of Fundamental Medicine, ORCID iD 0000-0001-5346-3285.
1Lomonosov Moscow State University. 1, Leninskiye gory, Moscow, 119991, Russian Federation.
2Moscow Research and Education Center of the Lomonosov Moscow State University. 27/10, Lomonosovskiy prosp., Moscow, 119192, Russian Federation.
Contact information: Dmitriy A. Okhobotov, e-mail: 14072003m@gmail.com. Financial Disclosure: no author has a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 20.11.2019.
2. McVary K.T. A review of combination therapy in patients with benign prostatic hyperplasia. Clin Ther. 2007;29(3):387–398. DOI: 10.1016/S0149-2918(07)80077-4.
3. Van Dijk M.M., de la Rosette J.J., Michel M.C. Effects of alpha — adrenoceptor antagonists on male sexual function. Drugs, 2006;66:287–301. DOI: 10.2165/00003495–200666030–00002.
4. McConnell J.D., Roehrborn C.G., Bautista O.M. et al. The long-term effect of doxazosin, finasteride, and combination therapy on the clinical progression of benign prostatic hyperplasia. N Engl J Med. 2003;349: 2387–2398. DOI: 10.1056/NEJMoa030656.
5. Roehrborn C.G. Siami P., Barkin J. et al. The effects of dutasteride, tamsulosin and combination therapy on lower urinary tract symptoms in men with benign prostatic hyperplasia and prostatic enlargement: 2-year results from the CombAT study. J Urol. 2008;179:616–616. DOI: 10.1016/j.juro.2007.09.084.
6. Roehrborn C.G., Siami P., Barkin J. et al. The effects of combination therapy with dutasteride and tamsulosin on clinical outcomes in men with symptomatic benign prostatic hyperplasia: 4-year results from the CombAT study. Eur Urol. 2010;57:123–131. DOI: 10.1016/j.eururo.2009.09.035.
7. Van der Sluis T.M., Vis A.N., van Moorstelaar R.J. et al. Intraprostatic testosterone and dihydrotestosterone. Part. 1: concentrations and methods of determination in men with benign prostatic hyperplasia and prostate cancer. BJU Int. 2012;109(2):176–182. DOI: 10.1111/j.1464-410X.2011.10651.x.
8. Shidaifat F., Lin Y.C. Testosterone effect on the expression of genes that mediate testosterone metabolism and genes that mediate the effect of those metabolites on the prostate. Life Sci. 2012;91(5–6):194–198. DOI: 10.1016/j.lfs.2012.07.012.
9. Тюзиков И.А., Братчиков О.И., Михайлов Д.В. и др. Роль возрастного андрогенного дефицита в патогенезе аденомы предстательной железы. Тихоокеанский медицинский журнал. 2016;1:14–18. [Tyuzikov I.A., Bratchikov O.I., Mikhailov D.V. et al. The role of age-related androgen deficiency in the pathogenesis of prostate adenoma. Tikhookeanskiĭ meditsinskiĭ zhurnal. 2016;1:14–18 (in Russ.)].
10. Vikram A., Jena G. Role of insulin and testosterone in prostatic growth: who is doing what? Med Hypotheses. 2011;76(4):474–478. DOI: 10.1016/j.mehy.2010.11.024.
11. Hammarsten J., Peeker R. Urological aspects of the metabolic syndrome. Nat Rev Urol. 2011;8(9):483–494. DOI: 10.1038/nrurol.2011.112.
12. Wang Z., Olumi A.F. Diabetes, growth hormone-insulin-like growth factor pathways and association to benign prostatic hyperplasia. Differentiation. 2011;82(4–5):261–271. DOI: 10.1016/j.diff.2011.04.004.
13. Gacci M., Corona G., Vignozzi L. et al. Metabolic syndrome and benign prostatic enlargement: a systematic review and meta‐analysis. BJU Int. 2015;115(1):24–31. DOI: 10.1111/bju.12728.
14. Berger A.P., Horninger W., Bektic J. et al. Vascular resistance in the prostate evaluated by colour Doppler ultrasonography: is benign prostatic hyperplasia a vascular disease? BJU Int. 2006;98(3):587–590. DOI: 10.1111/j.1464-410X.2006.06306.x.
15. Espinosa G., Esposito R., Kazzazi A., Djavan B. Vitamin D and benign prostatic hyperplasia — a review. Can J Urol. 2013;20(4):6820–6825. PMID: 23930605.
16. Eldhose A., Nandeesha H., Dorairajan L.N. et al. Thyroid and parathyroid hormones in benign prostatic hyperplasia. Br J Biomed Sci. 2016;73(2):94–96. DOI: 10.1080/09674845.2016.1173333.
17. Yassin A., Nettleship J.E., Talib R.A. et al. Effects of testosterone replacement therapy withdrawal and re-treatment in hypogonadal elderly men upon obesity, voiding function and prostate safety parameters. Aging Male. 2016;19(1):64–69. DOI: 10.3109/13685538.2015.1126573.
18. Moore A., Butcher M.J., Köhler T.S. Testosterone replacement therapy on the natural history of prostate disease. Curr. Urol. Rep. 2015;16(8): ID 51. DOI: 10.1007/s11934-015-0526-6.
19. Hammarsten J., Peeker R. Urological aspects of the metabolic syndrome. Nat Rev Urol. 2011;8(9):483–494. DOI: 10.1038/nrurol.2011.112.
20. Кирпатовский В.И., Мудрая И.С., Мкртчян К.Г. и др. Андрогены и хроническая ишемия — два независимых патогенетических фактора развития ДГПЖ. Экспериментальная и клиническая урология. 2014;2:20–26. [Kirpatovsky V.I., Wise I.S., Mkrtchyan K.G. et al. Androgens and chronic ischemia are two independent pathogenetic factors for the development of BPH. Eksperimental’naya i klinicheskaya urologiya. 2014;2:20–26 (in Russ.)].
21. McConnell J.D., Roehrborn C.G., Bautista O.M. et al. The long-term effect of doxazosin, finasteride, and combination therapy on the clinical progression of benign prostatic hyperplasia. N Engl J Med. 2003;349(25):2387–2398. DOI: 10.1056/NEJMoa030656
22. Djavan B., Waldert M., Ghawidel C., Marberger M. Benign prostatic hyperplasia progression and its impact on treatment. Curr Opin Urol. 2004;44:45–50. DOI: 10.1097/00042307-200401000-00010.
23. Emberton M., Fitzpatrick J.M., Rees J. Risk stratification for benign prostatic hyperplasia (BPH) treatment. BJU Int. 2011;107:876–880. DOI: 10.1111/j.1464-410X.2010.10041.x.
24. Кудрявцев Ю.В., Сивков А.В. Морфологические изменения в ткани предстательной железы при доброкачественной гиперплазии. Экспериментальная и клиническая урология. 2010;(1):18–22. [Kudryavtsev Yu.V., Sivkov A.V. Morphological changes in prostate tissue with benign hyperplasia. Eksperimental’naya i klinicheskaya urologiya. 2010;(1):18–22 (in Russ.)].
25. Konwar R., Chattopadhyay N., Bid H.K. Genetic polymorphism and pathogenesis of benign prostatic hyperplasia. BJU Int. 2008;102:536–544. DOI: 10.1111/j.1464-410X.2008.07667.x.
26. Zeegers M.P., Kiemeney L.A., Nieder A.M., Ostrer H. How strong is the association between CAG and GGN repeat length polymorphisms in the androgen receptor gene and prostate cancer risk? Cancer Epidemiol Biomarkers Prev. 2004;13:1765–1771.
27. Kramer G., Steiner G.E., Handisurya A. et al. Increased expression of lymphocyte-derived cytokines in benign hyperplastic prostate tissue, identification of the producing cell types, and effect of differentially expressed cytokines on stromal cell proliferation. Prostate. 2002;52(1):43–58. DOI: 10.1002/pros.10084.
28. Gu X., Na R., Huang T. et al. SRD5A1 and SRD5A2 are associated with treatment for benign prostatic hyperplasia with the combination of 5α-reductase inhibitors and α-adrenergic receptor antagonists. J Urol 2013;190(2):615–619. DOI: 10.1016/j.juro.2013.03.024.
29. Rył A., Rotter I., Grzywacz A. et al. Molecular Analysis of the SRD5A1 and SRD5A2 Genes in Patients with Benign Prostatic Hyperplasia with Regard to Metabolic Parameters and Selected Hormone Levels. Int J Environ Res Public Health. 2017;14(11):1318–1322. DOI: 10.3390/ijerph14111318.
30. Hennenberg M., Stief C.G., Gratzke C. Prostatic α1-adrenoceptors: new concepts of function, regulation, and intracellular signaling. Neurourol Urodyn. 2014;33(7):1074–1085. DOI: 10.1002/nau.22467.
31. Ficarra V. Is chronic prostatic inflammation a new target in the medical therapy of lower urinary tract symptoms (LUTS) due to benign prostate hyperplasia (BPH)? BJU Int. 2013;112(4):421–422. DOI: 10.1111/bju.12177.
32. Камалов А.А., Тахирзаде А.М. Подходы к медикаментозному лечению пациентов с высоким риском прогрессирования доброкачественной гиперплазией предстательной железы в зависимости от сопутствующей эректильной дисфункции. Урология. 2018;3:70–77. DOI: 10.18565/urology.2018.3.70-77. [Kamalov A.A., Tahirzade A.M. Approaches to medical treatment of patients with a high risk of progression of benign prostatic hyperplasia depending on concomitant erectile dysfunction. Urologiya. 2018;3:70–77 (in Russ.)]. DOI: 10.18565/urology.2018.3.70-77.
33. Bartram W. European Union herbal monograph on Serenoa repens. European Medicines Agency; 2016.
34. Oelke M., Bachmann A., Descazeaud A. et al. EAU guidelines on the management of male lower urinary tract symptoms, including benign prostatic obstruction. EAU guidelines; 2013.
35. De la Taille A. Therapeutic Approach: The Importance of Controlling Prostatic Inflammation. European Urology Supplements. 2013;12:116–122. DOI: 10.1016/j.eursup.2013.08.003.
36. Suzuki M., Ito Y., Fujino T. et al. Pharmacological effects of saw palmetto extract in the lower urinary tract. Acta Pharmacol Sin. 2009;30(3):271–281. DOI: 10.1038/aps.2009.1.
37. Scaglione F. How to Choose the Right Serenoa repens Extract. European Urology Supplements. 2015;14(9): e1464–e1469. DOI: 10.1016/S1569-9056 (15) 30501-7.
38. Bayne C.W., Ross M., Donnelly F., Habib F.K. The selectivity and specificity of the actions of the lipido-sterolic extract of Serenoa repens (Permixon) on the prostate. J Urol. 2000;164(3 Pt 1):876–881. DOI: 10.1016/S0022-5347(05)67330-2.
39. Bayne C.W., Donnelly F., Ross M., Habib F.K. Serenoa repens (Permixon): a 5alpha-reductase types I and II inhibitor-new evidence in a coculture model of BPH. Prostate. 1999;40(4):232–241. DOI: 10.1002/(SICI)1097-0045(19990901)40:4<232::AID-PROS4>3.0.CO;2-0.
40. Silvestri I., Cattarino S., Aglianò A. et al. Effect of Serenoa repens (Permixon®) on the expression of inflammation-related genes: analysis in primary cell cultures of human prostate carcinoma. J Inflamm (Lond). 2013;10:11. DOI: 10.1186/1476-9255-10-11.
41. Bernichtein S., Pigat N., Camparo P. et al. Anti-inflammatory properties of Lipidosterolic extract of Serenoa repens (Permixon®) in a mouse model of prostate hyperplasia. Prostate. 2015;75(7):706–722. DOI: 10.1002/pros.22953.
42. Gravas S., Samarinas M., Zacharouli K. et al. The effect of hexanic extract of Serenoa repens on prostatic inflammation: results from a randomized biopsy study. World J Urol. 2019 Mar;37 (3):539–544. DOI: 10.1007/s00345-018-2409-1.
43. Carraro J.C., Raynaud J.P., Koch G. et al. Comparison of phytotherapy (Permixon) with finasteride in the treatment of benign prostate hyperplasia: a randomized international study of 1,098 patients. Prostate. 1996;29(4):231–240. DOI: 10.1002/(SICI) 1097-0045(199610)29:4<231::AID-PROS4>3.0.CO;2-E.
44. Debruyne F., Koch G., Boyle P. et al. Comparison of a phytotherapeutic agent (Permixon) with an alpha-blocker (Tamsulosin) in the treatment of benign prostatic hyperplasia: a 1-year randomized international study. Prog Urol. 2002;12(3):384–392; discussion 394. PMID: 12189744.
45. Debruyne F., Boyle P., Calais Da Silva F. et al. Evaluation of the clinical benefit of permixon and tamsulosin in severe BPH patients-PERMAL study subset analysis. Eur Urol. 2004;45(6):773–779; disucssion 779–780. DOI: 10.1016/j.eururo.2004.01.015.
46. Pytel Y.A., Vinarov A., Lopatkin N. et al. Long-term clinical and biologic effects of the lipidosterolic extract of Serenoarepens in patients with symptomatic benign prostatic hyperplasia. Adv Ther. 2002;19(6):297–306. DOI: 10.1007/bf02853175.
47. Vela-Navarrete R., Alcaraz A., Rodríguez‐Antolín A. et al. Efficacy and safety of a hexanic extract of Serenoarepens (Permixon®) for the treatment of lower urinary tract symptoms associated with benign prostatic hyperplasia (LUTS/BPH): systematic review and meta-analysis of randomised controlled trials and observational studies. BJU Int. 2018;122(6):1049–1065. DOI: 10.1111/bju.14362.
48. Vacherot F., Azzouz M., Gil-Diez-De-Medina S. et al. Permixon in benign prostatic hyperplasia. Prostate. 2000;45(3):259–266. DOI: 10.1002/1097-0045(20001101)45:3<259:: aid-pros9>3.0.co;2-g.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
