Влияние таргетной противовоспалительной терапии на различные показатели активности псориатического артрита: данные МЕРА
DOI: 10.32364/2587-6821-2021-5-2-78-83
Введение: количество генно-инженерных биологических препаратов и таргетных синтетических препаратов для лечения псориатического артрита (ПсА) быстро возрастает. Данные об их сравнительной эффективности ограничены. Результаты отдельных исследований дают основания для предположения, что препараты могут демонстрировать отличающуюся эффективность в отношении разных проявлений заболевания (артрита, спондилита, энтезитов, поражения кожи и ногтей).
Цель исследования: сравнить влияние таргетных препаратов на достигаемые результаты в различных доменах ПсА в условиях реальной клинической практики.
Материал и методы: данные взяты из Московского Единого Регистра Артритов. Анализировали эпизоды лечения, в рамках которых имелся завершенный визит не ранее 6 мес. с начала лечения таргетным препаратом (адалимумабом, цертолизумаба пэголом, этанерцептом, голимумабом, инфликсимабом, тофацитинибом, устекинумабом). Сравнение препаратов проводилось по достигнутым величинам индексов DAS-28, BASDAI, MASES, LEI, DLQI, PASI и BSA. Для устранения влияния различий между пациентами, получавшими разные препараты, для каждой группы показателей были установлены наиболее значимые конфаундеры (факторы, характеризующие пациента и значимо связанные с исследуемым показателем). Сравнения проводились с поправкой на конфаундеры.
Результаты исследования: в анализ было включено 184 эпизода лечения таргетными препаратами 156 пациентов с ПсА. Не выявлено достоверных различий между препаратами по их влиянию ни на домен «суставы» (DAS-28), ни на домен «позвоночник/энтезы» (BASDAI, MASES, LEI), ни на домен «кожа» (DLQI, PASI, BSA).
Заключение: достигаемые значения показателей активности вовлечения суставов, позвоночника, энтезов и кожи у пациентов с ПсА существенно не отличаются при терапии различными таргетными препаратами.
Ключевые слова: псориатический артрит, энтезит, спондилит, сакроилеит, таргетная терапия, эффективность лечения, конфаундер.
Для цитирования: Лыткина К.А., Лукина Г.В., Кольцова Е.Н., Шмидт Е.И., Жиляев Е.В. Влияние таргетной противовоспалительной терапии на различные показатели активности псориатического артрита: данные МЕРА. РМЖ. Медицинское обозрение. 2021;5(2):78-83. DOI: 10.32364/2587-6821-2021-5-2-78-83.
K.A. Lytkina1, G.V. Lukina2,3, E.N. Koltsova4, E.I. Shmidt5,6, E.V. Zhilyaev6–8
1City Clinical Hospital No. 4, Moscow, Russian Federation
2Moscow Clinical Scientific Center n.a. A.S. Loginov, Moscow, Russian Federation
3Research Institute of Rheumatology named after V.A. Nasonova, Moscow, Russian Federation
4Research Institute for Healthcare and Medical Management, Moscow, Russian Federation
5City Clinical Hospital № 1 named after N.I. Pirogov, Moscow, Russian Federation
6Pirogov Russian National Research Medical University, Moscow, Russian Federation
7CJSC European Medical Center, Moscow, Russian Federation
8Russian Medical Academy of Continuous Professional Education, Moscow,
Russian Federation
Background: the number of genetically engineered biological drugs and targeted synthetic drugs for the treatment of psoriatic arthritis (PA) is rapidly increasing. Data on their comparative efficacy is limited. The results of individual studies suggest that the drugs may show different efficacy concerning different disease manifestations (arthritis, spondylitis, entesitis, cutaneous and nail lesions).
Aim: to compare the effect of targeted drugs on the results achieved in different PA domains in real clinical practice.
Patients and Methods: the data were taken from the Moscow Unified Arthritis Registry (MUAR). We analyzed treatment episodes in which there was a completed visit no earlier than 6 months from therapy initiation with targeted drug (adalimumab, certolizumab pegol, etanercept, golimumab, infliximab, tofacitinib, ustekinumab). Drug comparison was carried out according to the achieved values of the DAS-28, BASDAI, MASES, LEI, DLQI, PASI and BSA indices. The most significant confounders (factors that characterize the patient and are significantly related to the studied indicator) were established for each group of indicators to eliminate the impact of differences between patients who received different drugs. The comparisons were adjusted for confounders.
Results: the analysis included 184 treatment episodes with targeted drugs in 156 patients with PA. There were no significant differences between the drugs in their effect on the following domains: «joints» domain (DAS-28), «spine/entheses» domain (BASDAI, MASKS, LEI), «skin» domain (DLQI, PASI, BSA).
Conclusion: the achieved values of activity indicators concerning the involvement of joint, spine, entheses and skin in patients with PA didn’t significantly differ when treated with various targeted drugs.
Keywords: psoriatic arthritis, enthesitis, spondylitis, sacroiliitis, targeted therapy, treatment efficacy , confounder.
For citation: Lytkina K.A., Lukina G.V., Koltsova E.N. et al. Targeted anti-inflammatory therapy effect on various indicators of the psoriatic arthritis activity: Moscow Unified Arthritis Registry (MUAR) data. Russian Medical Inquiry. 2021;5(2):78–83. DOI: 10.32364/2587-6821-2021-5-2-78-83.
Введение
Псориатический артрит (ПсА) — это хроническое воспалительное заболевание суставов, позвоночника и энтезов, ассоциированное с псориазом. Ранняя эффективная терапия ПсА, целью которой является достижение минимальной активности заболевания путем реализации стратегии treat-to-target, может замедлить прогрессирование повреждения суставов [1].
При быстро увеличивающемся количестве таргетных препаратов для терапии ПсА наблюдается дефицит данных об их сравнительной эффективности [2, 3]. Особенностью заболевания можно считать широкий спектр вовлекаемых органов (суставы, позвоночник, энтезы, кожа, ногти). Есть основания предполагать, что некоторые таргетные препараты в большей степени воздействуют на определенные домены ПсА. Так, небольшое исследование ECLIPSA продемонстрировало большую эффективность устекинумаба в сравнении с ингибиторами фактора некроза опухоли α (иФНО) в отношении поражений кожи и энтезов. В то же время в отношении суставов таких преимуществ препарата не наблюдалось [4]. Такого рода данные могли бы быть очень полезны для персонализации лечения: пациентам с преобладающими проявлениями со стороны какого-либо домена можно было бы назначать препараты более эффективные в отношении именно этих проявлений. Тем не менее по ряду причин экономического порядка ожидать широкомасштабных сравнительных рандомизированных исследований не приходится. Необходимые для разработки персонализированных подходов к лечению данные, вероятнее всего, будут получены в наблюдательных исследованиях. Особенности дизайна наблюдательных исследований делают их уязвимыми в отношении ошибок, связанных с изначальными различиями в характеристиках пациентов и с потерей из-под наблюдения наиболее тяжелых и наиболее успешных пациентов. Однако современные подходы к анализу данных позволяют минимизировать такой риск.
Цель исследования: сравнить влияние таргетных противовоспалительных препаратов на достигаемые результаты в различных доменах ПсА в условиях реальной клинической практики.
Материал и методы
Московский Единый Регистр Артритов (МЕРА) начал работать в 2011 г. Первоначально в регистр включали пациентов с ревматоидным артритом, с января 2015 г. включают также пациентов с ПсА, а с 2018 г. — с анкилозирующим спондилоартритом. Включаемые в регистр пациенты с ПсА должны получать таргетную терапию или планироваться к назначению таргетной терапии.
В исследование включены пациенты c ПсА, внесенные в МЕРА, удовлетворявшие критериям СASPAR (Classification criteria for Psoriatic ARthritis, 2006), проживающие в г. Москве, получающие таргетную терапию за счет бюджетных средств и давшие информированное согласие на участие в регистре.
Осмотр пациентов на каждом визите проводился врачами Московского городского ревматологического центра. Подробно изучались и фиксировались анамнез жизни пациентов (в т. ч. уровень образования, социальный статус, статус курения), анамнез заболевания (время появления симптомов артрита, кожных проявлений псориаза, время установления диагноза ПсА, характер дебюта заболевания (острый или постепенный), симптомы в дебюте заболевания и эволюция симптомов за время наблюдения (артриты, энтезиты, дактилиты, спондилит, поражение ногтей, наличие сакроилеита, поражение глаз), наличие антигена HLA B-27, а также терапия, назначавшаяся пациентам за все время болезни.
На каждом визите заполнялись опросники: BASDAI (the Bath Ankylosing Spondylitis Disease Activity Index — Басовский индекс активности анкилозирующего спондилита (АС)), BASFI (the Bath Ankylosing Spondylitis Functional Index — Басовский функциональный индекс АС), BASMI (the Bath Ankylosing Spondylitis Metrology Index — Басовский метрологический индекс АС), ASDAS (The Ankylosing Spondylitis Disease Activity Score — индекс активности АС), EQ-5D (European Quality of Life Questionnaire — европейский опросник качества жизни), DLQI (Dermatology Life Quality Index — дерматологический индекс качества жизни), оценка активности заболевания пациентом по ВАШ, оценка боли по ВАШ. Оценивался индекс поражения кожи PASI (The Psoriasis Area Severity Index — индекс тяжести псориаза), площадь пораженной псориазом кожи (BSA — Body surface area), активность заболевания по ВАШ, индекс DAS-28, индексы энтезитов MASES, LEI, число болезненных и воспаленных суставов из 28, количество дактилитов. Производился подробный сбор данных обо всех событиях, произошедших за время между визитами, и обо всех изменениях в терапии. Также на каждом визите фиксировали результаты лабораторных данных (клинический анализ крови, С-реактивный белок, СОЭ).
В анализ включали эпизоды лечения, в рамках которых имелся завершенный визит не ранее 6 мес. с момента начала лечения.
Для устранения влияния изначальных различий между пациентами (которые могли оказать влияние на выбор препарата) проведен поиск показателей, не связанных с лечением, но коррелирующих с достигнутым результатом (конфаундеров).
Поиск конфаундеров проводили раздельно для трех доменов:
поражение суставов (в качестве зависимой переменной выбрана достигнутая величина индекса DAS-28);
спондилит/энтезит (зависимая переменная — достигнутое значение индекса BASDAI), в домен включены показатели BASDAI, MASES, LEI;
поражение кожи (достигнутое значение индекса качества жизни при кожном заболевании DLQI); к данному домену отнесены DLQI, PASI, BSA.
Процесс отбора конфаундеров осуществлялся в 2 этапа: предварительный отбор показателей, имеющих достоверную однофакторную связь с зависимой переменной и последующий прямой пошаговый отбор переменных в рамках обобщенной линейной модели из показателей, выявленных на первом этапе. Достигнутые значения показателей активности ПсА сравнивали в рамках обобщенной линейной модели с поправкой (коррекцией) на выявленные конфаундеры. Для коррекции всех показателей каждого домена использовали соответствующий набор конфаундеров. Статистический анализ проводили с помощью программы IBM SPSS Statistics version 22 (SPSS corp. 1989, 2013).
Результаты исследования
В анализ включено 184 эпизода лечения таргетными препаратами 156 пациентов с ПсА, наблюдавшихся в МЕРА в период с января 2015 г. по декабрь 2019 г. Средний возраст пациентов 50,3±11,3 года, мужчины составили 44,2% (табл. 1).
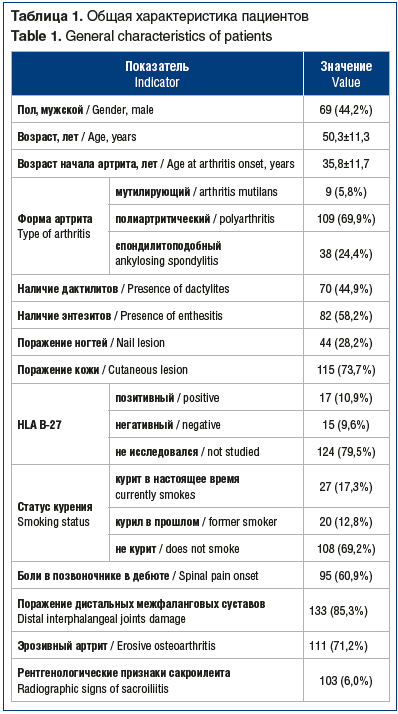
В лечении пациентов использовались следующие таргетные препараты: адалимумаб, цертолизумаба пэгол, этанерцепт, голимумаб, инфликсимаб, тофацитиниб, устекинумаб. Сведения о количестве соответствующих эпизодов лечения приведены в таблице 2.
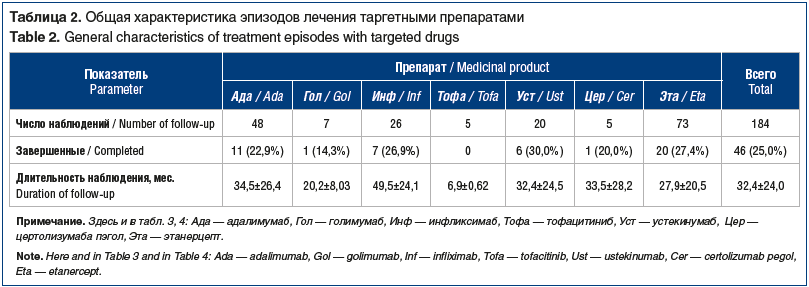
При первичном анализе эффективности различных генно-инженерных биологических препаратов, применяемых при ПсА, получены данные, представленные в таблице 3. Имелись достоверные различия в достигнутых значениях DAS-28 между таргетными препаратами.
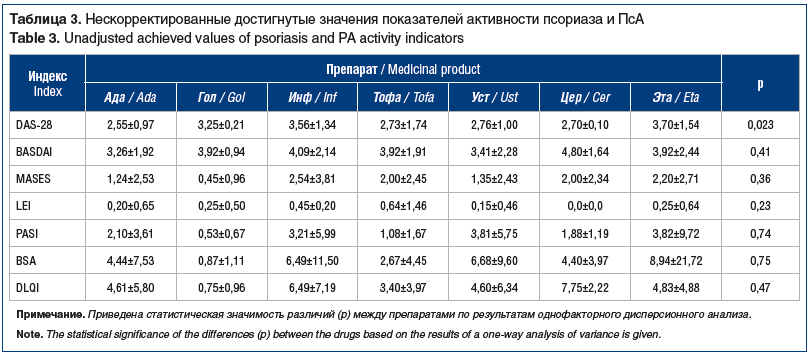
Поиск конфаундеров выявил следующие показатели (в табл. 4 приведены величины статистической значимости для показателей, полученные в рамках многофакторных моделей):
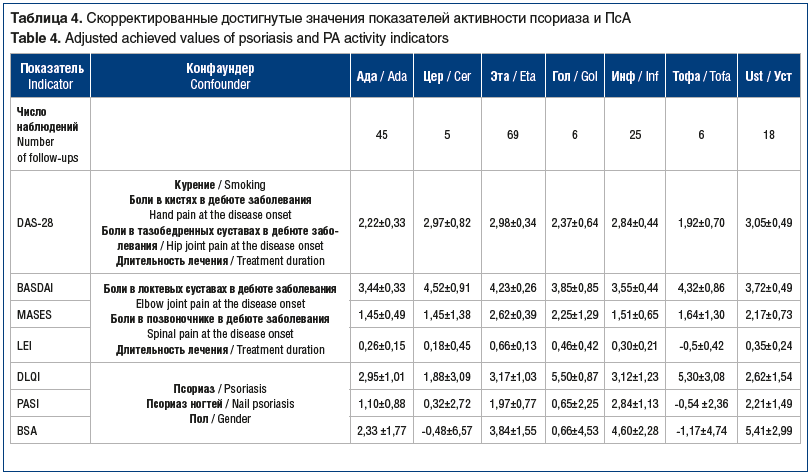
для достигнутой величины DAS-28: статус курения (p=0,046), боли в кистях в дебюте заболевания (p=0,069), боли в тазобедренных суставах в дебюте заболевания (p=0,010), длительность терапии соответствующим таргетным препаратом (p=0,053);
для достигнутой величины индекса BASDAI: боли в локтевых суставах в дебюте заболевания (p=0,014), боли в позвоночнике в дебюте заболевания (p=0,017), длительность лечения соответствующим таргетным препаратом (p=0,077);
для достигнутой величины индекса DLQI: псориаз (p<0,001), псориаз ногтей (p=0,033), пол (p=0,011).
После внесения поправок на выявленные конфаундеры не обнаружено достоверных различий между препаратами по их влиянию на домены «суставы» (DAS-28), «позвоночник/энтезы» (BASDAI, MASES, LEI), «кожа» (DLQI, PASI, BSA) (см. табл. 4).
Обсуждение
На сегодняшний день большой интерес представляет изучение проблемы возможного преимущества тех или иных таргетных препаратов в лечении ПсА. Сведения о сравнительной эффективности антицитокиновых средств в настоящее время начинают поступать из реальной практики, где выполняются наблюдательные, когортные и регистровые исследования. В литературе имеется мало данных о сравнительной эффективности различных биологических агентов и синтетических таргетных препаратов при лечении ПсА.
В 2004 г. были впервые опубликованы данные об эффективности применения этанерцепта при ПсА [5], что явилось началом эры биологической терапии ПсА. В ряде рандомизированных клинических исследований (РКИ) была доказана эффективность сначала иФНО, затем ингибиторов ИЛ-17, ИЛ-12/23, а в дальнейшем и ингибиторов ИЛ-23 и ИЛ-17А. Для лечения ПсА зарегистрированы синтетические таргетные препараты: ингибиторы JAK-киназ тофацитиниб, барицитиниб, упадацитиниб, а также селективный блокатор фосфодиэстеразы IV типа апремиласт. Несмотря на такой арсенал таргетных препаратов, часть пациентов остаются резистентными к проводимой терапии [3].
M. Rodgers et al. [6] опубликовали систематический обзор данных, собранных до июня 2009 г. включительно из 10 электронных баз данных (MEDLINE, EMBASE, Cochrane Central Register of Controlled Trials, Science Citation Index, Conference Proceedings Citation Index — Science, ClinicalTrials.gov, metaRegister of Current Controlled Trials, NHS Economic Evaluation Database, Health Economic Evaluations Database и EconLit), по использованию трех иФНО — этанерцепта, инфликсимаба и адалимумаба у больных ПсА. При оценке эффективности терапии анализировались данные 6 РКИ (43 публикации). Инфликсимаб показал несколько большую эффективность в отношении как суставных, так и кожных проявлений заболевания. По влиянию на суставы отмечалась тенденция к превосходству этанерцепта перед адалимумабом, и наоборот, адалимумаб был несколько эффективнее этанерцепта по уменьшению поражения кожи. Однако все эти различия в эффективности трех иФНО были статистически незначимыми [6].
K. Thorlund et al. [2] представили результаты метаанализа РКИ и систематических обзоров работ по лечению ПсА генно-инженерными биологическими препаратами (адалимумабом, этенерцептом, голимумабом, инфликсимабом). Имелись некоторые различия в эффективности препаратов (так, например, голимумаб оказался несколько более эффективным по индексу активности PsARC, несколько меньший результат показал этанерцепт, при лечении инфликсимабом и адалимумабом эффект был наименьшим), но эти различия были также статистически незначимыми [2].
Первый систематический обзор и сетевой метаанализ сравнительной эффективности и безопасности у пациентов с ПсА таргетных препаратов, не относящихся к иФНО, в 2017 г. представили G.G. Song et al. [7]. В метаанализ включено 8 РКИ эффективности и безопасности апремиласта, секукинумаба и устекинумаба. Статистически значимой разницы в эффективности препаратов не выявлено. Надо отметить, что исследования, включенные в метаанализ, различались по дизайну и характеристикам пациентов, не был проведен дополнительный субанализ пациентов, не ответивших на иФНО и биологически наивных.
В 2018 г. P. Kawalec et al. [8] также представили систематический обзор и метаанализ работ по сравнительной эффективности таргетных препаратов, не относящихся к иФНО (абатацепта, апремиласта, секукинумаба и устекинумаба). Проанализировано 8 РКИ. Авторами отмечена тенденция к большей эффективности секукинумаба в достижении ACR-20 (разница также статистически недостоверна).
Количественное сравнение эффективности препаратов в наблюдательных исследованиях в определенной мере затруднено. С одной стороны, для ПсА нет единого общепринятого индекса активности. Различные проявления заболевания оцениваются по разным показателям. С другой стороны, в наблюдательном исследовании, как правило, трудно оценить исходное состояние пациента. Из-за отсутствия «отмывочного» периода начальная оценка состояния проводится на момент какой-то другой терапии, которая по своему составу весьма разнообразна. В результате оценка динамики различных количественных показателей активности заболевания на фоне лечения препаратом слабо отражает эффект самого препарата. Больший интерес представляют достигаемые в ходе лечения значения индексов активности.
Однако следует помнить, что значения индексов зависят не только от препарата, но от особенностей самого пациента. Так, например, если в какой-то момент времени предполагается, что определенный препарат слабее воздействует на артрит, то он, вероятно, будет назначаться пациентам, у которых вовлечение суставов менее выражено. В результате при оценке достигнутых значений индекса активности артрита может оказаться, что для данного препарата они наименьшие. Для предотвращения такого рода ошибок необходимо математическое уравнивание включенных в анализ пациентов. Для этого вносятся поправки на так называемые конфаундеры. Такой порядок анализа и представления результатов наблюдательных исследований закреплен в международном стандарте STROBE [9, 10]. В ряде случаев конфаундеры заранее известны из предшествующих исследований. В нашем случае их предстояло выявить.
Проведенный нами анализ скорректированных значений индексов активности артрита, спондилита, энтезитов, кожного поражения не выявил достоверных различий между препаратами ни по одному из показателей. Это, безусловно, не означает, что их вообще нет. Их выявлению могло помешать относительно небольшое количество включенных эпизодов лечения некоторыми из препаратов (голимумабом, цертолизумаба пэголом, тофацитинибом). Кроме того, выявлению различий между препаратами препятствует большой разброс (дисперсия) достигаемых величин изучаемых индексов. Поправка на удачно выбранные конфаундеры в ряде случаев позволяет значительно уменьшить дисперсию изучаемого показателя и обнаружить трудно выявляемые различия. Тем не менее даже с пониманием статистической незначимости наблюдаемых различий интересно посмотреть на полученные сравнительные результаты применения таргетных препаратов у больных ПсА. Можно видеть, что на проявления артрита несколько лучший эффект оказали адалимумаб, голимумаб и тофацитиниб. Лучшая динамика симптомов спондилита была достигнута при применении адалимумаба и инфликсимаба. На проявления энтезитов наиболее активно влияли адалимумаб, цертолизумаба пэгол, инфликсимаб и тофацитиниб, на кожные проявления заболевания наилучший эффект оказали цертолизумаба пэгол, голимумаб и инфликсимаб. Возможно, при большем количестве наблюдений в дальнейшем удастся обнаружить значимые различия между эффектами таргетных препаратов относительно проявлений ПсА.
Заключение
Достигаемые значения показателей активности вовлечения суставов, позвоночника, энтезов и кожи у пациентов с ПсА существенно не отличаются при терапии различными таргетными препаратами. Поиски профилей пациентов для применения тех или иных таргетных препаратов при лечении ПсА, по нашему мнению, следует продолжать. Для этого потребуется дополнительное количественное накопление данных и, возможно, поиск дополнительных влияющих на достигаемый результат факторов, учет которых позволил бы уменьшить дисперсию наблюдаемых значений.
Сведения об авторах:
Лыткина Каринэ Арнольдовна — к.м.н., заведующая ревматологическим отделением ГБУЗ «ГКБ № 4 ДЗМ»; 115093, Россия, г. Москва, ул. Павловская, д. 25; ORCID iD 0000-0001-9647-7492.
Лукина Галина Викторовна — д.м.н., профессор, заведующая научно-исследовательским отделом ревматологии, руководитель Московского городского ревматологического центра ГБУЗ Московский клинический научный центр имени А.С. Логинова ДЗМ; Россия, 111123, г. Москва, шоссе Энтузиастов, д. 86; ведущий научный сотрудник лаборатории изучения коморбидных инфекций и мониторинга безопасности лекарственной терапии ФГБНУ НИИР им. В.А. Насоновой; 115522, Россия, г. Москва, Каширское шоссе, д. 34А; ORCID iD 0000-0001-7958-5926.
Кольцова Екатерина Николаевна — заведующая ОМО по ревматологии ГБУ «НИИОЗММ ДЗМ»; 115184, Россия, г. Москва, ул. Большая Татарская, д. 30; ORCID iD 0000-0002-5202-4878.
Шмидт Евгения Исааковна — к.м.н., заведующая ревматологическим отделением ГКБ № 1 им. Н.И. Пирогова; 117049, Россия, г. Москва, Ленинский проспект, д. 8; доцент кафедры факультетской терапии им. А.И. Нестерова лечебного факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0001-8814-9704.
Жиляев Евгений Валерьевич — д.м.н., профессор, главный врач АО «Европейский медицинский центр»; 129090, Россия, г. Москва, ул. Щепкина, д. 35; профессор кафедры ревматологии ФГБОУ ДПО РМАНПО Минздрава России, профессор кафедры факультетской терапии им. А.И. Нестерова лечебного факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-9443-1164.
Контактная информация: Жиляев Евгений Валерьевич, e-mail: zhilyayevev@mail.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 05.02.2021, поступила после рецензирования 04.03.2021, принята в печать 30.03.2021.
About the authors:
Karine A. Lytkina — Cand. of Sci. (Med.), Head of the Department of Rheumatology, City Clinical Hospital No. 4; 25, Pavlovskaya str., Moscow, 115093, Russian Federation; ORCID iD 0000-0001-9647-7492.
Galina V. Lukina — Dr. of Sci. (Med.), Professor, Head of the Research Department of Rheumatology, Moscow Clinical Research Center n.a. A.S. Loginov; 86, Entusiastov highway, Moscow, 111123, Russian Federation; Leading Researcher of the Laboratory for the study of comorbid Infections and monitoring the drug therapy safety, Research Institute of Rheumatology named after V.A. Nasonova; 34A, Kashirskoe highway, Moscow, 115522, Russian Federation; ORCID iD 0000-0001-7958-5926.
Ekaterina N. Koltsova — Head of the Organizational and Methodological Department of the Research Institute for Healthcare and Medical Management; 30, Bolshaya Tatarskaya str., Moscow, 115184, Russian Federation; ORCID iD 0000-0002-5202-4878.
Evgeniya I. Shmidt — Cand. of Sci. (Med.), Head of the Department of Rheumatology, City Clinical Hospital No. 1 named after N.I. Pirogov; 8, Leninskiy prospect, Moscow, 117049, Russian Federation; Associate Professor of the Department of Faculty Therapy named after A.I. Nesterov, Pirogov Russian National Research Medical University; 1, Ostrovityanova str., Moscow, 117997, Russian Federation; ORCID iD 0000-0001-8814-9704.
Evgeniy V. Zhilyaev — Dr. of Sci. (Med.), Professor, Chief physician of CJSC European Medical Center; 35, Schepkina str., Moscow, 129090, Russian Federation; Professor of the Department of Rheumatology of the Russian Medical Academy of Continuous Professional Education, Professor of the Department of Faculty Therapy named after A.I. Nesterov, Pirogov Russian National Research Medical University; 1, Ostrovityanova str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-9443-1164.
Contact information: Evgeniy V. Zhilyaev, e-mail: zhilyayevev@mail.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 05.02.2020, revised 04.03.2021, accepted 30.03.2021.
2. Thorlund K., Druyts E., Aviña-Zubieta J.A., Mills E.J. Anti-tumor necrosis factor (TNF) drugs for treatment of psoriatic arthritis: an indirect comparison meta-analysis. Biologics. 2012:6;417–427. DOI: 10.2147/btt.s37606.
3. Miyagawa I., Nakayamada S., Tanaka Y. Optimal biologic selection for treatment of psoriatic arthritis: the approach to precision medicine. Curr Rheumatol Rep. 2019;21(5):21. DOI: 10.1007/s11926-019-0817-x.
4. Araujo E.G., Englbrecht M., Hoepken S. et al. Ustekinumab is superior to TNF inhibitor treatment in resolving enthesitis in PsA patients with active entesitis — results from the Enthesial Clearance in Psoriatic Arthritis (ECLIPSA) study. Ann Rheum Dis. 2017;76(2):142. DOI: 10.1136/annrheumdis-2017-eular.5398.
5. Ungprasert P., Thongprayoon C., Davis J. Indirect comparisons of the efficacy of subsequent biological agents in patients with psoriatic arthritis with an inadequate response to tumor necrosis factor inhibitors: a meta-analysis. Clin Rheumatol. 2016;35:1795–1803. DOI: 10.1007/s10067-016-3204-2.
6. Rodgers M., Epstein D., Bojke L. et al. Etanercept, infliximab and adalimumab for the treatment of psoriatic arthritis: a systematic review and economic evaluation. Health Technol Assess. 2011;15(10): i–xxi, 1–329. DOI: 10.3310/hta15100.
7. Song G.G., Lee Y.H. Relative efficacy and safety of apremilast, secukinumab, and ustekinumab for the treatment of psoriatic arthritis. Z Rheumatol. 2018;77(7):613–620. DOI: 10.1007/s00393-017-0355-8.
8. Kawalec P., Holko P., Moćko P., Pilc A. Comparative effectiveness of abatacept, apremilast, secukinumab and ustekinumab treatment of psoriatic arthritis: a systematic review and network meta-analysis Rheumatology Int. 2018;38(2):189–201. DOI: 10.1007/s00296-017-3919-7.
9. Von Elm E., Altman D.G., Egger M. et al. Strengthening the Reporting of Observational Studies in Epidemiology (STROBE) statement: guidelines for reporting observational studies. BMJ. 2007;335(7624):806–808. DOI: 10.1136/bmj.39335.541782.AD.
10. Шальнова А., Деев А.Д. Как описывать результаты наблюдательных эпидемиологических исследований. Рациональная фармакотерапия в кардиологии. 2011;7(2):133–136. DOI: 10.20996/1819-6446-2011-7-2-133-136. [Shal’nova S.A., Deev A.D. How to describe the results of observational epidemiological studies. Rational Pharmacotherapy in Cardiology. 2011;7(2):133–136 (in Russ.)]. DOI: 10.20996/1819-6446-2011-7-2-133-136.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.