Результаты переключения на различные таргетные препараты пациентов с ревматоидным артритом после отмены этанерцепта
Цель исследования: оценка эффективности переключения на другие селективные иммуносупрессоры у пациентов с ревматоидным артритом (РА), получавших этанерцепт.
Материал и методы: в анализ включили пациентов с РА из Московского единого регистра артритов (МЕРА), которые соответствовали критериям EULAR (1987) или ACR и EULAR (2010) и получали таргетую терапию. Пациенты находились на лечении этанерцептом и прекратили его по любым причинам, а затем переключились на другой таргетный препарат. Переключение считали успешным, если применение второго препарата длилось не менее 6 мес. и была достигнута ремиссия или низкая активность заболевания (DAS28(СОЭ) <3,2).
Результаты исследования: 195 из 757 пациентов принимали этанерцепт. Среди 33 пациентов, которые с этанерцепта были переведены на другой таргетный препарат, 4 пациента произвели смену терапии 2 раза. 16 пациентов были переведены на другой ингибитор фактора некроза опухоли (иФНО), еще 16 — на генно-инженерные биологические препараты других классов и 5 — на синтетический таргетный препарат (тофацитиниб). 27 пациентов были женщины, средний возраст всех пациентов составил 53,4±13,7 года, средняя продолжительность лечения этанерцептом — 732±571 день.
Причинами прекращения приема этанерцепта были: нежелательные явления (10,5%), неэффективность терапии (60,5%), другие причины (29%). Уровень DAS28(СОЭ) снижался после переключения более значимо в группе неэффективности этанерцепта, чем в группе с нежелательными явлениями.
Среди пациентов, которые были переведены с этанерцепта не на иФНО, вероятность успеха была выше (p=0,001). Ремиссия по DAS28(СОЭ) была достигнута у 6 из 21 пациента. Среди пациентов, которые были переведены на иФНО, ремиссия не наблюдалась.
Вывод: результаты исследования дают основания предпочесть переход на препараты других классов в случае отмены этанерцепта по любой причине.
Ключевые слова: ревматоидный артрит, этанерцепт, энбрел, иФНО, генно-инженерные биологические препараты, таргетные иммуносупрессоры, таргетные препараты, переключение препаратов, смена терапии, Московский единый регистр артритов, МЕРА, ремиссия.
Для цитирования: Кольцова Е.Н., Лукина Г.В., Шмидт Е.И., Лыткина К.А., Жиляев Е.В. Результаты переключения на различные таргетные препараты пациентов с ревматоидным артритом после отмены этанерцепта. РМЖ. Медицинское обозрение. 2019;3(11(II)):81-84.
E.N. Koltsova1,2, G.V. Lukina2, E.I. Shmidt3, K.A. Lytkina4, E.V. Zhilyaev5,6
1Research Institute of Health Care Organization and Medical Management, Moscow
2Loginov Moscow Clinical Scientific Center
3First City Hospital named after N.I. Pirogov, Moscow
4City Clinical Hospital No 4, Moscow
5EMC, Moscow
6Russian Medical Academy of Postgraduate Education, Moscow
Aim: to evaluate the switching effectiveness to other selective immunosuppressive agents in patients with rheumatoid arthritis treated with etanercept.
Patients and Methods: the analysis included patients with rheumatoid arthritis from the Moscow Unified Register of Arthritis (MURA) who met the criteria of EULAR (1987) or ACR / EULAR (2010) and received targeted therapy. Patients were treated with etanercept and canceled it for any reason, and then switched to another targeted drug. The replacement is considered successful if the second drug use is at least 6 months and it achieved remission or low disease activity (DAS28 (ESR) <3.2).
Results: 195 of 757 patients took etanercept. Among 33 patients who switched to another targeted drug, 4 patients had 2 switchings after etanercept cancelation. 16 patients switched to another tumor necrosis factor inhibitor (TNFi). Another 16 patients switched to geneti cally engineered biological agents (GEBD) of other classes, and 5 — to the synthetic targeted agent (tofacitinib).
27 patients were women, the average age was 53.4±13.7 years, the average duration of etanercept treatment was 732±571 days.
Etanercept cancelation reasons were the following: adverse events (10.5%), ineffective therapy (60.5%) and other causes (29%). After switching, DAS-28 level decreased more significantly in the etanercept ineffectiveness group than in the adverse events group.
The success probability was higher (p = 0.001) among patients who switched etanercept to non-TNF. DAS-28 remission was achieved in 6 of 21 patients. Also, remission was not observed among the patients who were switched to TNFi.
Conclusion: the study results permit to prefer the switching to drugs of other classes in the case of etanercept cancellation for any reason.
Keywords: rheumatoid arthritis, etanercept, Enbrel, TNFi, genetically engineered biological dr ugs, targeted immunosuppressive agents, targeted drugs, drug switching, therapy change, Moscow Unified Register of Arthritis (MURA), remission.
For citation: Koltsova E.N., Lukina G.V., Shmidt E.I. et al. Results of different targeted drugs switching in patients with rheumatoid arthritis after etanercept discontinuation. RMJ. Medical Review. 2019;11(II):81–84.
В статье представлены результаты исследования, посвященные оценке эффективности переключения на другие селективные иммуносупрессоры у пациентов с ревматоидным артритом, получавших этанерцепт
Введение
Ревматоидный артрит (РА) — аутоиммунное ревматическое заболевание неизвестной этиологии, характеризующееся хроническим воспалением синовиальной оболочки и прогрессирующей деструкцией хрящевой и костной ткани [1].
Лечение РА включает в себя, главным образом, базисные противовоспалительные препараты (БПВП), которые подразделяют на обычные синтетические базисные противовоспалительные препараты (метотрексат, лефлуномид, сульфасалазин и гидроксихлорохин) и таргетные базисные противовоспалительные препараты (тБПВП) (генно-инженерные биологические препараты — ГИБП и таргетные синтетические базисные противовоспалительные препараты — тсБПВП).
В соответствии с действующими европейскими и российскими клиническими рекомендациями по ведению пациентов с РА лечение начинается с назначения метотрексата или его комбинации с другими БПВП. В случае невозможности достижения целевой активности заболевания (т. е. низкой активности или ремиссии) на фоне обычной базисной терапии к лечению добавляют тБПВП [2]. Данные рандомизированных и наблюдательных исследований показывают, что лишь около 40% пациентов достигают целевой активности заболевания на фоне применения первого таргетного препарата [3]. Остальные больные в соответствии с действующими рекомендациями должны быть переключены на лечение другим тБПВП.
Ингибиторы фактора некроза опухоли-α (иФНО) остаются самым многочисленным и самым широко используемым классом ГИБП. Это во многом объясняется тем, что иФНО стали первыми таргетными средствами лечения РА. Несмотря на то, что современные отечественные и международные рекомендации не определяют выбор первого таргетного препарата у пациента, не ответившего на лечение БПВП, в реальной практике ревматологи в качестве первого препарата чаще назначают иФНО. Однако нет единого мнения о том, должны ли пациенты в случае прекращения лечения одним из иФНО переходить на другой препарат того же класса или же следует выбирать таргетный препарат с другим механизмом действия.
Целью данного исследования явилась оценка результатов переключения на другие таргетные препараты у пациентов с РА, получавших этанерцепт (ЭТА).
Материал и методы
Для анализа взяты данные из Московского единого регистра артритов (МЕРА), в который с 2011 г. включаются пациенты, соответствующие критериям РА Американской коллегии ревматологов (American College of Rheumatology, ACR) 1991 г. или ACR и Европейской лиги против ревматизма (European League Against Rheumatism, EULAR) 2010 г. и получающие таргетные препараты.
Критериями включения в настоящий анализ были:
эпизод лечения ЭТА, завершенный по любой причине;
завершенный визит в рамках регистра на фоне терапии ЭТА не ранее 6 мес. с момента ее начала;
лечение другим тБПВП после завершения терапии ЭТА;
завершенный визит в рамках регистра на фоне терапии другим тБПВП (после отмены ЭТА) не ранее 6 мес. с момента ее начала.
Переключение считали успешным, если лечение новым препаратом продолжалось не менее 6 мес. и была достигнута ремиссия или низкая активность — DAS28(СОЭ) <3,2 (Disease Activity Score для 28 суставов (DAS28) — основной клинико-лабораторный показатель активности заболевания). Достижение ремиссии оценивалось также при DAS28(СОЭ) <2,6.
Результаты
На момент сбора данных в МЕРА было зарегистрировано 757 пациентов с РА. Из них ЭТА получали 195 человек. Критериям включения соответствовали 33 пациента, у которых было проанализировано 37 случаев переключения с ЭТА. У 4 пациентов произошло 2 смены таргетного препарата после отмены ЭТА.
Общая характеристика включенных в анализ пациентов приведена в таблице 1.
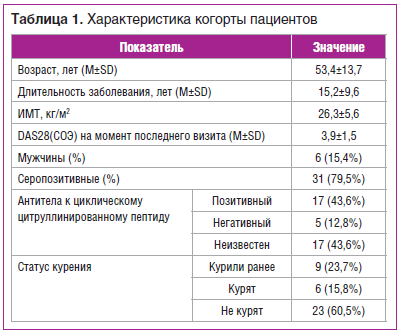
Среди пациентов, включенных в исследование, 27 человек (81,8%) были женщины, средний возраст — 53,4±13,7 года, средняя длительность удержания на ЭТА составила 732±531 день.
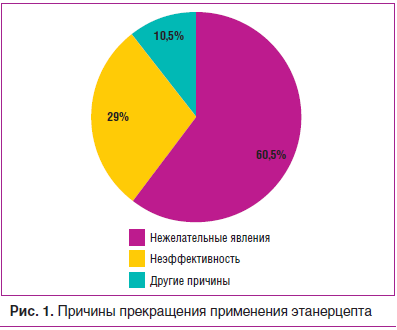
Причинами переключения были: нежелательные явления — 4 эпизода (10,5%), неэффективность ЭТА — 23 эпизода (60,5%) и события, не связанные с препаратом (завершение клинического исследования, проведение плановых операций и др.), — 11 эпизодов (29,0%) (рис. 1). У пациентов, у которых ЭТА был отменен из-за нежелательных явлений, среднее время его применения было короче и составило 53±39 дней (минимально — 17 дней, максимально — 104 дня). Средняя продолжительность эпизодов лечения, завершенных по причине неэффективности, составила 873±540 дней, по другим причинам — 671±576 дней.
Число переключений на другой иФНО — 16 (на адалимумаб — 10, на инфликсимаб — 4, на цертолизумаба пэгол — 2), на ГИБП с другим механизмом действия — 16 (на абатацепт — 8, на ритуксимаб — 5, на тоцилизумаб — 3, на тсБПВП тофацитиниб — 5).
Пациенты, у которых ЭТА отменен из-за неэффективности, несколько чаще переводились на другие классы таргетных препаратов (16 случаев — 66,7%). В группе отмены ЭТА по другим причинам переключение на другой иФНО произошло в 10 (56%) из 18 случаев (p=0,086). Показатель активности заболевания по DAS28(СОЭ) в группе пациентов с неэффективностью ЭТА после переключения на другие ГИБП снижался достоверно сильнее, чем при отмене в связи с нежелательными явлениями (p=0,031).
Переключение пациентов с ЭТА на препараты с другим механизмом действия было достоверно успешнее. Так, только 1 (6,25%) из 16 переключений на иФНО (адалимумаб) имело положительный эффект, тогда как из 21 переключения на препараты других классов успешными были 14 (66,7%) (p=0,001). Результаты смены терапии приведены в таблице 2.
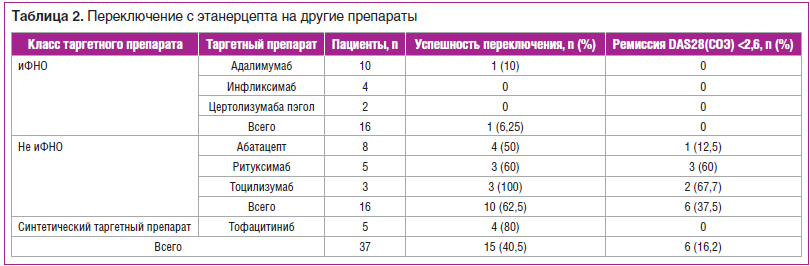
Наиболее успешными выглядят переключения на тоцилизумаб (успешны 3 из 3 переключений) и тофацитиниб (успешны 4 из 5 переключений). Однако значимых различий в эффективности между отдельными препаратами не выявлено.
В значительной части случаев в результате переключения были достигнуты ремиссии по DAS28(СОЭ) у 6 (28,6%) из 21 пациента: при переключении на ритуксимаб — у 3, на тоцилизумаб — у 2, на абатацепт — у 1. Ни у одного из пациентов, переключенных с ЭТА на другой иФНО, ремиссия не была достигнута.
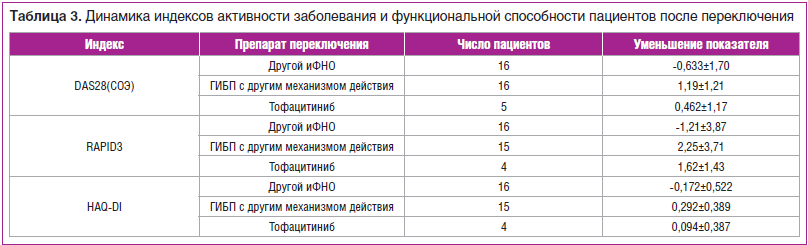
Динамика различных показателей, характеризующих активность заболевания и функциональные возможности пациента, в результате переключения представлена в таблице 3. Как основной клинико-лабораторный показатель активности заболевания DAS28(СОЭ), так и индекс активности, основанный на ощущениях пациента (RAPID3), и индекс функциональной способности пациента (Health assessment questionnaire disability index, HAQ-DI) после переключения на другой иФНО имели тенденцию к возрастанию (что соответствует ухудшению состояния больного). При переключении на препараты других классов указанные показатели снижались. Различия в динамике показателей между переключением на другой иФНО и переключением на ГИБП с другим действием были статистически значимыми для всех трех индексов (DAS28(СОЭ): p=0,001; RAPID3: p=0,008; HAQ-DI: p=0,008).
Обсуждение
Тактика смены таргетных препаратов при их неэффективности или непереносимости на настоящий момент является предметом активного изучения. Наблюдательные исследования представляются наиболее удобным инструментом для такого изучения. Ввиду того что в реальной клинической практике таргетная терапия чаще всего начинается с иФНО, вопрос о том, на какой препарат в дальнейшем следует при необходимости переключаться, является весьма актуальным.
По данным некоторых исследований, отмечался положительный эффект от перехода на второй иФНО после отмены первого. Особенно это касается отмены из-за побочных эффектов и при вторичной неэффективности (потеря со временем ранее наблюдавшегося хорошего эффекта) [4–6]. Например, одно исследование показало, что 75% пациентов, которые перешли с инфликсимаба (ИНФ) на адалимумаб, достигли критериев положительного ответа ACR (соответствует клинически значимому улучшению) через 12 мес. [7]. По данным других исследований, улучшение отмечалось после перехода с иФНО на препараты других классов [8–10]. Показано, что может быть эффективным переключение с ИНФ на ЭТА в случае неэффективности ИНФ, но не наоборот [3]. Действительно, неэффективность некоторых иФНО, в основном вторичная, в значительной мере обусловлена иммуногенностью этих препаратов (образование антилекарственных антител). При этом ЭТА в силу своих структурных особенностей характеризуется наименьшей иммуногенностью и практически не демонстрирует вторичной неэффективности при РА [11]. Таким образом, можно предположить, что в отсутствие иммуногенности переключение с одного иФНО на другой нецелесообразно.
Результаты настоящего исследования показывают, что после терапии ЭТА переключение на другие иФНО в целом очень редко позволяло достичь целевого ответа на лечение и показатели активности заболевания и функциональной способности пациента имели тенденцию к ухудшению. В то же время переключение на таргетные препараты с другими механизмами действия привело к улучшению индексов активности и функциональной способности и достижению целевой активности заболевания в 2/3 случаев. Полученные данные дают основания считать целесообразным в случае необходимости отмены ЭТА по любой причине переключение на препарат с другим механизмом действия.
Из нашего наблюдения следует и другой важный вывод: если после неудачи с ЭТА использование других иФНО редко приводит целевому результату лечения, то назначение ЭТА в качестве первого иФНО у пациентов с РА сокращает путь к эффективной таргетной терапии. Такое сокращение представляется весьма важным для пациентов с РА, т. к. дорогостоящее и не всегда безопасное лечение без достижения поставленных целей неоправданно повышает риск, ведет к потере качества жизни, трудоспособности, а также бесполезным затратам материальных средств.
Заключение
Таким образом, полученные данные дают основания, во-первых, делать выбор в пользу ЭТА при показаниях к иФНО, а во-вторых, переходить на препараты другого класса, если лечение ЭТА не позволяет достичь целевой активности заболевания. Сильной стороной настоящего исследования является то, что оно основывается на репрезентативной выборке (регистр МЕРА включает около 90% пациентов с РА, получающих таргетные препараты за счет бюджетных средств). Тем не менее объем выборки оказался небольшим. Из 195 пациентов, получавших ЭТА, в анализ было включено только 33. Это в значительной мере связано с хорошим удержанием на терапии ЭТА и относительно небольшим сроком работы регистра (6 лет на момент анализа данных).
На основании анализа данных МЕРА выявлено, что у пациентов, прекративших прием ЭТА по любым причинам, иФНО в качестве следующего таргетного препарата менее эффективны в сравнении с препаратами других классов.
2. Smolen J.S., Landewé R., Bijlsma J. et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2016 update. Ann Rheum Dis. 2017;76:960–977.
3. Tak P.P. Understanding drug resistance to biologic therapy. Rheumatology. 2012;51:600–609.
4. Gomez-Reino J.J., Carmona L., BIOBADASER Group. The switching TNF antagonists in patients with chronic arthritis: an observational study of 488 patients over a four-year period. Arthritis Res Ther. 2006;R29–R29.
5. Hjardem E., Østergaard M., Pødenphant J. et al. Do rheumatoid arthritis patients in clinical practice benefit from switching from infliximab to a second tumor necrosis factor alpha inhibitor? Ann Rheum Dis. 2007;66:1184–1189.
6. Laas K., Peltomaa R., Kautiainen H., Leirisalo-Repo M. Clinical impact of switching from infliximab to etanercept in patients with rheumatoid arthritis. Clin Rheumatol. 2008 Jul;27(7):927–932.
7. Nikas S.N., Voulgari P.V., Alamanos Y. et al. Efficacy and safety of switching from infliximab to adalimumab: a comparative controlled study. Ann Rheum Dis. 2006;65:257–260.
8. Chatzidionysiou K., van Vollenhoven R.F. Rituximab versus anti-TNF in patients who previously failed one TNF inhibitor in an observational cohort. Scand J Rheumatol. 2013;42:190–195.
9. Harrold L.R., Reed G.W., Kremer J.M. et al. The comparative effectiveness of abatacept versus anti-tumour necrosis factor switching for rheumatoid arthritis patients previously treated with an anti-tumour necrosis factor. Ann Rheum Dis. 2015;74:430–436.
10. Li N., Betts K.A., Messali A.J et al. Real-world effectiveness of biologic disease-modifying antirheumatic drugs for the treatment of rheumatoid arthritis after etanercept discontinuation in the United Kingdom, France, and Germany. Clin Ther. 2017;39(8):1618–1627.
11. Arstikyte I., Kapleryte G., Butrimiene I., Venalis A. Influence of immunogenicity on the efficacy of long-term treatment with TNFα blockers in rheumatoid arthritis and spondyloarthritis patients. Biomed Res Int. 2015;2015:604872. DOI: 10.1155/2015/604872.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
