Обзор эффективности и безопасности нестероидных противовоспалительных препаратов для лечения острого приступа подагрического артрита
DOI: 10.32364/2587-6821-2021-5-2-96-101
Подагра является одной из самых распространенных форм воспалительного артрита. Стандарт оказания медицинской помощи при подагре предполагает назначение нестероидных противовоспалительных средств (НПВС). Проведен обзор эффективности и безопасности НПВС, используемых для лечения острого приступа подагры, с оценкой терапевтических возможностей препарата АМБЕНИУМ® парентерал. По результатам литературного обзора, а также по результатам выгрузки нежелательных лекарственных реакций, полученной из АИС РЗН, установлено, что фенилбутазон является эффективным НПВС, обладающим выраженным анальгезирующим и противовоспалительным действием. Принимая во внимание широкий спектр возможных нежелательных реакций при терапии НПВС, назначение и использование этой группы лекарственных средств необходимо проводить с параллельным всесторонним анализом состояния пациента, сопутствующих заболеваний, степени их декомпенсации, а также с оценкой потенциальных межлекарственных взаимодействий. Кроме того, следует уделить особое внимание подбору оптимальной дозировки и длительности терапии НПВС. По результатам обзора сделано заключение о достаточной эффективности и безопасности препарата АМБЕНИУМ® парентерал при лечении подагры. Профиль, а также соотношение риск/польза препарата характеризуются как благоприятные в сравнении с другими НПВС.
Ключевые слова: подагра, артрит, болевой синдром, нестероидные противовоспалительные препараты, парентеральный, эффективность, безопасность.
Для цитирования: Василюк В.Б., Сыраева Г.И., Фарапонова М.В. Обзор эффективности и безопасности нестероидных противовоспалительных препаратов для лечения острого приступа подагрического артрита. РМЖ. Медицинское обозрение. 2021;5(2):96-101. DOI: 10.32364/2587-6821-2021-5-2-96-101.
V.B. Vasilyuk1,2, G.I. Syraeva1,3, M.V. Faraponova1
1LLC “Research Center Eco-safety”, St. Petersburg, Russian Federation
2I.I. Mechnikov North-Western State Medical University, St. Petersburg, Russian Federation
3I.P. Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
Gout is one of the most common forms of inflammatory arthritis. Medical care for gout includes non-steroidal anti-inflammatory drugs (NSAIDs). This paper reviews the efficacy and safety of NSAIDs prescribed for the acute attack of gout, in particular, AMBENIUM® parenteral. It was demonstrated that phenylbutazone is a powerful NSAID that provides significant analgesic and anti-inflammatory effects. Considering a broad spectrum of adverse reactions of NSAIDs, these agents should be prescribed and used under in-depth analysis of patient’s condition, comorbidities and the level of their decompensation, and potential drug interactions. In addition, optimal dosages and duration of NSAID treatment are of particular importance. The authors conclude that AMBENIUM® parenteral is an effective and safe therapeutic modality for gout. Its profile and risk/benefit ratio are regarded as “favorable” compared to other NSAIDs.
Keywords: gout, arthritis, pain, non-steroidal anti-inflammatory drugs, parenteral, efficacy, safety.
For citation: Vasilyuk V.B., Syraeva G.I., Faraponova M.V. Efficacy and safety of non-steroidal anti-inflammatory drugs for acute attack of gout. Russian Medical Inquiry. 2021;5(2):96–101. DOI: 10.32364/2587-6821-2021-5-2-96-101.
Введение
Эпидемиологические исследования последних лет демонстрируют увеличение уровня заболеваемости подагрой по всему миру. Распространенность подагры среди взрослого населения Европы составляет 0,9–2,5%, в США — 1,4–2,8% [1], в Российской Федерации — 0,31% по данным 2006 г. [2, 3]. Аналогичные данные были получены по результатам оценки заболеваемости во взрослой популяции в России, проведенной в 2018 г., — распространенность подагры составила 300 и 100 больных на 100 тыс. взрослого населения для мужчин и женщин соответственно [4].
Риск возникновения подагры напрямую зависит от уровня содержания мочевой кислоты в плазме крови. Бóльшая часть исследователей связывают положительную корреляцию установки диагноза «подагра» с такими провоцирующими факторами, как мужской пол, ожирение, изменение условий питания и малая двигательная активность [5]. Кроме того, также следует отметить, что современные методы диагностики позволяют установить диагноз на максимально ранних стадиях заболевания [6].
Отрицательная динамика эпидемиологической ситуации диктует необходимость оценки эффективности назначаемых лекарственных препаратов, главным образом из группы нестероидных противовоспалительных средств (НПВС), для минимизации потенциальных экономических затрат. Экономические затраты, в свою очередь, могут носить сочетанный характер, а именно: прямые потери, связанные с первичным назначением лекарственных средств, и косвенные потери, связанные с покрытием расходов в связи с нежелательными лекарственными реакциями (в т. ч. межлекарственными взаимодействиями) [7].
Этиология и патогенез
Подагра — хроническое заболевание, развивающееся в связи с воспалением в местах отложения кристаллов моноурата натрия (МУН) у лиц с гиперурикемией, обусловленной внешнесредовыми и/или генетическими факторами [8].
Формирование кристаллов МУН в основном обусловлено генетическими факторами и характеризуется снижением экскреции мочевой кислоты с мочой либо ее гиперпродукцией [9]. Формирование и отложение кристаллов МУН происходит преимущественно в хрящевой ткани и окружающих сухожилиях и связках, что запускает классический и альтернативный пути активации системы комплемента, фактора Хагемана и каскада кининов. Процесс фагоцитоза МУН происходит преимущественно с участием полиморфноядерных лейкоцитов, что сопровождается выделением целого ряда провоспалительных медиаторов: интерлейкинов ИЛ-1, -6, -8, кахексина и др. Совокупность описанных этиопатогенетических механизмов манифестирует массивной воспалительной реакцией, клиническое проявление которой представляет собой острый приступ подагры [10].
Критерии постановки диагноза
Патогенетические аспекты острого подагрического артрита обусловлены отложением и накоплением кристаллов уратов с образованием тофусов в мягких тканях, что в дальнейшем ведет к развитию таких состояний, как подагрическая нефропатия и нефролитиаз. Формирование тофусов является длительным рецидивирующим процессом и сопровождается выраженной клинической симптоматикой — повторяющимися атаками острого артрита [11].
При ведении пациентов с наличием ревматологических заболеваний со стороны медицинских служб различных стран мира была обозначена необходимость разработки единых подходов для диагностики и лечения данных состояний. В рамках этой задачи Американская коллегия ревматологов (American College of Rheumatology, ACR) и Европейская антиревматическая лига (European League Against Rheumatism, EULAR) приступили к разработке стандартизированных критериев диагностики (ACR-EULAR classification criteria for gout). Первая редакция классификационных критериев была одобрена ВОЗ в 2002 г. [12]. Документ проходит регулярный пересмотр ввиду появления новых данных об этиопатогенетических факторах, влияющих на течение ревматоидного артрита. Последняя редакция документа, одобренная в 2015 г. [13], сопоставима с федеральными клиническими рекомендациями, утвержденными на территории РФ в 2018 г. [14].
Классификационные критерии острого подагрического артрита, включенные в клинические рекомендации на территории Российской Федерации от 2018 г. [14], представлены ниже:
А. Наличие характерных кристаллов МУН в суставной жидкости.
Б. Наличие тофусов, содержание кристаллов мочевой кислоты в которых подтверждено химически или поляризационной микроскопией.
В. Наличие не менее чем 6 из 12 нижеперечисленных признаков:
более одной атаки острого артрита в анамнезе;
воспаление сустава достигает максимума в 1-й день
болезни;
моноартрит;
гиперемия кожи над пораженным суставом;
припухлость и боль в первом плюснефаланговом суставе;
одностороннее поражение первого плюснефалангового сустава;
одностороннее поражение суставов стопы;
подозрение на тофусы;
гиперурикемия;
асимметричный отек суставов;
субкортикальные кисты без эрозий (рентгенография);
отрицательные результаты при посеве синовиальной жидкости.
Для определения диагноза подагры достаточно выявления кристаллов МУН в синовиальной жидкости или тофусах (пункты А и Б рекомендаций); при невозможности указанных исследований диагноз должен быть обоснован наличием совокупности клинических, лабораторных и инструментальных признаков (пункт В рекомендаций) [14].
Лечение подагрического артрита
Для подбора оптимальной схемы терапии требуется комплексный подход, а именно данные анамнеза и физикального осмотра, оценка факторов риска (возраст, пол, наличие или отсутствие избыточной массы тела, сопутствующие заболевания) и данные лабораторно-инструментальных методов обследования (уровень мочевой кислоты, результаты рентгенографии) [15].
В соответствии с отечественными национальными клиническими рекомендациями по лечению подагры медицинские работники при лечении данного заболевания должны придерживаться алгоритма, представленного на рисунке 1.
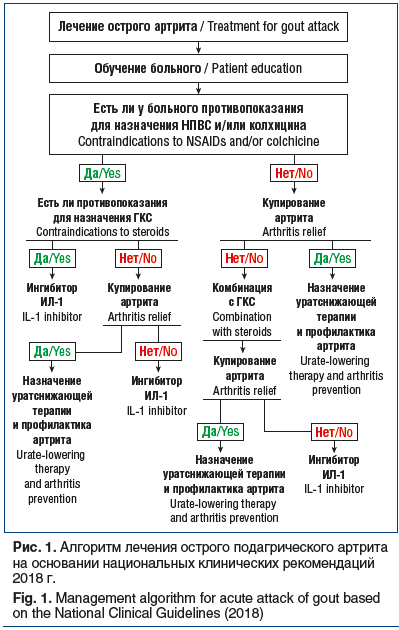
В качестве первой линии терапии принято рассматривать НПВС и/или колхицин [16].
Основной точкой приложения препаратов группы НВПС является ингибирование изофермента циклооксигеназы (ЦОГ). Существует два варианта данного изофермента — ЦОГ-1 и ЦОГ-2. Первый изофермент — ЦОГ-1 оказывает влияние на выработку простагландинов, медиаторов воспаления, образующихся при каскаде арахидоновой кислоты. Простагландины являются гормоноподобными веществами, влияющими на регуляцию кровяного давления, сокращение матки, целостность слизистых оболочек (в т. ч. ЖКТ), а также на систему гемостаза. Второй изофермент — ЦОГ-2 в нормальных условиях отсутствует, вырабатывается при наличии воспалительного процесса, образуется под действием тканевых факторов (цитокинов и др.) [17]. Классификация НПВС по селективности в отношении блокирования ЦОГ представлена в таблице 1 [18].
![Таблица 1. Классификация НПВС по селективности в отношении ингибирования ЦОГ [18] Table 1. Classification of NSAIDs based on the selectivity of COX inhibition [18] Таблица 1. Классификация НПВС по селективности в отношении ингибирования ЦОГ [18] Table 1. Classification of NSAIDs based on the selectivity of COX inhibition [18]](/upload/medialibrary/fd0/96-2.png)
Группа НПВС обладает широким фармакологическим профилем и включает в себя такие эффекты, как противовоспалительный, анальгезирующий, жаропонижающий, антиагрегантный и иммуносупрессивный.
Данные литературы демонстрируют, что наиболее эффективно оказывают противовоспалительный эффект следующие препараты группы НПВС: индометацин, диклофенак, фенилбутазон [19]. Указанные лекарственные препараты охватывают две фазы воспаления — экссудативную и пролиферативную. Таким образом, осуществляется склерозирующий и анальгезирующий эффекты соответственно. Степень анальгезии при этом достаточно высокая, в частности для диклофенака, кеторолака, кетопрофена, метамизола, фенилбутазона, что подтверждается данными обзоров литературы [20–22].
Вместе с тем применение НПВС ассоциировано с широким спектром нежелательных лекарственных реакций (НЛР). Согласно данным литературы наиболее частой НЛР является НПВС-гастропатия [23].
Авторами статьи была получена выгрузка НЛР из автоматизированной информационной системы Росздравнадзора (АИС РЗН) следующих препаратов: диклофенак, мелоксикам, фенилбутазон, ацетилсалициловая кислота, метамизол, целекоксиб, эторикоксиб — за период с 2010 по 2020 г. включительно. Количество зарегистрированных сообщений составило 8567. Полученные результаты обобщены в таблице 2.
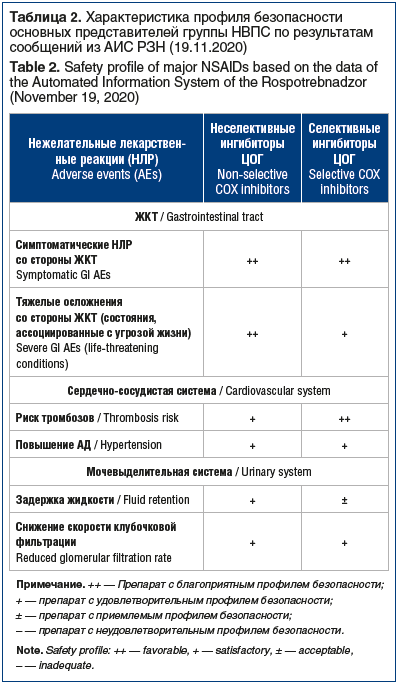
Полученные данные из АИС РЗН сопоставимы с результатами, представленными в других исследованиях. Так, в 2013 г. были опубликованы результаты ретроспективного когортного исследования по оценке рисков возникновения НЛР со стороны верхних отделов ЖКТ среди пациентов, принимающих НПВС (n=588 827), за период с 2001 по 2008 г. (Италия). У 3031 пациента были зарегистрированы случаи осложнений со стороны верхних отделов ЖКТ. Наиболее распространенным осложнением стало желудочно-кишечное кровотечение. Коэффициент частоты развития осложнений на 1000 пациенто-лет составил 3,8 (95% доверительный интервал 2,86, 3,76). При этом для лекарственных препаратов целекоксиб, нимесулид коэффициент частоты развития осложнений был <2, для напроксена, ибупрофена, диклофенака, эторикоксиба и мелоксикама данный показатель был в диапазоне от 2 до 5, а для кетопрофена, пироксикама и кеторолака — >5 [24].
В литературе имеются данные об использовании лекарственного препарата под торговым названием АМБЕНИУМ® (фенилбутазон + [лидокаин]) в качестве альтернативного НПВС. Препарат может применяться по следующим показаниям: острая боль, болевой синдром, обусловленный мышечно-скелетными расстройствами (в т. ч. при подагре, ревматоидном артрите и при анкилозирующем спондилите) [25].
Например, в исследовании, проведенном J. Boersma et al., была поставлена задача оценить ингибирующее влияние фенилбутазона на прогрессирование окостенения поясничного отдела позвоночника. Общая выборка пациентов составила 40 человек с анкилозирующим спондилитом, которые, в соответствии с дизайном исследования, были разделены на 3 группы: (А) непрерывное лечение фенилбутазоном; (B) лечение фенилбутазоном, но не в течение всего периода; (С) схема лечения без фенилбутазона. Наиболее быстрое прогрессирование окостенения произошло в группе С, в группе А формирование окостенения отсутствовало или было существенно замедленным. Таким образом, продемонстрировано, что на ранних (или относительно ранних) стадиях анкилозирующего спондилита терапия фенилбутазоном может полностью или в значительной степени контролировать оссификацию позвоночного столба [26]. Данные выводы также были подтверждены в ряде исследований [27].
Было проведено открытое сравнительное рандомизированное исследование в параллельных группах, в котором сравнивался анальгезирующий эффект препаратов АМБЕНИУМ® парентерал и диклофенак натрия у пациентов с острой болью в нижней части спины [28]. В исследовании приняли участие 164 пациента (возраст: от 18 до 72 лет), имеющих диагноз острой боли в нижней части спины, интенсивность которой составляла не менее 80 баллов по визуально-аналоговой шкале. Результаты проведенного исследования показали достаточную эффективность и безопасность препарата АМБЕНИУМ® парентерал в сравнении с диклофенаком натрия у этой категории пациентов. При этом анальгетический эффект после внутримышечного введения препарата АМБЕНИУМ® парентерал формировался через 1 ч и длился в течение 24 ч после введения.
Суммарно у пациентов, включенных в исследование, было зарегистрировано 14 НЛР, связанных с соматическим статусом: в 12 (86%) из 14 случаев зарегистрирована брадикардия неуточненная (код по МКБ — R00.1), в 1 (7%) случае — гиперемия (R23.2) и в 1 (7%) случае — головная боль (R51). При этом в группе применения препарата АМБЕНИУМ® парентерал было зарегистрировано 9 (64%) НЛР из 14 и в группе сравнения — 5 (36%) НЛР. Все НЛР были легкой степени, связь с препаратом была оценена как маловероятная, действия для купирования НЛР не предпринимались. В ходе вышеуказанного клинического исследования была показана хорошая общая и локальная переносимость препарата АМБЕНИУМ® парентерал.
Таким образом, резюмируя данные проведенных клинических исследований и литературных обзоров, профиль безопасности препарата АМБЕНИУМ® парентерал можно считать благоприятным. Кроме того, препарат АМБЕНИУМ® обладает относительно высокой биодоступностью, что во многом обусловлено его лекарственной формой.
Заключение
При назначении противоподагрической терапии со стороны лечащего врача требуется всесторонний анализ состояния пациента. НПВС при этом рассматриваются в качестве препаратов первой линии терапии острого подагрического артрита. Однако при назначении препаратов из группы НПВС следует принимать во внимание широкий спектр НЛР данного класса препаратов с оценкой риска их формирования и возможных межлекарственных взаимодействий, уделяя особое внимание подбору оптимальной дозировки и длительности терапии. Лекарственный препарат под торговым названием АМБЕНИУМ® (фенилбутазон + [лидокаин]), с учетом выраженного анальгетического эффекта и благоприятного профиля безопасности, может быть рекомендован в качестве альтернативного НПВС для купирования болевого синдрома при остром подагрическом артрите.
Благодарность
Редакция благодарит компанию «ЭйчБиЭм Фарма с.р.о.» за оказанную помощь в технической редактуре настоящей публикации.
Acknowledgement
Editorial Board is grateful to “HMB Pharma SRO” for the assistance in technical edition of this publication.
Сведения об авторах:
Василюк Василий Богданович — д.м.н., профессор кафедры токсикологии, экстремальной и водолазной медицины ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России; 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41; управляющий ООО «НИЦ Эко-безопасность»; 196143, Россия, г. Санкт-Петербург, просп. Юрия Гагарина, д. 65; ORCID iD 0000-0003-2503-4402.
Сыраева Гульнара Ислямовна — заместитель управляющего по качеству ООО «НИЦ Эко-безопасность»; 196143, Россия, г. Санкт-Петербург, просп. Юрия Гагарина, д. 65; очный аспирант кафедры клинической фармакологии и доказательной медицины, ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0001-6635-9786.
Фарапонова Мария Валерьевна — заместитель управляющего по научной работе ООО «НИЦ Эко-безопасность»; 196143, Россия, г. Санкт-Петербург, просп. Юрия Гагарина, д. 65; ORCID iD 0000-0003-4212-5453.
Контактная информация: Фарапонова Мария Валерьевна, e-mail: faraponova_mv@ecosafety.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 12.03.2021, поступила после рецензирования 25.03.2021, принята в печать 10.04.2021.
About the authors:
Vasiliy B. Vasilyuk — Doct. of Sci. (Med.), Professor of the Department of Toxicology, Extreme, and Diving Medicine, I.I. Mechnikov North-Western State Medical University; 41, Kirochnaya str., St. Petersburg, 191015, Russian Federation; Manager, LLC “Research Center Eco-safety”; 65, Yu. Gagarin av., St. Petersburg, 196143, Russian Federation; ORCID iD 0000-0003-2503-4402.
Gulnara I. Syraeva — Deputy Manager for Quality, LLC “Research Center Eco-safety”; 65, Yu. Gagarin av.,
St. Petersburg, 196143, Russian Federation; postgraduate of the Department of Clinical Pharmacology and Evidence-Based Medicine, I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0001-6635-9786.
Mariya V. Faraponova — Deputy Manager for Scientific Work, LLC “Research Center Eco-safety”; 65, Yu. Gagarin av.,
St. Petersburg, 196143, Russian Federation; ORCID iD 0000-0003-4212-5453.
Contact information: Mariya V. Faraponova, e-mail: faraponova_mv@ecosafety.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 12.03.2021, revised 25.03.2021, accepted 10.04.2021.
2. Теплякова О.В., Сарапулова А.В., Попов А.А. Качество ведения пациентов с подагрой в реальной клинической практике. Современная ревматология. 2019;13(1):80–85. DOI: 10.14412/1996-7012-2019-1-80-85.
3. Кушнаренко Н.Н., Мишко М.Ю., Медведев Т.А. Полиморфизм генов фолатного цикла у больных подагрой в популяции русских Забайкальского края. Сибирский журнал клинической и экспериментальной медицины. 2020;35(1):142–150. DOI: 10.29001/2073-8552-2020-35-1-142-150.
4. Галушко Е.А., Насонов Е.Л. Распространенность ревматических заболеваний в России. Альманах клинической медицины. 2018;46(1):32–39. DOI: 10.18786/2072-0505-2018-46-1-32-39.
5. Паневин Т.С., Елисеев М.С., Шестакова М.В. Влияние хирургического лечения ожирения на пуриновый обмен и подагру. Ожирение и метаболизм. 2020;17(2):138–146. DOI: 10.14341/omet12109.
6. Изотова А.В., Цветкова В.А., Городничев К.И. и др. Исследование подагры у мужчин. Фундаментальная наука в современной медицине. Минск: БГМУ; 2020.
7. Сыраева Г.И., Колбин А.С., Матвеев А.В., Панежина В.С. Сравнительный обзор методологий оценки стоимости нежелательных лекарственных реакций в Российской Федерации и Бразилии. Фармация и фармакология. 2020;8(5):336–344. DOI: 10.19163/2307-9266-2020-8-5-336-344.
8. Новикова А.М., Елисеев М.С. Место фебуксостата в терапии подагры. Современная ревматология. 2020;14(3):150–155. DOI: 10.14412/1996-7012-2020-3-150-155.
9. Атаханова Л.Е., Цурко В.В., Булева И.М. и др. Подагра: от этиологии и патогенеза к диагностике и рациональной фармакотерапии. Современная ревматология. 2007;1(1):13–18. DOI: 10.14412/1996-7012-2007-433.
10. Полстяной А.А. Современные представления об этиологии гиперурикемии как патогенетического фактора развития подагры. Актуальні проблеми сучасної медицини: Вісник української медичної стоматологічної академії. 2016;2(54):311–316.
11. Мухин Н.А., Мухин Н.А. Подагра: лики болезни. Современная ревматология. 2007;1(1):5–9. DOI: 10.14412/1996-7012-2007-431.
12. Neogi T., Jansen T.L.T.A., Dalbeth N. et al. Gout classification criteria: an American College of Rheumatology/European League Against Rheumatism collaborative initiative. Annals of the Rheumatic Diseases. 2015;74:1789–1798. DOI: 10.1136/annrheumdis-2015-208237.
13. Елисеев М.С. Новые международные рекомендации по диагностике и лечению подагры. Научно-практическая ревматология. 2014;52(2):141–146. DOI: 10.14412/1995-4484-2014-141-146.
14. Клинические рекомендации «Подагра» (утв. Минздравом России), 2018. (Электронный ресурс.) URL: https://legalacts.ru/doc/klinicheskie-rekomendatsii-podagra-utv-minzdravom-rossii/ (дата обращения: 02.03.2021).
15. Христуленко А.Л., Гнилицкая В.Б., Здиховская И.И. и др. Подагра — новое в тактике ведения и лечении. Архив клинической и экспериментальной медицины. 2019;28(3):267–271.
16. Лукьянчук Е. Эффективность фебуксостата в качестве первой линии терапии гиперурикемии, а также в случае неудачи при применении аллопуринола. Український ревматологічний журнал. 2016;2(64):62–65.
17. Страчунский Л.С. Нестероидные противовоспалительные средства. Методическое пособие. Смоленск: СГМУ; 2008.
18. Василевский И.В. Клинико-фармакологическая гетерогенность нестероидных противовоспалительных лекарственных средств: фокус на ацеклофенак. Медицинские новости. 2014;7:20–26.
19. Лесная О.А. Нестероидные противовоспалительные препараты: более 30 лет на пике актуальности. Трудный пациент. 2018;11(16):45–49.
20. Василюк В.Б., Фарапонова М.В., Сыраева Г.И. Анализ финансовых затрат медицинской организации на ведение нежелательных лекарственных реакций при проведении клинических исследований лекарственных препаратов с МНН: эторикоксиб. MedLine. 2020;21:206–223.
21. Taylor R.S., Fotopoulos G., Maibach H. Профиль безопасности препаратов для наружного применения, содержащих диклофенак: метаанализ слепых рандомизированных контролируемых исследований при лечении заболеваний опорно–двигательного аппарата. РМЖ. 2011;10(19):656–671.
22. Зырянов С.К., Нельга О.Н., Белоусов Ю.Б. Безопасность фармакотерапии боли: современное состояние проблемы. Трудный пациент. 2007;3:54–57.
23. Ивашкин В.Т., Шептулин А.А., Маев И.В. и др. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению язвенной болезни. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2016;26(6):40–54. DOI: 10.22416/1382-4376-2016-26-6-40-54.
24. Castellsague J., Pisa F., Rosolen V. et al. Risk of upper gastrointestinal complications in a cohort of users of nimesulide and other nonsteroidal anti-inflammatory drugs in Friuli Venezia Giulia, Italy. Pharmacoepidemiol Drug Saf. 2013;22(4):365–375. DOI: 10.1002/pds.3385.
25. Borges R.S., Palheta I.C., Ota S.S.B. et al. Toward of Safer Phenylbutazone Derivatives by Exploration of Toxicity Mechanism. Molecules. 2019;24(1):143. DOI: 10.3390/molecules24010143.
26. Baltus J.A., Boersma J.W., Hartman A.P., Vandenbroucke J.P. The occurrence of malignancies in patients with rheumatoid arthritis treated with cyclophosphamide: a controlled retrospective follow-up. Annals of the Rheumatic Diseases. 1983;42(4):368–373. DOI: 10.1136/ard.42.4.368.
27. Grahame R., Calin A. A controlled trial of ‘Froben’ (flurbiprofen) in ankylosing spondylitis — comparison with phenylbutazone. Current Medical Research and Opinion. 2008;(s4):42–44. DOI: 10.1185/03007997509111989.
28. Василюк В.Б., Фарапонова М.В., Сыраева Г.И. Выбор НПВС для лечения острой и хронической боли у пациентов с ревматоидным артритом на амбулаторно-поликлиническом этапе. РМЖ. 2020;12:30–34.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Распечатать

