Стеатогепатоз и стеатогепатит у детей с ожирением: терапевтические подходы
Д.м.н. А.А. Звягин, Н.Ю. Фатеева, к.м.н. Т.В. Чубаров, д.м.н. О.А. Жданова
ФГБОУ ВО ВГМУ им. Н.Н. Бурденко Минздрава России, Воронеж
В статье представлены данные о терапии неалкогольной жировой болезни печени (НАЖБП) у детей с ожирением, у которых частота этого заболевания достигает 77%. В основе НАЖБП лежит накопление жира в гепатоцитах и разрушение печеночных клеток с прогрессирующим воспалением, апоптозом и фиброзом. Эта патология имеет три формы/стадии: стеатоз, стеатогепатит, фиброз. Стеатоз и стеатогепатит обратимы под воздействием комплексной терапии. Так как указанные патологические состояния в большинстве случаев ассоциированы с избыточной массой тела или ожирением, лечение детей с НАЖБП включает как немедикаментозные методы (модификация образа жизни, диетотерапия, физическая нагрузка), так и применение фармакологических препаратов разных групп и биологически активных веществ. Наиболее изученными препаратами, использование которых возможно при неалкогольном стеатогепатозе и стеатогепатите, являются препараты урсодезоксихолевой кислоты. Гепатопротективное, желчегонное, холелитолитическое и гипохолестеринемическое действие в сочетании с диетотерапией и физической активностью делает эти препараты перспективными в терапии различных форм НАЖБП.
Ключевые слова: стеатогепатоз, стеатогепатит, неалкогольная жировая болезнь печени, урсодезоксихолевая кислота, лечение, дети.
Для цитирования: Звягин А.А., Фатеева Н.Ю., Чубаров Т.В., Жданова О.А. Стеатогепатоз и стеатогепатит у детей с ожирением: терапевтические подходы. РМЖ. Медицинское обозрение. 2022;30(3):9-12.
Steatohepatosis and steatohepatitis in overweight children: therapeutic methods
A.A. Zvyagin, N.Yu. Fateeva, T.V. Chubarov, O.A. Zhdanova
Voronezh State Medical University named after N.N. Burdenko, Voronezh
The article presents data on the treatment of non-alcoholic fatty liver disease (NAFLD), commonly presented in overweight children (up to 77%). This pathology is based on the lipid accumulation in hepatocytes and the cell death in the liver with progressive inflammation, apoptosis and fibrosis. NAFLD includes several forms: steatosis, steatohepatitis, fibrosis. Steatosis and steatohepatitis are reversible stages in complex therapy. Since these pathological conditions in most cases are associated with overweight or obesity, the treatment of children with this pathology includes both non-drug methods (lifestyle modification, diet therapy, physical activity) and the use of different pharmacological drugs, biologically active substances with antioxidant effects (omega-3, omega-6 fatty acids, α-tocopherol, docosahexagenoic acid, choline, astaxanthin). The best known drugs for non-alcoholic steatohepatosis and steatohepatitis are preparations with ursodeoxycholic acid (UDCA). These preparations can become a promising group to treat various NAFLD forms because of their hepatoprotective, choleretic, cholelitholytic, hypocholesterolemic effect in combination with diet therapy and physical activity.
Keywords: steatohepatosis, steatohepatitis, non-alcoholic fatty liver disease, children, ursodeoxycholic acid, treatment, children.
For citation: Zvyagin A.A., Fateeva N.Yu., Chubarov T.V., Zhdanova O.A. Steatohepatosis and steatohepatitis in overweight children: therapeutic methods. RMJ. 2022;3:–12.
Введение
Неалкогольный стеатогепатоз (НАС) и стеатогепатит (НАСГ) представляют собой формы/стадии неалкогольной жировой болезни печени (НАЖБП), которые при прогрессировании патологических процессов могут приводить к фиброзу, циррозу печени, а у части пациентов и к гепатоцеллюлярной карциноме. НАС характеризуется накоплением капель жира, жировых включений в гепатоцитах (стеатоз), а НАСГ — наличием участков воспаления, жировой инфильтрации печени, а также некротическими изменениями в гепатоцитах, а в некоторых случаях баллонной дегенерацией гепатоцитов и фиброзом. Именно в этих формах проявляется у детей и подростков НАЖБП — хроническое заболевание печени, возникающее в результате чрезмерного накопления жира в печени у пациентов с избыточной массой тела и ожирением [1]. Со стеатофиброзом в повседневной педиатрической практике врачи встречаются редко, так как, во-первых, развитие его требует времени и он формируется уже после перехода подростков под наблюдение во взрослых поликлиниках, а во-вторых, в практическом здравоохранении у детей почти не используются современные методы диагностики фибротических изменений печени (МРТ, КТ, эластография, специальные биохимические тесты) [2, 3]. Однако в исследованиях с применением фиброэластографии были выявлены признаки фиброза (повышение жесткости печени >5,5 кПа) у 51% детей с ожирением (в том числе с НАС и НАСГ) и отсутствие таковых у детей без ожирения в контрольной группе [4].
Эпидемиология НАЖБП
Эпидемиологические данные показывают, что НАЖБП весьма распространена среди детского населения и имеется у 3–10% современных детей и подростков в развитых странах. У детей с ожирением частота НАЖБП достигает 77%, а НАСГ — 12–26% [5]. Проведенные в последние годы российскими учеными исследования [6, 7] показали высокую частоту встречаемости избыточной массы тела и ожирения у детей в нашей стране (см. таблицу), что, соответственно, означает и высокую частоту НАС и НАСГ.
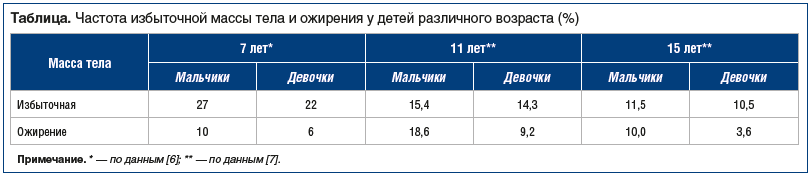
С каждым годом распространенность НАЖБП растет, так как все больше детей и подростков страдают избыточной массой тела и ожирением, в связи с этим актуальным становится вопрос терапии и профилактики НАС и НАСГ.
Патогенез НАЖБП
Накопление липидов в печени происходит вследствие нескольких патологических процессов: избыточного поступления жира в гепатоциты, активации накопления свободных жирных кислот в печени из белой жировой ткани, а также увеличения липогенеза de novo за счет гиперинсулинемии и избыточного поступления углеводов [8]. Накопление в гепатоцитах свободных жирных кислот и их метаболитов в результате указанных процессов сопровождается липотоксичностью [8], вызывающей оксидативный стресс. В результате этого происходит повреждение внутриклеточных структур (эндоплазматического ретикулума, митохондрий), что запускает каскад реакций с высвобождением гепатоцитами активных форм кислорода, фактора некроза опухоли, интерлейкинов 6, 10, 18, интерферона гамма и привлечением иммунных клеток (плазмоцитов, лимфоцитов) [8]. В результате воздействия этих биологически активных веществ разрушаются гепатоциты, прогрессирует воспаление, развивается апоптоз — запрограммированная гибель клеток и происходит ремоделирование ткани печени с развитием фиброза при отложении коллагена активированными звездчатыми клетками [8].
Лечение НАЖБП
Основным международным документом, регламентирующим лечение НАЖБП, являются рекомендации Североамериканского общества детских гастроэнтерологов, гепатологов и нутрициологов (NASPHGAN) 2017 г. [1], отечественные рекомендации в настоящее время отсутствуют. В рекомендациях NASPHGAN нет дифференцированного подхода к терапии разных форм НАЖБП, соответственно, рекомендации применяются для лечения как НАС, так и НАСГ. Основой терапии является изменение образа жизни, а именно соблюдение диеты, увеличение физической активности, ограничение по времени использования гаджетов (менее 2 ч в день). Фактически это рекомендации по лечению ожирения. В этой связи отметим наличие российских клинических рекомендаций Общества эндокринологов по ожирению у детей 2021 г. [9], основные положения которых могут и должны применяться у детей с ожирением и НАС или НАСГ. Важнейшим аспектом успешного лечения является формирование мотивации как у ребенка, так и у его родителей, направленной на снижение массы тела. Наличие поражения печени, особенно НАСГ, по нашему мнению, должно стать дополнительным мотивирующим фактором.
Диетотерапия [1, 9] предполагает нормокалорийный рацион по возрасту с достаточным количеством нутриентов, составленный с учетом вкусовых предпочтений ребенка. Все виды диет (в том числе гипокалорийная) служат альтернативным вариантом терапии и применяются по показаниям. Важнейшее условие диетотерапии — изменение пищевого поведения ребенка и в целом его семьи. Конкретные рекомендации сводятся к следующему:
ограничение сладких напитков: запрет (потребление не более 1 порции не чаще чем 1 раз в неделю) не только газированных сладких напитков, но и соков, компотов, морсов с разрешением приема питьевой воды по желанию ребенка;
ограничение сладких фруктов до 1 порции (100 г)
в день;
как минимум 4-разовое питание, обязательный зав-
трак;
запрет сладких молочных продуктов;
контроль размера/количества порций. Для наглядности желательного размера порций в настоящее время широко применяются «тарелки питания». Если ребенок хочет съесть вторую порцию обеда/ужина — разрешить через 20 мин после первой при условии регулярного (как минимум 4-разового приема пищи в день);
обогащение рациона овощами (для детей младшего возраста — 300 г, подростков — 400 г в день, с ограничением применения в таких количествах картофеля как единственного овоща), пищевыми волокнами, цельнозерновыми продуктами;
учить детей есть медленно, без компьютерного/телевизионного/мобильного сопровождения.
Физические нагрузки [10] умеренной и высокой интенсивности рекомендуются детям и подросткам 6–17 лет с ожирением и избыточной массой тела ежедневно в течение не менее чем 60 мин, а нагрузки высокой интенсивности — не менее 3 раз в неделю. Могут использоваться различные виды аэробных тренировок: дозированная ходьба, бег, плавание, аэробные танцы и гимнастика, работа на велоэргометре, бег на беговой дорожке и др. Для профилактики гиподинамии рекомендовано сокращение неактивного времяпрепровождения перед экраном телевизора, монитором компьютера до 2 ч в день или меньше.
M. Medrano et al. [11] в перекрестном исследовании установили, что более низкое процентное содержание печеночного жира (оценивалось по МРТ-исследованию) и менее выраженные биохимические изменения (соотношение АсАТ/АлАТ, γ-глутамилтранспептидаза, HOMA-IR, соотношение триглицериды/ЛПВП) наблюдались в группе детей с кардиореспираторными тренировками [11]. В обзоре [10] представлены более подробные данные исследований эффективности физической активности при НАЖБП, в том числе у детей, даже в тех случаях, когда масса тела не снижалась.
Вопросы о применении лекарственных препаратов и пищевых функциональных продуктов при поражении печени у детей с ожирением обсуждаются уже длительное время, однако единых рекомендаций по лечению у детей НАЖБП и отдельных ее форм не существует. NASPHGAN не рекомендует применение медикаментов и нутрицевтиков. В Российской Федерации применение медикаментов (гепатопротекторов), в официальных инструкциях которых зарегистрированы показания и возрастные нормы, относящиеся к НАС и НАСГ, разрешено. Это препараты урсодезоксихолевой кислоты (УДХК) и эссенциальные фосфолипиды. В настоящее время наибольшее количество исследований посвящено применению УДХК у взрослых, исследований же применения УДХК в педиатрической популяции значительно меньше [12, 13].
Желчные кислоты, такие как УДХК, играют важную роль в патогенезе НАЖБП, регулируя уровень белка, связывающего стероидные регуляторные элементы (SREBP). Все больше доказательств указывает на то, что сигнальный путь AKT/mTOR/SREBP-1 служит ключевым в регуляции метаболизма липидов в клетках печени, УДХК регулирует этот путь для улучшения липидного обмена в печени [14]. В эксперименте УДХК оказывала благоприятное влияние на стеатоз печени у крыс с НАЖБП путем активации AMP-активированной протеинкиназы. УДХК ингибирует апоптоз и индуцирует аутофагию, влияя на взаимодействие комплекса Bcl-2/Beclin-1 и Bcl-2/Bax, что указывает на УДХК как перспективное средство для лечения НАЖБП [15]. Таким образом, УДХК влияет на ведущую причину НАЖБП — отложение жира в гепатоцитах, активируя аутофагию и экзоцитоз, что ведет к выведению жира из клеток печени. Важно отметить, что такой эффект достигается и при соблюдении диеты.
В рандомизированном контролируемом фармакодинамическом исследовании M. Mueller et al. [16] проанализировали образцы сыворотки, печени и белой жировой ткани от 40 пациентов с ожирением, получавших УДХК (20 мг/кг/сут) и не получавших лечения за 3 нед. до бариатрической операции. Краткосрочный прием УДХК стимулировал синтез желчных кислот за счет снижения циркулирующего фактора роста фибробластов-19 и активации рецептора фарнезоида X (FXR), что приводило к индукции 7α-гидроксилазы холестерина с последующим повышением концентрации С4 и 7α-гидроксихолестерина. Усиленное образование желчных кислот истощает липопротеины низкой плотности (ЛПНП) с последующей активацией ключевого фермента синтеза холестерина 3-гидрокси-3-метилглутарил-КоА-редуктазы. Ингибированные антилипогенные эффекты FXR индуцировали липогенную десатуразу стеароил-КоА (SCD) в печени, тем самым увеличивая содержание триглицеридов в печени. Кроме того, индуцированная активность липогенной десатуразы стеароил-КоА в белой жировой ткани сдвинула метаболизм липидов белой жировой ткани в сторону образования менее токсичных и более мононенасыщенных жирных кислот, таких как олеиновая кислота [16]. УДХК может снижать содержание холестерина, уменьшая его биосинтез за счет подавления активности гидроксиметилглутарил-коэнзим-А-редуктазы и всасывания холестерина с пищей [17]. УДХК обладает и собственным гиполипидемическим эффектом, благодаря которому также снижается уровень общего холестерина и ЛПНП [18]. При монотерапии УДХК в дозе 12–15 мг/кг/сут на протяжении 2 лет достигается снижение активности АлАТ по сравнению с эффектом от плацебо, комбинированная схема лечения с витамином Е приводит к снижению гистологической активности патологического процесса [19].
В настоящее время на фармацевтическом рынке имеется несколько препаратов УДХК, один из них — Урсосан® (PRO.MED.CS.Praha a.s.). Важно, что препарат не имеет возрастных ограничений и может применяться при всех формах НАЖБП. В официальной инструкции по медицинскому применению препарата в показаниях указана НАЖБП, в том числе НАСГ. Препарат выпускается в двух формах, в виде капсул по 0,25 г и таблеток по 0,5 г, покрытых пленочной оболочкой, что делает удобным дозирование для детей разного возраста с повышенной массой тела. Урсосан® использовался при проведении ряда исследований на взрослых пациентах и показал свою эффективность. В международном несравнительном многоцентровом исследовании УСПЕХ, проведенном в условиях реальной клинической практики, было показано, что у пациентов, получающих Урсосан® в дозе 15 мг/кг/сут, через 24 нед. наблюдается статистически значимое снижение показателей цитолиза, холестаза, общего холестерина, триглицеридов и отсутствует прогрессирование фиброза. Особо следует отметить, что на фоне монотерапии данным препаратом наблюдалось достоверное снижение индекса стеатоза печени (fatty liver index, FLI), что свидетельствует об уменьшении содержания жира в печеночной ткани, при этом масса тела у пациентов достоверно не менялась. Это подтверждает способность УДХК выводить жир из печени [20]. В исследовании РАКУРС показано, что Урсосан® уменьшает гепатотоксические эффекты статинов и усиливает их гиполипидемическое действие при совместном применении [21]. Таким образом, Урсосан®, обладая гепатопротективным, желчегонным, холелитолитическим, гипохолестеринемическим действием, является эффективным средством патогенетической терапии НАЖБП и имеет все основания для применения у детей и подростков с данной патологией.
Эссенциальные фосфолипиды также применяются для терапии НАЖБП. В РФ препараты эссенциальных фосфолипидов, согласно официальной инструкции, показаны к применению при жировой дистрофии и дегенерации печени, однако существуют возрастные ограничения (с 3, 12 лет). Важно подчеркнуть, что исследования эффективности гепатопротекторов при НАЖБП у детей, отвечающие современным требованиям доказательной медицины, не проводились. Исследования на взрослых свидетельствуют об эффективности фосфолипидов, однако эти исследования имели наблюдательный характер [22]. По данным S.V. Feysa et al. [23], при включении в комплексное лечение эссенциальных фосфолипидов и омега-3 полиненасыщенных жирных кислот значимое снижение активности АлАТ и АсАТ произошло только под влиянием комбинации эссенциальных фосфолипидов и омега-3 полиненасыщенных жирных кислот.
Одним из направлений оптимизации терапии жирового повреждения печени, разрабатываемым в настоящее время, является использование биологически активных веществ, обладающих антиоксидантным действием. Внимание к таким препаратам обусловлено, во-первых, патогенетическим значением оксидативного стресса, развивающегося в результате липотоксичности накапливаемых в гепатоцитах свободных жирных кислот, а во-вторых, необходимостью длительной терапии в течение нескольких месяцев и даже лет. Поэтому предпочтение отдано биологически активным добавкам к пище. В качестве антиоксидантов для терапии НАЖБП в исследованиях используются омега-3, омега-6 полиненасыщенные жирные кислоты, α-токоферол, докозагексаеновая кислота, холин, астаксантин. Отмечается, что на фоне диеты, физической активности и применения указанных компонентов у больных снижаются уровни АлАТ, триглицеридов, ЛПНП, глюкозы, частота стеатоза, инсулинорезистентность и некоторые другие [24–26].
Заключение
Неалкогольный стеатогепатоз и стеатогепатит довольно часто встречаются у детей с ожирением. При прогрессировании патологического процесса НАЖБП приводит к формированию фиброзных изменений в печени, в том числе уже в детском возрасте. Часто наблюдаемое у детей отсутствие мотивации для снижения массы тела с помощью диеты и физической активности, а также приверженности длительному выполнению рекомендаций врача является фактором прогрессирования как ожирения, так и НАЖБП. Выявление у ребенка НАСГ должно стать для него и для его родителей дополнительным стимулом к выполнению рекомендаций по диетическим ограничениям и физической активности. Применение препаратов, снижающих воспалительные изменения в печени, регулирующих метаболизм липидов в гепатоцитах и обладающих антифибротическим действием, служит важным дополнением к терапии НАЖБП. В настоящее время наибольшую доказательную базу по эффективности при различных формах НАЖБП имеет УДХК, применение которой возможно у детей и подростков. На сегодняшний день УДХК — единственное лекарственное средство, влияющее на ведущую причину НАЖБП — отложение жира в гепатоцитах, путем выведения жира через активацию аутофагии и экзоцитоза. Препараты Урсосан® и Урсосан® форте в полной мере отвечают современным требованиям, которые предъявляются в педиатрической практике, они безопасны при длительном применении и эффективны для купирования НАСГ и предотвращения стеатофиброза.
Благодарность
Редакция благодарит компанию PRO.MED.CS.Praha a.s. за помощь в технической редактуре настоящей публикации.
2. Vajro P., Lenta S., Socha P. et al. Diagnosis of nonalcoholic fatty liver disease in children and adolescents: position paper of the ESPGHAN Hepatology Committee. J Pediatr Gastroenterol Nutr. 2012;54(5):700–713. DOI: 10.1097/MPG.0b013e318252a13f.
3. Звягин А.А., Фатеева Н.Ю., Чубаров Т.В., Жданова О.А. Стеатогепатит у детей с ожирением. Вопросы современной педиатрии. 2021;20(3):238–244. [Zvyagin A.A., Fateeva N.Yu., Chubarov T.V., Zhdanova O.A. Steatohepatitis in children with obesity. Current pediatrics. 2021;20(3):238–244 (in Russ.)]. DOI: 10.15690/vsp.v20i3/2275.
4. Kwon Y.D., Ko K.O., Lim J.W. et al. Usefulness of Transient Elastography for Non-Invasive Diagnosis of Liver Fibrosis in Pediatric Non-Alcoholic Steatohepatitis. J Korean Med Sci. 2019;34(23):e165. DOI: 10.3346/jkms.2019.34.e165.
5. Рекомендации по диагностике, лечению и профилактике ожирения у детей и подростков. М.: Практика; 2015. [Recommendations for the diagnosis, treatment and prevention of obesity in children and adolescents. M.: Praktika; 2015 (in Russ.)].
6. Rito A.I., Buoncristiano M., Spinelli A. et al. Association between Characteristics at Birth, Breastfeeding and Obesity in 22 Countries: The WHO European Childhood Obesity Surveillance Initiative — COSI 2015/2017. Obes Facts. 2019;12(2):226–243. DOI: 10.1159/000500425.
7. Намазова-Баранова Л.С., Елецкая К.А., Кайтукова Е.В. и др. Оценка физического развития детей среднего и старшего школьного возраста: анализ результатов одномоментного исследования. Педиатрическая фармакология. 2018;15(4):333–342. [Namazova-Baranova L.S., Yeletskaya K.A., Kaitukova E.V. et al. Assessment of the physical development of children of middle and high school age: analysis of the results of a single-stage study. Pediatric pharmacology. 2018;15(4):333–342 (in Russ.)]. DOI: 10.15690/pf.v15i4.1948.
8. Neuschwander-Tetri BA. Non-alcoholic fatty liver disease. BMC Med. 2017;15(1):45. DOI: 10.1186/s12916-017-0806-8.
9. Петеркова В.А., Безлепкина О.Б., Болотова Н.В. и др. Клинические рекомендации «Ожирение у детей». Проблемы эндокринологии. 2021;67(5):67–83. [Peterkova V.A., Bezlepkina O.B., Bolotova N.V. et al. Clinical guidelines "Obesity in children". Problems of Endocrinology. 2021;67(5):67–83 (in Russ.)]. DOI: 10.14341/probl12802.
10. Павловская Е.В., Строкова Т.В., Шавкина М.И. и др. Роль физической активности в лечении ожирения у детей и подростков. Вопросы детской диетологии. 2019;17(2):27–35. [Pavlovskaya E.V., Strokova T.V., Shavkina M.I. et al. The role of physical activity in the treatment of obesity in children and adolescents. Pediatric nutrition. 2019;17(2):27–35 (in Russ.)]. DOI: 10.20953/1727-5784-2019-2-27-35.
11. Medrano M., Arenaza L., Migueles J.H. et al. Associations of physical activity and fitness with hepatic steatosis, liver enzymes, and insulin resistance in children with over-weight/obesity. Pediatr Diabetes. 2020;21(4):565–574. DOI: 10.1111/pedi.13011.
12. Vajro P., Paolella G., Pierri L., D’Aniello R. Treatment of NASH with ursodeox-ycholic acid: pros and cons. More information in children. Clin Res Hepatol Gastroenterol. 2013;37(3):e93–94. DOI: 10.1016/j.clinre.2013.02.012.
13. Hu J., Hong W., Yao K.N. et al. Ursodeoxycholic acid ameliorates hepatic lipid metabolism in LO2 cells by regulating the AKT/mTOR/SREBP-1 signaling pathway. World J Gastroenterol. 2019;25(12):1492–1501. DOI: 10.3748/wjg.v25.i12.1492.
14. Hu J., Hong W., Yao K.N. et al. Ursodeoxycholic acid ameliorates hepatic lipid metabolism in LO2 cells by regulating the AKT/mTOR/SREBP-1 signaling pathway. World J Gastroenterol. 2019;25(12):1492–1501. DOI: 10.3748/wjg.v25.i12.1492.
15. Wu P., Zhao J., Guo Y. et al. Ursodeoxycholic acid alleviates nonalcoholic fatty liver disease by inhibiting apoptosis and improving autophagy via activating AMPK. Biochem Biophys Res Commun. 2020;529(3):834–838. DOI: 10.1016/j.bbrc.2020.05.128.
16. Mueller M., Thorell A., Claudel T. et al. Ursodeoxycholic acid exerts farnesoid X receptor-antagonistic effects on bile acid and lipid metabolism in morbid obesity. J Hepatol. 2015;62(6):1398–1404. DOI: 10.1016/j.jhep.2014.12.034.
17. Maton P.N., Ellis H.J., Higgins M.J., Dowling R.H. Hepatic HMGCoA reductase in human cholelithiasis: effects of chenodeoxycholic and ursodeoxycholic acids. Eur J Clin Invest. 1980;10(4):325–332. DOI: 10.1111/j.1365-2362.1980.tb00040.x.
18. Simental-Mendía L.E., Simental-Mendía M., Sánchez-García A. et al. Impact of ursodeoxycholic acid on circulating lipid concentrations: a systematic review and meta-analysis of randomized placebo-controlled trials. Lipids Health Dis. 2019;18(1):88. DOI: 10.1186/s12944-019-1041-4.
19. Dufour J.F., Oneta C.M., Gonvers J.J. et al. Randomized placebo-controlled trial of ursodeoxycholic acid with vitamin E in nonalcoholic steatohepatitis. Clin Gastroenterol Hepatol. 2006;4(12):1537–1543. DOI: 10.1016/j.cgh.2006.09.025.
20. Nadinskaia M., Maevskaya M., Ivashkin V. et al. Ursodeoxycholic acid as a means of pre-venting atherosclerosis, steatosis and liver fibrosis in patients with nonalcoholic fatty liver disease. World J Gastroenterol. 2021;27(10):959–975. DOI: 10.3748/wjg.v27.i10.959.
21. Марцевич С.Ю., Кутишенко Н.П., Дроздова Л.Ю. и др. Исследование РАКУРС: повышение эффективности и безопасности терапии статинами у больных с заболеваниями печени, желчного пузыря и/или желчевыводящих путей с помощью урсодезоксихолевой кислоты. Терапевтический архив. 2014;86(12):48–52. [Martsevich S.Yu., Kutishenko N.P., Drozdova L.Yu. et al. Ursodeoxycholic acid-enhanced efficiency and safety of statin therapy in patients with liver, gallbladder, and/or biliary tract diseases: The RACURS study. Terapevticheskii Arkhiv. 2014;86(12):48–52 (in Russ.)]. DOI: 10.17116/terarkh2014861248-52.
22. Ivashkin V.T., Maevskaya M.V., Shirokova E.N. et al. Correlation of Objective End-points and Subjective Patient-Reported Outcomes in NAFLD Treatment with Essential Phospholipids: Real-World Data Based on Pooled Analysis of Observational Studies. Drugs Real World Outcomes. 2021;8(3):369–382. DOI: 10.1007/s40801-021-00250-x.
23. Feysa S.V., Rudakova S.O. Influence of complex treatment on biochemical blood parameters of patients with non-alcoholic fatty liver disease and concomitant pre-diabetes. Wiad Lek. 2021;74(4):986–991. PMID: 34156017.
24. Caro-Sabido E.A., Larrosa-Haro A. Efficacy of dietary intervention and physical activity in children and adolescents with nonalcoholic fatty liver disease associated with obesity: A scoping review. Rev Gastroenterol Mex. 2019;84(2):185–194. DOI: 10.1016/j.rgmx.2019.02.001.
25. Pervez M.A., Khan D.A., Ijaz A., Khan S. Effects of Delta-tocotrienol Supplementation on Liver Enzymes, Inflammation, Oxidative stress and Hepatic Steatosis in Patients with Nonalcoholic Fatty Liver Disease. Turk J Gastroenterol. 2018;29(2):170–176. DOI: 10.5152/tjg.2018.17297.
26. Spahis S., Alvarez F., Ahmed N. et al. Non-alcoholic fatty liver disease severity and metabolic complications in obese children: impact of omega-3 fatty acids. J Nutr Biochem. 2018;58:28–36. DOI: 10.1016/j.jnutbio.2018.03.025.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
