Опыт проведения пассивной иммунизации против респираторно-синцитиальной вирусной инфекции — двенадцатый сезон
DOI: 10.32364/2587-6821-2022-6-11-659-666
Ведущая роль респираторно-синцитиального вируса (РСВ) в развитии респираторных вирусных инфекций у детей раннего возраста определяет актуальность исследований, направленных на создание средств эффективной защиты детей, особенно из групп высокого риска тяжелого течения РСВ-инфекции. Несмотря на непрекращающуюся разработку вакцин против РСВ, единственным надежным способом профилактики РСВ-инфекции у детей остается пассивная иммунизация препаратом паливизумаб. В статье представлены данные о проведении пассивной иммунизации в г. Москве в сезоне 2021–2022 гг.: маршрутизация пациентов, показания к проведению иммунизации, организация процесса иммунизации. Также представлены собственные данные о количестве иммунизированных за 11 сезонов недоношенных детей, родившихся с очень низкой и экстремально низкой массой тела. Представлена структура заболеваемости этой группы детей. Отмечена высокая частота сочетанной патологии дыхательной и сердечно-сосудистой системы.
Ключевые слова: респираторно-синцитиальный вирус, недоношенные дети, очень низкая масса тела, экстремально низкая масса тела, бронхолегочная дисплазия, иммунопрофилактика, паливизумаб.
Для цитирования: Миронова А.К. Опыт проведения пассивной иммунизации против респираторно-синцитиальной вирусной инфекции — двенадцатый сезон. РМЖ. Медицинское обозрение. 2022;6(11):659-666. DOI: 10.32364/2587-6821-2022-6-11-659-666.
A.K. Mironova1,2
1Z.A. Bashlyaeva Children’s City Clinical Hospital, Moscow, Russian Federation
2Russian Medical Academy of Continuous Professional Education, Moscow, Russian Federation
Respiratory syncytial virus (RSV) is the most common pathogenic agent responsible for respiratory viral infections in infants and young children. Therefore, the importance of research in the field has been driven by the need for effective preventive tools against RSV infection for children, especially those at high risk of severe RSV disease. Despite the on-going efforts to develop RSV vaccines, the passive immunization of children with a drug called palivizumab is the only reliable option for prophylactic use against RSV. The article presents data on the passive immunization carried out in Moscow in the 2021–2022 season, including the following: the patient routing, indications for immunization, and the organization of the immunization process. It also provides authors’ own data on the number of immunized preterm children born with low and extremely low birth weight which were collected during 11 immunization seasons. The article also reviews the structure of morbidity in this group of children. The authors emphasize a high prevalence of the comorbidity of respiratory and cardiovascular diseases.
Keywords: respiratory syncytial virus, preterm infants, very low body weight, very low birth weight (VLBW), extremely low birth weight (ELBW), bronchopulmonary dysplasia, immunoprophylaxis, palivizumab.
For citation: Mironova A.K. The experience of passive immunization against respiratory syncytial viral infection: the twelfth season. Russian Medical Inquiry. 2022;6(11):659–666 (in Russ.). DOI: 10.32364/2587-6821-2022-6-11-659-666.
Введение
Многочисленные исследования демонстрируют преобладание респираторно-синцитиального вируса (РСВ) среди других возбудителей респираторных вирусных инфекций у детей раннего возраста, не теряющее с годами своей значимости [1–5]. В частности, РСВ является основным возбудителем обструктивных бронхиолитов и пневмоний у детей первого года жизни [6]. Метаанализ 20 исследований за период с 2004 по 2018 г., включивший в себя более 16 000 детей раннего и младшего возраста, показал, что на долю РСВ-инфекции приходится 46% [7].
Клиническая картина РСВ во многом зависит от преморбидного фона. Так, недоношенные дети, дети с гемодинамически значимыми врожденными пороками сердца (ВПС), хроническими заболеваниями дыхательной системы (бронхолегочная дисплазия (БЛД), муковисцидоз и др.), иммунодефицитами, нервно-мышечными заболеваниями переносят РСВ-инфекцию крайне тяжело, а клиническая картина характеризуется преимущественно поражением нижних дыхательных путей с развитием обструктивных бронхиолитов и пневмоний, что требует длительного лечения в условиях стационара, сопровождается высокой потребностью в кислородной терапии, вплоть до искусственной вентиляции легких (ИВЛ) в условиях отделений реанимации и интенсивной терапии (ОРИТ) [6–12].
Ряд работ демонстрирует отсутствие единого подхода в лечении и широкое применение не показанных, ввиду неэффективности в борьбе с вирусной инфекцией, лекарственных средств, таких как бронхолитики, антибиотики и глюкокортикоиды [11, 13, 14].
Разработка вакцины против РСВ, продолжающаяся на протяжении многих лет, остается приоритетным направлением во многих странах [15–17]. Однако на сегодняшний день по-прежнему единственным эффективным и одобренным в педиатрической практике средством борьбы с РСВ является пассивная иммунизация препаратом паливизумаб.
Паливизумаб — препарат гуманизированных моноклональных антител, связывающийся с F-белком, находящимся на поверхности РСВ, и препятствующий тем самым слиянию вирусной оболочки с клеточной мембраной незараженной клетки, а также слиянию мембран соседних инфицированных и неинфицированных клеток [18, 19]. Слияние клеток и образование в результате этого многоядерных гигантских клеток — синцития, является характерной особенностью РСВ, за что он и получил такое название [20]. Следует отметить, что пассивная иммунизация принципиально отличается от вакцинации тем, что в результате нее не формируется иммунологической памяти, способной обеспечить долгосрочный антигенспецифический иммунитет. В ходе пассивной иммунизации вводятся готовые антитела, способные к быстрой компенсации иммунологически незащищенного организма за счет крат-косрочного, но эффективного иммунного ответа. В связи с этим пассивную иммунизацию паливизумабом проводят в эпидемический сезон у детей из групп высокого риска тяжелого течения РСВ.
Эффективность и безопасность паливизумаба доказаны его многолетним применением и многочисленными исследованиями. В США паливизумаб был одобрен и получил широкое распространение в 1998 г. [21]. Чуть позже стал использоваться в странах Европы и Японии. В РФ паливизумаб был зарегистрирован и одобрен к применению у детей из групп высокого риска тяжелого течения РСВ в 2010 г. В 2011 г. в рамках модернизации московского здравоохранения были созданы центры проведения пассивной иммунизации против РСВ на базе медицинских учреждений третьего уровня (детские стационары, консультационно-диагностические отделения (КДО), кабинеты катамнеза, центры восстановительного лечения (ЦВЛ). Один из подобных центров был организован на базе Центра восстановительного лечения детей, родившихся с очень низкой (ОНМТ) и экстремально низкой (ЭНМТ) массой тела, являющегося структурным подразделением ГБУЗ «ДГКБ им. З.А. Башляевой ДЗМ».
В Москве 01.09.2022 стартовал 12-й сезон пассивной иммунизации против РСВ. Ежегодно проводится большая организационная работа по оптимизации маршрутизации и налаживания преемственности между родильными домами, перинатальными центрами, детскими стационарами и детскими поликлиниками для того, чтобы максимальное количество детей, находящихся в группах риска, своевременно получили паливизумаб. В том числе и в связи с этим отмечается ежегодный прирост детей, получивших пассивную иммунизацию. Однако по-прежнему остаются дети из группы высокого риска тяжелого течения РСВ, не прошедшие иммунизацию или приступившие к ней позже положенного срока. Это может быть связано с недостаточной информированностью как родителей, так и медицинского персонала.
Целесообразно отметить, что в РФ показания к применению паливизумаба шире, чем во многих других странах, в том числе странах Европы, где отмечается отсутствие единых подходов, что отражено в систематическом обзоре R.M. Reeves et al. и других работах [6, 22–26].
В настоящее время в РФ пассивная иммунизация против РСВ-инфекции проводится более чем в 70 регионах. В Москве иммунизация регламентируется ежегодно пересматриваемым распоряжением Департамента здравоохранения города Москвы. В зависимости от эпидемиологической ситуации определяются даты начала иммунизации и ее планируемого завершения, пересматриваются показания к использованию паливизумаба.
Так, согласно Приложению 1 к распоряжению Департамента здравоохранения г. Москвы от 26.08.2022 № 2906-р иммунизации подлежат следующие группы детей:
1. Дети в возрасте до 6 мес. и 2 нед. жизни на момент начала сезона иммунизации, соответствующие критериям:
-
рожденные на 28–35-й неделе гестации;
-
рожденные на сроке 36 нед. и более с массой тела 2000 г и менее.
2. Дети в возрасте 24 мес. и менее, которым требовалось лечение по поводу БЛД в течение последних 6 мес.
3. Дети в возрасте 24 мес. и менее с гемодинамически значимыми ВПС при наличии:
-
сердечной недостаточности II–IV функционального класса, требующей медикаментозного лечения;
-
легочной гипертензии средней или тяжелой степени;
-
легочно-венозного застоя;
-
цианоза.
4. Дети в возрасте 24 мес. и младше после хирургической коррекции ВПС в условиях искусственного кровообращения в раннем послеоперационном периоде, получавшие в текущем эпидемическом сезоне пассивную иммунизацию от РСВ-инфекции до выполнения хирургической коррекции порока.
5. Дети в возрасте 12 мес. и младше, рожденные на 22–27-й неделе гестации.
Помимо этого, определены группы детей, для которых решение о проведении пассивной иммунизации паливизумабом принимает консилиум специалистов на основании оценки риска развития РСВ-инфекции тяжелого течения, к которым относятся дети в возрасте 24 мес. и младше:
-
с врожденными аномалиями дыхательных путей, интерстициальными легочными заболеваниями;
-
с врожденной диафрагмальной грыжей;
-
с генетически обусловленной патологией, затрагивающей бронхолегочную систему;
-
с генетически обусловленной патологией, получающие кислородную поддержку.
Целесообразно обратить внимание на то, что в 2022 г. были расширены показания к иммунизации за счет группы детей в возрасте до 6 мес. и 2 нед. жизни на момент начала сезона иммунизации, рожденных на сроке 36 нед. и более с массой тела 2000 г и менее.
Для обращения в центры иммунизации необходимо направление ф. 057/у-04, заполненное лечащим врачом детской городской поликлиники с указанием направительного диагноза и с рекомендацией проведения пассивной иммунизации, заверенное в установленном порядке. Всем пациентам, кроме указанных выше групп недоношенных детей, требуется заключение от специалистов (кардиолог, пульмонолог, хирург) согласно направляющим диагнозам.
Профилактику РСВ-инфекции необходимо начинать до начала эпидемиологического сезона. Первое введение препарата проводится еще на стационарном этапе — в неонатальных отделениях (отделения патологии новорожденных) накануне выписки ребенка домой. При вспышке РСВ возможно проведение иммунизации на этапе ОРИТ новорожденных. Продолжение курса пассивной иммунизации против РСВ осуществляется амбулаторно в центрах иммунизации. В настоящее время в Москве и Московской области функционируют 22 подобных центра, расположенных в различных районах для более удобной маршрутизации пациентов (табл. 1, 2).
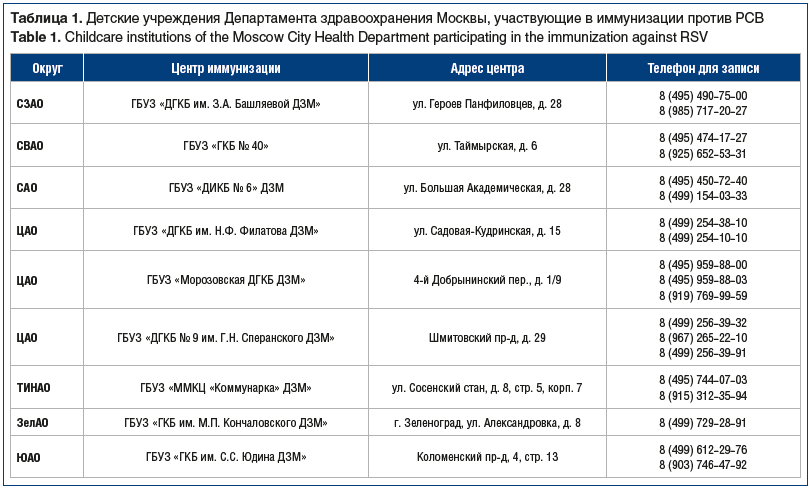
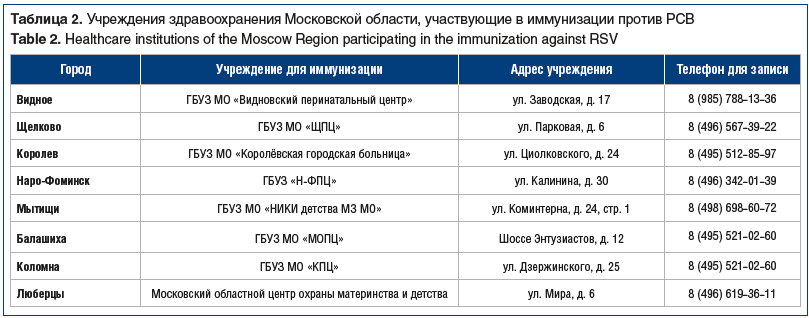
Схема применения паливизумаба включает 5 инъекций, первая из которых осуществляется перед началом сезонного подъема заболеваемости, вызываемой РСВ, остальные — в течение сезона с интервалом 30±5 дней. Регулярность введения препарата обеспечивает надежную защиту пациентов, и этому должно уделяться особое внимание, так как действие препарата сохраняется до 4–5 нед., после чего ребенок должен получить следующую инъекцию, в противном случае он остается незащищенным от РСВ. Это подтверждено исследованиями, в которых продемонстрировано, что риск инфицирования РСВ на фоне проведения пассивной иммунизации связан с незавершенным курсом или нерегулярным введением инъекций [26, 27]. Согласно исследованиям каждая последующая инъекция увеличивает среднюю 30-дневную концентрацию вещества и титр антител в сыворотке крови по сравнению с предыдущей. Эффективность менее и более 5 доз в течение эпидемического периода не установлена, что говорит о необходимости соблюдения 5-кратного введения препарата [28, 29].
С 2011 г. проведение иммунизации в среднем осуществлялось с конца октября по май включительно. В 2021–2022 гг. был отмечен более ранний подъем заболеваемости РСВ-инфекцией, что потребовало раннего начала проведения иммунизации (в 2021 г. начало иммунизации 20 сентября, в 2020 г. — 20 октября).
До 2020 г. паливизумаб поставлялся в сухой форме, разведение препарата проводили за 30 мин до предполагаемого введения. С 2020 г. стали доступны для использования жидкие формы препарата, которые не требуют разведения и специальной подготовки.
Перед каждой инъекцией паливизумаба все дети осматриваются педиатром, который в том числе проводит тщательный сбор анамнеза.
В периоды между инъекциями ведется учет побочных реакций и нежелательных явлений, таких как изменения температуры тела, появление сыпи или других симптомов в течение 2 сут после последней иммунизации, а также учет перенесенных вирусных инфекций с момента последней иммунизации.
Перед инъекцией детям проводятся термометрия, оценка состояния кожных покровов и слизистых, измерение частоты дыхания и сердечных сокращений за 1 мин в покое. Оцениваются результаты общих анализов крови и мочи.
При отсутствии выявленных противопоказаний детям вводят паливизумаб внутримышечно из расчета 15 мг/кг массы тела в наружную поверхность бедра (1 или 2 инъекции в зависимости от дозы препарата согласно инструкции). После введения препарата пациенты находятся под медицинским наблюдением не менее 30 мин.
Противопоказанием к иммунизации является повышенная чувствительность к паливизумабу или к одному из вспомогательных веществ препарата либо к другим моноклональным антителам [30].
Нежелательные явления, развившиеся у детей после введения препарата, оцениваются начиная с введения первой дозы паливизумаба и до 30-го дня после введения последней дозы.
Последующее наблюдение осуществляется педиатром ЦВЛ ежемесячно. При возникновении клинических признаков инфекционных процессов в верхних или нижних дыхательных путях, гипертермии, отклонений в анализах крови и мочи ребенок должен быть осмотрен внепланово.
Целесообразно отметить, что проведение пассивной иммунизации против РСВ препаратом паливизумаб не влияет на проведение вакцинопрофилактики согласно Национальному календарю профилактических прививок (приказы Минздрава России № 125н от 21.03.2014, № 1122н от 0612.2021), которая также, безусловно, имеет крайне важное значение, особенно для недоношенных детей ввиду их высокой восприимчивости к вакциноуправляемым инфекциям [31]. Паливизумаб не препятствует развитию иммунитета при проведении вакцинации и не осложняет течение поствакцинального периода. Профилактическая вакцинация должна проводиться параллельно с пассивной иммунизацией паливизумабом. Так, вакцинация может быть проведена как за сутки до введения препарата, так и на следующий день. В свою очередь, медицинские отводы от вакцинации со стороны специалистов (невролог, офтальмолог, кардиолог) не являются противопоказанием к проведению иммунизации паливизумабом.
Собственный опыт
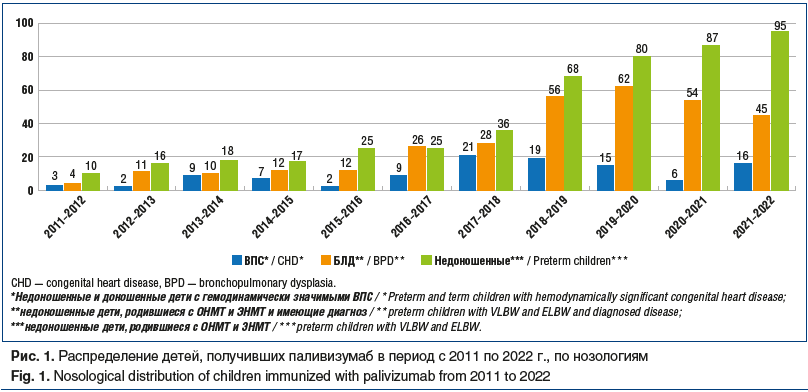
За 11 сезонов проведения пассивной иммунизации на базе ЦВЛ ГБУЗ «ДГКБ им. З.А. Башляевой ДЗМ» было иммунизировано более 900 детей, среди которых преобладали недоношенные дети, родившиеся с ОНМТ и ЭНМТ, что в том числе обусловлено спецификой центра, оказывающего помощь данному контингенту детей (рис. 1). На втором месте находятся недоношенные дети, родившиеся с ОНМТ и ЭНМТ и имеющие диагноз БЛД.
При этом важно подчеркнуть, что глубоко и экстремально недоношенные дети являются одной из наиболее уязвимых групп, что связано с высокой частотой и структурой заболеваемости данного контингента детей.
Нами был проведен анализ частоты и структуры заболеваемости недоношенных детей, родившихся с ОНМТ и ЭНМТ, состоящих на учете в ЦВЛ за период 2012–2021 гг. (n=2961). В таблице 3 представлены данные по заболеваемости данной группы детей на момент перехода на амбулаторное наблюдение и постановки на учет в ЦВЛ, в среднем на 3–4-м месяце жизни.
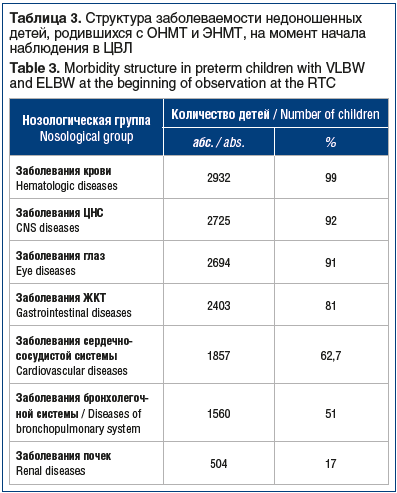
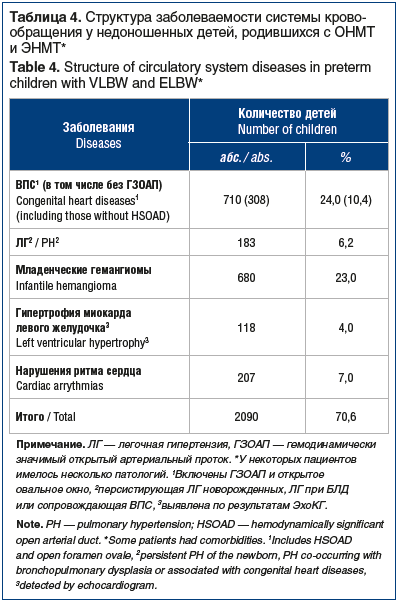
Как видно из таблицы 3, среди наблюдаемых детей, помимо заболеваний крови (которые в 98% случаев были представлены поздней анемией недоношенных), ЦНС, органов зрения и ЖКТ, у 62,7% были выявлены заболевания сердечно-сосудистой системы (из которых на долю гемодинамически значимых ВПС приходилось 24%, табл. 4) и бронхолегочной системы (51%), представленные в постнеонатальном периоде преимущественно БЛД.
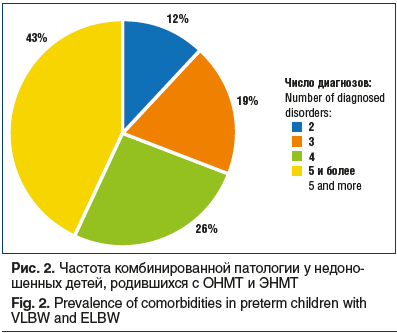
Помимо этого, при постановке на учет в ЦВЛ отмечалась высокая частота сочетанной патологии (большинство пациентов имели не менее 4 различных заболеваний, конкурирующих между собой по степени значимости) (рис. 2).
Таким образом, высокая частота сочетанной патологии дыхательной, сердечно-сосудистой системы и непосредственно глубокой недоношенности существенно повышает риск присоединения РСВ-инфекции и тяжелых форм ее течения. Это диктует необходимость проведения пассивной иммунизации против РСВ.
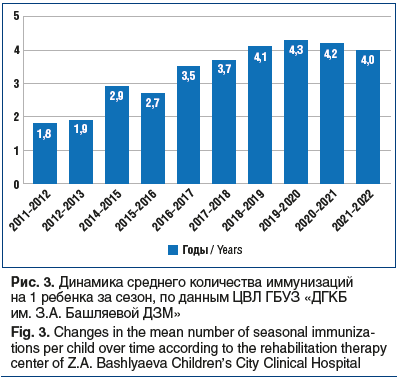
Среднее количество инъекций на одного ребенка в настоящее время в ЦВЛ составляет 4, притом что до 2016 г. оно было меньше 3 (рис. 3). Эта цифра выше, чем в целом по г. Москве (3,5–3,64), ввиду того что в нашем ЦВЛ иммунизируются преимущественно дети, состоящие на амбулаторном учете и регулярно посещающие специалистов центра. Это позволяет вести регулярную работу с родителями и не упускать детей, родившихся в межсезонье (с мая по август). Колебание цифр за последние годы от 3,7 до 4,1 связано преимущественно с моментом рождения малышей и их постановкой на учет в ЦВЛ. Дети, родившиеся в середине сезона иммунизации, получат меньше инъекций из-за окончания эпидемиологического сезона. При этом, согласно международным данным, целевой показатель частоты иммунизации паливизумабом составляет в среднем 3,2–3,5 инъекции на 1 ребенка.
Накопленный опыт пассивной иммунизации препаратом паливизумаб детей, наблюдаемых в ЦВЛ [32, 33], позволил сформулировать следующие критерии эффективности и безопасности, которые могут быть рекомендованы к использованию в клинической практике:
-
отсутствие побочных реакций при введении препарата;
-
значительное снижение обострений БЛД;
- отсутствие госпитализации по поводу тяжелых форм бронхиолитов и пневмоний в отделения реанимации и интенсивной терапии.
Заключение
Многолетний опыт участия в программе проведения пассивной иммунопрофилактики РСВ-инфекции позволяет судить о ее эффективности и безопасности.
У детей, своевременно получающих инъекции паливи-зумаба, РСВ-инфекция отсутствует в структуре заболеваемости респираторных инфекций.
Для максимального охвата иммунизацией детей из групп риска необходимо проведение комплекса мероприятий с активным информированием как родителей, так и врачей. Крайне важно информировать участковых педиатров и узких специалистов (пульмонологи, кардиологи, кардиохирурги) о пользе и необходимости проведения иммунизации против РСВ-инфекции, об актуальных регламентирующих документах, в частности о критериях отбора пациентов для проведения иммунопрофилактики и маршрутизации таких пациентов. Необходимо проводить разъяснительную работу среди родителей на всех этапах лечения — как стационарном (ОРИТ новорожденных, неонатальные отделения), так и на этапе амбулаторного наблюдения, в том числе в отделениях катамнеза и ЦВЛ.
Сведения об авторе:
Миронова Алена Константиновна — к.м.н., заведующая Центром восстановительного лечения детей до 3 лет ГБУЗ «ДГКБ им. З.А. Башляевой ДЗМ»; 125373, Россия, г. Москва, ул. Героев Панфиловцев, д. 28; ассистент кафедры педиатрии им. академика Г.Н. Сперанского ФГБОУ ДПО РМАНПО Минздрава России; 125993, Россия, г. Москва, ул. Баррикадная, д. 2/1; ORCID iD 0000-0002-7864-5090.
Контактная информация: Миронова Алена Константиновна, e-mail: dr_mironova1985@mail.ru.
Прозрачность финансовой деятельности: автор не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 12.09.2022.
Поступила после рецензирования 05.10.2022.
Принята в печать 28.10.2022.
About the author:
Alena K. Mironova — C. Sc. (Med.), Head of the Rehabilitation therapy center for children younger than 3 years old, Z.A. Bashlyaeva Children’s City Clinical Hospital; 28, Geroev Panfilovtsev str., Moscow, 125373, Russian Federation; assistant of the Academician G.N. Speransky Department of Pediatrics, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; ORCID iD 0000-0002-7864-5090.
Contact information: Alena K. Mironova, e-mail: dr_mironova1985@mail.ru.
Financial Disclosure: the author has no a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 12.09.2022.
Revised 05.10.2022.
Accepted 28.10.2022.
2. Bedoya V.I., Abad V., Trujillo H. Frequency of respiratory syncytial virus in hospitalized infants with lower acute respiratory tract infection in Colombia. Pediatr Infect Dis J. 1996;15(12):1123–1124. DOI: 10.1097/00006454-199612000-00014.
3. Hussey G.D., Apolles P., Arendse Z. et al. Respiratory syncytial virus infection in children hospitalised with acute lower respiratory tract infection. S Afr Med J. 2000;90(5):509–512. PMID: 10901825.
4. Moyes J., Cohen C., Pretorius M.; South African Severe Acute Respiratory Illness Surveillance Group. Epidemiology of respiratory syncytial virus-associated acute lower respiratory tract infection hospitalizations among HIV-infected and HIV-uninfected South African children, 2010–2011. J Infect Dis. 2013;208(Suppl 3):S217–S226. DOI: 10.1093/infdis/jit479.
5. Moyes J., Walaza S., Pretorius M. et al.; South African Severe Acute Respiratory Illness (SARI) Surveillance Group. Respiratory syncytial virus in adults with severe acute respiratory illness in a high HIV prevalence setting. J Infect. 2017;75(4):346–355. DOI: 10.1016/j.jinf.2017.06.007.
6. Овсянников Д.Ю., Цверава А.Г., Кршеминская И.В. и др. Пациенты с бронхолегочной дисплазией — группа риска тяжелого течения острого бронхиолита респираторно-синцитиальной вирусной этиологии. Неонатология: новости, мнения, обучение. 2022;10(4):63–74. DOI: 10.33029/2308-2402-2022-10-4-63-74.
7. Suleiman-Martos N., Caballero-Vázquez A., Gómez-Urquiza J.L. et al. Prevalence and Risk actors of Respiratory Syncytial Virus in Children under 5 Years of Age in the WHO European Region: A Systematic Review and Meta-Analysis. J Pers Med. 2021;11:416. DOI: 10.3390/jpm11050416.
8. Овсянников Д.Ю., Кршеминская И.В., Украинцев С.Е. Острый бронхиолит. Неонатальная пульмонология. Под ред. Д.Ю. Овсянникова. М.; 2022.
9. Овсянников Д.Ю., Кршеминская И.В. Острый бронхиолит. Детская пульмонология: национальное руководство. Под ред. Б.М. Блохина. М.: ГЭОТАР-Медиа, 2021:358–373. DOI: 10.33029/9704-5857-0-2021-DEP-1-960.
10. Бокерия Е.Л., Дегтярева Е.А., Ковалев И.А., Солдатова И.Г. Респираторно-синцитиальная вирусная инфекция у детей с врожденными пороками сердца: актуальность проблемы и рекомендации по профилактике. Российский вестник перинатологии и педиатрии. 2014;59(5):101–108.
11. Таточенко В.К., Бакрадзе М.Д. Педиатру на каждый день — 2022. Лихорадки: Справочник по диагностике и лечению. М.: ФГАУ «НМИЦ здоровья детей» Минздрава России; 2022:91–99.
12. Малахов А.Б., Анджель А.Е., Бережанский П.В. и др. Интерлейкиновый профиль у детей с острым бронхиолитом (предварительные данные). Доктор.ру. 2021;20(10):12–17. DOI: 10.31550/1727-2378- 2021-20-10-12-17.
13. Rocca A., Biagi C., Scarpini S. et al. Passive Immunoprophylaxis against Respiratory Syncytial Virus in Children: Where Are We Now? Int J Mol Sci. 2021;22(7):3703. DOI: 10.3390/ijms22073703.
14. Клинические рекомендации. Острый бронхиолит. М.; 2021.
15. Mascola J.R., Fauci A.S. Novel vaccine technologies for the 21st century. Nat Rev Immunol. 2020;20(2):87–88. DOI: 10.1038/s41577-019-0243-3.
16. Walsh E.E., Falsey A.R., Scott D.A. et al. A Randomized Phase 1/2 Study of a Respiratory Syncytial Virus Prefusion F Vaccine. J Infect Dis. 2022;225(8):1357–1366. DOI: 10.1093/infdis/jiab612.
17. Schmoele-Thoma B., Zareba A.M., Jiang Q. et al. Vaccine Efficacy in Adults in a Respiratory Syncytial Virus Challenge Study. N Engl J Med. 2022;386(25):2377–2386. DOI: 10.1056/NEJMoa2116154.
18. Garegnani L., Styrmisdóttir L., Roson Rodriguez P. et al. Palivizumab for preventing severe respiratory syncytial virus (RSV) infection in children. Cochrane Database Syst Rev. 2021;11(11):CD013757. DOI: 10.1002/14651858.CD013757.pub2.
19. Zimmer G., Budz L., Herrler G. Proteolytic activation of respiratory syncytial virus fusion protein. Cleavage at two furin consensus sequences. J Biol Chem. 2001;276(34):31642–3150. DOI: 10.1074/jbc.M102633200.
20. Lamb R.A., Parks G.D. Paramyxoviridae: the viruses and their replication. In: Knipe D.M., Howley P.M., eds. Fields Virology. 5.1. Wolters Kluver: Lippencott Williams and Wilkins. 2007:1449–1496.
21. Dessain S.K. Human antibody therapeutics for viral disease. Berlin: Springer Verlag. 2021.
22. Reeves R.M., van Wijhe M., Lehtonen T. et al.; RESCEU Investigators. A Systematic Review of European Clinical Practice Guidelines for Respiratory Syncytial Virus Prophylaxis. J Infect Dis. 2022;226(Suppl 1):S110–S116. DOI: 10.1093/infdis/jiac059.
23. Ginsberg G.M., Somekh E., Schlesinger Y. Should we use Palivizumab immunoprophylaxis for infants against respiratory syncytial virus? — a cost-utility analysis. Isr J Health Policy Res. 2018;7(1):63. DOI: 10.1186/s13584-018-0258-4.
24. Wang D., Bayliss S., Meads C. Palivizumab for immunoprophylaxis of respiratory syncytial virus (RSV) bronchiolitis in high-risk infants and young children: a systematic review and additional economic modelling of subgroup analyses. Health Technol Assess. 2011;15(5):iii–iv, 1–124. DOI: 10.3310/hta15050.
25. Lewis L., Sinha I., Losty P.D. Respiratory syncytial virus bronchiolitis in congenital diaphragmatic hernia: A systematic review of prevalence rates and palivizumab prophylaxis. Pediatr Pulmonol. 2022;57:239–244. DOI: 10.1002/ppul.25717.
26. Миронова А.К., Османов И.М., Шарыкин А.С. Опыт пассивной иммунопрофилактики против респираторно-синцитиальной вирусной инфекции у детей, рожденных с очень низкой и экстремально низкой массой тела. Российский вестник перинатологии и педиатрии. 2020;65:(4):134–141. DOI: 10.21508/1027-4065-2020-65-4-134-141.
27. Galvis C., Colmenares A., Cabrales L. et al. Impact of immunoprophylaxis with palivizumab on respiratory syncytial virus infection in preterm infants less than 35 weeks in Colombian hospitals. Pediatr Pulmonol. 2022;57(10):2420–2427. DOI: 10.1002/ppul.26051.
28. Narayan O., Bentley A., Mowbray K. et al. Updated cost-effectiveness analysis of palivizumab (Synagis) for the prophylaxis of respiratory syncytial virus in infant populations in the UK. J Med Econ. 2020;23(12):1640–1652. DOI: 10.1080/13696998.2020.1836923.
29. Sanders S.L., Agwan S., Hassan M. et al. Immunoglobulin treatment for hospitalised infants and young children with respiratory syncytial virus infection. Cochrane Database Syst Rev. 2019;8(8):CD009417. DOI: 10.1002/14651858.CD009417.pub2.
30. Yeo K.T., Yung C.F., Khoo P.C. et al. Effectiveness of Palivizumab Against Respiratory Syncytial Virus Hospitalization Among Preterm Infants in a Setting With Year-Round Circulation. J Infect Dis. 2021;224(2):279–287. DOI: 10.1093/infdis/jiaa749.
31. Инструкция по медицинскому применению лекарственного препарата Синагис®. (Электронный ресурс.) URL: https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=6f67839d-2d9d-4dc9-8676-43aeaf8eff03 (дата обращения: 03.09.2022).
32. Иммунопрофилактика инфекционных болезней у недоношенных детей: Методические рекомендации. Под ред. А.А. Баранова, Л.С. Намазовой-Барановой, И.А. Беляевой и др. М.: ПедиатрЪ; 2019.
33. Миронова А.К., Османов И.М. Опыт проведения пассивной иммунизации против РСВ-инфекции у глубоконедоношенных детей. Практика педиатра. 2021;(4):31–36.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
