Влияние аналогов простагландинов на колебания внутриглазного давления при изменении положения тела
DOI: 10.32364/2311-7729-2022-22-2-103-107
Цель исследования: изучить влияние аналогов простагландинов F2α на колебания внутриглазного давления (ВГД) при изменении положения тела.
Материал и методы: обследовано 38 пациентов (50 глаз) с впервые выявленной первичной открытоугольной глаукомой. Пациентов обследовали до назначения аналога простагландинов F2α травопроста и спустя 1 мес. после начала приема препарата. В ходе обследования в положении сидя выполняли точечную контактную тонометрию (Icare) и двунаправленную аппланационную тонометрию (IOPcc, IOPg — роговично-компенсированное ВГД и ВГД, приведенное к измерению по Гольдману). После этого выполняли измерение Icare в положении лежа дважды с интервалом в 5 мин. Затем в положении сидя оценивали Icare, IOPcc и IOPg.
Результаты исследования: при стартовом обследовании IOPcc, IOPg и Icare составили 25,4±3,2, 25,7±2,3, 22,9±3,4 мм рт. ст. соответственно. При измерении лежа показатели Icare составили 23,7±3,3 и 24,0±3,3 мм рт. ст. соответственно. При повторном измерении в положении сидя IOPcc, IOPg и Icare составили 25,4±3,2, 25,7±2,4, 22,3±3,4 мм рт. ст. При обследовании спустя 1 мес. после начала приема травопроста IOPcc, IOPg и Icare снизились до 18,2±2,7, 18,2±1,8, 16,6±2,5 мм рт. ст. соответственно. При измерении лежа данные Icare составили 17,3±2,8 и 17,2±2,7 мм рт. ст. соответственно. При повторном измерении сидя IOPcc, IOPg и Icare достигли 18,0±2,3, 18,4±1,8, 16,2±2,5 мм рт. ст. соответственно. Перепад ВГД при переходе в положение лежа составил при исходном обследовании 0,83±1,04 мм рт. ст., при повторном обследовании — 0,77±1,41 мм рт. ст. Перепад ВГД при обратном переходе в положение сидя при исходном наблюдении был равен 1,66±1,24 мм рт. ст., при повторном обследовании — 0,99±0,98 мм рт. ст.
Заключение: применение травопроста в качестве стартовой монотерапии глаукомы позволяет достичь стойкого снижения ВГД и минимизировать его колебания при изменениях положения тела.
Ключевые слова: глаукома, внутриглазное давление, положение тела, точечная контактная тонометрия, аналог простагландина, травопрост.
Для цитирования: Антонов А.А., Вострухин С.В., Волжанин А.В., Витков А.А., Акимов А.М., Асиновскова И.И. Влияние аналогов простагландинов на колебания внутриглазного давления при изменении положения тела. РМЖ. «Клиническая Офтальмология». 2022;22(2):103-107. DOI: 10.32364/2311-7729-2022-22-2-103-107.
A.A. Antonov1, S.V. Vostrukhin2, A.V. Volzhanin1, A.A. Vitkov1, A.M. Akimov3, I.I. Asinovskova4
1 Scientific Research Institute of Eye Diseases, Moscow, Russian Federation
2JSC MedSef Ramenskoe, Ramenskoe, Russian Federation
3 I.M. Sechenov First Moscow State Medical University (Sechenov University),
Moscow, Russian Federation
4A.I. Yevdokimov Moscow State University of Medicine and Dentistry, Moscow,
Russian Federation
Aim: to assess the effects of prostaglandin F2α analogues on intraocular pressure (IOP) fluctuations when changing body position.
Patients and Methods: thirty-eight patients (50 eyes) with newly diagnosed primary open-angle glaucoma (POAG). Patients were examined before and one month after prescribing travoprost, a prostaglandin F2α analogue. During the examination, IOP was measured by Icare pro rebound tonometry and applanation tonometry (corneal-compensated IOP/ccIOP and Goldmann-correlated IOP/IOPg) in a sitting position. Next, IOP was measured by Icare tonometer twice with a 5-min interval in a supine position. Finally, IOP was measured by Icare tonometry and applanation tonometry (IOPcc, IOPg) in the sitting position.
Results: baseline IOPcc, IOPg, and IOP measured by Icare were 25.4±3.2 mm Hg, 25.7±2.3 mm Hg, and 22.9±3.4 mm Hg, respectively. IOP levels (Icare tonometry) in the supine position were 23.7±3.3 mm Hg and 24.0±3.3 mm Hg, respectively. In repeated measurements in the sitting position, IOPcc, IOPg, and IOP measured by Icare were 25.4±3.2 mm Hg, 25.7±2.4 mm Hg, and 22.3±3.4 mm Hg. One month after starting treatment with travoprost, IOPcc, IOPg, and IOP measured by Icare reduced to 18.2±2.7 mm Hg, 18.2±1.8 mm Hg, and 16.6±2.5 mm Hg, respectively. IOP levels (Icare tonometry) in the supine position were 17.3±2.8 mm Hg and 17.2±2.7 mm Hg, respectively. In repeated measurements in the sitting position, IOPcc, IOPg, and IOP measured by Icare were 18.0±2.3 mm Hg, 18.4±1.8 mm Hg, and 16.2±2.5 mm Hg, respectively. When transiting in a supine position, the differences in IOP levels were 0.83±1.04 mm Hg at baseline and 0.77±1.41 mm Hg after one month. When transiting in a sitting position, the differences in IOP levels were 1.66±1.24 mm Hg at baseline and 0.99±0. 98 mm Hg after one month.
Conclusion: travoprost as a starting monotherapy for POAG provides a long-lasting IOP reduction and minimizes its fluctuations when changing body position
Keywords: glaucoma, intraocular pressure, body position, rebound tonometry, prostaglandin analogue, travoprost.
For citation: Antonov A.A., Vostrukhin S.V., Volzhanin A.V. et al. Influence of prostaglandin analogues on intraocular pressure fluctuations in body position change. Russian Journal of Clinical Ophthalmology. 2022;22(2):103–107 (in Russ.). DOI: 10.32364/2311-7729-2022-22-2-103-107.
Введение
Глаукома является одной из ведущих причин слабовидения и слепоты в мире [1, 2]. Единственным модифицируемым фактором риска развития глаукомной оптиконейропатии является внутриглазное давление (ВГД); однако помимо стойкого повышения ВГД разрушающее действие могут оказывать такж е его флюктуации. Так, подъем ВГД в ночные часы может приводить к прогрессированию глаукомы, не определяясь при этом в ходе обследования в дневное время [3, 4]. Несмотря на известный факт увеличения ВГД при переходе пациента в горизонтальное положение [5, 6], точное изучение таких флюктуаций было до недавнего времени затруднено из-за отсутствия тонометров, работающих в различных положениях тела.
Из всех методов тонометрии, позволяющих измерять ВГД в различных положениях тела, наиболее изучена точечная бесконтактная тонометрия (rebound tonometry), основанная на измерении отскока легкого наконечника от роговицы. Так, точность такой методики сопоставима с точностью тонометрии по Гольдману [7–9].
Среди местных препаратов для лечения глаукомы наиболее эффективными являются аналоги простагландинов F2α, благодаря чему они наиболее часто применяются в качестве стартовой монотерапии. Минимизация суточных колебаний ВГД при приеме этих препаратов хорошо известна [10, 11], однако влияние медикаментозной терапии на изменение ВГД при изменении положения тела изучено недостаточно.
Цель исследования: изучение влияния аналогов простагландинов F2α на колебания ВГД при изменении положения тела.
Материал и методы
Исследование выполнено в группе из 38 больных (50 глаз) с впервые выявленной первичной открытоугольной глаукомой. Среди исследуемых было 16 мужчин и 22 женщины, средний возраст составил 57,0±4,8 года. Стадию глаукомы верифицировали на основании данных статической периметрии, полученных на приборе Humphrey Field Analyzer II 750i (Zeiss, Германия) в режиме порогового исследования по протоколу 24–2. На момент включения в исследование пациенты не принимали антиглаукомных препаратов, также в составе системной терапии не было диуретиков либо иных препаратов, потенциально влияющих на внутриглазную гидродинамику. В исследование не включали больных с аметропией более ±4,0 дптр, имеющих признаки воспаления и перенесших какие-либо офтальмологические операции помимо плановой факоэмульсификации. Все испытуемые были осведомлены о сути исследования и подписали согласие на обезличенное использование персональных данных. Исследование было одобрено локальным этическим комитетом ФГБНУ «НИИГБ».
В х eeде исследования у пациента сначала в положении сидя измеряли ВГД с помощью точечного контактного тонометра ТА03 Icare Pro (Icare Finland Oy, Финляндия) в центре роговицы (Icare). Затем проводили обследование на биомеханическом анализаторе Ocular Response Analyzer (ORA; Reichert Inc, США) для определения роговично-компенсированного ВГД и ВГД без учета биомеханических свойств роговицы, приближенного к измерению по Гольдману (IOPcc, intraocular pressure corneal compensated; IOPg, intraocular pressure Goldmann).
После этого пациента укладывали на спину на кушетку в том же кабинете и выполняли два измерения Icare с разницей в 5 мин. Затем вновь исследовали Icare и ORA в положении сидя.
В завершение первичного исследования пациентам назначали препарат травопроста 0,04 мг / 1 мл Травиолан® (ООО «Бауш Хелс») 1 р/сут на ночь в пораженный глаз.
Повторный осмотр обследованных пациентов назначали спустя 4 нед. после первичного обследования. В ходе повторного визита оценивали переносимость препарата и повторяли описанное выше исследование с помощью ORA и Icare.
Статистическую обработку данных выполняли в программном комплексе IBM SPSS Statistics версии 21.0.0.0. Нормальность распределения оценивали с помощью критерия Шапиро — Уилка и оценки асимметрии и эксцесса. Так как распределение показателей соответствовало нормальному, результаты измерений представлены в формате среднее ± стандартное отклонение (М±SD). Значимость изменений показателей ВГД оценивали с п омощью критерия знаковых рангов Вилкоксона для связанных выборок. Изменения считали статистически значимыми при p≤0,05.
Результаты исследования
Ни у одного пациента не наблюдалось побочных эффектов; 14 человек отметили небольшое покраснение конъюнктивы, прошедшее спустя 1–3 дня после начала лечения без дополнительной терапии.
Полученные в ходе исследования данные представлены в таблице.
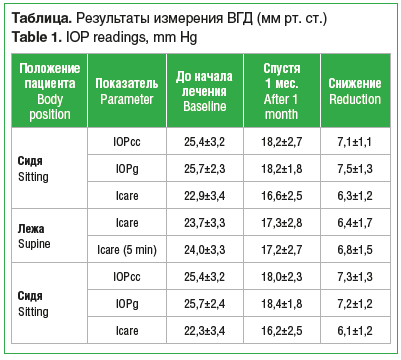
По данным исследования Icare наблюдалось статистически значимое уменьшение флюктуаций ВГД при изменении положения тела. До назначения лечения при переходе в положение лежа ВГД увеличивалось в среднем на 0,83±1,04 мм рт. ст., а между измерениями в положении лежа разница составляла 0,27±1,57 мм рт. ст. На фоне терапии травопростом данные показатели достоверно изменились, составив 0,77±1,41 и 0,10±1,21 мм рт. ст. соответственно (p<0,05).
Перепад ВГД после обратного перехода в положение сидя при первичном обследовании составил 1,7±1,24 мм рт. ст., при повторном — 0,99±0,98 мм рт. ст.
По данным ORA, на фоне медикаментозной терапии также уменьшилась разница в значениях ВГД до и после положения лежа (см. рисунок) (p<0,05).
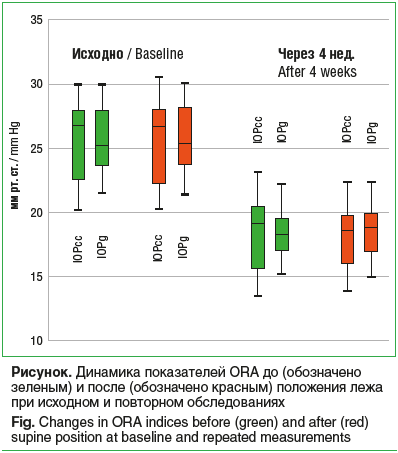
Обсуждение
Колебания ВГД, обусловленные изменением положения тела, являются актуальной проблемой: у больных глаукомой их амплитуда увеличена почти вдвое по сравнению со здоровыми людьми [12]. Влияние медикаментозной терапии на флюктуации ВГД практически не изучено. Известно о минимизации таких колебаний после трабекулэктомии [13], однако проникающая хирургия крайне редко является оптимальным методом первичного лечения.
Выбор препарата Травиолан® в качестве первичного лечения глаукомы в исследуемой группе был обусловлен рядом факторов. Так, аналоги простагландинов являются оптимальным вариантом стартовой монотерапии глаукомы благодаря их сравнительно высокой эффективности и необходимости инстиллировать препарат всего 1 р/сут [14, 15]. Актуальной проблемой медикаментозной терапии глаукомы является отсроченное развитие синдрома «сухого глаза» вследствие деструктивного воздействия консервантов на переднюю поверхность глаза [16]. Это обусловливает актуальность использования бесконсервантных форм антиглаукомных препаратов [17], которые, однако, в большинстве случаев обладают более высокой стоимостью из-за необходимости использования особой одноразовой тары. Выбранный нами препарат не содержит консервантов, но благодаря особому дозатору и традиционной форме упаковки не обладает повышенной ценой.
В нашей работе ВГД снизилось в среднем на 7,12±1,07 мм рт. ст., что составило 28% от исходного значения. Эти данные сопоставимы с результатами других исследований эффективности травопроста [18, 19]. По данным сравнительных исследований, травопрост обладает схожей переносимостью и гипотензивным эффектом по сравнению с другими аналогами простагландинов — латанопростом и тафлупростом [20, 21].
Подавляющее большинство работ, посвященных колебаниям ВГД при изменении пол eeжения тела, выполнены с участием здоровых добровольцев [22–24]. Наши данные частично соотносятся с результатами этих исследований, что, вероятнее всего, обусловлено умеренным повышением ВГД у больных в нашем исследовании. Имеющиеся исследования по сравнению колебаний ВГД у здоровых людей и у пациентов с глаукомой показывают бóльшую разницу, чем в нашей работе [12, 25]. Для оценки влияния медикаментозной терапии на колебания ВГД, вызванные изменением положения тела, необходимы дополнительные исследования.
Заключение
Применение бесконсервантной формы травопроста позволяет стабилизировать ВГД и снизить его колебания, ассоциированные с изменением положения тела. Отсутствие консерванта позволяет минимизировать влияние длительного приема препарата на потенциальное развитие дисфункции слезной пленки. В долгосрочной перспективе стойкая компенсация ВГД, достигнутая на монотерапии, нивелирующей колебания ВГД при изменении положение тела, позволит замедлить прогрессирование глаукомы и сохранить зрительные функции. Таким образом, с позиции максимально возможного сохранения качества жизни монотерапия аналогами простагландинов, в частности бесконсервантной формой травопроста, является одной из оптимальных тактик лечения впервые выявленной глаукомы.
Сведения об авторах:
Антонов Алексей Анатольевич — к.м.н., ведущий научный сотрудник отдела глаукомы ФГБНУ «НИИГБ»; 119021, Россия, г. Москва, ул. Россолимо, д. 11, корп. А, Б; ORCID iD 0000-0002-5171-8261.
Вострухин Сергей Викторович — к.м.н., врач-офтальмолог ООО «МедСэф»; 140105, Россия, г. Раменское, ул. Чугунова, д. 43; ORCID iD 0000-0002-7803-2550.
Волжанин Андрей Вячеславович — к.м.н., младший научный сотрудник отдела глаукомы ФГБНУ «НИИГБ»; 119021, Россия, г. Москва, ул. Россолимо, д. 11, корп. А, Б; ORCID iD 0000-0002-1421-8882.
Витков Александр Александрович — младший научный сотрудник отдела глаукомы ФГБНУ «НИИГБ»; 119021, Россия, г. Москва, ул. Россолимо, д. 11, корп. А, Б; ORCID iD 0000-0001-7735-9650.
Акимов Артемий Михайлович — студент 6-го курса лечебного факультета ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0002-9193-0582.
Асиновскова Ирина Ильинична — студентка 6-го курса лечебного факультета ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России; 127473, Россия, г. Москва, ул. Делегатская, д. 20, стр. 1; ORCID iD 0000-0003-2893-0173.
Контактная информация: Антонов Алексей Анатольевич, e-mail: niigb.antonov@gmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 04.03.2022.
Поступила после рецензирования 31.03.2022.
Принята в печать 25.04.2022.
About the authors:
Aleksey A. Antonov — C. Sc. (Med.), leading researcher of the Division of Glaucoma, Scientific Research Institute of Eye Diseases; 11A, B, Rossolimo str., Moscow, 119021, Russian Federation; ORCID iD 0000-0002-5171-8261.
Sergey V. Vostrukhin — C. Sc. (Med.), ophthalmologist, JSC MedSef Ramenskoe; 43, Chugunov str., Ramenskoe, 140105, Russian Federation; ORCID iD 0000-0002-7803-2550.
Andrey V. Volzhanin — C. Sc. (Med.), junior researcher of the Division of Glaucoma, Scientific Research Institute of Eye Diseases; 11A, B, Rossolimo str., Moscow, 119021, Russian Federation; ORCID iD 0000-0002-1421-8882.
Aleksandr A. Vitkov — junior researcher of the Division of Glaucoma, Scientific Research Institute of Eye Diseases; 11A, B, Rossolimo str., Moscow, 119021, Russian Federation; ORCID iD 0000-0001-7735-9650.
Artemiy M. Akimov — student of the 6th course of the Medical Faculty, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8 Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0002-9193-0582.
Irina I. Asinovskova — student of the 6th course of the Medical Faculty, A.I. Yevdokimov Moscow State University of Medicine and Dentistry; 20/1, Delegatskaya str., Moscow, 127473, Russian Federation; ORCID iD 0000-0003-2893-0173.
Contact information: Aleksey A. Antonov, e-mail: niigb.antonov@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 04.03.2022.
Revised 31.03.2022.
Accepted 25.04.2022.
2. Tham Y.C., Li X., Wong T.Y. et al. Global prevalence of glaucoma and projections of glaucoma burden through 2040: a systematic review and meta-analysis. Ophthalmology. 2014;121(11):2081–2090. DOI: 10.1016/j.ophtha.2014.05.013.
3. Asrani S., Zeimer R., Wilensky J. et al. Large diurnal fluctuations in intraocular pressure are an independent risk factor in patients with glaucoma. J Glaucoma. 2000;9(2):134–142. DOI: 10.1097/00061198-200004000-00002.
4. Yang Z., Mansouri K., Moghimi S., Weinreb R.N. Nocturnal variability of intraocular pressure monitored with contact lens sensor is associated with visual field loss in glaucoma. J Glaucoma. 2021;30(3):e56–e60. DOI: 10.1097/IJG.0000000000001727.
5. Prata T.S., De Moraes C.G., Kanadani F.N. et al. Posture-induced intraocular pressure changes: considerations regarding body position in glaucoma patients. Surv Ophthalmol. 2010;55(5):445–453. DOI: 10.1016/j.survophthal.2009.12.002.
6. Mansouri K., Tanna A.P., De Moraes C.G. et al. Review of the measurement and management of 24-hour intraocular pressure in patients with glaucoma. Surv Ophthalmol. 2020;65(2):171–186. DOI: 10.1016/j.survophthal.2019.09.004.
7. Gao F., Liu X., Zhao Q., Pan Y. Comparison of the iCare rebound tonometer and the Goldmann applanation tonometer. Exp Ther Med. 2017;13(5):1912–1916. DOI: 10.3892/etm.2017.4164.
8. Takagi D., Sawada A., Yamamoto T. Evaluation of a New Rebound Self-tonometer, Icare HOME: Comparison With Goldmann Applanation Tonometer. J Glaucoma. 2017;26(7):613–618. DOI: 10.1097/IJG.0000000000000674.
9. Iliev M.E., Goldblum D., Katsoulis K. et al. Comparison of rebound tonometry with Goldmann applanation tonometry and correlation with central corneal thickness. Br J Ophthalmol. 2006;90(7):833–835. DOI: 10.1136/bjo.2005.089870.
10. Konstas A.G., Mikropoulos D., Kaltsos K. et al. 24-hour intraocular pressure control obtained with evening- versus morning-dosed travoprost in primary open-angle glaucoma. Ophthalmology. 2006;113(3):446–450. DOI: 10.1016/j.ophtha.2005.10.053.
11. Петров С.Ю., Волжанин А.В., Кравчик М.В. и др. Влияние тафлупроста на суточные колебания офтальмотонуса при первичной открытоугольной глаукоме. Национальный журнал глаукома. 2018;17(4):91–96. DOI: 10.25700/NJG.2018.04.08.
12. Ireka O.J., Ogbonnaya C.E., Arinze O.C. et al. Comparing posture induced intraocular pressure variations in normal subjects and glaucoma patients. Int J Ophthalmol. 2021;14(3):399–404. DOI: 10.18240/ijo.2021.03.11.
13. Kang Y.S., Helong P., Sung M.S., Park S.W. Posture-induced Changes in Intraocular Pressure After Trabeculectomy in Patients With Primary Open-angle Glaucoma. J Glaucoma. 2021;30(9):827–833. DOI: 10.1097/IJG.0000000000001911.
14. Столяров Г.М., Лебедев О.И., Золотарев А.В. и др. Увеосклеральный отток и клинико-патогенетическое обоснование применения простагландинов у больных глаукомой. Национальный журнал глаукома. 2013;1:35–39.
15. Авдеев Р.В., Александров А.С., Бакунина Н.А., Белая Д.А. и др. Сопоставление режимов лечения больных первичной открытоугольной глаукомой с характеристиками прогрессирования заболевания. Часть 2. Эффективность инициальных режимов гипотензивного лечения. Национальный журнал глаукома. 2018;17(2):65–83. DOI: 10.25700/NJG.2018.02.07.
16. Егоров Е.А., Егоров А.Е., Елисеева Т.О., Егорова Т.Е. Нежелательные явления гипотензивной терапии глаукомы. РМЖ. Клиническая офтальмология. 2011;12(3):111–113.
17. Егоров Е.А., Романова Т.Б., Рыбакова Е.Г., Оганезова Ж.Г. Современные подходы к профилактике и лечению вторичного синдрома «сухого глаза». РМЖ. Клиническая офтальмология. 2017;17(1):61–64.
18. Denis P., Covert D., Realini A. Travoprost in the management of open-angle glaucoma and ocular hypertension. Clin Ophthalmol. 2007;1(1):11–24. PMID: 19668462.
19. Waugh J., Jarvis B. Travoprost. Drugs Aging. 2002;19(6):465–471; discussion 472–463. DOI: 10.2165/00002512-200219060-00005.
20. Cai Z., Cao M., Liu K., Duan X. Analysis of the Responsiveness of Latanoprost, Travoprost, Bimatoprost, and Tafluprost in the Treatment of OAG/OHT Patients. J Ophthalmol. 2021;2021:5586719. DOI: 10.1155/2021/5586719.
21. Faseeh A.E., Allam R.S., Shalash A.B., Abd Elmohsen M.N. Comparison between Latanoprost, Travoprost, and Tafluprost in reducing intraocular pressure fluctuations in patients with glaucoma. Eur J Ophthalmol. 2021;31(6):3018–3026. DOI: 10.1177/1120672121990540.
22. Nakakura S., Mori E., Yamamoto M. et al. Intradevice and Interdevice Agreement Between a Rebound Tonometer, Icare PRO, and the Tonopen XL and Kowa Hand-held Applanation Tonometer When Used in the Sitting and Supine Position. J Glaucoma. 2015;24(7):515–521. DOI: 10.1097/IJG.0000000000000016.
23. De Bernardo M., Borrelli M., Cembalo G., Rosa N. Intraocular Pressure Measurements in Standing Position with a Rebound Tonometer. Medicina (Kaunas). 2019;55(10):701. DOI: 10.3390/medicina55100701.
24. Sobczak M., Asejczyk M., Geniusz M. Does body position, age, and heart rate induce IOP’s changes? Eur J Ophthalmol. 2022;32(3):1530–1537. DOI: 10.1177/11206721211023313.
25. Tsukahara S., Sasaki T. Postural change of IOP in normal persons and in patients with primary wide open-angle glaucoma and low-tension glaucoma. Br J Ophthalmol. 1984;68(6):389–392. DOI: 10.1136/bjo.68.6.389.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Распечатать

