Современные возможности хирургического лечения при глазных осложнениях синдромов Стивенса — Джонсона и Лайелла
DOI: 10.32364/2311-7729-2023-23-2-99-106
Эпидермолитические лекарственные реакции (ЭЛР) — острые тяжелые аллергические реакции, индуцированные применением лекарственных препаратов и характеризующиеся обширными поражениями кожи и слизистых оболочек. Лекарственно-обусловленные синдромы Стивенса — Джонсона и Лайелла, проявляющиеся острыми заболеваниями кожи и слизистых оболочек и нередко приводящие к летальному исходу, в различной степени поражают веки и глазную поверхность, угрожая тяжелыми нарушениями функции органа зрения. Авторами представлены два клинических наблюдения пациентов с глазными проявлениями ЭЛР в остром и отдаленном периодах, продемонстрированы эффективные современные подходы к лечению пациентов с такими поражениями глаз и их последствиями. Представлены хирургические методы лечения, позволившие добиться в основном удовлетворительных анатомических и функциональных результатов при рассматриваемой патологии. Своевременное лечение синдромов Стивенса — Джонсона и Лайелла — системное и местное консервативное в сочетании с хирургическими пособиями в остром периоде играет важную роль в предупреждении тяжелых поздних осложнений со стороны органа зрения. Устранение глазных последствий описанных синдромов связано с многоэтапным реконструктивным хирургическим лечением. Авторы отмечают, что пациенты, перенесшие лекарственно-обусловленные синдромы Стивенса — Джонсона и Лайелла, требуют длительного наблюдения офтальмолога.
Ключевые слова: эпидермолитические лекарственные реакции, синдром Стивенса — Джонсона, синдром Лайелла, трансплантация амниона, синдром сухого глаза, псевдомембранозный блефароконъюнктивит, многоэтапное реконструктивное хирургическое лечение.
Для цитирования: Черныш В.Ф., Харитонова Н.Н., Куликов А.Н., Качерович П.А., Кольбин А.А. Современные возможности хирургического лечения при глазных осложнениях синдромов Стивенса — Джонсона и Лайелла. РМЖ. «Клиническая Офтальмология». 2023;23(2):99-106. DOI: 10.32364/2311-7729-2023-23-2-99-106.
V.F. Chernysh, N.N. Haritonova, A.N. Kulikov, P.A. Kacherovich, A.A. Kol'bin
S.M. Kirov Military Medical Academy, St. Petersburg, Russian Federation
Epidermolytic drug reactions (EDR) are severe acute drug-induced allergic disorders characterized by extensive lesions of the skin and mucous membranes. Drug-induced Stevens-Johnson and Lyell's syndromes manifested with acute skin and mucous membrane disorders and often leading to lethal outcome may affect eyelids and ocular surface with different levels of severity and thus can cause serious functional ocular complications. The authors present two clinical reports of patients with ocular EDR manifestations in acute and long-term time periods and review the currently available effective treatment options for patients with such ocular complications and their consequences. The article describes surgical treatments which enabled to achieve satisfactory anatomical and functional results in patients with the above disorders. Timely treatment of Stevens-Johnson and Lyell's syndromes comprising systemic and topical conservative therapy in combination with surgical procedures during the acute stage plays an important role for the prediction of severe long-term ocular complications. The elimination of ocular complications caused by these syndromes is associated with multistage reconstructive surgery. The authors emphasize that long-term follow-up by ophthalmologist will be required for patients who survived Stevens-Johnson and Lyell's syndromes.
Keywords: epidermolytic drug reactions, Stevens–Johnson syndrome, Lyell's syndrome, amniotic membrane transplantation, dry eye syndrome, pseudomembranous blepharoconjunctivitis, multistage reconstructive surgery.
For citation: Chernysh V.F., Haritonova N.N., Kulikov A.N. et al. Current surgical treatment options for ocular complications of Stevens-Johnson and Lyell's syndromes. Russian Journal of Clinical Ophthalmology. 2023;23(2):99–106 (in Russ.). DOI: 10.32364/2311-7729-2023-23-2-99-106.
Введение
Эпидермолитические лекарственные реакции (ЭЛР) — это острые тяжелые аллергические реакции, индуцированные применением лекарственных препаратов и характеризующиеся обширными поражениями кожи и слизистых оболочек [1]1. На сегодняшний день в зависимости от площади поражения кожных покровов выделяют следующие формы ЭЛР:
-
Синдром Стивенса — Джонсона (ССД) — менее 10% поверхности тела.
-
Токсический эпидермальный некролиз (ТЭН), или синдром Лайелла, — более 30% поверхности тела.
-
Промежуточная форма (поражение 10–30% кожи).
Описано более 100 лекарственных препаратов разных групп, вызывающих развитие ЭЛР. В основном это антибиотики, нестероидные противовоспалительные и противоэпилептические препараты, однако в некоторых случаях причину заболевания выяснить не удается [2]. Патогенез ЭЛР связан с массовой гибелью базальных кератиноцитов кожи и эпителия слизистых оболочек за счет резкой активизации процессов апоптоза, что проявляется некрозом всех слоев эпидермиса, образованием диастаза над базальной мембраной и отслойкой эпидермиса [1–3].
Клиническая картина ЭРЛ характеризуется появлением преимущественно на коже лица и туловища множественных полиморфных высыпаний в виде багрово-красных пятен с синюшным оттенком, папул, пузырьков, мишеневидных очагов с последующей отслойкой поверхностных слоев кожи и слизистых оболочек желудочно-кишечного тракта, половых органов и глазной поверхности. Заболевание имеет непредсказуемое течение. Первоначально доброкачественно выглядевший дерматоз может быстро прогрессировать, а когда происходит отслойка кожи и слизистых, трудно прогнозировать завершение процесса. Это сопровождается тяжелыми общими расстройствами: высокой температурой тела (38–40 °С), головной болью, сопорозным состоянием, диспепсическими явлениями и др. На фоне поражения многих внутренних органов и присоединения инфекции и сепсиса возможен летальный исход. Чем старше возраст пациента, серьезнее сопутствующее заболевание и обширнее поражение кожи, тем хуже прогноз заболевания [1–3].
Согласно данным литературы заболеваемость ССД оценивается как 1–6 случаев на 1 млн человек (летальность — менее 5%), тогда как синдром Лайелла встречается с частотой 0,4–1,2 случая (летальность — до 30%)1.
Быстрая идентификация и отмена причинного лекарства признаны главными факторами улучшения исхода при ССД и ТЭН [1, 2].
В остром периоде при поражении глаз наблюдаются мембранозный блефароконъюнктивит, эрозии роговицы и конъюнктивы, возникает риск развития язвы роговицы и увеита. В отдаленном периоде, с которым офтальмологу приходится сталкиваться значительно чаще, развиваются хронический псевдомембранозный блефароконъюнктивит, рубцовые изменения в виде сглаживания заднего ребра, заворота век, трихиаза, симблефарона, анкилоблефарона, синдром «сухого глаза», лимбальная недостаточность (с формированием васкуляризированного помутнения роговицы), а также кератинизация краев век и глазной поверхности. Задний сегмент глазного яблока, как правило, не страдает [4, 5].
Международных стандартов по ведению пациентов с ССД/ТЭН, основанных на доказательной медицине, к настоящему моменту нет. Зарубежные и отечественные публикации, посвященные этому вопросу, допускают различные подходы к лечению. Единый согласительный национальный документ в РФ представлен в виде профессионального руководства Общероссийской общественной организации «Российское общество дерматовенерологов и косметологов» — клинических рекомендаций (проекта) «Синдром Стивенса — Джонсона», 2020 г.2
Собственные клинические наблюдения
Представляем два клинических наблюдения пациентов, находившихся на лечении в клинике офтальмологии Военно-медицинской академии имени С.М. Кирова (в период с 2007 по 2020 г.) по поводу осложнений со стороны органа зрения в различные сроки после перенесенных синдромов Лайелла и Стивенса — Джонсона. Применялись некоторые современные методы консервативного и хирургического лечения таких пациентов в зависимости от характера поражения.
Клиническое наблюдение 1
Пациент С., 18 лет, военнослужащий срочной службы, находился на лечении в реанимационном отделении клиники инфекционных болезней с синдромом Лайелла. Синдром развился в ответ на лечение острой респираторной вирусной инфекции иммуномодулирующим противовирусным препаратом с действующим веществом тилорон. В остром периоде заболевания у пациента было поражено 35% поверхности кожи, а также слизистые оболочки трахеобронхиального дерева, желудочно-кишечного тракта, половых органов. В отделении реанимации была выполнена трахеостомия, проводилось парентеральное питание, катетеризация мочевого пузыря.
На обоих глазах определялись выраженный отек век, гиперемия и множественные корочки на коже, а по свободному краю век — обильное рыхлое пленчатое отделяемое белого цвета (за счет слущивания поверхностных слоев эпителия конъюнктивы). На конъюнктиве и роговице — обширные асептические эрозии. Глубжележащие структуры глаз в процесс вовлечены не были. Во время нахождения пациента в реанимации пациента регулярно осматривал офтальмолог. Были назначены: туалет век и конъюнктивальной полости, инстилляции бензилдиметил-миристоиламино-пропиламмония и 0,1% бесконсервантного дексаметазона в течение 2 нед. с постепенной отменой, стимулятора регенерации на основе декспантенола, а также с бандажной целью — силикон-гидрогелевые мягкие контактные линзы [6, 7]. На правом глазу, где эрозия роговицы была более обширной, выполнена простая блефарорафия [8] с использованием провизорного шва, однако в результате эрозия роговицы сократилась лишь частично. К моменту выписки из отделения интенсивной терапии на 34-й день после начала заболевания поверхность век обоих глаз очистилась от корочек, отек и гиперемия кожи значительно уменьшились, однако сохранялось утолщение и гиперемия свободного края век и умеренно выраженное рыхлое пленчатое отделяемое из конъюнктивальной полости. Появились также признаки легкого трихиаза и тенденция к завороту нижних век. На правом глазу на фоне умеренной гиперемии и очаговой деэпителизации конъюнктивы эрозия роговицы в параоптической зоне сохранялась (4,0×4,0 мм). На левом глазу эрозии глазной поверхности эпителизировались полностью, но отмечалось островковое окрашивание эпителия роговицы флюоресцеином.
Пациент был переведен в клинику офтальмологии, где лечение было продолжено. Острота зрения: правого глаза 0,5 (не корр.), левого глаза 1,0. Внутриглазное давление в норме.
Одним из наиболее эффективных современных методов, способствующих эпителизации при персистирующих эрозиях роговицы, является покрытие ее амниотической мембраной в качестве временной биологической повязки. Это обусловлено противовоспалительным, иммуносупрессивным и антигипоксическим действием амниона, его свойствами способствовать регенерации и дифференцировке эпителия, ингибировать васкуляризацию, иммунные реакции, а также защищать глазную поверхность от внешних воздействий. Раннее использование амниона в острой стадии химического ожога, синдромов Стивенса — Джонсона и Лайелла также предотвращает возникновение лимбальной недостаточности, сохраняя оставшиеся неповрежденными эпителиальные стволовые клетки лимба. Эти сохранившиеся клетки реализуют свой высокий регенеративный потенциал, предотвращая рубцовые осложнения [9].
В связи с персистирующим характером эрозии роговицы и упорным мембранозным блефароконъюнктивитом на правом глазу было выполнено временное покрытие всей глазной поверхности амнионом. После лизиса амниона через 8 дней эрозии конъюнктивы эпителизировались, а эрозия роговицы сократилась (рис. 1).
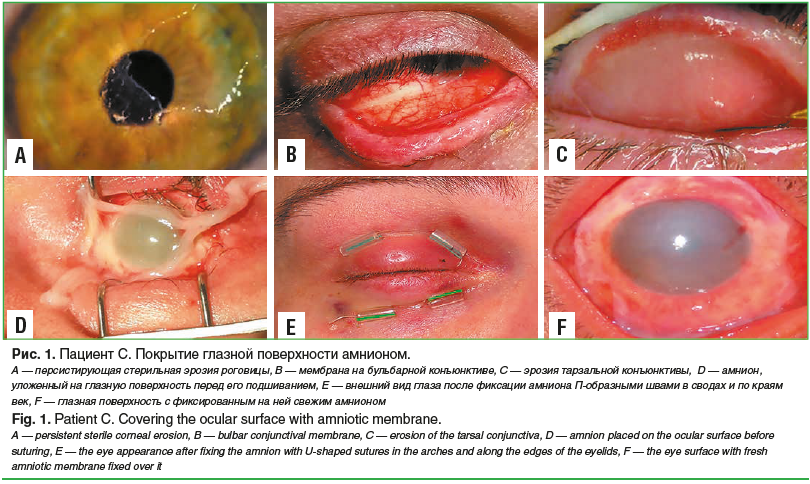
Несмотря на проводившееся лечение, в зоне эрозии появилось изъязвление стромы роговицы, которое постепенно углублялось. Учитывая углубление дефекта стромы роговицы, было выполнено трехслойное покрытие язвы амнионом (рис. 2) [8]. В ходе операции поверхностный листок амниона был подшит к краям язвы, а полость ее заполнена амниотической тканью с последующим покрытием всей роговицы еще одним слоем амниона. После лизиса этого листка через 7 дней амнион, подшитый к краям язвы, был полностью эпителизирован. В ходе дальнейшего заживления ткань амниона, заполнявшая полость язвы, интегрировалась в ткань стромы и выглядела как легкое очаговое помутнение в параоптической зоне.
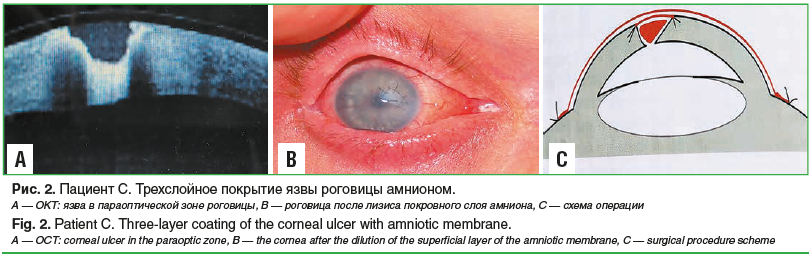
Через 2 мес. пациент был госпитализирован в клинику по поводу рецидива глубокой язвы (до десцеметовой мембраны) размерами 3,0×4,0 мм с захватом оптической зоны роговицы правого глаза. Была выполнена аутоконъюнктивальная пластика роговицы лоскутом «на ножке» (рис. 3) [10, 11].
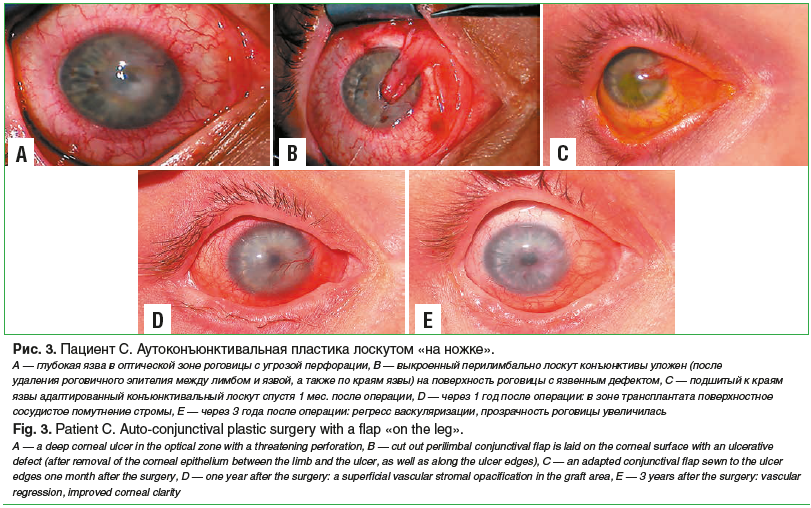
При осмотре через 1 год роговица на обоих глазах была полностью эпителизирована. На роговице правого глаза в области аутоконъюнктивальной пластики — поверхностная васкуляризация с частичным захватом оптической зоны и умеренным помутнением стромы. Острота зрения 0,2.
В дальнейшем наряду с явлениями рецидивирующего псевдомембранозного блефароконъюнктивита у пациента развился трихиаз и рубцовый заворот нижних век обоих глаз, а также тяжелый синдром «сухого глаза» (ССГ) (тест Ширмера I — 4 мм). На обоих глазах было выполнено устранение заворота нижних век с пересадкой слизистой оболочки полости рта по Сапежко и электролиз отдельных неправильно растущих ресниц. По поводу ССГ на правом глазу в дополнение к консервативной терапии слезозаместителем на основе гиалуроната натрия и местного цитостатика 0,05% суспензии циклоспорина проведена пересадка малых слюнных желез из полости рта по J. Murube (2001) [12]. После операции увлажнение глазной поверхности несколько улучшилось (тест Ширмера I — 7 мм), и пациент отмечал уменьшение неприятных, характерных для ССГ субъективных ощущений.
В дальнейшем он в течение 5 лет наблюдался 1 раз в 6 мес. При контрольных осмотрах периодически отмечали умеренные обострения псевдомембранозного блефароконъюнктивита. В настоящее время пациент социально адаптирован, окончил высшее учебное заведение, успешно работает по специальности, женат.
Клиническое наблюдение 2
Пациентка Н. в возрасте 9 лет после применения противоэпилептического препарата ламотриджин перенесла ССД. В последующем находилась под амбулаторным наблюдением офтальмологов. С 13 лет периодически проходит обследование и лечение в клинике офтальмологии Военно-медицинской академии имени С.М. Кирова (в течение последних 9 лет).
При первичном осмотре жалобы на легкую светобоязнь, ощущение сухости, зуда, легкого жжения в глазах. Оба глаза: острота зрения — движение руки у лица. Глазные щели укорочены за счет частичного латерального анкилоблефарона. Лагофтальм около 3 мм. Умеренный заворот век, субтотальный симблефарон (конъюнктивальные своды укорочены — около 3,0–4,0 мм). Тяжелый ССГ (тест Ширмера I — 0 мм). Полупрозрачное васкуляризированное помутнение роговицы с признаками ксерофтальмии (более выраженной на правом глазу): эпителий практически без признаков увлажнения, утолщен, тусклый, мутный, с неравномерной поверхностью и мелкоочаговым прокрашиванием флюоресцеином. По данным импрессионной цитологии [13], фенотип эпителия роговицы на обоих глазах конъюнктивальный (полная лимбальная недостаточность). Структуры передней камеры достоверно не просматриваются. Проводилось консервативное лечение ССГ с использованием заместителей слезы и 0,05% глазной эмульсии циклоспорина.
Реконструктивное хирургическое лечение носило многоэтапный характер. На обоих глазах было выполнено рассечение частичного анкилоблефарона и устранение субтотального симблефарона с пересадкой лоскутов слизистой оболочки полости рта и амниона. Затем проводили устранение рубцового заворота верхнего и нижнего век с пересадкой лоскутов слизистой оболочки полости рта по Сапежко (рис. 4).
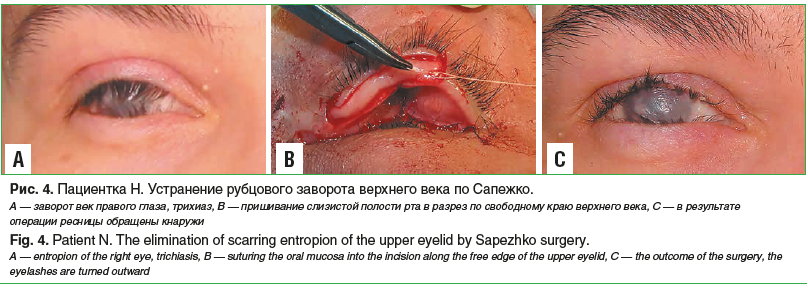
Дополнительно неоднократно выполняли электролиз отдельных неправильно растущих ресниц. С целью улучшения увлажнения глазной поверхности на обоих глазах была проведена лазеркоагуляция слезных точек, а на правом глазу — пересадка малых слюнных желез в верхний конъюнктивальный свод (рис. 5).
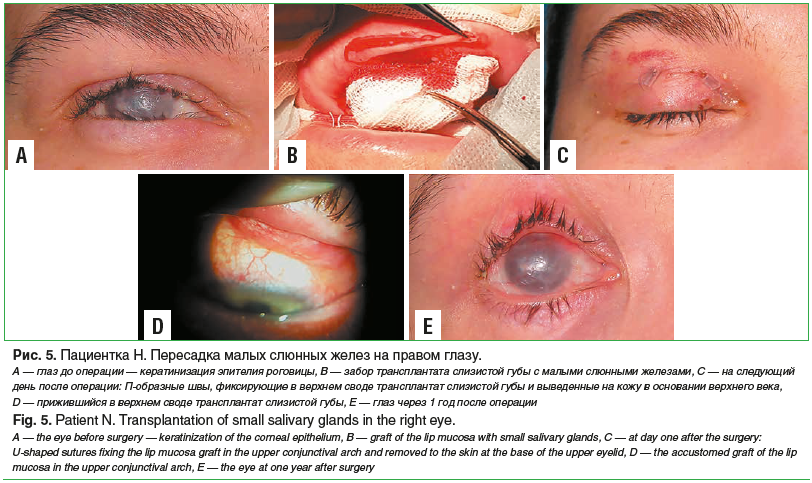
После операции слезопродукция глаза увеличилась незначительно (тест Ширмера I — 3 мм), однако появились признаки легкого увлажнения роговичного эпителия, он просветлел, поверхность его стала более гладкой. Пациентка субъективно отметила ощущение влажности и большего комфорта в глазу, а также некоторое улучшение зрения.
Спустя еще 3 года, по достижении пациенткой совершеннолетия, для устранения лимбальной недостаточности и создания условий для оптической кератопластики на правом глазу была выполнена конъюнктивально-лимбальная аллотрансплантация с забором материала у ее матери (рис. 6) [14].
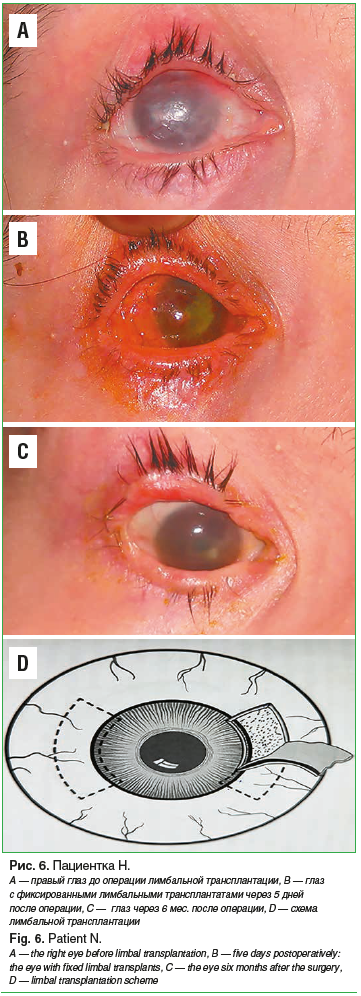
Через 3 мес. после операции с приживлением лимбальных трансплантатов: эпителий роговицы слегка увлажнен, гладкий. Строма заметно просветлела, с легким диффузным помутнением и отдельными поверхностными и глубокими сосудами. Острота зрения 0,04 (см. рис. 6). Качество жизни пациентки улучшилось. Зрение вблизи позволяло ей даже самостоятельно рисовать. Однако в последующие месяцы роговица вновь помутнела и умеренно васкуляризировалась. Эффект операции оказался непродолжительным, по-видимому, в связи с рецидивом конъюнктивализации роговицы по причине отсутствия гистосовместимости после аллогенной лимбальной трансплантации. В настоящее время острота зрения глаз 0,02/0,01.
Обсуждение
Пациент с синдромом ЭЛР в остром периоде, как правило, оказывается в отделении реанимации и интенсивной терапии, где на первый план выходит поддержание витальных функций. Офтальмолог зачастую является лишь консультантом, а не профильным врачом таких больных. К сожалению, не всегда они госпитализируются в многопрофильный стационар, где есть возможность офтальмологического осмотра, что ухудшает дальнейший прогноз для органа зрения.
При первичном обследовании важно своевременно выявить эрозии глазной поверхности с использованием красителя. Для создания условий заживления эрозий, во избежание присоединения вторичной инфекции, развития кератоконъюнктивита и изъязвления роговицы целесообразно назначение антисептического и противовоспалительного лечения кортикостероидными препаратами, применение лечебных мягких контактных линз и осуществление динамического наблюдения. Важен также инструктаж персонала реанимационных отделений о необходимости и кратности тщательного туалета век и конъюнктивальной полости растворами антисептиков перед инстилляциями глазных капель и мазей.
В случаях длительно незаживающих персистирующих эрозий в остром периоде ЭЛР применяется ряд оперативных вмешательств. Одним из них является временное покрытие роговицы и конъюнктивы свежим или консервированным амнионом в качестве биологического бандажа для стимуляции эпителизации. Если имеет место изъязвление роговицы, возможна многослойная пластика его амнионом. Проверенным и щадящим методом закрытия язвенного дефекта при наличии угрозы перфорации роговицы является аутоконъюнктивальная пластика лоскутом конъюнктивы «на ножке». В период лечения пациента в неофтальмологической клинике в случае персистирования эрозии роговицы на помощь приходит простая блефарорафия с возможностью контроля состояния глазного яблока при развязывании провизорного шва.
Чаще офтальмологам приходится иметь дело с отдаленными последствиями ЭЛР. По данным литературы [2–5] и нашим наблюдениям, тяжесть их не связана с исходным объемом пораженных тканей, а скорее, с качеством и своевременностью оказанной в остром периоде офтальмологической помощи.
Недостаток муцина в слезной жидкости приводит к ССГ (встречается в 100% случаев), когда тест Ширмера I, как правило, не превышает 3–5 мм. При этом традиционно применяются заменители слезы и препараты с местной цитостатической активностью. Для улучшения увлажнения глазной поверхности можно также применить пересадку малых слюнных желез по J. Murube [12]. В исходе операции достигается незначительное увеличение увлажнения (на 3–4 мм по тесту Ширмера I), но субъективно пациент обычно отмечает уменьшение дискомфорта.
Для предотвращения инфекционных осложнений важно обучение пациента тщательной гигиене конъюнктивальной полости и век растворами антисептиков.
Рубцовый заворот и различной выраженности трихиаз также являются частыми отдаленными проявлениями синдромов Стивенса — Джонсона и Лайелла. При ограниченном единичном трихиазе эффективным является электролиз 1–3 неправильно растущих ресниц. Чаще у пациентов, перенесших ЭЛР, встречается распространенный трихиаз, с дополнительным рядом неправильно растущих ресниц за счет рубцового заворота века. Пациенты в поликлинике или самостоятельно удаляют себе ресницы пинцетом, однако при отрастании «пеньки» ресниц травмируют роговицу, доставляя дискомфорт. Таким пациентам показано ношение мягких контактных линз в течение 1–1,5 мес. По мере отрастания ресниц выполняется устранение заворота по Сапежко. При симблефаронах и анкилоблефаронах используется рассечение рубцовых спаек с пластикой амнионом при небольших дефектах конъюнктивы или лоскутами слизистой оболочки полости рта при выраженных дефектах, аналогично тактике при ожоговых поражениях [8].
Самым серьезным осложнением синдромов Лайелла и Стивенса — Джонсона, вызывающим значительное понижение зрительных функций, является тотальная лимбальная недостаточность с формированием сосудистого бельма роговицы. Как правило, она развивается при длительном нахождении пациентов в реанимации и несвоевременном или неадекватном офтальмологическом пособии в остром периоде. Оптические операции на таких глазах возможны только после устранения рубцовых деформаций век и слизистой оболочки, нормализации увлажнения глазной поверхности, внутриглазного давления и восстановления нормального эпителиального покрова роговицы посредством лимбальной трансплантации.
Заключение
В остром периоде синдромов Стивенса — Джонсона и Лайелла своевременное системное и местное консервативное лечение в сочетании с хирургическими пособиями (простая блефарорафия с провизорным швом, временное покрытие глазной поверхности амнионом или его трансплантация в роли субстрата для эпителизации, аутоконъюнктивальная пластика лоскутом «на ножке» и др.) играют важную роль в предупреждении тяжелых поздних осложнений со стороны органа зрения. Устранение глазных последствий ЭЛР связано с длительным динамическим наблюдением офтальмологом, пожизненным консервативным лечением ССГ, многоэтапным реконструктивным хирургическим лечением. В зависимости от тяжести поражения органа зрения оно может включать пересадку малых слюнных желез, устранение трихиаза, рубцового заворота век, анкилоблефарона, симблефарона, конъюнктивально-лимбальную аллотрансплантацию, оптическую кератопластику и др.
1 Общероссийская общественная организация «Российское общество дерматовенерологов и косметологов». Клинические рекомендации 2020 г. Синдром Стивенса – Джон- сона (проект). (Электронный ресурс.) URL: https://cnikvi.ru/docs/clinic_recs/klinicheskie-rekomendatsii-2019-2020.docx (дата обращения: 12.12.2021).
Сведения об авторах:
Черныш Валерий Федорович — к.м.н., доцент, доцент кафедры офтальмологии Военно-медицинской академии имени С.М. Кирова; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, литера Ж; ORCID iD 0000-0003-0122-4164.
Харитонова Наталья Николаевна — к.м.н., доцент кафедры офтальмологии Военно-медицинской академии имени С.М. Кирова; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, литера Ж; ORCID iD 0000-0002-8550-7171.
Куликов Алексей Николаевич — д.м.н., профессор, начальник кафедры офтальмологии Военно-медицинской академии имени С.М. Кирова; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, литера Ж; ORCID iD 0000-0002-5274-6993.
Качерович Полина Андреевна — преподаватель кафедры офтальмологии Военно-медицинской академии имени С.М. Кирова; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, литера Ж; ORCID iD 0000-0001-9629-5437.
Кольбин Алексей Анатольевич — преподаватель кафедры офтальмологии Военно-медицинской академии имени С.М. Кирова; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, литера Ж; ORCID iD 0000-0002-8305-3049.
Контактная информация: Харитонова Наталья Николаевна, e-mail: natal56@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 24.03.2022.
Поступила после рецензирования 18.04.2022.
Принята в печать 17.05.2022.
About the authors:
Valery F. Chernysh — C. Sc. (Med.), associate professor of the Ophthalmology Department, S.M. Kirov Military Medical Academy; 6Zh, Academician Lebedev str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0003-0122-4164.
Natalya N. Haritonova — C. Sc. (Med.), associate professor of the Ophthalmology Department, S.M. Kirov Military Medical Academy; 6Zh, Academician Lebedev str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0002-8550-7171.
Aleksey N. Kulikov — Dr. Sc. (Med.), Professor, Head of the Ophthalmology Department, S.M. Kirov Military Medical Academy; 6Zh, Academician Lebedev str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0002-5274-6993.
Polina A. Kacherovich — lecturer of the Ophthalmology Department, S.M. Kirov Military Medical Academy; 6Zh, Academician Lebedev str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0001-9629-5437.
Aleksis A. Kol'bin — lecturer of the Ophthalmology Department, S.M. Kirov Military Medical Academy; 6Zh, Academician Lebedev str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0002-8305-3049. Contact information: Natalya N. Haritonova, e-mail: natal56@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 24.03.2022.
Revised 18.04.2022.
Accepted 17.05.2022.
2. Metcalfe D., Iqbal O., Chodosh J. et al. Acute and Chronic Management of Ocular Disease in Stevens Johnson Syndrome/Toxic Epidermal Necrolysis in the USA. Front Med (Lausanne). 2021;8:662897. DOI: 10.3389/fmed.2021.662897.
3. Roujeau J.C., Bastuji-Garin S. Systematic review of treatments for Stevens-Johnson syndrome and toxic epidermal necrolysis using the SCORTEN score as a tool for evaluating mortality. Ther Adv Drug Saf. 2011;2(3):87–94. DOI: 10.1177/2042098611404094.
4. Sotozono C., Ueta M., Koizumi N. et al. Diagnosis and treatment of Stevens-Johnson syndrome and toxic epidermal necrolysis with ocular complications. Ophthalmology. 2009;116(4):685–690. DOI: 10.1016/j.ophtha.2008.12.048.
5. Min Ho Kang. Ocular Manifestations of Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis. Hanyang Med Rev. 2016;36(3):174–181. DOI: 10.7599/hmr.2016.36.3.174.
6. Ушаков Н.А. Мягкие контактные линзы в лечении ожогов глаз легких и средней тяжести. Офтальмологический журнал. 1988:7:440–441.
7. Pakarinen M., Tervo T., Tarkkanen A. Tarsorraphy in the treatment of persistent corneal lesions. Acta Ophthalmol Suppl (1985). 1987;182:69–73. DOI: 10.1111/j.1755-3768.1987.tb02595.x.
8. Черныш В.Ф., Бойко Э.В. Ожоги глаз. Состояние проблемы и новые подходы. 2-е изд. дополн. М.: ГЭОТАР-Медиа, 2017.
9. Liang L., Sheha H., Li J., Tseng S.C. Limbal stem cell transplantation: new progresses and challenges. Eye (Lond). 2009;23(10):1946–1953. DOI: 10.1038/eye.2008.379.
10. Одинцов В.П., Орлов К.Х. Руководство по глазной хирургии. М.; Л.: Биомедгиз, 1934.
11. Бржеский В.В., Сомов Е.Е. Роговично-конъюнктивальный ксероз (диагностика, клиника, лечение). СПб.: Левша; 2003.
12. Murube J., Wilson St., Ramos-Esteban J. The important developments in dry eye. Highlist Ophthalmol. 2001;29(5):54–66.
13. Злобин И.А., Черныш В.Ф., Чурашов В.С. и др. Роль импрессионной цитологии в оценке фенотипа эпителия роговицы при решении вопроса о показаниях к операции оптической кератопластики. Вестник Pоссийской военно-медицинской академии. 2016;1(53):89–93.
14. Черныш В.Ф., Бойко Э.В., Шишкин М.М. Лимбальная трансплантация в лечении и зрительной реабилитации пациентов с тяжелыми химическими ожогами глаз. Вестник офтальмологии. 2004;120(2):8–11.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
