Клиническая эффективность и безопасность применения препарата Ракстан-сановель у пациентов с острой болью в поясничном отделе позвоночника (результаты многоцентрового постмаркетингового обсервационного исследования)
DOI: 10.32364/2587-6821-2022-6-10-541-550
Цель исследования: анализ эффективности (скорость наступления, сила и продолжительность обезболивания) и безопасности нестероидного противовоспалительного препарата (НПВП) Ракстан-сановель (флурбипрофен; далее — Ракстан) в комплексном лечении пациентов с острой БНЧС.
Материал и методы: в исследовании приняли участие 210 пациентов с острой БНЧС, рандомизированные на 2 однотипные группы по 105 человек. В контрольной группе (КГ) применялась стандартная схема лечения в течение двух последовательных недель. Медикаментозная терапия включала любой НПВП (кроме препарата Ракстан), миорелаксанты, витамины группы В в дозах, рекомендованных в инструкции по применению препарата; немедикаментозная терапия — физические упражнения или физиотерапию (пациенты могли получать один из этих методов лечения или их комбинацию) по усмотрению врача. В основной группе (ОГ) для купирования болевого синдрома использовался Ракстан в сочетании с другой необходимой сопутствующей терапией (миорелаксанты, витамины группы В, физические упражнения и физиотерапия). Динамику клинического статуса анализировали по следующим шкалам: ВАШ боли, опросники Роланда — Морриса, CGI (для оценки общего клинического впечатления врача и пациента), EQ-5D-5L. Общая длительность наблюдения составила 10 дней приема препарата, а также 2 последующие недели.
Результаты исследования: большинство пациентов составили женщины (количественная пропорция мужчин и женщин 1:1,4); средний возраст 43,5 [29; 57] года с длительностью заболевания 14,4±6,3 сут. Спондилоартроз на уровне поясничного отдела позвоночника оказался преимущественным триггером боли у 105 (50%) пациентов, поражение крестцово-подвздошного сочленения — у 39 (18,6%), дегенеративно-дистрофические изменения межпозвонкового диска — у 66 (31,4%). Большинство (68%) пациентов в обеих группах имели умеренный уровень боли со значением по ВАШ 45–74 баллов. К концу курса терапии средняя разница между группами по ВАШ составила 19 баллов. К окончанию курса терапии 90% пациентов ОГ достигли нулевого уровня боли по ВАШ, в то время как в КГ — только 50%. Кроме того, через 2 нед. после окончания лечения в ОГ не зарегистрировано ни одного рецидива боли, а улучшение оценки функционального состояния по опроснику Роланда — Морриса в ОГ составило 69% (41,6 балла), в КГ — только 24% (14,3 балла). Оценка общего клинического впечатления врача по опроснику CGI в ОГ показала, что 86 пациентов из 105 оценили свое состояние как «полностью нормальное», в то время как в КГ только 1 пациент дал такую оценку. Нежелательные явления (тошнота, боль в желудке, головокружение, диарея) отмечены у 4 пациентов КГ.
Заключение: применение препарата Ракстан позволяет ускорить выздоровление пациентов с острой БНЧС без развития дополнительных побочных явлений, что может иметь существенное преимущество в рациональной терапии, профилактике хронизации и повторных обострений у больных данной категории.
Ключевые слова: острая боль в области нижней части спины, нестероидные противовоспалительные препараты, флурбипрофен, Ракстан, рецидив.
Для цитирования: Данилов А.Б., Меркулова Д.М., Живолупов С.А., Девликамова Ф.И., Доронин Б.М., Широков В.А., Балязина Е.В., Комаров А.Н. Клиническая эффективность и безопасность применения препарата Ракстан-сановель у пациентов с острой болью в поясничном отделе позвоночника (результаты многоцентрового постмаркетингового обсервационного исследования). РМЖ. Медицинское обозрение. 2022;6(10):541-550. DOI: 10.32364/2587-6821-2022-6-10-541-550.
Введение
Боль в области нижней части спины (БНЧС) предполагает неприятные ощущения или дискомфорт в области, располагающейся между нижними ребрами и ягодичными складками, с проекцией или без проекции в нижнюю конечность и возникает ежегодно у 25–40% людей во всем мире, а вероятность того, что в течение жизни у человека возникнет острая БНЧС, составляет 70% [1]. Острая БНЧС продолжается не больше 6 нед., в случае рациональной терапии или вследствие естественных причин (саногенез) регрессирует, но примерно у трети больных хронизируется — сохраняется более года, а еще примерно у 50–80% больных в первый год после неполного купирования острой БНЧС те или иные симптомы основного заболевания (дорсопатия, сакроилеит и др.) повторяются [1, 2].
Острая боль может быть первичной или вторичной (обострение хронически протекающего заболевания); в любом случае она инициируется триггерами, формирующимися вследствие развития дегенеративно-дистрофических процессов в дугоотростчатых суставах, межпозвонковых дисках и крестцово-подвздошном сочленении, а также стеноза позвоночного канала и др. Несмотря на повсеместное применение нейровизуализационного обследования (МРТ, КТ пояснично-крестцового отдела позвоночника) в дифференциальной диагностике патогенетических форм острой БНЧС, достоверной корреляции между выявленными по данным МРТ изменениями и степенью выраженности болевого синдрома, снижением качества жизни, а также психоэмоциональными расстройствами у данной категории пациентов выявлено не было [3, 4].
Учитывая главенство воспалительной составляющей в генезе острой БНЧС, в базовую схему медикаментозного лечения пациентов данного профиля обычно включают нестероидные противовоспалительные препараты (НПВП), миорелаксанты, витамины группы В, хондропротекторы и лечебные блокады, что позволяет дезактивировать триггеры боли и предупредить хронизацию болевого синдрома и других проявлений основного заболевания (например, нарушение статической и динамической функции позвоночника) [2]. Базовая терапия, как правило, дополняется немедикаментозными методами лечения, такими как мануальная терапия, массаж, кинезиологическое тейпирование, лечебная гимнастика, вытяжение позвоночника, физиотерапия, направленные на постепенное увеличение двигательных возможностей больного, коррекцию осанки и неадаптивного двигательного стереотипа.
Однако разные НПВП неодинаково контролируют острую БНЧС, особенно в части длительности обезболивающего эффекта и качества жизни пациента во время лечения.
Цель исследования: анализ эффективности (скорость наступления, сила и продолжительность обез-боливания) и безопасности НПВП Ракстан-сановель (флурбипрофен, далее — Ракстан) в комплексном лечении пациентов с острой БНЧС. Выбор данного препарата обусловлен тем, что флурбипрофен обладает выраженным обезболивающим и противовоспалительным действием при высокой биодоступности [4].
Материал и методы
Для реализации поставленной цели на территории Российской Федерации было проведено многоцентровое постмаркетинговое обсервационное исследование. Препарат Ракстан назначался в рамках рутинной клинической практики согласно утвержденной локальной инструкции по применению препарата с указанием доз, продолжительности терапии, популяции и показаний.
Критерии включения в исследование:
возраст пациентов от 18 до 65 лет;
длительность БНЧС не менее 1 нед. и не более 6 нед. независимо от наличия данных о БНЧС в анамнезе;
интенсивность боли по ВАШ не менее 30 баллов;
отсутствие указаний на непереносимость флурбипрофена в анамнезе;
подписанное пациентом информированное согласие на участие в наблюдательной программе.
Критерии невключения в исследование:
применение НПВП менее чем за 1 мес. до момента включения в программу;
наличие органических заболеваний нервной системы, психических заболеваний или онкологической патологии;
гиперчувствительность к исследуемому препарату или вспомогательным компонентам, в том числе к другим НПВП или ацетилсалициловой кислоте;
эрозивно-язвенные поражения или воспалительные заболевания ЖКТ в стадии обострения;
бронхиальная астма в сочетании с полипозом слизистой носа;
тяжелая почечная и печеночная недостаточность;
применение антидепрессантов, антиконвульсантов, опиоидных анальгетиков в период проведения исследования;
беременность или лактация;
лечение глюкокортикоидами в течение последних 2 мес.;
другие состояния, которые делали участие пациента в исследовании невозможным (по мнению исследователя).
Критерии исключения из исследования. Пациент считался исключенным из исследования, если его участие было прекращено до завершения планируемых визитов/оценок, указанных в протоколе. Пациенты могли быть исключены из исследования по любой из следующих причин: развитие нежелательных явлений, непереносимость препарата Ракстан, добровольный отказ пациента от участия, по решению исследователя, другие причины.
В программу были включены 210 пациентов с острой БНЧС, не требующей хирургического лечения. Большинство пациентов составили женщины (количественная пропорция мужчин и женщин 1:1,4); средний возраст 43,5 [29; 57] года с длительностью заболевания 14,4±6,3 сут.
Спондилоартрит на уровне поясничного отдела позвоночника оказался преимущественным триггером боли у 105 (50%) пациентов, поражение крестцово-подвздошного сочленения — у 39 (18,6%), дегенеративно-дистрофические изменения межпозвонкового диска — у 66 (31,4%). Наибольшее количество (68%) пациентов в обеих группах имели умеренный уровень боли с оценкой по ВАШ 45–74 баллов, 20% — сильную боль (75–100 баллов по ВАШ).
До включения в программу все пациенты в полном объеме были проинформированы об условиях участия в программе и подписали форму информированного согласия.
Пациенты, включенные в исследование, были случайным образом (методом конвертов) рандомизированы в 2 однотипные группы. В контрольной группе (КГ) применялась стандартная схема лечения в течение 10 дней: медикаментозная терапия — любой неселективный НПВП, кроме изучаемого препарата (диклофенак по 50 мг 3 р/сут у 70% пациентов и мелоксикам по 15 мг/сут у 30%), миорелаксанты в дозах, рекомендованных в инструкции по применению препарата; немедикаментозная терапия — физические упражнения или физиотерапия (пациенты могли получать один из этих методов лечения или их комбинацию) по усмотрению врача. В основной группе (ОГ) для купирования болевого синдрома использовался Ракстан (по 100 мг 2 р/сут) в сочетании с другой необходимой сопутствующей терапией — миорелаксантами, физическими упражнениями и физиотерапией. Каждый пациент, включенный в исследование, находился под наблюдением в течение 10 дней приема препаратов, а также последующие 2 нед. (всего 4 визита: визит 0 — скрининг, визит 1 — через 1 нед. от начала лечения, визит 2 — через 2 нед. от начала лечения, визит 3 — через 2 нед. после завершения лечения).
Первичной конечной точкой исследования являлась оценка степени снижения интенсивности болевого синдрома после курса лечения препаратом Ракстан (10 дней) по ВАШ в сравнении с другими НПВП. Минимальное клинически значимое различие (МКЗР) для показателя ВАШ составляет 15 пунктов, или 30%. В качестве вторичных конечных точек приняты оценка динамики качества жизни и длительность бессимптомного периода после курса лечения на основании общепринятых критериев:
оценка интенсивности боли и связанных с ней функциональных расстройств по опроснику Роланда — Морриса (МКЗР для показателя составляет 5 пунктов);
определение качества жизни по опроснику EQ-5D-5L;
впечатления врача и пациента об эффективности лечения (7-балльная система оценки общего клинического впечатления по шкале CGI);
наличие или отсутствие БНЧС через 2 нед. после окончания лечения.
Особое внимание уделялось контролю безопасности применения исследуемого препарата. Каждое нежелательное явление было задокументировано со ссылкой на интенсивность, дату начала, продолжительность, частоту, лечение, результаты, изменения и дату окончания.
Все данные о включенных пациентах вводили в специально разработанные индивидуальные регистрационные карты для статистической обработки результатов и были обезличены для сохранения конфиденциальности пациентов. Для статистического анализа полученные в ходе исследования данные вносили в базу, сформированную на основе программного обеспечения Excel. Для статистического анализа результатов исследования использовали общепринятые методы из пакета программ Statisticа 7.0 (StatSoft, Inc., США) в соответствии с рекомендациями по обработке результатов медико-биологических исследований [17]. Для сравнительного анализа качественных параметров пользовались критерием χ2 или критерием Фишера. Значимость различий между количественными величинами оценивали по критерию t Стьюдента в модификации Уэлча (для нормально распределенных величин) или критерию Манна — Уитни (в случае непараметрических данных). Пороговый уровень значимости был принят равным 0,05. Сравнение показателей по ВАШ в группах между визитами осуществляли с использованием непараметрического критерия Вилкоксона для зависимых выборок и теста Краскела — Уоллиса. Разницу терапевтического эффекта между визитами оценивали с помощью теста Бхапкара с поправкой Бонферрони для всех парных сравнений.
Результаты исследования
Группы были сопоставимы по половому составу (χ2=0,02, p=0,088), большинство составили женщины — 60 и 62 пациентки в КГ и ОГ соответственно. Средний возраст пациентов КГ составил 44 [33; 52] года, ОГ — 46 [29; 57] лет (p=0,43, критерий Манна — Уитни). Все пациенты завершили исследование. Базовое среднее значение интенсивности боли во всей выборке (n=210) по ВАШ составило 60 [50; 70] мм; в рассматриваемых группах по 60 [50; 70] мм, что соответствовало «умеренно выраженной» боли и не имело достоверного различия между группами (p=0,833, критерий Манна — Уитни). При этом количество больных из общей выборки со слабой интенсивностью боли (5–44 мм) составило 25 (12%), умеренной (45–74 мм) — 143 (68%), сильной (75–100 мм) — 42 (20%).
В обеих группах от проводимого лечения получен достоверный позитивный эффект по ВАШ, причем улучшение оцениваемых параметров в ОГ оказалось значимо выше на всех визитах (рис. 1). На момент завершения исследования (визит 3, через 2 нед. после терапии) в ОГ отмечался значимо более полный контроль над БНЧС по данным ВАШ по сравнению с КГ — количество (доля) больных с отсутствием боли и слабой болью было статистически значимо выше. Оценка по ВАШ составила 20 [20; 30] мм в КГ и 5 [0; 10] мм — в ОГ (рис. 1, 2). При межгрупповом сравнении на каждом визите получены статистически значимые различия (критерий Манна — Уитни, p<0,0001).
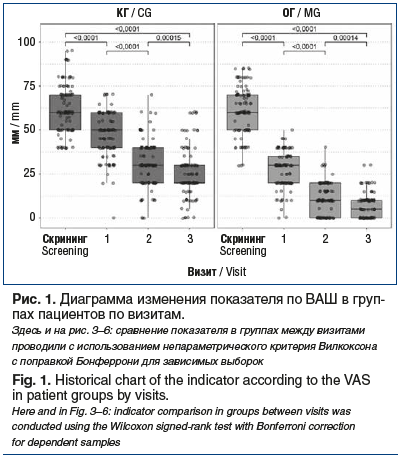
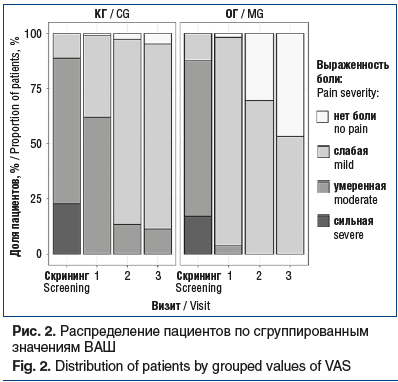
Согласно данным опросника Роланда — Морриса интенсивность острой БНЧС была непосредственно связана с функциональными расстройствами у пострадавших, исходная оценка в КГ составила 11 [6; 16], в ОГ — 10 [7; 15] (p=0,496). В процессе лечения в обеих группах наблюдалось клинически и статистически значимое снижение значений показателя между визитами (p<0,0001); однако эффективность снижения функциональных расстройств по шкале Роланда — Морриса между группами статистически значимо различалась на всех визитах (критерий Манна — Уитни, p<0,0001). Так, в ОГ уже на визите 2 рассматриваемый показатель составил 2 [1; 3], в то время как у больных КГ — 6 [5; 8]; величина эффекта снижения относительно исходных значений составила 0,868 и 0,641 соответственно. К визиту 3 значения показателя в ОГ и КГ были равны 1 [0; 2] и 5 [3; 6] соответственно (рис. 3).
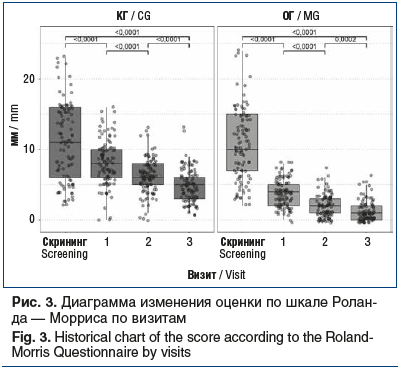
Снижение интенсивности болевого синдрома и уменьшение степени функциональных нарушений у обследованных больных в обеих группах коррелировало с позитивными изменениями общего клинического впечатления врача по опроснику CGI в виде статистически значимого снижения тяжести расстройств между 1-м и 3-м визитами (p<0,0001): у больных ОГ с 2 [1; 2] до 1 [1; 1], у больных КГ с 4 [3; 4] до 3 [2; 3] (рис. 4). При этом эффективность терапевтического снижения тяжести расстройств по шкале CGI между группами достоверно различалась на визите 2 по абсолютным значениям (p=0,0041) и на визите 3 по относительным (p=0,047).
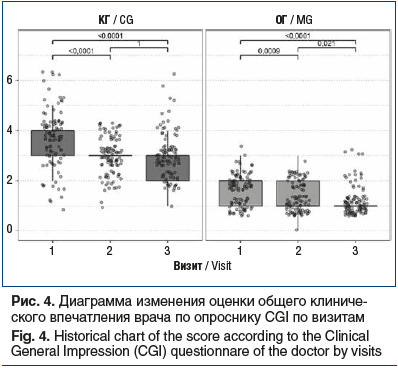
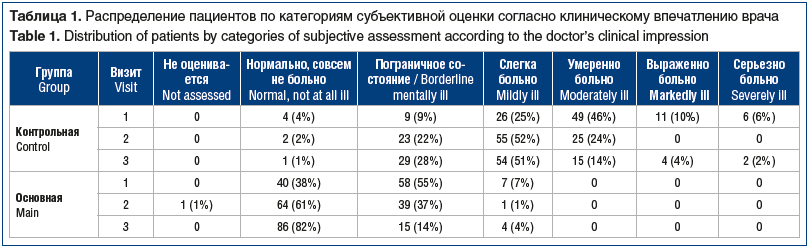
Для системного анализа эффективности терапии по общему клиническому впечатлению врача больные в обеих группах были распределены по категории «тяжесть состояния» (табл. 1). Как видно из представленных данных, количество больных в категориях субъективной оценки «нормально, совсем не больно», «пограничное состояние», «слегка больно» было значительно большим в ОГ; а больных в категориях субъективной оценки «умеренно больно», «выраженно больно» и «серьезно больно» не было совсем. Анализ перераспределения пациентов между категориями тяжести по шкале CGI показал статистическую значимость (p<0,0001, тест Бхапкара) в обеих группах между визитами 1 и 3.
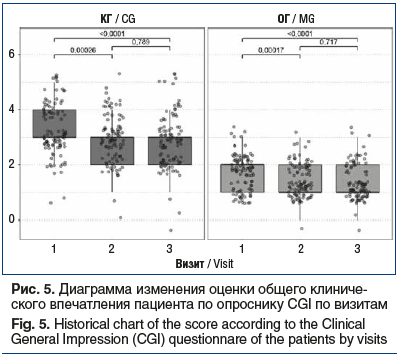
Аналогичные позитивные изменения общего клинического впечатления по опроснику CGI выявлены с точки зрения пациентов. В обеих группах (рис. 5) наблюдалось статистически значимое снижение тяжести расстройств, вызванных острой БНЧС, по данным оценки общего клинического впечатления пациента по опроснику CGI между 1-м (в ОГ — 2 [1; 2], в КГ — 3 [3; 4]) и 2-м (в ОГ — 1 [1; 2], в КГ — 3 [2; 3]) (p<0,001) и 1-м и 3-м (в ОГ — 1 [1; 2], в КГ — 3 [2; 3]) визитами (p<0,0001).
Кроме сравнительного анализа отдельных параметров состояния здоровья больных с острой БНЧС (ВАШ, шкала функциональных нарушений Роланда — Морриса, общее клиническое впечатление по опроснику CGI) особое внимание было уделено оценке конечного терапевтического эффекта по мнению врача, в соответствии с которым больные распределялись на следующие категории: «значительное улучшение», «умеренное улучшение», «минимальное (незначительное) улучшение, которое не меняет состояние больного», «без эффекта или ухудшение» (табл. 2).

В обеих группах наблюдался статистически значимый терапевтический эффект между 1-м (в ОГ — 54 человека со значительным улучшением, 51 — с умеренным; в КГ — 6 и 30 человек соответственно) и 2-м (в ОГ — 79 человек со значительным улучшением, 25 — с умеренным; в КГ — 3 и 56 человек соответственно) визитами по тесту Бхапкара с поправкой Бонферрони для всех парных сравнений (p<0,01) и между визитами 1 и 3 (в ОГ 89 человек со значительным улучшением, 16 — с умеренным; в КГ — 4 и 55 человек соответственно) (p<0,01).
Изменение терапевтического эффекта между визитами 2 и 3 было статистически незначимо в обеих группах (в ОГ р=0,935, в КГ р=0,072). Однако на каждом визите наблюдались статистически значимые (p<0,01) различия между группами; более того, отсутствие эффекта или ухудшение на последнем визите наблюдалось у 8 (7,6%) пациентов КГ, в то время как в ОГ таких больных не было.
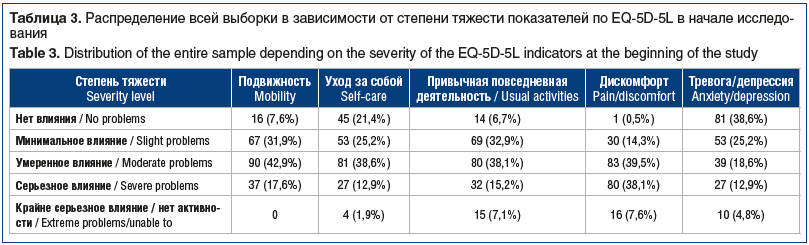
Острая БНЧС, по данным опросника EQ-5D-5L, влияла на качество жизни больных, особенно на подвижность (умеренное влияние у 42,9% пациентов), уход за собой (умеренное влияние у 38,6%), привычную повседневную деятельность (умеренное влияние у 38,1%) и дискомфорт (умеренное влияние у 39,5%). При этом только у 25,2% больных выявлено минимальное влияние на формирование тревоги/депрессии, а крайне серьезное влияние обнаружено в части некоторых показателей (уход за собой, привычная повседневная деятельность, дискомфорт, тревога/депрессия) в 1,9–7,6% случаев (табл. 3).
В процессе лечения в обеих группах наблюдалось статистически значимое улучшение качества жизни пациентов по данным опросника EQ-5D-5L относительно скрининга на визитах 2 и 3 (табл. 4). В КГ на визите 3 сохранялось от 2 до 4 пациентов (2–4%) с крайне серьезным влиянием по всем показателям опросника (подвижность, уход за собой, привычная повседневная деятельность, дискомфорт, тревога/депрессия) и от 16 до 29 (15–27%) — с умеренным влиянием.
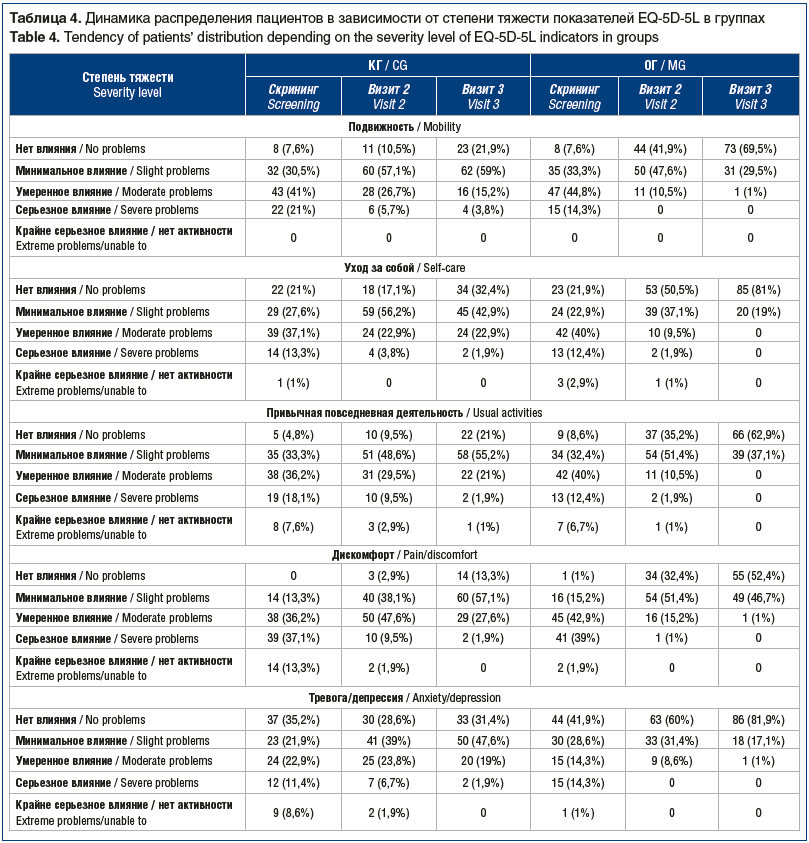
В ОГ к визиту 3 отсутствовали пациенты с серьезным влиянием, а умеренное влияние на качество жизни наблюдалось в единичных случаях (1%). При этом на визитах 2 и 3 различия показателей (подвижность, уход за собой, привычная повседневная деятельность, дискомфорт, тревога/депрессия) между группами были статистически значимыми (тест Бхапкара, р<0,0001 с поправкой на множественные сравнения Бонферрони). На этапе скрининга статистической значимости достигали только различия показателей «дискомфорт» и «тревога/депрессия» (р=0,017, р=0,32 соответственно).
Изменение тяжести нарушений согласно опроснику EQ-5D-5L в каждой группе на визитах 2 и 3 по сравнению с базовым значением, полученным на этапе скрининга, во всех случаях было статистически значимым (p<0,0001).
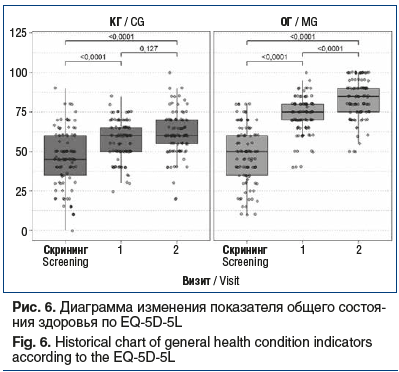
С учетом представленных выше данных закономерным было статистически значимое улучшение общего состояния здоровья на основании суммарного балла по опроснику EQ-5D-5L в обеих группах между скрининговым визитом и визитами 2 и 3 (p<0,0001). Динамика общего состояния здоровья по EQ-5D-5L статистически значимо (p<0,0001) различалась в обеих группах: суммарный балл на визите 2 в ОГ составил 75 [70; 80], в КГ — 60 [50; 65], на визите 3 — 85 [75; 90] и 60 [55; 70] соответственно (рис. 6). Это свидетельствует в пользу большей терапевтической эффективности противовоспалительного препарата Ракстан в составе комплексной терапии больных с острой БНЧС.
Кроме этого, включение препарата Ракстан в комплексное лечение острой БНЧС позволило добиться значительного сокращения количества нежелательных реакций, которые обычно свойственны препаратам группы НПВП: в ОГ, принимавшей исследуемый препарат, не было зафиксировано ни одной нежелательной реакции, в то время как в КГ они отмечены у 4 пациентов (у 1-го — тошнота, боль в желудке; у 2-го — тошнота, головокружение; у 3-го — боль в желудке, диарея; у 4-го — тошнота), что потребовало применения симптоматических средств лечения. Данное обстоятельство представляется очень важным аргументом в пользу выбора препарата Ракстан, поскольку нежелательные реакции отрицательно влияют на приверженность пациентов терапии и на долгосрочный прогноз развития основного заболевания, сопровождающегося острой БНЧС.
Обсуждение
Выполненное исследование согласуется с современной доктриной рациональной терапии острой БНЧС, в основе которой лежит применение НПВП, обладающих противоболевым и противовоспалительным действием, в качестве препаратов первой линии. Несмотря на относительную сопоставимость выраженности обезболивающего действия различных НПВП, назначаемых в терапевтических дозировках, соотношение противоболевого и противовоспалительного эффектов данных лекарственных средств может различаться, что следует учитывать при выборе оптимального препарата для конкретного пациента с острой БНЧС [5, 6].
Особенно это связано с тем, что качественное купирование острых болевых синдромов при патологии позвоночника является обязательным условием для профилактики хронизации боли вследствие «лечебно-обусловленного истощения ноцицептивного трафика». Поэтому проблема выбора НПВП в зависимости от патогенетического варианта дорсопатии с учетом анализа триггеров боли (структурных изменений опорно-двигательного аппарата позвоночника) находится в стадии интенсивного изучения [2, 3, 5, 6].
Флурбипрофен (Ракстан) — производное фенилпропионовой кислоты — является типичным представителем НПВП. Данный препарат угнетает активность циклооксигеназ 1-го и 2-го типов, подавляя реакции арахидонового каскада и ингибируя синтез как простагландинов, так и тромбоксана A2, что позволяет ему оказывать мощное системное противоболевое и противовоспалительное действие. Флурбипрофен отличается от других НПВП длительной историей клинического применения, которая насчитывает несколько десятилетий, так же как и некоторые другие широко используемые в клинической практике препараты данной группы, например диклофенак [7, 8].
Проведенные клинические исследования позволили установить высокую терапевтическую эффективность флурбипрофена (быстрое наступление обезболивающего эффекта и продолжительное действие) для купирования острой боли средней и высокой интенсивности наряду с высоким профилем безопасности и хорошей переносимостью [7]. Особенно это относится к такой распространенной группе заболеваний, как дорсопатии.
В одном из исследований, включившем 40 пациентов с хронической дорсалгией, проведен сравнительный анализ эффективности флурбипрофена (20 пациентов получали его по 100 мг 2 р/сут в течение 4 нед.) и плацебо в отношении влияния на выраженность болевого синдрома, сроки купирования боли, результаты лечения по мнению самого пациента и лечащего врача, выраженность депрессивных проявлений, а также значимость влияния заболевания на качество жизни больного [7]. Авторами установлено, что флурбипрофен приводит к более полному и раннему купированию болевого синдрома, более раннему расширению возможности самообслуживания по сравнению с группой больных, получавших плацебо. Кроме того, лечение флурбипрофеном оказалось более эффективным по сравнению с плацебо, по мнению как врача, так и больного; а нежелательные явления одинаково часто регистрировались в обеих группах.
Аналогичный профиль результатов получен в нашем исследовании с участием 210 пациентов с острой БНЧС. Все пациенты были случайным образом рандомизированы на 2 однотипные группы: ОГ, в которой для лечения больных в составе комплексной терапии использовался флурбипрофен, и КГ, в которой для лечения больных в составе комплексной терапии использовались другие НПВП. В большинстве (68%) случаев боль характеризовалась как умеренная. Разница в темпах снижения выраженности боли по ВАШ между группами была очевидна уже с визита 1 (7 дней от начала лечения) и в среднем составляла 20 баллов на каждом последующем визите. К концу наблюдения средняя разница между группами составляла 19 баллов (75%) по ВАШ в пользу больных ОГ; в частности, на визите 3 90% пациентов ОГ достигли нулевого уровня боли по ВАШ, в то время как в КГ — только 50%.
Кроме того, пациенты, получавшие Ракстан, через 2 нед. после окончания лечения (визит 3) продемонстрировали 100% отсутствие рецидива болевого синдрома после курса лечения препаратом — ни у одного пациента не было отмечено рецидива болевого синдрома.
Кроме обезболивающего эффекта, большое значение имеет оценка безопасности флурбипрофена. Так, в одном из исследований на основании анализа данных 200 пациентов (средний возраст 52,7 (22–72) года, 71% — женщины) с остеоартритом (n=50), ревматоидным артритом (n=130), анкилозирующим спондилитом (n=20), которые ежедневно принимали по 200 мг флурбипрофена, были получены убедительные доказательства безопасности данного препарата [8]. Это согласуется с результатами нашего и других исследований [9].
Существенным преимуществом флурбипрофена является умеренное хондропротективное действие, что очень важно при лечении дорсопатий, поскольку, к сожалению, некоторые представители НПВП негативно влияют на костную и хрящевую ткань, что продемонстрировано в условиях эксперимента и в клинических исследованиях [10, 11]. Применение флурбипрофена способно замедлять резорбцию костной ткани, предупреждать внекостное накопление солей кальция, что предотвращает оссификацию связок при остеоартрите [12, 13]. Наличие указанных свойств флурбипрофена дает веские основания рассматривать его не только как обезболивающее лекарственное средство, но и как болезньмодифицирующее средство, замедляющее прогрессирование спондилоартрита. В связи с этим становится понятным более значительное снижение степени функциональных нарушений, связанных с острой БНЧС, у больных ОГ по опроснику Роланда — Морриса: в среднем улучшение повседневной активности составило 69% (41,6 балла), в то время как в КГ — 24% (14,3 балла).
Наше прямое сравнительное исследование — первое в своем роде, в котором предпринята попытка оценить эффективность и безопасность кратковременного применения флурбипрофена в лечении пациентов с острой БНЧС. Поэтому была проведена оценка эффективности терапии на основании общего клинического впечатления врача и пациента по опроснику CGI; в ОГ 86 пациентов из 105 оценили свое состояние как «полностью нормальное», в то время как в КГ только 1 пациент дал такую оценку. В свою очередь, индекс эффективности лечения статистически значимо различался между группами на каждом визите; к окончанию курса терапии значительное улучшение и ремиссия наблюдались у 89 пациентов ОГ, в то время как в КГ — лишь у 4 пациентов, а у 50% пациентов этой группы удалось добиться только частичной ремиссии. Отсутствие эффекта или ухудшение на последнем визите в КГ наблюдалось у 8 (7,6%) пациентов, тогда как в ОГ таких пациентов не было, что позволяет рассматривать флурбипрофен в качестве препарата выбора для лечения пациентов с острой БНЧС.
Одним из преимуществ флурбипрофена, по нашим данным и сведениям других авторов, является низкий риск лекарственных взаимодействий, что обеспечило возможность его применения в комбинации с другими средствами противоболевого действия (миорелаксанты, витамины группы В), а также хорошая переносимость [14].
Заключение
Таким образом, кратковременное (до 10 сут) применение флурбипрофена (Ракстан-сановель) в дозе 200 мг/сут эффективно и безопасно при острой БНЧС. Данный препарат уменьшает выраженность болевого синдрома (по ВАШ), увеличивает повседневную активность пациентов и улучшает качество их жизни (по опросникам Роланда — Морриса и EQ-5D-5L) уже к 7-м суткам лечения достоверно значительнее, чем другие НПВП, в частности диклофенак. С учетом отсутствия нежелательных явлений (по нашим данным) это позволяет рекомендовать флурбипрофен в качестве эффективного обезболивающего средства для широкой клинической практики.
Сведения об авторах:
Данилов Алексей Борисович — д.м.н., заведующий кафедрой нервных болезней ИПО ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0003-2958-4479.
Меркулова Дина Мироновна — д.м.н., профессор, врач-невролог высшей квалификационной категории, главный невролог Центральной дирекции здравоохранения — филиала ОАО «РЖД», руководитель Неврологического центра им. Б.М. Гехта ЧУЗ «Центральная клиническая больница «РЖД-медицина»; 129128, Россия, г. Москва, ул. Будайская, д. 2; ORCID iD 0000-0003-0368-683X.
Живолупов Сергей Анатольевич — д.м.н., полковник медицинской службы, профессор кафедры нервных болезней Военно-медицинской академии имени С.М. Кирова; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, литера Ж; ORCID iD 0000-0003-0363-102X.
Девликамова Фарида Ильдусовна — д.м.н., профессор кафедры неврологии и мануальной терапии КГМА — филиала ФГБОУ ДПО РМАНПО Минздрава России; 420012, Россия, г. Казань, ул. Муштари, д. 11.
Доронин Борис Матвеевич — д.м.н., профессор, заведующий кафедрой неврологии ФГБОУ ВО НГМУ Минздрава России; 630091, Россия, г. Новосибирск, Красный пр-т, д. 52; ORCID iD 0000-0001-7213-759X.
Широков Василий Афанасьевич — д.м.н., профессор кафедры нервных болезней с курсом нейрохирургии, мануальной терапии ФГБОУ ВО УГМУ Минздрава России; 620028, Россия, г. Екатеринбург, ул. Репина, д. 3; ведущий научный сотрудник ФБУН ЕМНЦ ПОЗРПП Роспотребнадзора; 620014, Россия, г. Екатеринбург, ул. Попова, д. 30; ORCID iD 0000-0003-1461-1761.
Балязина Елена Викторовна — д.м.н., профессор кафед-ры неврологии и нейрохирургии с курсом мануальной терапии и рефлексотерапии ФПК и ППС ФГБОУ ВО РостГМУ Минздрава России; 344022, Россия, г. Ростов-на-Дону, пер. Нахичеванский, д. 29; ORCID iD 0000-0002-9967-4405.
Комаров Александр Николаевич — д.м.н., доцент кафедры фундаментальной и клинической неврологии и нейрохирургии РНИМУ им. Н.И. Пирогова Минздрава России; 117437, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0001-5373-4006.
Контактная информация: Данилов Алексей Борисович, e-mail: danilov@intermeda.ru.
Источник финансирования: исследование проведено при поддержке «ASFARMA Медикал Дентал Урюнлер Ве Илач Санайи Тиджарет Аноним Ширкети» в г. Москве.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 23.07.2022.
Поступила после рецензирования 16.08.2022.
Принята в печать 08.09.2022.
About the authors:
Alexey B. Danilov — Dr. Sc. (Med.), Head of the Department of Nervous System Diseases, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8 Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0003-2958-4479.
Dina M. Merkulova — Dr. Sc. (Med.), Professor, neurologist, Chief Neurologist of the Central Directorate of Health Care — Branch of JSC "Russian Railways", Head of the B.M. Gekht Neurological Center, Central Clinical Hospital "Russian Railways-Medicine"; 2, Budayskaya str., Moscow, 129128, Russian Federation; ORCID iD 0000-0003-0368-683X.
Sergey A. Zhivolupov — Dr. Sc. (Med.), Colonel of the Medical Service, Professor of the Department of Nervous Diseases; S.M. Kirov Military Medical Academy; 6Zh, Academician Lebedev str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0003-0363-102X.
Farida I. Devlikamova — Dr. Sc. (Med.), Professor of the Department of Neurology and Manual Therapy, Kazan State Medical Academy — Branch of the Russian Medical Academy of Continuous Professional Education; 11, Mushtari str., Kazan, 420012, Russian Federation.
Boris M. Doronin — Dr. Sc. (Med.), Professor, Head of the Department of Neurology, Novosibirsk State Medical University; 52, Krasnyi prospect, Novosibirsk, 630091, Russian Federation; ORCID iD 0000-0001-7213-759X.
Vasily A. Shirokov — Dr. Sc. (Med.), Professor of the Department of Nervous Diseases with Faculty of Neurosurgery and Manual Therapy, Ural State Medical University; 3, Repin str., Yekaterinburg, 620028, Russian Federation; Leading Researcher of the Medical Research Center for Prevention and Health Protection of Workers of Industrial Enterprises of Rospotrebnadzor; 30, Popov str., Yekaterinburg, 620014, Russian Federation; ORCID iD 0000-0003-1461-1761.
Elena V. Balyazina — Dr. Sc. (Med.), Professor of the Department of Neurology and Neurosurgery with Faculty of Manual Therapy and Reflexology of the ATF and Faculty Staff, Rostov State Medical University; 29, Nakhichevanskiy lane, Rostov-on-Don, 344022, Russian Federation; ORCID iD 0000-0002-9967-4405.
Alexander N. Komarov — Dr. Sc. (Med.), Associate Professor of the Department of Fundamental and Clinical Neurology and Neurosurgery, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117997, Russian Federation; ORCID iD 0000-0001-5373-4006.
Contact information: Alexey B. Danilov, e-mail: danilov@intermeda.ru.
Funding Source: the study was conducted with the support of ASFARMA Medikal Dental Urunler ve Ilac Sanayi Ticaret Anonim Shirketi.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 23.07.2022.
Revised 16.08.2022.
Accepted 08.09.2022.
2. Живолупов С.А., Самарцев И.Н., Яковлев Е.В. Болевые синдромы в клинической практике врача-невролога: патофизиология и принципы фармакотерапии. Клиническая фармакология и терапия. 2017;27(5):10–18. [Zhivolupov S.A., Samartsev I.N., Yakovlev E.V. Pain syndromes in neurological clinical practice: pathophysiology and principles of pharmacotherapy. Сlinical pharmacology and therapy. 2017;27(5):10–18 (in Russ.)].
3. Enthoven W.T., Roelofs P.D., Deyo R.A. et al. Non-steroidal anti-inflammatory drugs for chronic low back pain. Cochrane Database Syst Rev. 2016;2(2):CD012087. DOI: 10.1002/14651858.CD012087.
4. Чугунов А.В., Камчатнов П.Р., Ханмурзаева С.Б., Шемшединова А.М. Возможность применения флурбипрофена у пациентов с дорсалгией. Consilium Medicum. 2020;22(9):71–75. DOI: 10.26442/20751753.2020.9.200366. [Chugunov A.V., Kamchatnov P.R., Khanmurzayeva S.B., Shemshetdinova A.M. The possibility of the use of the flurbiprofen in patients with dorsalgia. Consilium Medicum. 2020;22(9):71–75 (in Russ.)]. DOI: 10.26442/20751753.2020.9.200366.
5. Wang R., Bathon J.M., Ward M.M. Nonsteroidal Antiinflammatory Drugs as Potential Disease-Modifying Medications in Axial Spondyloarthritis. Arthritis Rheumatol. 2020;72(4):518–528. DOI: 10.1002/art.41164.
6. Chou R., Côté P., Randhawa K. et al. The Global Spine Care Initiative: applying evidence-based guidelines on the non-invasive management of back and neck pain to low- and middle-income communities. Eur Spine J. 2018;27(Suppl. 6):851–860. DOI: 10.1007/s00586-017-5433-8.
7. Guven Z., Ofluoglu D., Ozaras N., Kayhan O. [Efficacy of flurbiprofen in the treatment of chronic low back pain: A double blind placebo-controlled study]. Archives of Rheumatology. 2000;15(3):161–166 (in Turkish).
8. Rovenský J., Miceková D. Six-month prospective study to monitor the treatment of rheumatic diseases with sustained-release flurbiprofen. Drugs Exp Clin Res. 2000;26(1):19–24. PMID: 10761533.
9. Bally M., Dendukuri N., Rich B. et al. Risk of acute myocardial infarction with NSAIDs in real world use: bayesian meta-analysis of individual patient data. BMJ. 2017;357:j1909. DOI: 10.1136/bmj.j1909.
10. Janssen M., Caron M., van Rietbergen B. et al. Impairment of the chondrogenic phase of endochondral ossification in vivo by inhibition of cyclooxygenase-2. Eur Cell Mater. 2017;34:202–216. DOI: 10.22203/eCM.v034a13.
11. Pourakbari R., Khodadadi M., Aghebati-Maleki A. et al. The potential of exosomes in the therapy of the cartilage and bone complications; emphasis on osteoarthritis. Life Sci. 2019;236:116861. DOI: 10.1016/j.lfs.2019.116861.
12. Salari P., Abdollahi M. Controversial effects of non-steroidal anti-inflammatory drugs on bone: a review. Inflamm Allergy Drug Targets. 2009;8(3):169–175. DOI: 10.2174/187152809788681065.
13. Cui X., Ding Q., Shan R.-N. et al. Enantioseparation of flurbiprofen enantiomers using chiral ionic liquids by liquid-liquid extraction. Chirality. 2019;31(6):457–467. DOI: 10.1002/chir.23071.
14. Fujii Y., Itakura M. Comparison of lidocaine, metoclopramide, and flurbiprofen axetil for reducing pain on injection of propofol in japanese adult surgical patients: a prospective, randomized, double-blind, parallel-group, placebo-controlled study. Clin Ther. 2008;30(2):280–286. DOI: 10.1016/j.clinthera.2008.02.018.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.

