Разработка состава, методики получения и стандартизация лекарственного растительного препарата «Марены красильной сироп»
Целью исследования явилась разработка состава, подбор методики получения и стандартизация лекарственного растительного препарата «Марены красильной сироп». Объектом исследования служили корневища и корни марены красильной. Электронные спектры измерялись на УФ-спектрофотометре UNICO 2800, с использованием ультразвуковой ванны «Вилитек VBS». В ходе исследования сравнивались 4 метода экстрагирования: мацерация, перколяция, реперколяция и дробная мацерация с использованием ультразвука. Наиболее эффективным способом экстрагирования для сырья марены красильной оказался метод дробной мацерации с ультразвуком. Для изготовления сиропа использовали густой экстракт марены красильной, который получали упариванием водного извлечения, и сахарный сироп, изготовленный по фармакопейной методике. Разработан следующий состав сиропа марены красильной: густой экстракт марены красильной — 3,5 г, 96,6% спирт — 7,0 г, сахарный сироп — 32,25 г. В результате проведенных исследований были разработаны методики количественного анализа суммы антраценпроизводных в пересчете на руберитриновую кислоту в густом экстракте и сиропе марены красильной методом спектрофотометрии. Содержание суммы антраценпроизводных в густом экстракте марены красильной составило 8,7%±0,002%, а в сиропе марены красильной — 0,75±0,002%. Авторами была подобрана методика получения экстракта для изготовления лекарственного препарата «Марены красильной сироп» методом дробной мацерации с ультразвуком. Был обоснован состав изготовления лекарственного препарата «Марены красильной сироп» и разработаны методики количественного анализа суммы антраценпроизводных в густом экстракте и лекарственном препарате «Марены красильной сироп» в пересчете на руберитриновую кислоту с использованием спектрофотометрии.
Ключевые слова: марена красильная, Rubia tinctorum L., корневища и корни, антраценпроизводные, руберитриновая кислота, спектрофотометрия, густой экстракт, сироп.
Для цитирования: Рыбалко М.В., Куркин В.А., Шмыгарева А.А., Саньков А.Н. Разработка состава, методики получения и стандартизация лекарственного растительного препарата «Марены красильной сироп». РМЖ. Медицинское обозрение. 2020;28(9):77-80.
Rubia tinctorum L. syrup — composition development, techniques and standardization of medicinal plant preparation
M.V. Rybalko, V.A. Kurkin, A.A. Shmygareva, A.N. Sankov
Orenburg State Medical University, Orenburg
The aim of the study was to develop composition, techniques and standardization of medicinal plant preparation – Rubia tinctorum L. syrup. The study objects were rhizomes and roots of Rubia tinctorum L. Electronic spectra were measured using Unico 2800 UV spectrophotometer and Vilitek VBS ultrasonic bath. The study compared four extraction methods: maceration, percolation, repercolation, and fractional maceration using ultrasound. The method of fractional maceration with ultrasound proved to be the most effective extraction method for Rubia tinctorum L. raw materials. For syrup preparation, a spissum extract of Rubia tinctorum L. was used. It was obtained by evaporation of water extraction and sugar syrup (made according to the compendial procedure). The following composition of Rubia tinctorum L. syrup has been developed: spissum extract of Rubia tinctorum L. — 3.5 g; 96.6% alcoh ol — 7.0 g; sugar syrup — 32.25 g. The result of the study was the development of methods for the assay of the anthracene derivatives content on the basis of ruberitrinic acid in the Rubia tinctorum L. spissum extract and syrup by spectrophotometry. The content of anthracene derivatives in the spissum extract of Rubia tinctorum L. was 8.7%±0.002 %, in the syrup — 0.75±0.002 %. During the study, the authors selected a method aimed at obtaining an extract for the manufacturing of Rubia tinctorum L. syrup by fractional maceration with ultrasound. The composition of Rubia tinctorum L. syrup was justified and methods for assay of anthracene derivatives content in the Rubia tinctorum L. spissum extract and syrup on the basis of ruberitrinic acid using spectrophotometry were developed.
Keywords: Rubia tinctorum L., Rubia tinctorum L., rhizomes and roots, anthracene derivatives, ruberitrinic acid, spectrophotometry, spissum extract, syrup.
For citation: Rybalko M.V., Kurkin V.A., Shmygareva A.A., Sankov A.N. Rubia tinctorum L. syrup — composition development, techniques and standardization of medicinal plant preparation. RMJ. 2020;9:77–80.
Введение
Одним из наиболее распространенных нарушений минерального обмена является мочекаменная болезнь (МКБ). Она характеризуется образованием в различных участках мочевыводящих путей различных по составу патологических конкрементов, которые состоят из нерастворимых солей (в основном это кальций-оксалатные и кальций-фосфатные камни [1, 2]). Конкременты образуются вследствие разных причин, чаще при нарушениях водно-солевого обмена и нарушениях в питании. Заболевание длительное время проходит бессимптомно, однако при движении конкрементов возникает болевой синдром. Один из способов профилактики и лекарственной терапии данной патологии — использование препаратов для профилактики образования и растворения камней в почках. Фитотерапия наряду с медикаментозным лечением способствует устранению данной проблемы. Фитопрепараты применяются в урологии [3], но на сегодняшний день препаратов для лечения МКБ, зарегистрированных в Государственном реестре Российской Федерации, немного [4].
В настоящей работе обсуждаются актуальные вопросы, связанные с разработкой нового метода получения экстракта из лекарственного растительного сырья марены красильной (Rubia tinctorum L.) и его последующим использованием для изготовления сиропа. Разработка такой лекарственной формы, как сироп, позволяет расширить номенклатуру профилактических препаратов для лечения МКБ у детей дошкольного и школьного возраста. Марена красильная содержит антраценпроизводные ализаринового ряда, а именно руберитриновую кислоту, которая обладает спазмолитическим, мочегонным, антимикробным действием и применяется для лечения МКБ. Руберитриновая кислота способствует подкислению мочи, используется для растворения фосфатных камней. Также она снимает спазм мочеточников и почечных лоханок, что облегчает отхождение мелких камней, кроме того, имеет мочегонный эффект, что тоже способствует выведению камней из почек. Благодаря свойству снижать тонус гладкой мускулатуры с последующим усилением ее перистальтики марена способствует безболезненному изгнанию мелких конкрементов и песка у больных с МКБ. Применение данного препарата приводит к уменьшению болевого синдрома, улучшению общего состояния больных. Таким образом, препараты марены красильной можно рекомендовать как профилактическое и лечебное средство для лечения МКБ [5].
Жидкие лекарственные формы составляют более 60% от общего числа всех лекарственных препаратов в аптечном ассортименте. Нами был разработан способ получения лекарственного растительного препарата «Марены красильной сироп» из густого экстракта. Лекарственная форма «сироп» используется для внутреннего применения и является концентрированным сахарным раствором с основными действующими и вспомогательными веществами. По физическим свойствам сироп — прозрачная, вязкая жидкость со сладким вкусом [6, 7]. Критерии, влияющие на выбор сиропа в качестве лекарственной формы, могут быть различными:
эффективность — высокая скорость всасывания;
безопасность — мягкое, пролонгированное действие, в связи с этим риск осложнений и побочных реакций снижается;
низкая себестоимость — стоимость препаратов на основе лекарственного растительного сырья гораздо ниже стоимости синтетических препаратов;
приятный вкус — за счет присутствия сахара, а также различных подсластителей и вкусовых добавок;
хорошая переносимость организмом [8–10].
Сиропы производят при нагревании до температуры кипения, с помощью растворения сахаров или других сиропообразующих веществ (таких как полиспирты) в воде. Концентрация сахара или других сиропообразующих веществ в готовом сиропе должна быть не менее 45% (м/м). После фильтрации сиропа и охлаждения его до температуры 55±5 °C добавляют различные действующие вещества, экстракты, настойки, консерванты. Спирт этиловый, сорбиновую кислоту, метилпарагидроксибензоат, калия сорбат, пропилпарагидроксибензоат и натрия бензоат вводят в состав сиропов в качестве антимикробных консервантов [11, 12]. В Государственном реестре лекарственных средств, а также в Государственной фармакопее РФ XIV издания отсутствует упоминание о лекарственной форме марены красильной в виде сиропа [6, 7]. Таким образом, перспективной является разработка способа получения экстракта марены красильной с его последующим использованием для изготовления сиропа.
Целью нашего исследования являлась разработка состава, подбор методики получения и стандартизация лекарственного растительного препарата «Марены красильной сироп». Объектом исследования служили корневища и корни марены красильной. Электронные спектры измерялись на УФ-спектрофотометре UNICO 2800, с использованием ультразвуковой ванны «Вилитек VBS».
Собственные результаты
Получение водного экстракта марены для изготовления сиропа возможно несколькими путями: методом мацерации или перколяции (от лат. percolatio — процеживание), т. е. пропусканием экстрагента через сырье; для повышения выхода конечного продукта используется многократная повторная перколяция сырья (реперколяция). Наиболее эффективным способом получения экстракта оказался метод дробной мацерации с ультразвуком, который заключается в экстракции корневищ и корней марены красильной в соотношении сырья и экстрагента (вода) 1:10. Экстрагент делили на 4 части и последовательно настаивали сырье в каждой части, общее время настаивания составило 2 сут. Последовательная смена экстрагента позволила максимально истощить сырье. Далее проводили экстракцию в течение 30 мин на водяной бане, 15 мин с использованием ультразвука и фильтровали извлечение. Данный метод показал наибольший выход антраценпроизводных по сравнению с другими способами получения экстракта, что было подтверждено при изучении УФ-спектров водного извлечения сырья марены красильной в щелочно-аммиачной среде (рис. 1).
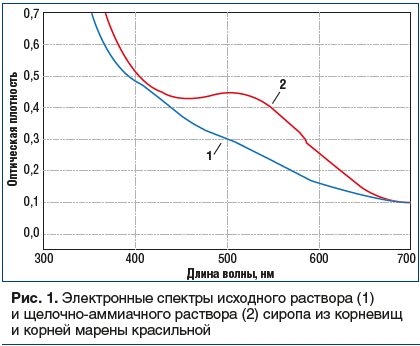
Содержание суммы антраценпроизводных в густом экстракте марены красильной, полученном методом дробной мацерации с ультразвуком, в пересчете на руберитриновую кислоту составило 8,7%. Результаты количественного содержания антраценпроизводных в густом экстракте представлены в таблице 1.
Полученное водное извлечение из корневищ и корней марены красильной упаривалось до густого экстракта с содержанием влаги не более 25%. Далее готовили простой сахарный сироп, для этого отвешивали 64 г сахара-рафинада, отмеривали цилиндром воду 18 мл, заливали в сахар и оставляли на 15–20 мин. После распада сахара добавляли еще 18 мл воды, осторожно нагревали на водяной бане до кипения и кипятили 3–5 мин. Горячий сироп процеживали через тройной слой марли в сухой флакон. Густой экстракт марены красильной (3,5 г) растворяли в 90% этаноле (7,0 г), фильтровали, добавляли сахарный сироп, нагревали и доводили до кипения.
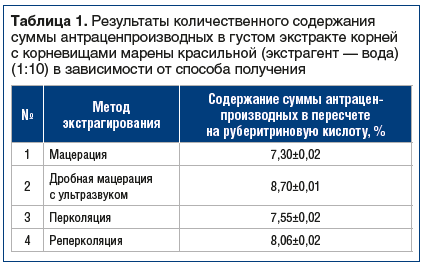
Исследование показало, что электронные спектры сиропа марены совпадают со спектрами извлечения из корневищ и корней марены, а максимум поглощения отмечается при 510±2 нм, что характерно и для щелочно-аммиачного раствора водно-спиртового извлечения из сырья марены (рис. 2).
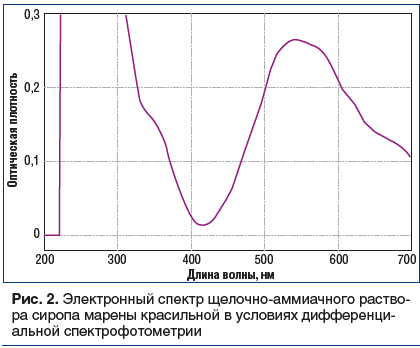
В длинноволновой области электронного спектра щелочно-аммиачного раствора руберитриновой кислоты наблюдался максимум поглощения при 510±2 нм
(рис. 3).
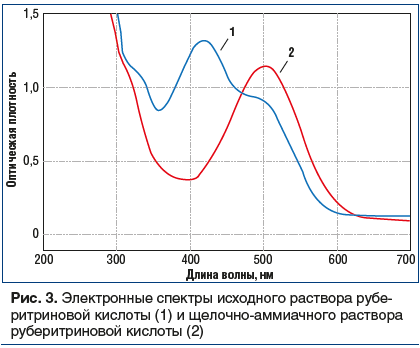
Следовательно, в качестве аналитической длины волны может быть использовано значение 510 нм, а стандартным образцом может служить доминирующий антрагликозид — руберитриновая кислота, причем в случае отсутствия стандарта в расчетной формуле может быть использовано теоретическое значение удельного показателя поглощения (E1%/1см = 520).
Методика количественного анализа антраценпроизводных в густом экстракте марены красильной была следующей: точную навеску густого экстракта (0,2000 г) вводили в мерную колбу объемом 100 мл, добавляли 50 мл 80% этилового спирта. 1,0 мл изготовленного раствора вводили в мерную колбу объемом 50 мл и доводили до метки щелочно-аммиачным раствором, изготовленным в соответствии с Государственной фармакопеей РФ XIV издания, далее в течение 15 мин нагревали на водяной бане. После охлаждения определяли оптическую плотность анализируемого раствора на спектрофотометре при 510 нм. Раствором сравнения служила вода очищенная [13]. Методика количественного анализа антраценпроизводных в лекарственном препарате «Марены красильной сироп»: 2 г сиропа вводили в мерную колбу объемом 25 мл и доводили до метки водой очищенной, 2 мл изготовленного раствора вводили в мерную колбу объемом 25 мл и добавляли до метки щелочно-аммиачный раствор, изготовленный в соответствии с Государственной фармакопеей РФ XIV издания, далее в течение 15 мин нагревали на водяной бане. После охлаждения определяли оптическую плотность анализируемого раствора на спектрофотометре при 510 нм. Раствором сравнения служила вода очищенная [13].
Содержание суммы антраценпроизводных в густом экстракте марены красильной (Х) в пересчете на руберитриновую кислоту в процентах вычисляли по формуле:
Х = E × 50 ×50 / m×520 ×1
где Е — оптическая плотность анализируемого раствора; m — масса навески сиропа, г; 520 — удельный показатель поглощения (E 1%/1см) щелочно-аммиачного раствора стандартного образца руберитриновой кислоты А при 510 нм.
Содержание суммы антраценпроизводных в лекарственном препарате «Марены красильной сироп» (Х) в пересчете на руберитриновую кислоту в процентах вычисляют по формуле:
Х = E × 25 ×25 / m×520 ×2
Содержание суммы антраценпроизводных в густом экстракте марены красильной, полученном методом дробной мацерации с ультразвуком, в пересчете на руберитриновую кислоту составило 8,70±0,02%.
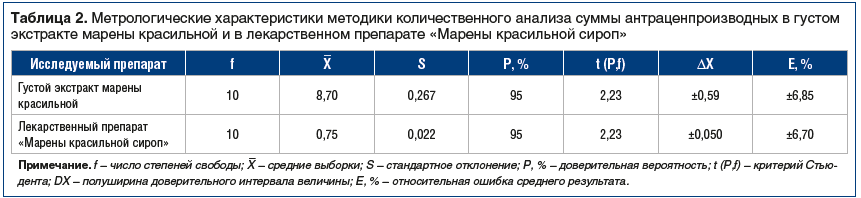
Метрологические характеристики методики количественного анализа суммы антраценпроизводных в экстракте марены красильной, полученном методом дробной мацерации с ультразвуком, представлены в таблице 2.
Содержание суммы антраценпроизводных в лекарственном препарате «Марены красильной сироп», полученном методом дробной мацерации с ультразвуком, в пересчете на руберитриновую кислоту составило 0,75±0,002%.
Результаты статистической обработки проведенных опытов показывают, что ошибка единичного определения суммы антраценпроизводных в лекарственном препарате «Марены красильной сироп» с доверительной вероятностью 95% составляет ±6,70%.
Метрологические характеристики методики количественного анализа суммы антраценпроизводных в лекарственном препарате «Марены красильной сироп» представлены в таблице 2.
Заключение
Авторами была подобрана методика получения экстракта для изготовления лекарственного препарата «Марены красильной сироп» методом дробной мацерации с ультразвуком. Был обоснован состав лекарственного препарата «Марены красильной сироп» и разработаны методики количественного анализа суммы антраценпроизводных в густом экстракте и лекарственном препарате «Марены красильной сироп» в пересчете на руберитриновую кислоту с использованием спектрофотометрии. Появление лекарственного препарата «Марены красильной сироп» повысит доступность лечения для пациентов с МКБ.
2. Акопян В.Б., Ершов Ю.А. Основы взаимодействия ультразвука с биологическими объектами. М.: МГТУ им. Н.Э. Баумана; 2005. [Akopyan V.B., Yershov Yu.A. The basics of the interaction of ultrasound with biological objects. M.: MSTU im. N.E. Bauman; 2005 (in Russ.)].
3. Кульчавеня Е.В. Возможности фитотерапии заболеваний предстательной железы. РМЖ. Медицинское обозрение. 2018;2(I):30–35. [Kulchavenya E.V. Possibilities of herbal medicine for prostate diseases. RMJ. Medical Review. 2018;2(I):30–35 (in Russ.)].
4. Государственный реестр лекарственных средств (Электронный ресурс). URL: https://grls.rosminzdrav.ru/Default.aspx (дата обращения: 09.02.2020). [State Register of Medicines (Electronic resource). URL: https://grls.rosminzdrav.ru/Default.aspx (access date: 09.02.2020) (in Russ.)].
5. Куркин В.А. Фармакогнозия. Учебник для студентов фармацевтических вузов (факультетов). 3-е изд., перераб. и доп. Самара: ООО «Офорт». ФБГОУ ВО СамГМУ Минздрава России; 2016. [Kurkin V.A. Pharmacognosy. Textbook for students of pharmaceutical universities (faculties). 3rd ed., Revised. and add. Samara: Ofort LLC, Federal State Budget Educational Institution of Higher Education, Samara State Medical University; 2016 (in Russ.)].
6. Государственная фармакопея Российской Федерации. XIV издание, том II. М.: Медицина; 2018. [State Pharmacopoeia of the Russian Federation. XIV Edition, Volume II. M.: Medicine; 2018 (in Russ.)].
7. Государственная фармакопея Российской Федерации: Том IV. М.: Медицина; 2018. [State Pharmacopoeia of the Russian Federation: Volume IV. M.: Medicine; 2018 (in Russ.)].
8. Куркин В.А. Основы фитотерапии. Учебное пособие для студентов фармацевтических вузов. Самара: ООО «Офорт». ГОУ ВПО «СамГМУ Росздрава»; 2009. [Kurkin V.A. The basics of herbal medicine. Textbook for students of pharmaceutical universities. Samara: Ofort LLC GOU VPO SamGMU of Roszdrav; 2009 (in Russ.)].
9. Муравьева Д.А., Самылина И.А., Яковлев Г.П. Фармакогнозия. М.: Медицина; 2002. [Muravyova D.A., Samylina I.A., Yakovlev G.P. Pharmacognosy. M.: Medicine; 2002 (in Russ.)].
10. Пономарев В.Д. Экстрагирование лекарственного сырья. М.: Медицина, 1976. [Ponomarev V.D. Extraction of medicinal raw materials. M.: Medicine; 1976 (in Russ.)].
11. Чуешов В.И., Чернов М.Ю., Хохлова Л.М. Промышленная технология лекарств: Учебник для студентов высших учебных заведений. Харьков: НФАУ МТК «Книга»; 1999. [Chueshov V.I., Chernov M.Yu., Khokhlova L.M. Industrial Technology of Drugs: A Textbook for University Students. Kharkov: NFAA MTK Book; 1999 (in Russ.)].
12. Брук М.М. Получение лекарственных препаратов из животного и растительного сырья под действием ультразвука. Ультразвук в физиологии и медицине: сборник статей. Ростов-на-Дону; 1972. [Brooke M.M. Obtaining drugs from animal and vegetable raw materials under the influence of ultrasound. Ultrasound in physiology and medicine: a collection of articles. Rostov-on-Don; 1972 (in Russ.)].
13. Правдивцева О.Е., Куркин В.А., Авдеева Е.В. и др. Актуальные вопросы стандартизации антраценсодержащих видов лекарственного растительного сырья, включенных в Государственную фармакопею Российской Федерации. Международный журнал прикладных и фундаментальных исследований. 2016;12(2):272–276. [Pravdivtseva O.E., Kurkin V.A., Avdeeva E.V. and others. Actual issues of standardization of anthracene-containing types of medicinal plant materials included in the State Pharmacopoeia of the Russian Federation. International Journal of Applied and Basic Research. 2016;12(2):272–276 (in Russ.)].

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
