Оптимизация местного лечения больных флегмонами лица и шеи с использованием современных антисептических средств
Рубрика:
Хирургия
Одной из наиболее сложных и актуальных проблем современной гнойной хирургии является лечение больных флегмонами лица и шеи.
Цель исследования: оценка эффективности крема Аргосульфан® в комплексном местном лечении больных флегмонами лица и шеи.
Материал и методы: сравнительное исследование эффективности местного лечения послеоперационных ран у 38 пациентов с диагнозом флегмоны лица и шеи при помощи комбинированного препарата на основе сульфатиазола серебра (Аргосульфан®) и мазевых повязок с мазью Левомеколь. Перевязки в обеих группах исследования выполнялись дважды в сутки, производилась санация раны водным 0,02% раствором хлоргексидина биглюконата и накладывалась повязка с исследуемым лекарственным препаратом. Оценивалось время очищения раны, время появления грануляционной ткани, время готовности раны к ушиванию, а также цитологический состав раневой поверхности методом мазков-отпечатков. Для идентификации возбудителя использовался метод посева раневого экссудата.
Результаты исследования: использование препарата на основе сульфатиазола серебра позволяет в среднем на 2 сут сократить время очищения раны, а также на 2 сут раньше, по сравнению с использованием мазевых повязок с Левомеколем, выполнить наложение вторичных швов. Применение данного комбинированного средства также позволяет добиться лучших косметических результатов за счет поддержания в ране влажной среды. Наиболее частыми возбудителями флегмон лица и шеи выступили бактерии группы стафилококков (Staphylococcus aureus и Staphylococcus epidermidis) и стрептококков (Streptococcus anginosus и Streptococcus pyogenes).
Выводы: сульфатиазол серебра (крем Аргосульфан®) оказывает антибактериальное воздействие на возбудителей гнойно-воспалительного процесса и сохраняет необходимую для оптимального заживления раны влажность.
Ключевые слова: флегмона шеи, рана, раневые повязки, серебро, сульфатиазол серебра.
Цель исследования: оценка эффективности крема Аргосульфан® в комплексном местном лечении больных флегмонами лица и шеи.
Материал и методы: сравнительное исследование эффективности местного лечения послеоперационных ран у 38 пациентов с диагнозом флегмоны лица и шеи при помощи комбинированного препарата на основе сульфатиазола серебра (Аргосульфан®) и мазевых повязок с мазью Левомеколь. Перевязки в обеих группах исследования выполнялись дважды в сутки, производилась санация раны водным 0,02% раствором хлоргексидина биглюконата и накладывалась повязка с исследуемым лекарственным препаратом. Оценивалось время очищения раны, время появления грануляционной ткани, время готовности раны к ушиванию, а также цитологический состав раневой поверхности методом мазков-отпечатков. Для идентификации возбудителя использовался метод посева раневого экссудата.
Результаты исследования: использование препарата на основе сульфатиазола серебра позволяет в среднем на 2 сут сократить время очищения раны, а также на 2 сут раньше, по сравнению с использованием мазевых повязок с Левомеколем, выполнить наложение вторичных швов. Применение данного комбинированного средства также позволяет добиться лучших косметических результатов за счет поддержания в ране влажной среды. Наиболее частыми возбудителями флегмон лица и шеи выступили бактерии группы стафилококков (Staphylococcus aureus и Staphylococcus epidermidis) и стрептококков (Streptococcus anginosus и Streptococcus pyogenes).
Выводы: сульфатиазол серебра (крем Аргосульфан®) оказывает антибактериальное воздействие на возбудителей гнойно-воспалительного процесса и сохраняет необходимую для оптимального заживления раны влажность.
Ключевые слова: флегмона шеи, рана, раневые повязки, серебро, сульфатиазол серебра.
Savchenko Yu.P., Paramonova OA , Malyshko V.V., Kalinina M.I. , Denisova N.Yu.
Kuban State Medical University, Krasnodar
One of the most difficult and urgent problems of modern purulent surgery is the treatment of patients with face and neck phlegmons.
Aim: to evaluate the effectiveness of the use of Argosulfan® cream in complex topical treatment of patients with face and / or neck phlegmons.
Patients and Methods: a comparative study of the efficacy of topical treatment of postoperative wounds in 38 patients with phlegmons of the neck and / or face using a silver sulphadiazine dressings (Argosulfan®) and salve dressing with Levomekol ointment was conducted. In both groups the dressings were applied twice a day, the wound was first sanitized with an aqueous 0.02% solution of chlorhexidine bigluconate and then a dressing with the investigative drug was applied. The time of wound cleansing, the time of appearance of the granulation tissue, and the time of the wound readiness for suturing was assessed. The cytological composition of the wound surface was also assessed by the smear-print method. To identify the pathogen, the method of seeding the wound exudate was used.
Results: the use of the silver sulphadiazine drug allowed to shorten the time of wound cleansing on average by 2 days, and to apply secondary seams 2 days earlier in comparison with the use of Levemekol dressings. The use of this combined preparation also allowed to achieve the best cosmetic results by maintaining a moist wound environment. The most frequent pathogens of face and / or neck phlegmons were Staphylococci (Staphylococcus aureus and Staphylococcus epidermidis) and Streptococci (Streptococcus anginosus and Streptococcus pyogenes).
Conclusion: the use of silver sulphadiazine (Argosulfan® cream) allowed to provide antibacterial effect on pathogens of purulent-inflammatory process and to maintain a moist wound environment necessary for optimal wound healing.
Key words: phlegmon of the neck, wound, wound dressings, silver, silver sulphadiazine.
For citation: Savchenko Yu.P., Paramonova OA , Malyshko V.V. et al. Optimization of topical treatment of patients with phlegmons of face and neck with the use of modern antiseptic drugs // RMJ. Medical Review. 2018. № 2(II). P. 47–51.
В статье представлены результаты сравнительного исследования эффективности местного лечения послеоперационных ран у пациентов с диагнозом флегмоны лица и шеи при помощи комбинированного препарата на основе сульфатиазола серебра
Одной из наиболее сложных и актуальных проблем современной гнойной хирургии является лечение больных флегмонами лица и шеи. Данная патология характеризуется широкой распространенностью, трудностями в диагностике на ранней стадии заболевания и тяжелым течением, зачастую приводящим к летальному исходу.Флегмоны лица и шеи возникают вследствие эндогенного инфицирования, что обусловливает широкий спектр микробных возбудителей данного гнойно-воспалительного процесса и, часто, низкую реактивность организма больного. Флегмоны лица и шеи подразделяются в зависимости от источника инфицирования:
при воспалительных процессах зуба формируются одонтогенные флегмоны [1–3];
при распространении инфекции из очагов хронического воспаления верхних дыхательных путей образуются тонзиллогенные флегмоны;
нередко причиной развития флегмон шеи становится перфорация пищевода или нагноение срединной кисты шеи [2, 4].
Наиболее частыми возбудителями флегмон лица и шеи становятся различные штаммы стрептококков и стафилококков [5, 6], персистирующие на слизистых оболочках, кариозных зубах, хронических очагах воспаления ротовой полости. Значительную роль в возникновении и развитии заболевания играет и более агрессивная микрофлора, зачастую попадающая в рану вторично, вследствие реинфицирования. В таком случае возбудителями нередко становятся внутрибольничные штаммы микроорганизмов, обладающие всеми характерными для этой группы признаками: значительной антибиотикорезистентностью [7–9], высокой вирулентностью, способностью к формированию на поверхности раны бактериальных биопленок и устойчивостью в отношении большинства используемых для местного лечения ран антисептических средств [10, 11].
У больных с диагнозом флегмоны лица или шеи зачастую наблюдается снижение иммунного статуса [12–14], что приводит к затяжному течению заболевания. При наличии тяжелой сопутствующей патологии, особенно у лиц пожилого и старческого возраста, иммунодефицит приводит к частому возникновению осложнений. Наиболее часто встречающиеся осложнения флегмон лица и шеи — это тромбоз пещеристого синуса, передний (как правило) медиастинит, полиорганная недостаточность и тяжелые септические состояния [15]. Как следствие, при тяжелом и затяжном течении обсуждаемой патологии достаточно высокая летальность, составляющая, в зависимости от используемых методов хирургического лечения, применяемых антибактериальных препаратов и местных антисептических средств, от 10 до 25% [9].
Тяжелое течение заболевания, высокая летальность и распространенная полирезистентность возбудителей к антибактериальным препаратам, существенно снижающая эффективность антибиотикотерапии, приводят к необходимости поиска новых средств и комплексных лекарственных композиций, предназначенных в первую очередь именно для местного лечения этой патологии [16–18].
Наиболее перспективное научно-практическое направление — это разработка средств с выраженным антибактериальным действием, препятствующих инфицированию раны внутрибольничными штаммами и вызывающих как можно более медленное формирование устойчивости у возбудителей гнойного процесса, а также поддерживающих в ране необходимую для нормального заживления влажность.
В последние годы было разработано и предложено для внедрения в клиническую практику достаточно большое количество антисептиков и лекарственных композиций, так или иначе удовлетворяющих этим требованиям. К примеру, хорошо себя зарекомендовали раневые повязки, которые содержат антибактериальные компоненты, обеспечивают отток раневого экссудата и поддерживают на поверхности послеоперационной раны влажную среду. Но их использование ограничивается активным нагноением в ране.
Одним из перспективных направлений является применение в комплексном местном лечении больных флегмонами лица и шеи средства Аргосульфан®, удовлетворяющего всем необходимым требованиям и представляющего собой комбинированный препарат на основе серебра (сульфатиазол серебра) и сульфаниламидных препаратов. Спектр применения сульфатиазола серебра достаточно широк: пиодермии, пролежни, трофические язвы различного генеза (при хронической венозной недостаточности, посттромбофлебитическом синдроме, облитерирующем эндартериите, нарушениях кровообращения на фоне сахарного диабета), гнойные и хронические длительно незаживающие раны, а также мелкие бытовые травмы (порезы, ссадины).
В последние годы данный препарат начинает активно использоваться в лечении ряда хирургических заболеваний [19–22]. Таким образом, имеется перспектива применения препарата при флегмонах лица и шеи для местного лечения ран в послеоперационном периоде.
Широко известны антибактериальные свойства различных соединений серебра (ионов, солей, наночастиц) в отношении многих возбудителей гнойно-воспалительных заболеваний, в т. ч. антибиотикорезистентной внутрибольничной микрофлоры. Соединения серебра способны повреждать клеточную стенку микроорганизмов, инактивировать ферменты дыхательной цепи, связываться с нуклеиновыми кислотами возбудителя гнойного процесса [23, 24]. При этом примечательны способность серебра оказывать выраженное угнетающее действие на бактериальные и грибковые клетки (отмечено влияние соединений серебра и на вирусные частицы [25]) и значительно меньшая его токсичность в отношении клеток человека [26, 27]. Важным аспектом также является способность серебра проникать в бактериальные биопленки, как правило, устойчивые к антибактериальным препаратам и антисептическим средствам [28–30].
Совместное использование соединений серебра и сульфаниламидных препаратов позволяет усилить бактерицидные свойства полученной композиции и компенсировать сравнительно слабую устойчивость соединений серебра к физико-химическим факторам окружающей среды, таким как присутствующие в ране хлориды и световое излучение. Помимо этого, согласно некоторым литературным источникам [31, 32], сульфатиазол серебра способен усиливать процессы регенерации в ране, ускорять пролиферацию фибробластов и кератиноцитов, способствуя росту грануляций и эпителизации раневого дефекта.
Цель исследования: оценка эффективности крема Аргосульфан® в комплексном местном лечении больных флегмонами лица и шеи.
Материал и методы
Нами проведено лечение 38 пациентов с диагнозом флегмоны лица и шеи в возрасте от 21 года до 66 лет с легким и среднетяжелым течением заболевания. Критерии включения в исследование: распространенность гнойно-воспалительного процесса на 3 и более клетчаточных пространств лица и шеи и отсутствие осложнений на момент начала лечения (медиастинита, сепсиса, полиорганной недостаточности), добровольное информированное согласие на участие в исследовании. Все пациенты получали системное лечение согласно протоколу.
Участники исследования были случайным образом разделены на 2 равные группы, схожие по полу, возрасту и наличию сопутствующей патологии.
В группу сравнения (группа 1) было включено 19 человек, которым выполнялось стандартное местное лечение гнойно-воспалительного процесса клетчаточных пространств, включавшее активную хирургическую обработку флегмоны, дренирование послеоперационной раны с использованием полихлорвиниловых однопросветных дренажей, а также антибактериальную терапию согласно результатам посева раневого экссудата. Помимо этого, проводилась десенсибилизирующая, инфузионная, дезинтоксикационная терапия соответственно степени тяжести заболевания и сопутствующей патологии. Местное лечение включало туалет послеоперационной гнойной раны водным 0,02% раствором хлоргексидина биглюконата и наложение мазевых повязок (мазь Левомеколь) с раствором йодопирона дважды в сутки.
В основную группу (группа 2) вошли 19 человек, которым, помимо описанной выше схемы лечения, назначался местно препарат Аргосульфан®. Перед наложением повязки рана дополнительно обрабатывалась данным препаратом, после чего выполнялось стандартное лечение.
Повязки в обеих группах менялись 2 раза в сутки до появления признаков роста грануляционной ткани, после чего рана ушивалась вторичными швами.
Для оценки эффективности используемого средства выполнялся комплекс клинических, цитологических, микробиологических и лабораторных методов исследования.
Идентификация возбудителя гнойно-воспалительного процесса и его чувствительности к антибиотикам проводилась путем аспирации раневого экссудата с помощью стерильного ватного тампона. Полученный материал помещался в питательную среду, идентифицировался клинический изолят и оценивалась резистентность к антибактериальным препаратам методом дисков. Исследование материала на наличие анаэробной микрофлоры не выполнялось. Забор материала на исследование выполняли на 1, 4 и 7-е сутки от момента госпитализации и проведения оперативного вмешательства.
Площадь раневого дефекта определяли по Ю.П. Савченко [33], методом компьютерной обработки снимка раневого дефекта совместно с эталоном известной площади.
Клиническая оценка течения заболевания в послеоперационном периоде включала определение сроков окончательного очищения раны, сроков ушивания раны, периода купирования болевого синдрома, сроков появления признаков роста грануляционной ткани и эпителизации ушитой раны, температуры тела. Выполнялся общий анализ крови, определялся лейкоцитарный индекс интоксикации.
Для оценки динамики заживления послеоперационных ран использовался метод мазков-отпечатков с раневой поверхности, позволяющий получить информацию о приоритетном клеточном составе раневой поверхности и степени готовности раны к ушиванию, а также выявить ранние признаки возможного повторного нагноения раны.
Для определения достоверности полученных результатов, в связи с малой выборкой, использовались непараметрические методы статистического анализа. Различия между группами считались достоверными при p<0,05.
Результаты и обсуждение
При микробиологическом исследовании раневого отделяемого наиболее часто высевались бактерии группы стафилококков (Staphylococcus aureus и Staphylococcus epidermidis) и стрептококков (Streptococcus anginosus и Streptococcus pyogenes). Количество микроорганизмов в ране прогрессивно снижалось с 105–106 КОЕ/мл раневого отделяемого в 1-е сутки до 102–103 КОЕ/мл на 7-е сутки исследования. При этом в основной группе уже к 4-м суткам лечения было отмечено снижение уровня бактериальной загрязненности, а к 7-м суткам практически полная элиминация возбудителя. В группе сравнения отмечалось лишь незначительное снижение уровня микробных тел на 4-е сутки и к 7-м суткам по-прежнему в небольшом количестве обнаруживались бактериальные тела.У больных опытной группы наблюдалась нормализация температуры тела на 3–4-е сутки (3,57±0,43), в то время как у больных группы сравнения снижение температуры отмечено на 5–6-е (5,64±0,28) сутки после проведения оперативного лечения (p<0,05).
Общий анализ крови и лейкоцитарный индекс интоксикации не выявили достоверных различий между клиническими группами, тогда как отличия в клиническом течении раневого процесса были достоверны. Купирование болевого синдрома у пациентов опытной группы наступало раньше и занимало 2,34±0,12 сут против более чем 4-х суток у пациентов группы сравнения (p<0,05).
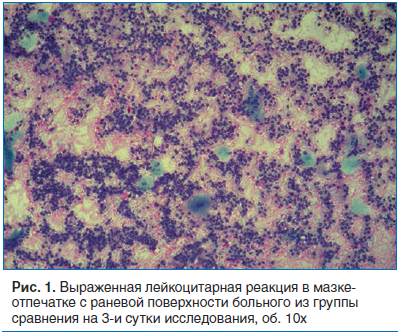
При использовании крема Аргосульфан® также наблюдалось более раннее очищение раны, появление грануляционной ткани (на 4–6-е сутки), изменение характера раневого отделяемого и соответственно наложение вторичных швов (на 10-е сутки). Необходимости в проведении повторной хирургической обработки раны в послеоперационном периоде не возникло. Случаев развития повторного нагноения раны и/или расхождения швов после ушивания не было ни в одной из групп исследования. Оценка клеточного состава мазков-отпечатков также подтверждает ускорение процессов заживления ран при использовании серебросодержащего средства Аргосульфан®. На 3-и сутки при использовании мазевых повязок наблюдалось большое количество нейтрофилов (рис. 1).
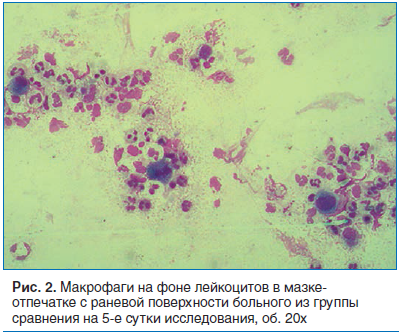
На 5-е сутки применения мази Левомеколь было отмечено появление макрофагов в мазках-отпечатках, но в то же время сохранялось большое количество нейтрофильных лейкоцитов, фибробласты были представлены единичными клетками или отсутствовали (рис. 2).
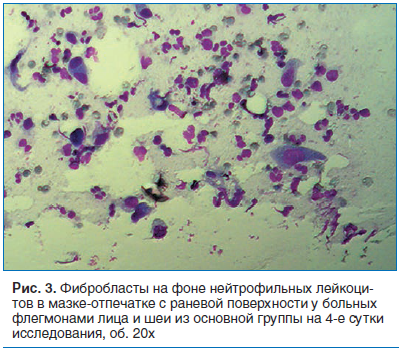
При использовании же комбинированного препарата серебра и сульфаниламидных соединений уже на 4-е сутки в мазках-отпечатках были обнаружены фибробласты (рис. 3).
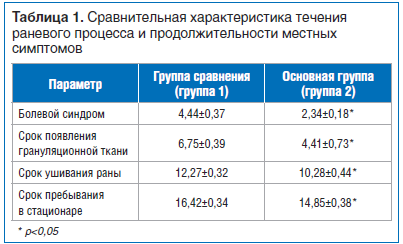
При использовании мазевых повязок в среднем на 2 сут дольше продолжался болевой синдром, на 2 сут позже, по сравнению с применением препарата сульфатиазола серебра, наблюдалось появление грануляционной ткани. Ушивание раны выполнялось при использовании средства Аргосульфан® в среднем на 10-е сутки, при использовании мазевых повязок — на 12-е сутки. Срок пребывания в стационаре при применении препарата Аргосульфан® также сократился в среднем на 1,5 сут (табл. 1).
При использовании комбинированного препарата Аргосульфан® не отмечалось присыхания повязки к раневой поверхности, что в целом было характерно для лечения с помощью мазевых повязок и свидетельствовало о пересыхании раневой поверхности. В целом высыхание повязок приводило к увеличению времени, затрачиваемого на выполнение перевязок, и замедлению процессов регенерации в ране. Нельзя не отметить, что при использовании препарата Аргосульфан® наблюдались лучшие косметические свойства послеоперационных рубцов.
Выводы
В результате проведенного клинического исследования была доказана сравнительно высокая эффективность местного применения крема Аргосульфан® в комплексном лечении флегмон лица и шеи. Использование сульфатиазола серебра позволило обеспечить антибактериальное воздействие на возбудителей гнойно-воспалительного процесса и сохранить необходимую для оптимального заживления раны влажность. Использование данного средства позволило уменьшить сроки очищения и ушивания раны в послеоперационном периоде. Также применение данного препарата позволило добиться наилучшего косметического эффекта за счет менее выраженного рубца при заживлении ушитой раны.
Литература
1. Ильяно В.М. Состояние системы простагландинов у больных с хроническим периодонтитом // Загальна патологія та патологічна фізіологія. 2012. Т.7. №4. С.191–196 [Il’jano V.M. Sostojanie sistemy prostaglandinov u bol’nyh s hronicheskim periodontitom // Zagal’na patologіja ta patologіchna fіzіologіja. 2012. T.7. №4. S.191–196 (in Russian)].
2. Marchiano E., Raikundalia M.D., Carniol E.T. et al. Characteristics of patients treated for orbital cellulitis: An analysis of inpatient data // Laryngoscope. 2016. Vol. 126(3). Р.9.
3. Юлдашев И.М., Ургуналиев Б.К., Ашиналиев А.А. и др. Тотальный одонтогенный медиастинит как осложнение гнилостно некротической флегмоны дна полости рта // Тихоокеанский медицинский журнал. 2011. №3. С.97–98 [Juldashev I.M., Urgunaliev B.K., Ashinaliev A.A. i dr. Total’nyj odontogennyj mediastinit kak oslozhnenie gnilostnonekroticheskoj flegmony dna polosti rta // Tihookeanskij medicinskij zhurnal. 2011. №3. S.97–98 (in Russian)].
4. Brea Álvarez B., Esteban García L., Tuñón Gómez M., Cepeda Ibarra Y. Nontraumatic head and neck injuries: a clinical approach. Part 2 // Radiologia. 2017. Vol. 59(3). P.182–195.
5. Гусейнова М.Г., Бисаев У.И. Фармакотерапия флегмоны и одонтогенного остеомиелита челюстных костей // Бюллетень медицинских интернет-конференций. 2017. Т.7. №6. С.1279 [Gusejnova M.G., Bisaev U.I. Farmakoterapija flegmony i odontogennogo osteomielita cheljustnyh kostej // Bjulleten’ medicinskih internet-konferencij. 2017. T.7. №6. S.1279 (in Russian)].
6. Hirasawa K., Tsukahara K., Motohashi R. et al. Deep neck cellulitis: limitations of conservative treatment with antibiotics // Acta Otolaryngol. 2017. Vol. 137(1). P.86–89.
7. Монаков В.А., Иващенко А.В., Решетникова В.П Особенности микробиологической картины ран у больных с одонтогенными флегмонами челюстно-лицевой области при использовании вакуум-терапии // Клиническая стоматология. 2014. №1(69). С.40–43 [Monakov V.A., Ivashhenko A.V., Reshetnikova V.P Osobennosti mikrobiologicheskoj kartiny ran u bol’nyh s odontogennymi flegmonami cheljustno-licevoj oblasti pri ispol’zovanii vakuum-terapii // Klinicheskaja stomatologija. 2014. №1(69). S.40–43 (in Russian)].
8. Куликовский В.Ф., Оганесян В.Ф. Летальность при неклостридиальной анаэробной инфекции мягких тканей челюстно-лицевой области и шеи // Вестник экспериментальной и клинической хирургии. 2010. Т.3. №4. С.373–376 [Kulikovskij V.F., Oganesjan V.F. Letal’nost’ pri neklostridial’noj anajerobnoj infekcii mjagkih tkanej cheljustno-licevoj oblasti i shei // Vestnik jeksperimental’noj i klinicheskoj hirurgii. 2010. T.3. №4. S.373–376 (in Russian)].
9. Lin Y.Q., An L.F., Li L. New treatment choice of head and neck cellulitis: multi-catheter drainage guided by ultrasound percutaneous puncture // Zhonghua Er Bi Yan Hou Tou Jing Wai Ke Za Zhi. 2017. Vol. 52(2). P.110–112.
10. Субханова Г.С. Сравнительный анализ эффективности перевязочных средств в лечении гнойных ран лица и шеи // Вестник Авиценны. 2013. №2(55). С.117–123 [Subhanova G.S. Sravnitel’nyj analiz jeffektivnosti perevjazochnyh sredstv v lechenii gnojnyh ran lica i shei // Vestnik Avicenny. 2013. №2(55). S.117–123 (in Russian)].
11. Кетова Г.Г., Латюшина Л.С., Долгушин И.И. Фармакоэкономический анализ местного применения иммунопрепаратов в комплексном лечении больных с одонтогенными флегмонами // Проблемы стандартизации в здравоохранении. 2009. №3–4. С.30–35 [Ketova G.G., Latjushina L.S., Dolgushin I.I. Farmakojekonomicheskij analiz mestnogo primenenija immunopreparatov v kompleksnom lechenii bol’nyh s odontogennymi flegmonami // Problemy standartizacii v zdravoohranenii. 2009. №3–4. S.30–35 (in Russian)].
12. Баранник Н.Г., Варжапетян С.Д., Сидоряко А.В. и др. Изменение иммунного статуса при флегмонах челюстно-лицевой области в зависимости от распространенности гнойного процесса // Запорожский медицинский журнал. 2016. №1(94). С.44–49 [Barannik N.G., Varzhapetjan S.D., Sidorjako A.V. i dr. Izmenenie immunnogo statusa pri flegmonah cheljustno-licevoj oblasti v zavisimosti ot rasprostranjonnosti gnojnogo processa // Zaporozhskij medicinskij zhurnal. 2016. №1(94). S.44–49 (in Russian)].
13. Taub D., Yampolsky A., Diecidue R., Gold L. Controversies in the Management of Oral and Maxillofacial Infections // Oral Maxillofac Surg Clin North Am. 2017. Vol. 29(4) P.465–473.
14. Кабанова С.А. Изучение иммунного статуса при гнойно-воспалительных заболеваниях челюстно-лицевой области // Новости хирургии. 2005. Т.13. №1–4. С.28–32 [Kabanova S.A. Izuchenie immunnogo statusa pri gnojno-vospalitel’nyh zabolevanijah cheljustno-licevoj oblasti // Novosti hirurgii. 2005. T.13. №1–4. S.28–32 (in Russian)].
15. Hirasawa K., Tsukahara K., Motohashi R. et al. Deep neck cellulitis: limitations of conservative treatment with antibiotics // Acta Otolaryngol. 2017. Vol. 137(1). P.86–89.
16. Монаков В.А. Гидродинамическое обоснование аспирационно-промывного дренирования гнойных ран // Южно-Уральский медицинский журнал. 2015. №2. С.16–21 [Monakov V.A. Gidrodinamicheskoe obosnovanie aspiracionno-promyvnogo drenirovanija gnojnyh ran // Juzhno-Ural’skij medicinskij zhurnal. 2015. №2. S.16–21 (in Russian)].
17. Лишов Е.В., Харитонов А.А., Путинцев А.М. Особенности хирургического лечения анаэробных инфекций глубоких пространств шеи, осложненных медиастинитом // Acta Biomedica Scientifica. 2017. Т.2. №6. С.130–133 [Lishov E.V., Haritonov A.A., Putincev A.M. Osobennosti hirurgicheskogo lechenija anajerobnyh infekcij glubokih prostranstv shei, oslozhnjonnyh mediastinitom // Acta Biomedica Scientifica. 2017. T.2. №6. S.130–133 (in Russian)].
18. Pérez-Díaz M.A., Silva-Bermudez P., Jiménez-López B. et al. Silver-pig skin nanocomposites and mesenchymal stem cells: suitable antibiofilm cellular dressings for wound healing. Nanobiotechnology. 2018. Vol. 16(1). P.2.
19. Винник Ю.С., Серова Е.В., Куконков В.А. и др. Возможности применения сульфатиазола серебра в хирургии // РМЖ. 2017. Т.25. №8. С.529–532 [Vinnik Ju.S., Serova E.V., Kukonkov V.A. i dr. Vozmozhnosti primenenija sul’fatiazola serebra v hirurgii // RMZh. 2017. T.25. №8. S.529–532 (in Russian)].
20. Самцов А.В., Теличко И.Н., Стаценко А.В. Применение наружных средств, содержащих соединения серебра, в терапии больных пиодермиями // Вестник дерматологии и венерологии. 2014. №1. С.75–80 [Samcov A.V., Telichko I.N., Stacenko A.V. Primenenie naruzhnyh sredstv, soderzhashhih soedinenija serebra, v terapii bol’nyh piodermijami // Vestnik dermatologii i venerologii. 2014. №1. S.75–80 (in Russian)].
21. Федота Н.В., Лукьянова Д.А. Влияние мазей на основе серебра и цинка на регенерацию кожи при моделировании термических ожогов // Известия Оренбургского государственного аграрного университета. 2014. №6 (50). С.77–78 [Fedota N.V., Luk’janova D.A. Vlijanie mazej na osnove serebra i cinka na regeneraciju kozhi pri modelirovanii termicheskih ozhogov // Izvestija Orenburgskogo gosudarstvennogo agrarnogo universiteta. 2014. №6(50). S.77–78 (in Russian)].
22. Белоусова Т.А., Парамонов А.А., Горячкина М.В. Местная терапия бактериальных и некротически-язвенных поражений кожи и мягких тканей: поиск оптимальных решений // Фарматека. 2014. №10 (283). С.62–66 [Belousova T.A., Paramonov A.A., Gorjachkina M.V. Mestnaja terapija bakterial’nyh i nekroticheski-jazvennyh porazhenij kozhi i mjagkih tkanej: poisk optimal’nyh reshenij // Farmateka. 2014. №10 (283). S.62–66 (in Russian)].
23. Букина Ю.А., Сергеева Е.А. Антибактериальные свойства и механизм бактерицидного действия наночастиц и ионов серебра // Вестник Казанского технологического университета. 2012. Т.15. №14. С.170–172 [Bukina Ju.A., Sergeeva E.A. Antibakterial’nye svojstva i mehanizm baktericidnogo dejstvija nanochastic i ionov serebra // Vestnik Kazanskogo tehnologicheskogo universiteta. 2012. T.15. №14. S.170–172 (in Russian)].
24. Kim M.H., Park H., Nam H.C. et al. Injectable methylcellulose hydrogel containing silver oxide nanoparticles for burn wound healing. Carbohydr Polym. 2018. Vol. (181). P.579–586.
25. Мосин О.В. Бактерицидные свойства наночастиц коллоидного серебра // Нанотехнологии. Экология. Производство. 2013. №6(25). С.54–59 [Mosin O.V. Baktericidnye svojstva nanochastic kolloidnogo serebra // Nanotehnologii. Jekologija. Proizvodstvo. 2013. №6(25). S.54–59 (in Russian)].
26. Гмошинский И.В., Шипелин В.А., Ворожко И.В. и др. Токсикологическая оценка наноразмерного коллоидного серебра, стабилизированного поливинилпирролидоном. III. Энзимологические, биохимические маркеры, состояние системы антиоксидантной защиты // Вопросы питания. 2016. Т.85. №2. С.14–23 [Gmoshinskij I.V., Shipelin V.A., Vorozhko I.V. i dr. Toksikologicheskaja ocenka nanorazmernogo kolloidnogo serebra, stabilizirovannogo polivinilpirrolidonom. III. Jenzimologicheskie, biohimicheskie markery, sostojanie sistemy antioksidantnoj zashhity // Voprosy pitanija. 2016. T.85. №2. S.14–23 (in Russian)].
27. Фастовец И.А., Верховцева Н.В., Пашкевич Е.Б. и др. Наночастицы серебра: токсическое действие на микроорганизмы и взаимодействие с высшими растениями // Проблемы агрохимии и экологии. 2017. №1. С.51–62 [Fastovec I.A., Verhovceva N.V., Pashkevich E.B. i dr. Nanochasticy serebra: toksicheskoe dejstvie na mikroorganizmy i vzaimodejstvie s vysshimi rastenijami // Problemy agrohimii i jekologii. 2017. №1. S.51–62 (in Russian)].
28. Ullah Khan S., Saleh T.A., Wahab A. et al. Nanosilver: new ageless and versatile biomedical therapeutic scaffold. Nanomedicine. 2018. Vol. 2(13). P.733–762.
29. Тапальский Д.В., Осипов В.А., Сухая Г.Н. и др. Биосовместимые композиционные антибактериальные покрытия для защиты имплантатов от микробных биопленок // Проблемы здоровья и экологии. 2013. №2 (36). С.129–134 [Tapal’skij D.V., Osipov V.A., Suhaja G.N. i dr. Biosovmestimye kompozicionnye antibakterial’nye pokrytija dlja zashhity implantatov ot mikrobnyh bioplenok // Problemy zdorov’ja i jekologii. 2013. №2(36). S.129–134 (in Russian)].
30. Percival S.L. Restoring balance: biofilms and wound dressings // J Wound Care. 2018. Vol. 27(2). P.102–113. doi: 10.12968/jowc.2018.27.2.102
31. Федота Н.В., Лукьянова Д.А. Влияние мазей на основе серебра и цинка на регенерацию кожи при моделировании термических ожогов // Известия Оренбургского государственного аграрного университета. 2014. №6(50). С.77–78 [Fedota N.V., Luk’janova D.A. Vlijanie mazej na osnove serebra i cinka na regeneraciju kozhi pri modelirovanii termicheskih ozhogov // Izvestija Orenburgskogo gosudarstvennogo agrarnogo universiteta. 2014. №6(50). S.77–78 (in Russian)].
32. Зиновьев Е.В., Ивахнюк Г.К., Лагвилава Т.О. и др. Обоснование целесообразности разработки ранозаживляющих рецептур на основе карбополов для лечения ран при декомпенсированном диабете // Хирург. 2013. №6. С.47–53 [Zinov’ev E.V., Ivahnjuk G.K., Lagvilava T.O. i dr. Obosnovanie celesoobraznosti razrabotki ranozazhivljajushhih receptur na osnove karbopolov dlja lechenija ran pri dekompensirovannom diabete // Hirurg. 2013. №6. S.47–53 (in Russian)].
33. Савченко Ю.П., Федосов С.Р., Плаксин А.М. Способ определения площади дефекта кожи и контроля ее измерений. Патент на изобретение № 2301626. Заявл. 17.11.2005. Oпубл. 27.06.2007. Б.18. 5 с. [Savchenko Ju.P., Fedosov S.R., Plaksin A.M. Sposob opredelenija ploshhadi defekta kozhi i kontrolja ejo izmerenij. Patent na izobretenie № 2301626. Zajavl. 17.11.2005. Opubl. 27.06.2007. B.18. 5 s. (in Russian)].
2. Marchiano E., Raikundalia M.D., Carniol E.T. et al. Characteristics of patients treated for orbital cellulitis: An analysis of inpatient data // Laryngoscope. 2016. Vol. 126(3). Р.9.
3. Юлдашев И.М., Ургуналиев Б.К., Ашиналиев А.А. и др. Тотальный одонтогенный медиастинит как осложнение гнилостно некротической флегмоны дна полости рта // Тихоокеанский медицинский журнал. 2011. №3. С.97–98 [Juldashev I.M., Urgunaliev B.K., Ashinaliev A.A. i dr. Total’nyj odontogennyj mediastinit kak oslozhnenie gnilostnonekroticheskoj flegmony dna polosti rta // Tihookeanskij medicinskij zhurnal. 2011. №3. S.97–98 (in Russian)].
4. Brea Álvarez B., Esteban García L., Tuñón Gómez M., Cepeda Ibarra Y. Nontraumatic head and neck injuries: a clinical approach. Part 2 // Radiologia. 2017. Vol. 59(3). P.182–195.
5. Гусейнова М.Г., Бисаев У.И. Фармакотерапия флегмоны и одонтогенного остеомиелита челюстных костей // Бюллетень медицинских интернет-конференций. 2017. Т.7. №6. С.1279 [Gusejnova M.G., Bisaev U.I. Farmakoterapija flegmony i odontogennogo osteomielita cheljustnyh kostej // Bjulleten’ medicinskih internet-konferencij. 2017. T.7. №6. S.1279 (in Russian)].
6. Hirasawa K., Tsukahara K., Motohashi R. et al. Deep neck cellulitis: limitations of conservative treatment with antibiotics // Acta Otolaryngol. 2017. Vol. 137(1). P.86–89.
7. Монаков В.А., Иващенко А.В., Решетникова В.П Особенности микробиологической картины ран у больных с одонтогенными флегмонами челюстно-лицевой области при использовании вакуум-терапии // Клиническая стоматология. 2014. №1(69). С.40–43 [Monakov V.A., Ivashhenko A.V., Reshetnikova V.P Osobennosti mikrobiologicheskoj kartiny ran u bol’nyh s odontogennymi flegmonami cheljustno-licevoj oblasti pri ispol’zovanii vakuum-terapii // Klinicheskaja stomatologija. 2014. №1(69). S.40–43 (in Russian)].
8. Куликовский В.Ф., Оганесян В.Ф. Летальность при неклостридиальной анаэробной инфекции мягких тканей челюстно-лицевой области и шеи // Вестник экспериментальной и клинической хирургии. 2010. Т.3. №4. С.373–376 [Kulikovskij V.F., Oganesjan V.F. Letal’nost’ pri neklostridial’noj anajerobnoj infekcii mjagkih tkanej cheljustno-licevoj oblasti i shei // Vestnik jeksperimental’noj i klinicheskoj hirurgii. 2010. T.3. №4. S.373–376 (in Russian)].
9. Lin Y.Q., An L.F., Li L. New treatment choice of head and neck cellulitis: multi-catheter drainage guided by ultrasound percutaneous puncture // Zhonghua Er Bi Yan Hou Tou Jing Wai Ke Za Zhi. 2017. Vol. 52(2). P.110–112.
10. Субханова Г.С. Сравнительный анализ эффективности перевязочных средств в лечении гнойных ран лица и шеи // Вестник Авиценны. 2013. №2(55). С.117–123 [Subhanova G.S. Sravnitel’nyj analiz jeffektivnosti perevjazochnyh sredstv v lechenii gnojnyh ran lica i shei // Vestnik Avicenny. 2013. №2(55). S.117–123 (in Russian)].
11. Кетова Г.Г., Латюшина Л.С., Долгушин И.И. Фармакоэкономический анализ местного применения иммунопрепаратов в комплексном лечении больных с одонтогенными флегмонами // Проблемы стандартизации в здравоохранении. 2009. №3–4. С.30–35 [Ketova G.G., Latjushina L.S., Dolgushin I.I. Farmakojekonomicheskij analiz mestnogo primenenija immunopreparatov v kompleksnom lechenii bol’nyh s odontogennymi flegmonami // Problemy standartizacii v zdravoohranenii. 2009. №3–4. S.30–35 (in Russian)].
12. Баранник Н.Г., Варжапетян С.Д., Сидоряко А.В. и др. Изменение иммунного статуса при флегмонах челюстно-лицевой области в зависимости от распространенности гнойного процесса // Запорожский медицинский журнал. 2016. №1(94). С.44–49 [Barannik N.G., Varzhapetjan S.D., Sidorjako A.V. i dr. Izmenenie immunnogo statusa pri flegmonah cheljustno-licevoj oblasti v zavisimosti ot rasprostranjonnosti gnojnogo processa // Zaporozhskij medicinskij zhurnal. 2016. №1(94). S.44–49 (in Russian)].
13. Taub D., Yampolsky A., Diecidue R., Gold L. Controversies in the Management of Oral and Maxillofacial Infections // Oral Maxillofac Surg Clin North Am. 2017. Vol. 29(4) P.465–473.
14. Кабанова С.А. Изучение иммунного статуса при гнойно-воспалительных заболеваниях челюстно-лицевой области // Новости хирургии. 2005. Т.13. №1–4. С.28–32 [Kabanova S.A. Izuchenie immunnogo statusa pri gnojno-vospalitel’nyh zabolevanijah cheljustno-licevoj oblasti // Novosti hirurgii. 2005. T.13. №1–4. S.28–32 (in Russian)].
15. Hirasawa K., Tsukahara K., Motohashi R. et al. Deep neck cellulitis: limitations of conservative treatment with antibiotics // Acta Otolaryngol. 2017. Vol. 137(1). P.86–89.
16. Монаков В.А. Гидродинамическое обоснование аспирационно-промывного дренирования гнойных ран // Южно-Уральский медицинский журнал. 2015. №2. С.16–21 [Monakov V.A. Gidrodinamicheskoe obosnovanie aspiracionno-promyvnogo drenirovanija gnojnyh ran // Juzhno-Ural’skij medicinskij zhurnal. 2015. №2. S.16–21 (in Russian)].
17. Лишов Е.В., Харитонов А.А., Путинцев А.М. Особенности хирургического лечения анаэробных инфекций глубоких пространств шеи, осложненных медиастинитом // Acta Biomedica Scientifica. 2017. Т.2. №6. С.130–133 [Lishov E.V., Haritonov A.A., Putincev A.M. Osobennosti hirurgicheskogo lechenija anajerobnyh infekcij glubokih prostranstv shei, oslozhnjonnyh mediastinitom // Acta Biomedica Scientifica. 2017. T.2. №6. S.130–133 (in Russian)].
18. Pérez-Díaz M.A., Silva-Bermudez P., Jiménez-López B. et al. Silver-pig skin nanocomposites and mesenchymal stem cells: suitable antibiofilm cellular dressings for wound healing. Nanobiotechnology. 2018. Vol. 16(1). P.2.
19. Винник Ю.С., Серова Е.В., Куконков В.А. и др. Возможности применения сульфатиазола серебра в хирургии // РМЖ. 2017. Т.25. №8. С.529–532 [Vinnik Ju.S., Serova E.V., Kukonkov V.A. i dr. Vozmozhnosti primenenija sul’fatiazola serebra v hirurgii // RMZh. 2017. T.25. №8. S.529–532 (in Russian)].
20. Самцов А.В., Теличко И.Н., Стаценко А.В. Применение наружных средств, содержащих соединения серебра, в терапии больных пиодермиями // Вестник дерматологии и венерологии. 2014. №1. С.75–80 [Samcov A.V., Telichko I.N., Stacenko A.V. Primenenie naruzhnyh sredstv, soderzhashhih soedinenija serebra, v terapii bol’nyh piodermijami // Vestnik dermatologii i venerologii. 2014. №1. S.75–80 (in Russian)].
21. Федота Н.В., Лукьянова Д.А. Влияние мазей на основе серебра и цинка на регенерацию кожи при моделировании термических ожогов // Известия Оренбургского государственного аграрного университета. 2014. №6 (50). С.77–78 [Fedota N.V., Luk’janova D.A. Vlijanie mazej na osnove serebra i cinka na regeneraciju kozhi pri modelirovanii termicheskih ozhogov // Izvestija Orenburgskogo gosudarstvennogo agrarnogo universiteta. 2014. №6(50). S.77–78 (in Russian)].
22. Белоусова Т.А., Парамонов А.А., Горячкина М.В. Местная терапия бактериальных и некротически-язвенных поражений кожи и мягких тканей: поиск оптимальных решений // Фарматека. 2014. №10 (283). С.62–66 [Belousova T.A., Paramonov A.A., Gorjachkina M.V. Mestnaja terapija bakterial’nyh i nekroticheski-jazvennyh porazhenij kozhi i mjagkih tkanej: poisk optimal’nyh reshenij // Farmateka. 2014. №10 (283). S.62–66 (in Russian)].
23. Букина Ю.А., Сергеева Е.А. Антибактериальные свойства и механизм бактерицидного действия наночастиц и ионов серебра // Вестник Казанского технологического университета. 2012. Т.15. №14. С.170–172 [Bukina Ju.A., Sergeeva E.A. Antibakterial’nye svojstva i mehanizm baktericidnogo dejstvija nanochastic i ionov serebra // Vestnik Kazanskogo tehnologicheskogo universiteta. 2012. T.15. №14. S.170–172 (in Russian)].
24. Kim M.H., Park H., Nam H.C. et al. Injectable methylcellulose hydrogel containing silver oxide nanoparticles for burn wound healing. Carbohydr Polym. 2018. Vol. (181). P.579–586.
25. Мосин О.В. Бактерицидные свойства наночастиц коллоидного серебра // Нанотехнологии. Экология. Производство. 2013. №6(25). С.54–59 [Mosin O.V. Baktericidnye svojstva nanochastic kolloidnogo serebra // Nanotehnologii. Jekologija. Proizvodstvo. 2013. №6(25). S.54–59 (in Russian)].
26. Гмошинский И.В., Шипелин В.А., Ворожко И.В. и др. Токсикологическая оценка наноразмерного коллоидного серебра, стабилизированного поливинилпирролидоном. III. Энзимологические, биохимические маркеры, состояние системы антиоксидантной защиты // Вопросы питания. 2016. Т.85. №2. С.14–23 [Gmoshinskij I.V., Shipelin V.A., Vorozhko I.V. i dr. Toksikologicheskaja ocenka nanorazmernogo kolloidnogo serebra, stabilizirovannogo polivinilpirrolidonom. III. Jenzimologicheskie, biohimicheskie markery, sostojanie sistemy antioksidantnoj zashhity // Voprosy pitanija. 2016. T.85. №2. S.14–23 (in Russian)].
27. Фастовец И.А., Верховцева Н.В., Пашкевич Е.Б. и др. Наночастицы серебра: токсическое действие на микроорганизмы и взаимодействие с высшими растениями // Проблемы агрохимии и экологии. 2017. №1. С.51–62 [Fastovec I.A., Verhovceva N.V., Pashkevich E.B. i dr. Nanochasticy serebra: toksicheskoe dejstvie na mikroorganizmy i vzaimodejstvie s vysshimi rastenijami // Problemy agrohimii i jekologii. 2017. №1. S.51–62 (in Russian)].
28. Ullah Khan S., Saleh T.A., Wahab A. et al. Nanosilver: new ageless and versatile biomedical therapeutic scaffold. Nanomedicine. 2018. Vol. 2(13). P.733–762.
29. Тапальский Д.В., Осипов В.А., Сухая Г.Н. и др. Биосовместимые композиционные антибактериальные покрытия для защиты имплантатов от микробных биопленок // Проблемы здоровья и экологии. 2013. №2 (36). С.129–134 [Tapal’skij D.V., Osipov V.A., Suhaja G.N. i dr. Biosovmestimye kompozicionnye antibakterial’nye pokrytija dlja zashhity implantatov ot mikrobnyh bioplenok // Problemy zdorov’ja i jekologii. 2013. №2(36). S.129–134 (in Russian)].
30. Percival S.L. Restoring balance: biofilms and wound dressings // J Wound Care. 2018. Vol. 27(2). P.102–113. doi: 10.12968/jowc.2018.27.2.102
31. Федота Н.В., Лукьянова Д.А. Влияние мазей на основе серебра и цинка на регенерацию кожи при моделировании термических ожогов // Известия Оренбургского государственного аграрного университета. 2014. №6(50). С.77–78 [Fedota N.V., Luk’janova D.A. Vlijanie mazej na osnove serebra i cinka na regeneraciju kozhi pri modelirovanii termicheskih ozhogov // Izvestija Orenburgskogo gosudarstvennogo agrarnogo universiteta. 2014. №6(50). S.77–78 (in Russian)].
32. Зиновьев Е.В., Ивахнюк Г.К., Лагвилава Т.О. и др. Обоснование целесообразности разработки ранозаживляющих рецептур на основе карбополов для лечения ран при декомпенсированном диабете // Хирург. 2013. №6. С.47–53 [Zinov’ev E.V., Ivahnjuk G.K., Lagvilava T.O. i dr. Obosnovanie celesoobraznosti razrabotki ranozazhivljajushhih receptur na osnove karbopolov dlja lechenija ran pri dekompensirovannom diabete // Hirurg. 2013. №6. S.47–53 (in Russian)].
33. Савченко Ю.П., Федосов С.Р., Плаксин А.М. Способ определения площади дефекта кожи и контроля ее измерений. Патент на изобретение № 2301626. Заявл. 17.11.2005. Oпубл. 27.06.2007. Б.18. 5 с. [Savchenko Ju.P., Fedosov S.R., Plaksin A.M. Sposob opredelenija ploshhadi defekta kozhi i kontrolja ejo izmerenij. Patent na izobretenie № 2301626. Zajavl. 17.11.2005. Opubl. 27.06.2007. B.18. 5 s. (in Russian)].

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Предыдущая статья
Следующая статья