Интегральные гематологические индексы как маркер развития пострезекционной печеночной недостаточности
Цель исследования: определить особенности изменений интегральных гематологических индексов (ИГИ), оценить их диагностическую ценность у пациентов при развитии пострезекционной печеночной недостаточности.
Материал и методы: в исследование вошло 54 пациента, среди них 32 (59%) женщины (средний возраст пациентов — 59,5 [49,7; 66] года), которым была выполнена сегментарная резекция или гемигепатэктомия по поводу злокачественных и доброкачественных новообразований печени. Пациенты были разделены на две группы: 1-ю группу (n=44) составили пациенты, у которых в послеоперационном периоде не было диагностировано пострезекционной печеночной недостаточности, у пациентов 2-й группы (n=10) послеоперационный период осложнился развитием печеночной недостаточности. У всех пациентов при поступлении, а также на 3-и сутки после операции исследовали показатели общего анализа крови с подсчетом лейкоцитарной формулы, определяли значения лейкоцитарных индексов клеточной реактивности.
Результаты исследования: при сравнительном анализе интегральных гематологических индексов у пациентов с различным течением послеоперационного периода выявлены статистически значимые различия большинства исходных показателей. Установлено, что лейкоцитарный индекс интоксикации, рассчитанный по формуле Я.Я. Кальф-Калифа, модифицированный лейкоцитарный индекс интоксикации Б.А. Рейса, модифицированный лейкоцитарный индекс интоксикации В.К. Островского и гематологический показатель интоксикации в послеоперационном периоде в группе пациентов с печеночной недостаточностью достоверно (р=0,005, р=0,041, р=0,041, р=0,001 соответственно) отличались от показателей пациентов без печеночной недостаточности. Повышение данных индексов может служить ранним диагностическим критерием развития пострезекционной печеночной недостаточности.
Заключение: метод подсчета интегральных гематологических индексов является простым и дешевым методом диагностики, который можно применять, имея только результаты лейкоцитарной формулы. Определение диагностически значимых индексов в динамике можно использовать как прогностический и скрининговый метод выявления пострезекционной печеночной недостаточности.
Ключевые слова: печеночная недостаточность, резекция печени, диагностика, скрининг, интегральные гематологические показатели, лейкоцитарный индекс.
Для цитирования: Дунаевская С.С., Сачивко К.В., Косик А.А., Бережная М.А., Наркевич А.Н. Интегральные гематологические индексы как маркер развития пострезекционной печеночной недостаточности. РМЖ. Медицинское обозрение. 2021;29(6):101-104.
Integral hematological indices as a marker of the postresection liver failure
S.S. Dunaevskaya, K.V. Sachivko, A.A. Kosik, M.A. Berezhnaya, A.N. Narkevich
Krasnoyarsk State Medical University named after Prof. V.F. Voino-Yasenetsky, Krasnoyarsk
Background: acute liver failure is the most dangerous complication after liver resection, characterized by acute, rapidly developing a hepatic injury.
Aim: to determine the patterns of changes in the integral hematological indices (IHI), to assess their diagnostic value in patients with the development of postresection liver failure (PLF).
Patients and Methods: the study included 54 patients, among them 32 (59%) women (the average age of patients was 59.5 [49.7; 66] years), who underwent segmental resection or hemihepatectomy for malignant and benign liver tumors. The patients were divided into two groups: group 1 (n=44) — consisted of patients who had not been diagnosed with PLF in the postoperative period, group 2 (n=10) — the postoperative period was complicated by the development of hepatic failure. In all patients at admission, as well as on the 3rd day after surgery, the indicators of the complete blood count with the calculation of the WBC count were studied, and the values of the leukocyte indices of cellular reactivity were determined.
Results: IHI comparative analysis in patients with different postoperative period revealed statistically significant differences in most of the base indicators. It was found that the leukocyte intoxication index by J.J. Kalf-Kalif, modified leukocyte intoxication index of B.A. Reis, modified leukocyte intoxication index of V.K. Ostrovsky and hematological intoxication index in the postoperative period in the group of patients with the liver failure significantly (p=0.005, p=0.041, p=0.041, p=0.001, respectively) differed from the indicators of patients without liver failure. An increase in these indices can serve as an early diagnostic criterion for PLF development.
Conclusion: the method of calculating IHI is a simple and cheap diagnostic method that can be used only with the results of the leukocyte formula. The determination of diagnostically significant indices in dynamics can be used as a prognostic and screening method for detecting PLF.
Keywords: liver failure, liver resection, diagnosis, screening, integral hematological indices, leukocyte index.
For citation: Dunaevskaya S.S., Sachivko K.V., Kosik A.A. et al. Integral hematological indices as a marker of the postresection liver failure. RMJ. 2021;6:101–104 (in Russ.).
Введение
Острая печеночная недостаточность (ОПН) — одно из наиболее частых осложнений после резекции печени, характеризующееся острым, быстроразвивающим поражением печени. Исход заболевания зависит от различных факторов, но в первую очередь от своевременной диагностики и правильной этиотропной и патогенетической терапии [1–3].
Оперативное лечение очаговых заболеваний печени остается чаще всего методом выбора и единственным способом достижения радикального результата лечения пациентов с объемными образованиями печени доброкачественного и злокачественного генеза [4, 5]. Локализация и размер опухоли, особенности сосудистой структуры печени, а также желание хирурга радикально удалить опухоль и минимизировать риск рецидива болезни требуют обширных резекций печени. По мнению разных авторов, объем паренхимы печени, удаленной при обширных резекциях, может составлять 50–80% от ее объема [6–12].
Для ранней диагностики послеоперационных осложнений эффективны оценка и динамика показателей интегральных гематологических индексов, позволяющих оценить степень интоксикационного синдрома и выраженность неспецифического иммунного ответа [13–15], однако в доступной нам литературе исследований, посвященных изменениям показателей интегральных гематологических показателей при развитии пострезекционной печеночной недостаточности, не было найдено.
Цель исследования: определить особенности изменений интегральных гематологических индексов, оценить их диагностическую ценность у пациентов при развитии пострезекционной печеночной недостаточности.
Материал и методы
В исследование вошли 54 пациента, из них 32 (59%) женщины, находившиеся в хирургических отделениях ФГБУ ФСНКЦ ФМБА России и КГБУЗ «КККОД им. А.И. Крыжановского» в период с 2018 по 2020 г. Средний возраст пациентов составил 59,5 [49,7; 66] года, индекс массы тела — 26,6 [22,3; 30,5] кг/м2.
Обследованные больные имели следующие показания к проведению резекции печени: первичный рак печени — 15 (28%) человек, метастатические поражения печени — 29 (54%), паразитарные заболевания печени — 3 (5%), доброкачественные образования печени — 7 (13%). Были выполнены следующие операции: у 36 (67%) пациентов — сегментарная резекция печени, у 10 (18%) — левосторонняя гемигепатэктомия и у 8 (15%) — правосторонняя гемигепатэктомия. В послеоперационном периоде проводилась терапия, которая назначалась с учетом особенностей проведенной операции и состояния пациента. Средняя продолжительность нахождения больных в стационаре составила 14 [10,25; 25] дней.
Пациенты были разделены на две клинические группы: 1-ю группу (n=44) составили пациенты, у которых в послеоперационном периоде не было диагностировано пострезекционной печеночной недостаточности, у пациентов 2-й группы (n=10) послеоперационный период осложнился развитием печеночной недостаточности.
У всех пациентов при поступлении, а также в динамике (на 3-и сутки после операции) исследовали показатели общего анализа крови с подсчетом лейкоцитарной формулы. Определяли значения следующих лейкоцитарных индексов клеточной реактивности: лейкоцитарный индекс интоксикации (ЛИИ) по формуле Я.Я. Кальф-Калифа, модифицированный лейкоцитарный индекс интоксикации (МЛИИ) Б.А. Рейса, МЛИИ В.К. Островского, индекс резистентности организма (ИРО), ядерный индекс Г.Д. Даштаянца (ЯИ), реактивный ответ нейтрофилов (РОН) (Хабиров Т.Ш., 2000), индекс сдвига лейкоцитов крови (ИСЛК), индекс соотношения лейкоцитов и СОЭ (ИЛСОЭ), лимфоцитарно-гранулоцитарный индекс (ИЛГ), лейкоцитарный индекс (ЛИ), индекс соотношения нейтрофилов и лимфоцитов (ИСНЛ), индекс соотношения нейтрофилов и моноцитов (ИСНМ), индекс соотношения лимфоцитов и моноцитов (ИСЛМ), индекс соотношения лимфоцитов и эозинофилов (ИСЛЭ), гематологический показатель интоксикации (ГПИ), изменения показателей оценивались по средним нормативным значениям.
Обработку данных, полученных в результате исследования, выполняли с помощью программы Statistica 6.1, а результаты представляли в виде процентов (%) и в виде медианы и 25-го и 75-го перцентилей Me [Q1; Q3]. Для оценки статистической значимости различий между группами применяли точный критерий Фишера. Статистически значимыми считали различия при уровне значимости p меньше 0,05.
Результаты и обсуждение
Как видно из таблицы 1, до операции практически у половины больных 1-й группы интегральные гематологические показатели соответствовали нормальным значениям, тогда как после операции значения практически всех индексов выходили за пределы референсных показателей. Так, например, ИРО и до, и после операции был выше нормативных значений. Показатель РОН до операции был ниже нормы, составив 1,17, а на 3-и сутки после операции произошло увеличение почти в 4 раза от референсных значений — до 10,77. ИЛГ в динамике снизился с 3,56 до 1,04, став ниже нормы. ЛИ исходно был несколько снижен, продолжив снижение в послеоперационном периоде. ИСЛМ продемонстрировал аналогичную динамику, а ИСНЛ, напротив, вырос относительно практически нормальных исходных значений. ИСНМ до операции был существенно ниже нормы, а после операции был в пределах нормальных значений (см. таблицу 1).
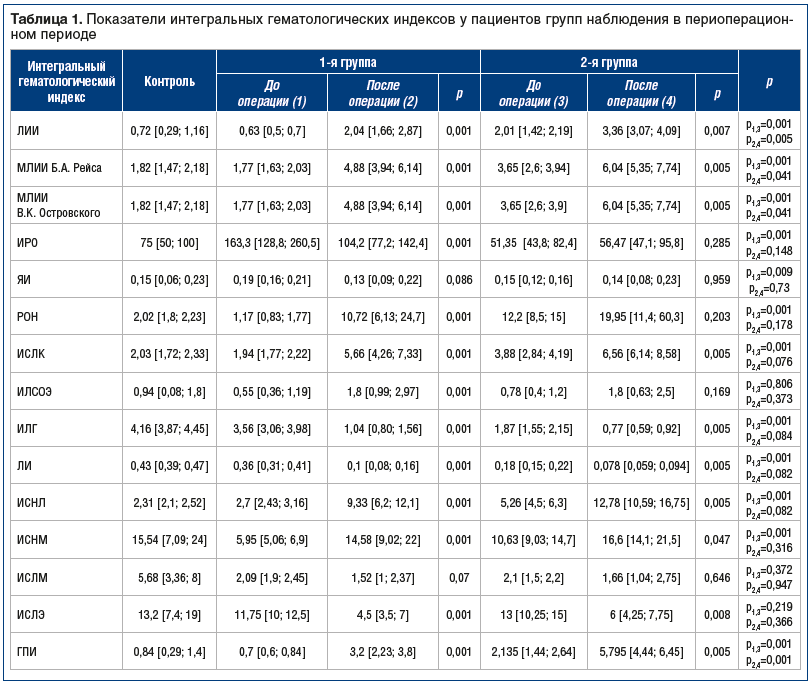
После операции в 1-й группе произошло изменение следующих индексов, значения которых в предоперационном периоде были в пределах нормальных границ: повышение ЛИИ, МЛИИ Рейса, МЛИИ Островского, ИСЛК, ГПИ, снижение ИСЛЭ. Можно предположить, что в ходе операционного стресса в раннем послеоперационном периоде нарастает эндотоксикоз, а также активность неспецифического иммунитета, что обусловлено операционной травмой [13, 15].
Динамика ЯИ и ИСЛМ была статистически незначимой. Для всех остальных индексов установлена статистически значимая разница значений показателей до и после операции (p<0,001).
При анализе интегральных гематологических индексов у пациентов 2-й группы выявлено (см. табл. 1), что до и после операции часть показателей соответствовала норме, а часть показателей изменялась в большую или меньшую сторону относительно референсных значений. Так, например, ЛИИ, МЛИИ Рейса, МЛИИ Островского, РОН, ИСЛК, ИСНЛ, ГПИ были повышены и до, и после операции. ИЛГ, ЛИ, ИСЛМ до операции были ниже контрольных цифр, снизившись еще больше после операции. ИСЛЭ до операции был в норме, а после вмешательства снизился почти в 2 раза. Наиболее важным является изменение интегральных гематологических индексов уже в предоперационном периоде, что можно расценивать как предикторы осложненного течения послеоперационного периода. В дальнейшем происходило более выраженное увеличение показателей, отражающих интоксикацию, в сравнении с 1-й группой, что согласуется с данными о развитии эндотоксикоза, сопровождающего другие патологии [13, 14].
Для показателей ИРО, ЯИ, РОН, ИЛСОЭ и ИСЛМ во 2-й группе не получено статистически значимых различий до- и послеоперационных значений (см. табл. 1).
Следующим этапом исследования было сравнение значений интегральных гематологических показателей в предоперационном периоде между 1-й и 2-й группами. Исходно нормальными в 1-й группе и повышенными во 2-й группе были ЛИИ, МЛИИ Рейса и МЛИИ Островского, ИСЛК, ГПИ. ИРО в 1-й группе был повышен, во 2-й — соответствовал нормальным значениям. Исходно снижены в обеих группах были ИЛГ, ЛИ, ИСЛМ, исходно повышен — ИСНЛ. ИСНМ в 1-й группе был снижен, а во 2-й не отличался от нормы. Статистическая значимость различий исходных показателей между группами отсутствовала для следующих показателей: ИЛСОЭ, ИСЛМ и ИСЛЭ. Во всех остальных случаях разница исходных показателей была статистически значимой (p<0,001). Таким образом, уже в предоперационном периоде выявлены достоверные отличия в интегральных гематологических показателях между 1-й и 2-й группами, что можно использовать как предикторы развития пострезекционной печеночной недостаточности после операции.
Следующим этапом исследования было сравнение интегральных гематологических показателей в послеоперационном периоде (см. табл. 1). Так, повышенные значения относительно нормативных значений в обеих группах определялись для ЛИИ, МЛИИ, РОН, ИСЛК, ИЛСОЭ, ИСНЛ, ГПИ. Более низкие относительно нормы значения в обеих группах были характерны для ИЛГ, ЛИ, ИСЛМ, ИСЛЭ. Показатель ИРО в 1-й группе после операции был повышен, во 2-й группе — снижен.
Статистический анализ не выявил различий между большинством послеоперационных показателей обеих групп (p>0,05). Однако ЛИИ, оба МЛИИ и ГПИ достоверно отличались друг от друга (р=0,005; р=0,041; р=0,041 и р=0,001 соответственно, см. таблицу 1).
Заключение
Проведенный в ходе исследования сравнительный анализ интегральных гематологических индексов выявил наличие статистически значимых различий дооперационных показателей пациентов с и без печеночной недостаточности после резекции печени. Сопоставимыми (p>0,05) оказались только 3 показателя: ИЛСОЭ, ИСЛМ и ИСЛЭ. В послеоперационном периоде достоверно отличались ЛИИ, МЛИИ и ГПИ. Повышение данных индексов может служить ранним диагностическим критерием развития
пострезекционной печеночной недостаточности.
Таким образом, метод подсчета интегральных гематологических индексов является простым и дешевым методом диагностики, который можно применять, имея только результаты лейкоцитарной формулы. Изменения в показателях диагностически значимых индексов можно использовать как метод прогноза и скрининг диагностики развития пострезекционной печеночной недостаточности.
2. Lillemoe H.A., Marcus R.K., Kim B.J. et al. Severe preoperative symptoms delay readiness to Return to Intended Oncologic Therapy (RIOT) after liver resection. Ann Surg Oncol. 2019;26(13):4548–4555. DOI: 10.1245/s10434-019-07719-8.
3. Zhao L.Y., Yang D.D., Ma X.K. et al. The prognostic value of aspartate aminotransferase to lymphocyte ratio and systemic immune-inflammation index for overall survival of hepatocellular carcinoma patients treated with palliative treatments. J Cancer. 2019;10(10):2299–2311. DOI: 10.7150/jca.30663.
4. Кит О.И., Франциянц Е.М., Никипелова Е.А., Комарова Е.Ф. Состояние свободнорадикальных процессов в ткани злокачественной опухоли толстой кишки. Сибирское медицинское обозрение. 2014;1:30–34. [Kit O.I., Frantsiyants E.M., Nikipelova E.A., Komarova E.F. Condition of free radical processes in the tissue of a malignant tumor of the colon. Siberian Medical Review. 2014;1:30–34 (in Russ.)].
5. Wang L., Ye G., Zhan C. et al. Clinical factors predictive of a better prognosis of pulmonary metastasectomy for hepatocellular carcinoma. Ann Thorac Surg. 2019;108(6):1685–1691. DOI: 10.1016/j.athoracsur.2019.06.086.
6. Вишневский В.А., Ефанов М.Г., Паклина О.В. и др. Анатомические сегментарные резекции при метастазах колоректального рака в печень. Анналы хирургической гепатологии. 2010;15(3):48–57. [Vishnevskiy V.A., Efanov M.G., Paklina O.V. et al. Anatomical segmental resections in colorectal cancer metastases to the liver. Annaly khirurgicheskoy gepatologii. 2010;15(3):48–57 (in Russ.)].
7. Даминова Н.М., Курбонов К.М. Экономные и атипичные резекции печени при очаговых заболеваниях. Известия Академии наук Республики Таджикистан. Отделение биологических и медицинских наук. 2001;2:82–86. [Daminova N.M., Kurbonov K.M. Economical and atypical liver resections in focal diseases. News of the Academy of Sciences of the Republic of Tajikistan. Department of Biological and Medical Sciences. 2001;2:82–86 (in Russ.)].
8. Kim D.S., Lim T.S., Jeon M.Y. et al. Transarterial chemoembolization in treatment-naïve and recurrent hepatocellular carcinoma: a propensity-matched outcome analysis. Dig Dis Sci. 2019;64(12):3660–3668. DOI: 10.1007/s10620-019-05701-8.
9. Okumura S., Tabchouri N., Leung U. et al. Laparoscopic parenchymal-sparing hepatectomy for multiple colorectal liver metastases improves outcomes and salvageability: a propensity score-matched analysis. Ann Surg Oncol. 2019;26(13):4576–4586. DOI: 10.1245/s10434-019-07902-x.
10. Liu Z., Li Q., Shen R. et al. Betaine/GABA transporter-1 (BGT-1) deficiency in mouse prevents acute liver failure in vivo and hepatocytes apoptosis in vitro. Biochim Biophys Acta Mol Basis Dis. 2020;1866(3):165634. DOI: 10.1016/j.bbadis.2019.165634.
11. De Miguel M.P., Prieto I., Moratilla A. et al. Mesenchymal stem cells for liver regeneration in liver failure: from experimental models to clinical trials. Stem Cells Int. 2019;2:3945672. DOI: 10.1155/2019/3945672.
12. Zhou P., Chen B., Miao X.Y. et al. 2019. Comparison of FIB-4 index and child-pugh score in predicting the outcome of hepatic resection for hepatocellular carcinoma. J Gastrointest Surg. 2020;24(4):823–831. DOI: 10.1007/s11605-019-04123-1.
13. Бензаракшеев В.Г. Лейкоцитарные индексы как способ оценки эндогенной интоксикации организма. Бюллетень Восточно-Сибирского научного центра Сибирского отделения Российской академии медицинских наук. 2010;3(73):390–391. [Benzaraksheev V.G. Leukocyte indices as a way to assess endog-enous body intoxication. Acta Biomedica Scientifica. 2010;3(73):390–391 (in Russ.)].
14. Гомоляко А.В., Ярец Ю.И. Лейкоцитарные индексы в динамике лечения хронических ран. Хирургия. Восточная Европа. 2012;3(3):251–252. [Gomolyako A.V., Yarets Yu.I. Leukocyte indices in chronic wound management dynamics. Khirurgiya. Vostochnaya Evropa. 2012;3(3):251–251 (in Russ.)].
15. Дябкин Е.В., Дунаевская С.С., Винник Ю.С. Состояние иммунной системы при патологии печени. Новости хирургии. 2011;19(1):112–116. [Dyabkin E.V., Dunaevskaya S.S., Vinnik Yu.S. State of the immune system in liver pathology. Novosti khirurgii. 2011;19(1):112–116 (in Russ.)].

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.

