Влияние дапаглифлозина на маркеры фиброза и воспаления у пациентов с сахарным диабетом 2 типа и очень высоким риском сердечно-сосудистых событий
DOI: 10.32364/2587-6821-2021-5-4-185-188
Введение: дапаглифлозин, как и другие ингибиторы натрий-глюкозного котранспортера 2 типа (ИНГТ2) в ряде рандомизированных клинических исследований продемонстрировал значимое положительное влияние на сердечно-сосудистые и почечные исходы у пациентов с сахарным диабетом 2 типа (СД2). Однако лежащие в основе этих результатов механизмы не до конца изучены.
Цель исследования: оценить динамику уровня сывороточных маркеров, ассоциированных с процессами фиброза и воспаления при СД2, на фоне терапии дапаглифлозином.
Материал и методы: в проспективное одноцентровое исследование включено 27 пациентов в возрасте от 40 до 65 лет с СД2 длительностью более 1 года, без верифицированной атеросклеротической болезни сердца и сосудов, но с множественными факторами риска сердечно-сосудистых событий (дислипидемией, ожирением, артериальной гипертензией). Все пациенты в дополнение к базовой терапии СД2 получали дапаглифлозин по 10 мг/сут в течение 6 мес. До лечения и через 6 мес. после лечения оценивали содержание маркеров фиброза, в том числе карбокситерминального фрагмента проколлагена I типа (PIСP), и маркеров воспаления.
Результаты исследования: медиана возраста пациентов составила 56 [49; 61] лет, длительность СД2 — 4 (7 [4; 12]) года. Через 6 мес. лечения дапаглифлозином наблюдалось значимое снижение концентрации PICP с 136,8 [100,4; 200,6] нг/мл до 104,8 [79,7; 162,0] нг/мл (р=0,019). Содержание галектина-3, матриксной металлопротеиназы-9, тканевого ингибитора матриксных металлопротеиназ-1, стимулирующего фактора роста, экспрессируемого геном 2, высокочувствительного С-реактивного белка и N-концевого пропептида предсердного натрийуретического гормона значимо не различалось при сравнении исходных значений и значений через 6 мес. лечения.
Заключение: терапия дапаглифлозином в течение 6 мес. приводила к снижению уровня PICP, что, наряду с другими механизмами, может отражать положительные эффекты дапаглифлозина на сердечно-сосудистые и почечные исходы у пациентов с СД2.
Ключевые слова: сахарный диабет 2 типа, фиброз, хроническое воспаление, дапаглифлозин, сердечно-сосудистые заболевания.
Для цитирования: Лебедев Д.А., Бабенко А.Ю. Влияние дапаглифлозина на маркеры фиброза и воспаления у пациентов с сахарным диабетом 2 типа и очень высоким риском сердечно-сосудистых событий. РМЖ. Медицинское обозрение. 2021;5(4):185-188. DOI: 10.32364/2587-6821-2021-5-4-185-188.
D.A. Lebedev, A.Yu. Babenko
V.A. Almazov National Medical Research Center, St. Petersburg, Russian Federation
Background: several randomized clinical trials have demonstrated that dapagliflozin, like other inhibitors of sodium-glucose cotransporter 2 (SGLT2), significantly improves cardiovascular and renal outcomes in type 2 diabetes (T2D). However, underlying mechanisms remain unclear.
Aim: to assess changes in the levels of serum markers associated with fibrosis and inflammation in patients with T2D receiving dapagliflozin.
Patients and Methods: this prospective single-center study included 27 patients aged 40–65 years with T2D that lasts more than 1 year and without verified atherosclerosis but multiple cardiovascular risk factors (i.e., dyslipidemia, obesity, hypertension). In addition to basic treatment for T2D, all patients received dapagliflozin 10 mg daily for 6 months. Before and 6 months after treatment, the levels of the markers of fibrosis (including procollagen type I carboxy-terminal propeptide/PICP) and inflammation were measured.
Results: the median age was 56 [49; 61] years and the median duration of T2D was 7 [4; 12] years. After 6-month treatment with dapagliflozin, significant reduction in the concentration of PICP from 136.8 [100,4; 200,6] ng/ml to 104.8 [79.7; 162.0] ng/ml (р = 0.019). The levels of galectin-3, matrix metalloproteinase (MMP) 9, tissue inhibitor of MMP-1, growth stimulating expressed gene 2, high-sensitivity C-reactive protein, and N-terminal pro-atrial natriuretic peptide were similar at baseline and after 6-month treatment.
Conclusions: 6-month treatment with dapagliflozin reduced the levels of PICP. Together with other mechanisms, this phenomenon illustrates the positive effects of dapagliflozin on cardiovascular and renal outcomes in T2D.
Keywords: type 2 diabetes, fibrosis, chronic inflammation, dapagliflozin, cardiovascular diseases.
For citation: Lebedev D.A., Babenko A.Yu. Effects of dapagliflozin of the markers of fibrosis and inflammation in type 2 diabetes and very high cardiovascular risk. Russian Medical Inquiry. 2021;5(4):185–188 (in Russ.). DOI: 10.32364/2587-6821-2021-5-4-185-188.

Введение
Ингибиторы натрий-глюкозного котранспортера 2 типа (ИНГТ2) продемонстрировали значимые кардиоваскулярные преимущества у пациентов с сахарным диабетом 2 типа (СД2) как с установленными сердечно-сосудистыми заболеваниями, так и с множественными факторами риска таковых [1–3]. Было выдвинуто несколько теорий, объясняющих положительное влияние ИНГТ2 на сердечно-сосудистые исходы. Так, в исследованиях получены данные по снижению преднагрузки на сердце вследствие усиления натрийуреза, улучшению метаболизма кардиомиоцитов, снижению выраженности фибротических и воспалительных процессов в миокарде и сосудистой стенке [4–6]. Однако данная тема продолжает оставаться предметом активного изучения.
Cахарный диабет 2 типа ассоциирован с развитием хронического воспаления вследствие действия различных механизмов. При этом показано, что ИНГТ2 могут снижать уровни некоторых цитокинов, таких как фактор некроза опухоли α, интерлейкин-6, высокочувствительный С-реактивный белок (вчСРБ) [7]. Кроме того, хорошо известно, что фибротические процессы в миокарде развиваются у пациентов с СД2 независимо от наличия артериальной гипертензии и выраженности коронарного атеросклероза [8]. В связи с этим изучение процессов фиброза и воспаления у пациентов с СД2 является актуальным.
Цель исследования: оценить динамику уровня сывороточных маркеров, ассоциированных с процессами фиброза и воспаления при СД2, на фоне лечения дапаглифлозином.
Материал и методы
Проведено одноцентровое проспективное исследование, одобренное этическим комитетом ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России. До вступления в исследование все пациенты подписывали информированное согласие. Включали пациентов с СД2 длительностью более 1 года, уровнем гликированного гемоглобина от 7% до 10%, без верифицированной атеросклеротической болезни сердца и сосудов, но с множественными факторами риска сердечно-сосудистых событий (дислипидемией, ожирением, артериальной гипертензией). Кроме того, критериями включения были возраст от 40 до 65 лет, стабильная сахароснижающая, гиполипидемическая и антигипертензивная терапия как минимум в течение 12 нед. до включения в исследование. В исследование не включали пациентов с фибрилляцией предсердий, клапанными пороками сердца, ревматологическими заболеваниями, обострением хронических заболеваний, сахарным диабетом 1 типа, симптомами гипотензии и уровнем систолического артериального давления (САД) ниже 95 мм рт. ст., уровнем N-концевого пропептида натрийуретического гормона (NT-proBNP) >125 нг/мл, скоростью клубочковой фильтрации (СКФ) <60 мл/мин/1,73 м2 и хронической болезнью почек, заболеваниями печени а также получающих инсулинотерапию, терапию глюкокортикостероидами, антагонистами минералокортикоидных рецепторов. Пациенты получали дапаглифлозин в дозе 10 мг/сут в течение 6 мес. в дополнение к базовой терапии СД2.
В ходе исследования проводили забор образцов крови до начала лечения дапаглифлозином и через 6 мес. лечения. Образцы крови забирали натощак (после 8 ч голодания), оценивали следующие показатели: гликированный гемоглобин (HbA1c), аланинаминотрансферазу, аспартатаминотрансферазу, креатинин, липидограмму (общий холестерин, липопротеины низкой плотности (ЛПНП), липопротеины высокой плотности (ЛПВП), триглицериды), NT-proBNP, вчСРБ, галектин-3, тканевой ингибитор матриксных металлопротеиназ-1 (TIMP-1), матриксную металлопротеиназу-9 (MMP-9), стимулирующий фактор роста, экспрессируемый геном 2 (ST2), карбокситерминальный фрагмент проколлагена I типа (PIСP). Уровень вчСРБ определяли на анализаторе Cobas Integra 400+ иммунотурбидиметрическим методом. Концентрацию NT-proBNP определяли электрохемилюминесцентным методом c применением тест-системы Elecsys (Roche Diagnostic). Оценку сывороточных уровней галектина-3 (R&D system), ММР-9 и TIMP-1 (R&D system), sST2 (Clinical diagnostics, Presage ST2 kit), PICP (USCN Life Science) проводили методом иммуноферментного анализа. Кроме того, в начале и в конце исследования оценивали массу тела, рост, окружность талии, уровень артериального давления (АД). С целью оценки нормальных значений биомаркеров фиброза в исследование дополнительно были включены 15 пациентов сходного возраста без СД2 и других хронических заболеваний, в том числе сердечно-сосудистых и заболеваний почек (группа контроля).
Для статистического анализа использовали программу SPSS Statistics. Количественные данные представлены в виде медианы и 25-го и 75-го квартилей — Me [Q25; Q75], качественные признаки — в виде абсолютного и относительного (%) показателей. Различия между количественными показателями выявляли с помощью критерия Вилкоксона. Корреляционный анализ проводили с использованием рангового коэффициента корреляции Спирмена. Нулевая гипотеза отвергалась при р<0,05.
Результаты исследования
В исследование включено 27 пациентов (возраст 56 [49; 61] лет), у большинства из которых были СД2 длительностью более 4 лет (7 [4; 12] лет) и ожирение I степени. Базовая сахароснижающая терапия включала комбинацию метформина с препаратами сульфонилмочевины или ингибиторами дипептидилпептидазы 4 типа (иДПП-4).
Основная характеристика пациентов и динамика изучаемых маркеров фиброза и воспаления представлена в таблице 1. За 6 мес. лечения дапаглифлозином наблюдалось значимое снижение уровня HbA1c с 8,2 [7,6; 8,8]% до 7,8 [7,2; 8,1]% (р=0,001), снижение ИМТ и уменьшение окружности талии. За время наблюдения не отмечено значимых изменений содержания липопротеинов и триглицеридов, СКФ и АД.
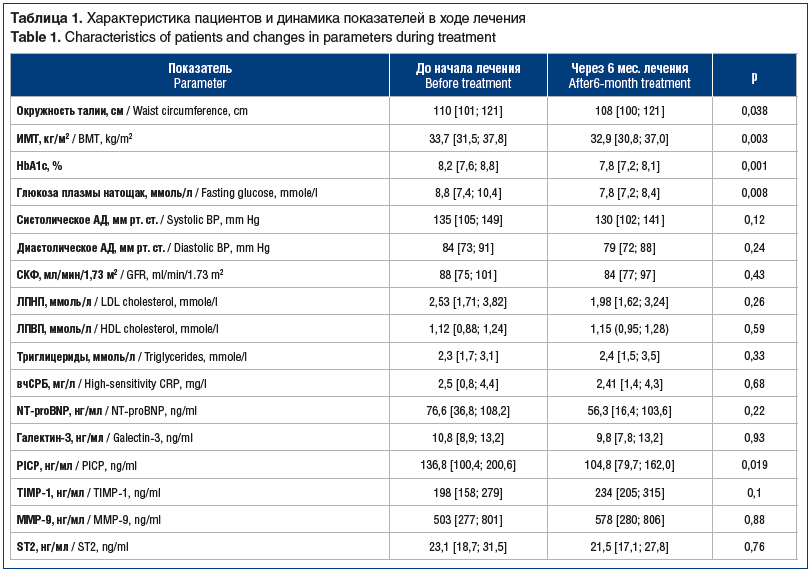
Содержание вчСРБ и NT-proBNP не отличалось от нормальных значений и не претерпело статистически значимых изменений по прошествии 6 мес. лечения дапаглифлозином. Исходно пациенты имели значимо бóльшие концентрации галектина-3, PICP и MMP-9 по сравнению с группой контроля (p=0,017, p=0,006 и p=0,008 соответственно). При оценке динамики содержания галектина-3, MMP-9, TIMP-1, ST2 не было получено значимых различий с исходными значениями (см. табл. 1). В то же время через 6 мес. лечения дапаглифлозином наблюдалось статистически значимое снижение концентрации PICP с 136,8 [100,4; 200,6] нг/мл до 104,8 [79,7; 162,0] нг/мл (р=0,019) и повышение концентрации TIMP-1 с 188 [138; 270] нг/мл
до 234 [205; 315] нг/мл (р=0,011).
Обсуждение
Преобладание синтеза коллагена I типа над его деградацией приводит к накоплению в миокарде избытка волокон коллагена и указывает на процесс фиброза, который происходит в интерстициальном и периваскулярном пространстве, в том числе при диабетической кардиомиопатии [9]. Уровни PICP, который является маркером образования и деградации коллагена I типа, надежно коррелируют с объемом образующегося коллагена как у пациентов с хронической сердечной недостаточностью (ХСН), так и без таковой [9].
В исследованиях показано, что концентрации PICP выше у пациентов с СД2, чем у пациентов без СД2 [10]. Сходные различия были продемонстрированы и в нашем исследовании. Терапия дапаглифлозином в течение 6 мес. приводила к значимому снижению уровня P1CP по сравнению с исходным. Сходная динамика была получена в исследовании другого ИНГТ2 у пациентов с СД2 и очень высоким риском сердечно-сосудистых событий [11].
В нашем исследовании не установлено значимого снижения концентраций NT-proBNP на фоне лечения дапаглифлозином в течение 6 мес., что можно объяснить включенной в исследование популяцией пациентов без ХСН и без высоких концентраций NT-proBNP. Поскольку NT-proBNP является маркером ХСН и его уровень коррелирует с ее тяжестью, даже в исследованиях пациентов с СД2 и ХСН с сохранной фракцией выброса не было выявлено значимого снижения концентрации NT-proBNP [12]. Тем не менее исследование DAPA-HF продемонстрировало, что риск ухудшения течения ХСН или смерти от сердечно-сосудистых заболеваний был ниже в группе дапаглифлозина, чем в группе плацебо [13]. Таким образом, несмотря на ограниченное влияние на уровень NT-proBNP, ИНГТ2 улучшают клинические исходы у пациентов с ХСН, что говорит о несоответствии между краткосрочными изменениями уровней NT-proBNP и клиническими исходами.
Концентрации ST2, вчСРБ, MMP-9 и ее ингибитора TIMP-1 значимо не изменились на фоне терапии дапаглифлозином, что согласуется с данными других исследований [11, 14, 15]. Вероятно, отсутствие значимой динамики показателей ряда маркеров в ходе нашего исследования связано с тем, что пациенты без ХСН и сердечно-сосудистых событий находятся на том этапе сердечно-сосудистого континуума, когда концентрации маркеров не могут в полной мере отражать тяжесть и прогноз у данных пациентов, а их изменения не могут быть зафиксированы за 6-месячный период наблюдения. Кроме того, отсутствие отрицательной динамики содержания данных биомаркеров может говорить о замедлении воспалительных и фиброзных процессов, имеющих место при СД2, и потенциально реализовываться в улучшении сердечно-сосудистых исходов. Также стоит принимать во внимание наличие ожирения и других неучтенных факторов, которые могут влиять на значения оцениваемых нами маркеров.
Заключение
Терапия дапаглифлозином в течение 6 мес. приводила к снижению уровня PICP, что наряду с другими механизмами может свидетельствовать о положительном воздействии дапаглифлозина на сердечно-сосудистые и почечные исходы у пациентов с СД2. Требуется проведение дальнейших проспективных исследований с более длительным наблюдением на больших выборках для детального изучения динамики фибротических процессов и отражающих их биомаркеров. Кроме того, представляется целесообразным проведение оценки процессов фиброза у двух различных групп пациентов с СД2 — с сердечно-сосудистыми событиями в анамнезе и с факторами риска таких событий.
Сведения об авторах:
Лебедев Денис Андреевич — младший научный сотрудник НИЛ диабетологии ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России; 197341, Россия, г. Санкт-Петербург, ул. Аккуратова, д. 2; ORCID iD 0000-0003-1808-1331.
Бабенко Алина Юрьевна — д.м.н., заведующая НИЛ диабетологии ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России; 197341, Россия, г. Санкт-Петербург, ул. Аккуратова, д. 2; ORCID iD 0000-0002-0559-697X.
Контактная информация: Бабенко Алина Юрьевна, e-mail: alina_babenko@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 18.02.2021.
Поступила после рецензирования 18.03.2021.
Принята в печать 12.04.2021.
About the authors:
Denis A. Lebedev — junior researcher of the Research Laboratory of Diabetology, V.A. Almazov National Medical Research Center; 2, Akkuratov str., St. Petersburg, 197341, Russian Federation; ORCID iD 0000-0003-1808-1331.
Alina Yu. Babenko — Dr. Sc. (Med.), Head of the Research Laboratory of Diabetology, V.A. Almazov National Medical Research Center; 2, Akkuratov str., St. Petersburg, 197341, Russian Federation; ORCID iD 0000-0002-0559-697X.
Contact information: Alina Yu. Babenko, e-mail: alina_babenko@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 18.02.2021.
Revised 18.03.2021.
Accepted 12.04.2021.
2. Neal B., Perkovic V., Mahaffey K.W. et al. Canagliflozin and cardiovascular and renal events in type 2 diabetes. N Engl J Med. 2017;377(7):644–657. DOI: 10.1056/NEJMoa1611925.
3. Wiviott S.D., Raz I., Bonaca M.P. et al. Dapagliflozin and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med. 2019;380(4):347–357. DOI: 10.1056/NEJMoa1812389.
4. Nikolic M., Zivkovic V., Jovic J.J. et al. SGLT2 inhibitors: a focus on cardiac benefits and potential mechanisms. Heart Fail Rev. 2021 Feb 3. DOI: 10.1007/s10741-021-10079-9. Online ahead of print.
5. Uthman L., Baartscheer A., Bleijlevens B. et al. Class effects of SGLT2 inhibitors in mouse cardiomyocytes and hearts: inhibition of Na+/H+ exchanger, lowering of cytosolic Na+ and vasodilation. Diabetologia. 2018;61:722–726. DOI: 10.1007/s00125-017-4509-7.
6. Lee T.M., Chang N.C., Lin S.Z. Dapagliflozin, a selective SGLT2 inhibitor, attenuated cardiac fibrosis by regulating the macrophage polarization via STAT3 signaling in infarcted rat hearts. Free Radic Biol Med. 2017;104:298–310. DOI: 10.1016/j.freeradbiomed.2017.01.035.
7. Bonnet F., Scheen A.J. Effects of SGLT2 inhibitors on systemic and tissue low-grade inflammation: The potential contribution to diabetes complications and cardiovascular disease. Diabetes Metab. 2018;44(6):457–464. DOI: 10.1016/j.diabet.2018.09.005.
8. Russo I., Frangogiannis N.G. Diabetes-associated cardiac fibrosis: cellular effectors, molecular mechanisms and therapeutic opportunities. J Mol Cell Cardiol. 2016;90:84–93. DOI: 10.1016/j.yjmcc.2015.12.011.
9. López B., González A., Ravassa S. et al. Circulating Biomarkers of Myocardial Fibrosis: The Need for a Reappraisal. J Am Coll Cardiol. 2015;65(22):2449–2456. DOI: 10.1016/j.jacc.2015.04.026.
10. Ihm S.H., Youn H.J., Shin D.I. et al. Serum carboxy-terminal propeptide of type I procollagen (PIP) is a marker of diastolic dysfunction in patients with early type 2 diabetes mellitus. Int J Cardiol. 2007;122(3):e36–e38. DOI: 10.1016/j.ijcard.2007.07.057.
11. Лебедев Д.А., Бабенко А.Ю. Маркеры фиброза у пациентов с сахарным диабетом 2 типа и очень высоким риском сердечно-сосудистых заболеваний: результаты проспективного исследования. РМЖ. 2020;1:3–6. [Lebedev D.A., Babenko A.Yu. Markers of fibrosis in patients with type 2 diabetes mellitus and cardiovascular high-risk patients: prospective study results. RMJ. 2020;1:3–6 (in Russ.)].
12. Nassif M., Windsor S., Tang F. et al. Dapagliflozin effects on biomarkers, symptoms, and functional status in patients with heart failure with reduced ejection fraction: the DEFINE‐HF trial. Circulation. 2019;140:1463–1476. DOI: 10.1161/CIRCULATIONAHA.119.042929.
13. McMurray J., Solomon S., Inzucchi S. et al. Dapagliflozin in patients with heart failure and reduced ejection fraction. N Engl J Med. 2019;381:1995–2008. DOI: 10.1056/NEJMoa1911303.
14. Garvey W., van Gaal L., Leiter L. et al. Effects of canagliflozin versus glimepiride on adipokines and inflammatory biomarkers in type 2 diabetes. Metabolism. 2018;85:32–37. DOI: 10.1016/j.metabol.2018.02.002.
15. Januzzi J.L. Jr., Butler J., Jarolim P. et al. Effects of Canagliflozin on Cardiovascular Biomarkers in Older Adults With Type 2 Diabetes. J Am Coll Cardiol. 2017;70(6):704–712. DOI: 10.1016/j.jacc.2017.06.016.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Распечатать