Некоторые особенности клинической картины ишемической болезни сердца и качества жизни пациентов при депрессивных расстройствах
DOI: 10.32364/2587-6821-2020-4-7-412-417
Цель исследования: выявить особенности клинического течения ишемической болезни сердца (ИБС) и качества жизни при наличии у больных коморбидных депрессивных расстройств (ДР).
Материал и методы: проведено открытое клиническое контролируемое исследование методом параллельного сравнения. Обследовано 93 больных с ИБС (стенокардия напряжения II–III функционального класса), у 59 из которых имелись ДР (1-я группа), а у 34 — отсутствовали (2-я группа). Оценивали наличие и уровень депрессии, тревоги, социальной адаптации с помощью шкал тревоги и депрессии (HADS), депрессии Бека (BDI), тревоги Шихана (ShARS), социальной адаптации (Bosc), толерантность к физической нагрузке (тест 6-минутной ходьбы, велоэргометрия), вариабельность ритма сердца (ВРС) при проведении холтеровского мониторинга.
Результаты исследования: у пациентов с ДР в сравнении с пациентами без ДР выявлены: повышенный уровень депрессии (по HADS — 8,8±2,4 балла против 4,8±1,9 балла, р=0,000001; по BDI — 21,2±4,4 балла против 16,0±5,1 балла, р=0,0000003) и тревоги (по HADS — 9±3,2 балла против 5,5±2,8 балла, р=0,000002; по Шихану — 37,3±19,2 балла против 22,1±2,8 балла, р=0,0006); более низкий уровень социального функционирования (по Bosc — 33,4±6,4 балла против 36,5±6,6 балла, р=0,03); большее количество ангинозных приступов (8 [6; 12] против 6 [4; 7], р=0,0005) и бóльшая потребность в нитроглицерине в течение недели (3,6±4,8 таблетки против 1,6±2,3 таблетки, р=0,0005); снижение толерантности к физической нагрузке (по велоэргометрии — 52,8±26,8 Вт против 69±30,4 Вт, р=0,03; по тесту 6-минутной ходьбы — 375,7±128,9 м против 410±100,3 м, р=0,09), снижение параметров ВРС: pNN50% (5,2±4,8 против 8,8±7,5, р=0,03), SDANN (81,3±22,4 мс против 91±16,9 мс, р=0,04), SDNNindx (46 [36; 56] мс против 55 [48; 66] мс, p=0,005), rMSSD (29 [23; 38] мс против 33 [29; 41] мс, p=0,04), SDNN (98,2±24,7 мс против 112±20 мс, р=0,01).
Заключение: для больных ИБС в сочетании с ДР характерны повышенный уровень тревоги, более низкое качество жизни, ухудшение клинического течения коронарной болезни, что требует своевременной диагностики и коррекции расстройств психики.
Ключевые слова: депрессивные расстройства, вариабельность ритма сердца, ишемическая болезнь сердца, инфаркт миокарда, качество жизни, стенокардия напряжения.
Для цитирования: Нонка Т.Г., Лебедева Е.В., Репин А.Н. Некоторые особенности клинической картины ишемической болезни сердца и качества жизни пациентов при депрессивных расстройствах. РМЖ. Медицинское обозрение. 2020;4(7):412-417. DOI: 10.32364/2587-6821-2020-4-7-412-417.
T.G. Nonka1, E.V. Lebedeva1,2, A.N. Repin1
1Research Institute of Cardiology at the Tomsk National Research Medical Center of the Russian Academy of Sciences, Tomsk, Russian Federation
2Mental Health Research Institute Clinic at the Tomsk National Research Medical Center of the Russian Academy of Sciences, Tomsk, Russian Federation
Aim: to identify the patterns of coronary heart disease (CHD) clinical course and life quality of patients with comorbid depressive disorders (DD).
Patients and Methods: an open-label clinical controlled study was conducted using a parallel comparison method. 93 patients with CHD (angina pectoris of the functional class II–III) were examined, 59 of them had DD (group 1), and 34 had no DD (group 2). The presence and level of depression, anxiety, and social adaptation were assessed using Hospital Anxiety and Depression Scale (HADS), Beck Depression Inventory (BDI), Sheehan Anxiety Rating Scale (ShARS), social adaptation (Bosc), exercise tolerance (6-minute walk test, bicycle ergometry), and heart rate variability (HRV) during Holter monitoring.
Results: patients with DD versus patients without DD showed the following indications: increased levels of depression (HADS — 8.8±2.4 points vs. 4.8±1.9 points, p=0.000001; BDI — 21.2±4.4 points vs. 16.0±5.1 points, p=0.0000003) and anxiety (HADS — 9±3.2 points vs. 5.5±2.8 points, p=0.000002; ShARS — 37.3±19.2 points vs. 22.1±2.8 points, p=0.0006); a lower level of social functioning (Bosc — 33.4±6.4 points vs. 36.5±6.6 points, p=0.03); a greater number of anginal episodes (8 [6; 12] vs. 6 [4; 7], p=0.0005) and a greater need for nitroglycerin during the week (3.6±4.8 tablets vs. 1.6±2.3 tablets, p=0.0005); reduced exercise tolerance (according to bicycle ergometry — 52.8±26.8 W vs. 69±30.4 W, p=0.03; 6-minute walk test — 375.7±128.9 m vs. 410±100.3 m, p=0.09), HRV parameters reduction: pNN50% (5.2±4.8 vs. 8.8±7.5, p=0.03), SDANN (81.3±22.4 ms vs. 91±16.9 ms, p=0.04), SDNNindx (46 [36; 56] ms vs. 55 [48; 66] ms, p=0.005), rMSSD (29 [23; 38] ms vs. 33 [29; 41] ms, p=0.04), SDNN (98.2±24.7 MS vs. 112±20 MS, p=0.01).
Conclusion: patients with CHD in combination with DD were characterized by an increased level of anxiety, a lower life quality, and a worsening of the coronary disease clinical course, which requires timely diagnosis and correction of mental disorders.
Keywords: depressive disorders, heart rate variability, coronary heart disease, myocardial infarction, life quality, angina of effort.
For citation: Nonka T.G., Lebedeva E.V., Repin A.N. Clinical picture patterns of coronary heart disease and the life quality of patients with depressive disorders. Russian Medical Inquiry. 2020;4(7):412–417. DOI: 10.32364/2587-6821-2020-4-7-412-417.
Введение
Депрессивные расстройства (ДР) все чаще встречаются как в общей популяции (страдают более 350 млн человек), так и среди больных с сердечно-сосудистыми заболеваниями, особенно с ишемической болезнью сердца (ИБС). ВОЗ прогнозирует, что к 2030 г. ИБС и ДР станут ведущими причинами инвалидности и нетрудоспособности в цивилизованных странах мира. Распространенность ДР на популяционном уровне колеблется от 2,5% до 10% [1, 2]. Депрессия является фактором риска развития коронарной болезни, негативно влияет на течение сердечно-сосудистых заболеваний, а также выступает значимым предиктором неблагоприятного прогноза у данной категории больных [3]. ДР повышают частоту появления ИБС в 1,5 раза независимо от соматических факторов риска сердечно-сосудистых заболеваний [4]. Исследование Whitehall II показало, что чем более выражены симптомы депрессии, тем выше риск развития ИБС [5]. Также существует и прямая зависимость между выраженностью депрессии и риском смерти у больных с сердечно-сосудистыми заболеваниями [6–10]. ДР ухудшает клиническую картину ИБС в виде утяжеления класса стенокардии, снижения толерантности к физической нагрузке [9, 11]. Так как ДР своевременно не диагностируются и не лечатся, пациенты чаще обращаются за амбулаторно-поликлинической помощью и госпитализируются [11]. В связи с утяжелением стенокардии, а также множеством жалоб некоронарогенного характера у пациентов снижено качество жизни. Так, у больных ИБС в послеоперационном периоде на фоне ДР отмечается дополнительное снижение функциональных возможностей [12].
Негативное влияние ДР на течение ИБС обусловлено поведенческими и физиологическими механизмами. На фоне депрессии наблюдается дисфункция в гипоталамо-гипофизарно-надпочечниковой, тиреоидной, иммунной системах организма, нарушение активности серотониновых, мелатониновых и дофаминовых рецепторов. Один из наиболее важных механизмов влияния ДР на прогноз коронарной болезни — активация симпатоадреналовой системы повышает риск развития жизнеугрожающих нарушений сердечного ритма [3, 5, 8, 13–15]. Депрессия существенно изменяет поведение пациентов с сердечно-сосудистыми заболеваниями и снижает качество жизни: больные плохо выполняют рекомендации по соблюдению диеты и режима лечения, отказу от курения, увеличению физической активности, ограничению алкоголя, неохотно придерживаются здорового образа жизни [16–19].
Очень часто ДР сопровождаются тревогой. Тревога ассоциируется с повышением риска ИБС примерно на 41%, других сердечно-сосудистых заболеваний — на 52% [20, 21], а также увеличивает риск фатальных сердечно-сосудистых событий [22] и снижает социальное функционирование больных [23].
Таким образом, не вызывает сомнений необходимость своевременной диагностики аффективных расстройств у больных ИБС. Также необходимо изучение одного из важнейших механизмов влияния ДР на ИБС — вегетативной дисфункции. Именно дисбаланс в симпатоадреналовой системе больного с коморбидной патологией может предрасполагать к развитию желудочковых аритмий и существенно повлиять на прогноз заболевания.
Цель исследования: выявить особенности клинического течения ИБС, в частности вариабельности ритма сердца (ВРС), оценить качество жизни больных на фоне ДР в отдаленном периоде после инфаркта миокарда.
Материал и методы
На базе отделения кардиологии проведено открытое клиническое контролируемое исследование методом параллельного сравнения. Обследовано 93 пациента со стенокардией напряжения II–III функционального класса, перенесших инфаркт миокарда более 6 мес. назад. Больные дали письменное согласие на проведение тестирований, консультацию психиатра, обследование.
При поступлении проводилось тестирование с использованием госпитальной шкалы тревоги и депрессии (HADS), шкалы самооценки депрессии Бека (BDI), шкалы тревоги Шихана. Качество жизни оценивали по шкале социальной адаптации (Bosc). При отклонении результатов тестирования от нормальных значений и при выявлении тревоги, снижения настроения, нарушения сна пациентов консультировал психиатр на базе кардиологического отделения. Психиатр определял ДР, их тяжесть, необходимость коррекции. В исследование были включены больные с депрессией средней степени тяжести. Пациентов распределили по группам: в 1-ю группу вошли 59 больных ИБС с ДР, во 2-ю группу — 34 больных ИБС без ДР.
Особенности клинической картины ИБС оценивали по жалобам (частота приступов стенокардии в неделю, частота купирования ангинозных приступов нитроглицерином под язык в неделю), толерантности к физической нагрузке (проведение велоэргометрии, теста 6-минутной ходьбы). Кроме того, с помощью суточного мониторинга электрокардиограммы по Холтеру определяли показатели ВРС: процент последовательных интервалов, различающихся более чем на 50 мс, — pNN50; стандартное отклонение интервала RR — SDNN; корень квадратный из средней суммы квадратов разниц между соседними нормальными RR-интервалами — r-MSSD; стандартное отклонение средних значений RR-интервалов за все 5-минутные фрагменты — SDANN; среднее значение стандартных отклонений по всем 5-минутным участкам — SDNNindex. ВРС определяли только на синусовом ритме.
В 1-й группе было 56 (95%) мужчин и 3 (5%) женщины, их средний возраст составил 57,6±6,7 года; во 2-й группе — соответственно 31 (91%) мужчина и 3 (9%) женщины, 57,5±7,4 года (р>0,5). По клинико-анамнестическим данным группы статистически значимо не различались (р>0,05; табл. 1).
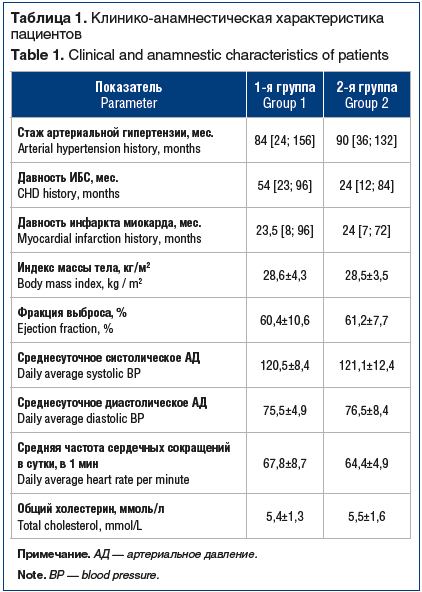
По распределению пациентов в соответствии с функциональным классом стенокардии группы пациентов с ДР и без ДР не различались: с классом II — 46 (78%) и 27 (79%) человек (p=0,9), с классом III — 13 (22%) и 7 (21%) соответственно (p=0,9). Пациенты получали стандартную терапию по поводу ИБС и артериальной гипертензии, в результате чего достигнуты целевые значения артериального давления и пульса.
Статистическую обработку данных проводили с помощью программы Statistica for Windows v. 10.0. Данные представлены в виде M±SD, n (%), Me [25%; 75%]. Нормальность распределения фактических данных проверяли с использованием критерия Шапиро — Уилка, статистическую значимость различий — с помощью критерия Манна — Уитни и t-критерия. Для сравнения двух зависимых выборок по какому-либо признаку использовали t-критерий Стьюдента (при нормальном распределении выборки) и критерий Вилкоксона (при ненормальном распределении выборки). Анализ таблиц сопряженности и критерий χ2 Пирсона применяли для проверки достоверности различий качественных переменных. Взаимосвязи между переменными выявляли с помощью коэффициентов корреляции: при соответствии нормальному закону распределения — R Пирсона, при несоответствии нормальному закону распределения или балльных оценках — R Спирмена; значению 0,5>R>0 соответствовала слабая взаимосвязь, 0,75>R≥0,5 — средняя взаимосвязь, R≥0,75 — сильная взаимосвязь. Статистически значимым считали результат при p<0,05.
Результаты исследования
Результаты тестирования психометрическими шкалами представлены в таблице 2.
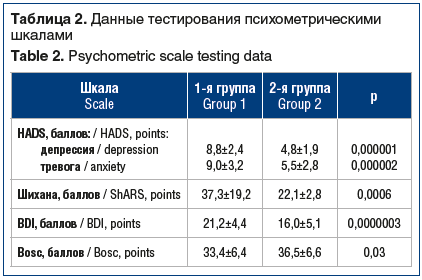
При обработке тестов у больных с верифицированным диагнозом ДР наблюдался более высокий уровень депрессии. Кроме того, в группе пациентов с ДР отмечен повышенный уровень тревоги как по HADS, так и по шкале Шихана, что еще в большей мере ухудшает течение ИБС. По данным Bosc, у пациентов с ДР обнаружен более низкий уровень социального функционирования (преимущественно в семейном и профессиональном аспектах), что расценивается как затрудненная социальная адаптация.
Группы больных были сопоставимы по функциональному классу стенокардии напряжения, однако у пациентов 1-й группы по сравнению с пациентами 2-й группы значительно чаще развивались ангинозные приступы в течение недели (8 [6; 12] против 6 [4; 7], р=0,0005) и была повышена потребность в нитроглицерине (3,6±4,8 таблетки против 1,6±2,3 таблетки в неделю, р=0,0005). Также у пациентов с ДР выявлено значимое снижение толерантности к физической нагрузке по данным велоэргометрии (52,8±26,8 Вт против 69±30,4 Вт, р=0,03) и тенденция к снижению показателей теста 6-минутной ходьбы (375,7±128,9 м против 410±100,3 м, р=0,09).
Для пациентов с коронарной болезнью в сочетании с ДР характерным оказалось достоверное снижение всех параметров ВРС (табл. 3).
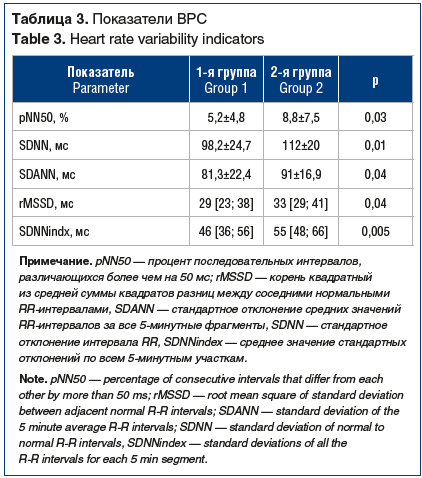
Мы провели корреляционный анализ исследованных нами параметров. Установлена достоверная сильная отрицательная связь между социальной адаптацией и уровнем общего холестерина (R=-0,96), частотой ангинозных приступов в неделю (R=-0,9), потребностью в нитроглицерине в неделю (R=-0,96), между уровнем депрессии (HADS) и SDNNindx (R=-0,9), rMSSD (R=-0,98); уровнем тревоги (HADS) и SDANN (R=-0,88), SDNN (R=-0,92), SDNNindx (R=-0,88). Таким образом, выявлена закономерность: чем ниже адаптационные возможности пациента, тем выше уровень холестерина, чаще возникают приступы стенокардии и наблюдается бóльшая потребность в нитроглицерине. Чем выше уровень депрессии и тревоги, тем ниже параметры ВРС, а соответственно, ухудшается течение коронарной болезни.
Обсуждение
Результаты крупных исследований MONICA, INTERHEART, ENRICHD, SADHART показали значимость депрессии в качестве предиктора сердечно-сосудистых катастроф [24–27]. Большинство крупных исследований включали больных с острым инфарктом миокарда. Мы оценили особенности клинической картины ИБС у стабильных больных в отдаленном периоде после инфаркта миокарда (давностью более 6 мес.) на фоне ДР. По анамнезу сердечно-сосудистых заболеваний и сопутствующей терапии группы были сопоставимы. Выявление ДР и степени их тяжести в значительной степени облегчается при использовании психометрических шкал и тестов. Во многих работах для скрининга депрессивных расстройств применяются стандартизированные опросники, наиболее популярные из них: PHQ-9, BDI, HADS [28]. Мы в своей работе использовали наиболее известные и распространенные шкалы BDI, HADS, Шихана, для оценки качества жизни — Bosc. Их применение позволяет минимизировать затраты времени врача на обследование, при этом интерпретация результатов обследования не требует специальных знаний. По результатам тестирования и, в дальнейшем, консультации психиатра верифицирован диагноз: ДР средней степени тяжести. Повышенный уровень тревоги, подтвержденный как по HADS, так и по шкале Шихана, у пациентов с ДР приводит к снижению социального функционирования, что подтверждено тестированием по Bosc. Таким образом, у больных ИБС в сочетании с ДР отмечается снижение качества жизни, в первую очередь в профессиональной и семейной сферах.
Исходно пациенты не отличались по функциональному классу стенокардии напряжения. Однако больные с ДР значительно чаще жаловались на боли в области сердца и чаще купировали их нитроглицерином. Возможно, пациенты с ДР еще и преувеличивали тяжесть и серьезность симптомов основного заболевания. Конечно же, частые жалобы ухудшают и качество жизни больных, что приводит к изменению образа жизни, иногда и к потере социального статуса. По данным корреляционного анализа отмечена закономерность: чем ниже адаптационные возможности пациента, тем выше уровень холестерина (вероятно, пациент хуже выполняет рекомендации по диете), чаще возникают ангинозные боли и, соответственно, используется нитроглицерин. В результате учащаются повторные обращения в поликлинику и стационар, что повышает затраты на лечение таких пациентов. Это говорит о необходимости адекватной социальной поддержки больных с коморбидной патологией (ИБС и ДР) для ускорения стабилизации состояния и повышения качества жизни. Ухудшение клинической картины ИБС на фоне ДР также подтверждено снижением толерантности к физической нагрузке по данным велоэргометрии. Кроме того, пациенты проходили значительно меньшее расстояние при выполнении теста 6-минутной ходьбы. Таким образом, мы подтвердили результаты ранее проведенных исследований о негативном влиянии ДР на течение ИБС [3, 6, 7, 11, 17, 18].
Аффективные расстройства сопровождаются изменением нервных и гормональных реакций, приводящих к нарушению функционирования вегетативной нервной системы. Гиперсимпатикотония способствует возникновению нарушений ритма сердца, что в значительной степени ухудшает прогноз больных ИБС [3, 6, 8, 13–15]. Так, в исследовании ENRICHD у 311 пациентов, перенесших острый инфаркт миокарда и страдающих ДР, отмечалось значительное снижение ВРС [24]. Очень важно изучение такого патофизиологического механизма, как вегетативная дисфункция у больных ИБС в сочетании с ДР, в отдаленном периоде после инфаркта миокарда. Мы оценили наличие вегетативной дисфункции, используя временной метод анализа ВРС по данным холтеровского мониторинга. Нами было обнаружено, что у больных коронарной болезнью на фоне ДР значительно снижены все параметры ВРС (pNN50%, SDNN, SDANN, rMSSD, SDNNindx), что является прогностически неблагоприятным фактором, определяющим риск внезапной коронарной смерти и прогрессирование ИБС (вследствие возникновения желудочковых аритмий). Кроме того, корреляционный анализ показал, что чем выше уровень депрессии и тревоги, тем ниже показатели ВРС.
Заключение
У больных ИБС в сочетании с ДР отмечается значительное ухудшение клинического течения ИБС в виде частых приступов стенокардии, повышенной потребности в приеме нитроглицерина, снижения толерантности к физической нагрузке (при проведении нагрузочных проб) и ВРС, что значительно ухудшает качество жизни данной категории больных. Сниженная ВРС говорит о вегетативной дисфункции и может ухудшить прогноз сердечно-сосудистой патологии ввиду высокого риска развития тяжелых нарушений ритма сердца.
Полученные данные определяют необходимость своевременного распознавания ДР с использованием современных психометрических шкал. Также целесообразно всем больным ИБС в сочетании с ДР проводить анализ ВРС по данным холтеровского мониторинга для оценки прогноза заболевания. Выявление ДР в отдаленном периоде после инфаркта миокарда требует раннего назначения антидепрессантов и пристального наблюдения таких пациентов совместно кардиологом и психиатром.
Сведения об авторах:
Нонка Татьяна Геннадьевна — к.м.н., научный сотрудник отделения общеклинической кардиологии и эпидемиологии сердечно-сосудистых заболеваний НИИ кардиологии, Томский НИМЦ; 634012, Россия, г. Томск, ул. Киевская, д. 111а; ORCID iD 0000-0002-7913-3732.
Репин Алексей Николаевич — д.м.н., профессор, руководитель отделения общеклинической кардиологии и эпидемиологии сердечно-сосудистых заболеваний НИИ кардиологии, Томский НИМЦ; 634012, Россия, г. Томск, ул. Киевская, д. 111а; ORCID iD 0000-0001-7123-0645.
Лебедева Елена Владимировна — к.м.н., научный сотрудник отделения общеклинической кардиологии и эпидемиологии сердечно-сосудистых заболеваний НИИ кардиологии, Томский НИМЦ; 634012, Россия, г. Томск, ул. Киевская, д. 111а; старший научный сотрудник отделения аффективных состояний НИИ психического здоровья, Томский НИМЦ; 634014, Россия, г. Томск, ул. Алеутская, д. 4; ORCID iD 0000-0001-6117-6454.
Контактная информация: Нонка Татьяна Геннадьевна, e-mail: ntg@sibmail.com. Прозрачность финансовой деятельности: исследование выполнено в рамках государственного задания (бюджетное финансирование в рамках комплексной темы НИР АААА-А15-115123110026-3-0 «Фундаментальные аспекты возникновения и развития социально значимых сердечно-сосудистых заболеваний; выявление мишеней для диагностики, лечения и улучшения прогноза; механизмы защиты»). Конфликт интересов отсутствует. Статья поступила 11.09.2020, поступила после рецензирования 25.09.2020, принята в печать 09.10.2020.
About the authors:
Tatyana G. Nonka — Cand. of Sci. (Med.), Research Officer of the Department of General Clinical Cardiology and Epidemiology of Cardiovascular Diseases, Research Institute of Cardiology at the Tomsk National Research Medical Center of the Russian Academy of Sciences: 111A, Kievskaya str., Tomsk, 634012, Russian Federation; ORCID iD 0000-0002-7913-3732.
Alexey N. Repin — Dr. of Sci. (Med.), Professor, Head of the Department of General General Clinical Cardiology and Epidemiology of Cardiovascular Diseases, Research Institute of Cardiology at the Tomsk National Research Medical Center of the Russian Academy of Sciences: 111A, Kievskaya str., Tomsk, 634012, Russian Federation; ORCID iD 0000-0001-7123-0645.
Elena V. Lebedeva — Cand. of Sci. (Med.), Research Officer at the Department of General General Clinical Cardiology and Epidemiology of Cardiovascular Diseases, Research Institute of Cardiology at the Tomsk National Research Medical Center of the Russian Academy of Sciences: 111A, Kievskaya str., Tomsk, 634012, Russian Federation; Senior Researcher at the Department of Affective Disorders, Mental Health Research Institute Clinic at the Tomsk National Research Medical Center of the Russian Academy of Sciences: 4, Aleutskaya str., Tomsk, 634014, Russian Federation; ORCID iD 0000-0001-6117-6454.
Contact information: Tatyana G. Nonka, e-mail: ntg@sibmail.com. Financial disclosure: the study was carried out within the framework of the state assignment (budgetary funding within the framework of the complex R&D project No. AAAA-A15-115123110026-3-0 “Fundamental aspects of the emergence and development of socially significant cardiovascular diseases; identification of targets for diagnosis, treatment and improvement of prognosis; defense mechanisms”). There is no conflict of interests. Received 11.09.2020, revised 25.09.2020, accepted 09.10.2020.
2. Patel H., Mazur W., Williams K.A., Kalra D.K. Myocardial viability-State of the art: Is it still relevant and how to best assess it with imaging? Trends Cardiovasc Med. 2018;28(1):24–37. DOI: 10.1016/j. tcm.2017.07.001.
3. Погосова Г.В. Депрессия — фактор развития ишемической болезни сердца и предиктор коронарной смерти: 10 лет научного поиска. Кардиология. 2012;52(12):4–11.
4. Gan Y., Gong Y., Tong X. et al. Depression and the risk of coronary heart disease: a meta-analysis of prospective cohort studies. BMC Psychiatry. 2014;14:371. DOI: 10.1186/s12888-014-0371-z.
5. Brunner E.J, Shipley M.J., Britton A.R. et al. Depressive disorder, coronary heart disease, and stroke: dose-response and reverse causation effects in the Whitehall II cohort study. Eur J Prev Cardiol. 2014;21(3):340–346. DOI: 10.1177/2047487314520785.
6. Лебедева Е.В., Нонка Т.Г., Репин А.Н. и др. Современная психокардиология. Томск: Интегральный переплет; 2019.
7. Пушкарев Г.С., Кузнецов В.А., Фишер Я.А. и др. Влияние депрессивной симптоматики на риск смерти от всех причин у пациентов с хронической сердечной недостаточностью, перенесших сердечную ресинхронизирующую терапию. Кардиология. 2019;59(1):5–11. DOI: 10.18087/cardio.2019.1.10211.
8. Смулевич А.Б. Депрессии при психических и соматических заболеваниях. 4-е изд. М.: Медицинское информационное агентство; 2015.
9. Leung Y.W., Flora D.B., Gravely S. et al. The impact of premorbid and postmorbid depression onset on mortality and cardiac morbidity among patients with coronary heart disease: meta-analysis. Psychosom Med. 2012;74(8):786–801. DOI: 10.1097/PSY.0b013e31826ddbed.
10. Shah A.J., Veledar E., Hong Y. et al. Depression and history of attempted suicide as risk factors for heart disease mortality in young individuals. Arch Gen Psychiatry. 2011;68(11):1135–1142. DOI: 10.1001/archgenpsychiatry.2011.125.
11. Лебедева Е.В., Счастный Е.Д., Симуткин Г.Г. и др. Клиническая характеристика аффективных расстройств и эффективность антидепрессивной терапии у больных хронической ишемической болезнью сердца. Бюллетень сибирской медицины. 2018;17(4):85–93. DOI: 10.20538/1682-0363-2018-4-85-93.
12. Morone N.E., Weiner D.K., Herbeck Belnap B. et al. The impact of pain and depression on recovery after coronary artery bypass grafting. Psychosom Med. 2010;72(7):620–625. DOI: 10.1097/PSY.0b013e3181e6df90.
13. Стаценко М.Е., Тыщенко И.А. Патогенез и возможности терапии коморбидной депрессии у пациентов с ишемической болезнью сердца: взгляд кардиолога. Лекарственный вестник. 2018;12(1):28–34.
14. Дробижев М.Ю., Овчинников А.А., Кикта С.В. Механизмы действия антидепрессантов и патогенез психических расстройств. В чем соответствия? Социальная и клиническая психиатрия. 2017;27(3): 94–101.
15. Дробижев М.Ю., Сердюк О.В., Овчинников А.А. и др. Патогенетический и фармакологический подход при выборе антидепрессантов. Социальная и клиническая психиатрия. 2014;24(2):86–91.
16. Глущенко В.А., Ирклиенко Е.К. Депрессия у кардиологических пациентов (обзор литературы). Медицина: теория и практика. 2017;1(2):23–27.
17. Гарганеева Н.П., Петрова М.М., Евсюков А.А. и др. Влияние депрессии на течение ишемической болезни сердца и качество жизни пациентов. Клиническая медицина. 2014;12:30–37.
18. Чапала Т.В. Исследование депрессии у пациентов с ишемической болезнью сердца. Научно-методический электронный журнал «Концепт». 2015;28:31–35. (Электронный ресурс). URL: http://e-koncept.ru/2015/75375.htm. (дата обращения: 15.08.2020).
19. Крючкова О.Н., Костюкова Е.А., Ицкова Е.А. и др. Оценка вероятности коморбидной патологии: сердечно-сосудистые заболевания и депрессия. Ульяновский медико-биологический журнал. 2016;2:20–26.
20. Emdin C.A., Odutayo A., Wong C.X. et al. Meta-analysis of anxiety as a risk factor for cardiovascular disease. Am J Card. 2016;118(4):511–519. DOI: 10.1016/j.amjcard.2016.05.041.
21. Batelaan N.M., Seldenrijk A., Bot M. et al. Anxiety and new onset of cardiovascular disease: critical review and meta-analysis. Br J Psych. 2016;208(3):223–231. DOI: 10.1192/bjp.bp.114.156554.
22. Wang G., Cui J., Wang Y. et al. Anxiety and adverse coronary artery disease outcomes in chinese patients. Psychosom Med. 2013;75(6):530–536. DOI: 10.1097/PSY.0b013e3182984317.
23. Белан И.А., Ложникова Л.Е., Барбухатти К.О. Влияние уровня тревожности на течение ишемической болезни сердца после аортокоронарного шунтирования. Cardioсоматика. 2015;1:9–10.
24. Taylor C.B., Youngblood M.E., Catellier D. et al. Effects of antidepressant medication on morbidity and mortality in depressed patients after myocardial infarction. ENRICHD trial Arch. Gen. Psychiatry. 2005;62(7):792–798. DOI: 10.1001/archpsyc.62.7.792.
25. Yusuf S., Hawken S., Ounpuu S. et al. INTERHEART Study Investigators. Obesity and the risk of myocardial infarction in 27000 participants from 52 countries: a case-control study. Lancet. 2005;366(9497):1640–1649. DOI: 10.1016/S0140-6736 (05) 67663-5.
26. Serebruany V.L., Glassman A.H., Malinin A.I. et al. Sertraline Anti Depressant Heart Attack Randomized Trial Study Group. Platelet/endothelial biomarkers in depressed patients treated with the selective serotonin reuptake inhibitor sertraline after acute coronary events: the Sertraline AntiDepressant Heart Attack Randomized Trial (SADHART) Platelet Substudy. Circulation. 2003;108(8):939–944. DOI: 10.1161/01.CIR.0000085163.21752.0A.
27. Гафаров В.В., Громова Е.А., Гагулин И.В. Восьмилетнее изучение влияния депрессии на риск возникновения инфаркта миокарда в популяции мужчин 25–64 лет (эпидемиологическое исследование на основе программы ВОЗ MONICA). Терапевтический архив. 2005;9:60–64.
28. Белялов Ф.И. Депрессия, тревога и стресс у пациентов с ишемической болезнью сердца. Терапевтический архив. 2017;8:104–109. DOI: 10.17116/terarkh2017898104-109.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
