Метаболическая нейропротекция у пациента с хронической сердечной недостаточностью: клинический разбор и результаты исследований
DOI: 10.32364/2587-6821-2023-7-1-49-55
Сердечно-сосудистые заболевания являются ведущей причиной смертности населения. Относительное бремя острых форм ишемической болезни сердца (ИБС) в развитых странах постепенно снижается, а распространенность и число госпитализаций по поводу хронической сердечной недостаточности (ХСН) за последние несколько десятилетий, напротив, имеют тенденцию к росту. В ретроспективном анализе данных пациентов с декомпенсацией ХСН кардиогенная энцефалопатия (КЭ) была выявлена в 43,4% случаев. В группе пациентов с КЭ отмечена более высокая частота и длительность повторных госпитализаций. Также у пациентов с КЭ показатель смертности в течение 2 лет с момента индексной госпитализации был выше в 2 раза по сравнению с пациентами без КЭ. Для интенсификации основных терапевтических опций в лечении больных ХСН с КЭ возможно рассмотреть добавление ряда препаратов с дополнительными фармакологическими эффектами, которые могут потенцировать действие кардиотропной терапии. Среди метаболически активных препаратов следует выделить миокардиальные цитопротекторы. Результаты нескольких исследований продемонстрировали убедительные данные по применению цитопротекторов в рутинной кардиологической практике. В настоящей работе представлен клинический опыт применения этилметилгидроксипиридина сукцината у пожилого пациента с КЭ, а также данные об эффективности этого лекарственного средства в составе симптоматической и патогенетической терапии пациентов с хронической ишемией головного мозга на фоне ИБС и ХСН.
Ключевые слова: сердечно-сосудистые заболевания, ишемическая болезнь сердца, хроническая сердечная недостаточность, кардиогенная энцефалопатия, цитопротекция, этилметилгидроксипиридина сукцинат, кардиотропная терапия.
Для цитирования: Резник Е.В., Алиева А.М., Ушакова Н.А., Крупнова Е.С. Метаболическая нейропротекция у пациента с хронической сердечной недостаточностью: клинический разбор и результаты исследований. РМЖ. Медицинское обозрение. 2023;7(1):49-55. DOI: 10.32364/2587-6821-2023-7-1-49-55.
E.V. Reznik1,2, A.M. Alieva1, N.A. Ushakova1, E.S. Krupnova1
1Pirogov Russian National Research Medical University, Moscow, Russian Federation
2City Clinical Hospital No. 31, Moscow, Russian Federation
Cardiovascular diseases (CVD) are the leading cause of global mortality. The relative burden of acute forms of coronary heart disease (CHD) is gradually decreasing in the industrially developed countries, while the prevalence of chronic heart failure (CHF) and the number of hospitalizations of patients with CHF, on the contrary, has demonstrated an upward trend over the last decades. This retrospective analysis was performed to evaluate the data of patients with CHF decompensation. In such patients, cardiogenic encephalopathy (CE) was found in 43.4% of cases. A higher frequency and longer duration of hospitalizations was observed in the group of patients with CE. Also, in patients with CE the mortality rate within two years from the date of index hospitalization was twice as high as in patients without CE. For intensifying the major therapeutic options in the treatment of CHF patients with CE, it is feasible to consider the addition of numerous medications with supplementary pharmacological effects which may potentiate the efficacy of cardiotropic therapy. Among metabolically active drugs, an emphasis should be made on myocardial cytoprotectors. The results of several studies have provided persuasive data supporting the use of cytoprotectors in routine cardiological practice. This article describes a clinical case of using ethylmethylhydroxypyridine succinate for the treatment of an elderly patient with cardiogenic encephalopathy (CE) and presents the data proving the efficacy of this drug as a part of the combined symptomatic and pathogenetic therapy administered to patients with chronic cerebral ischemia amid CHD and CHF.
Keywords: cardiovascular diseases, ischemic heart disease, chronic heart failure, cardiogenic encephalopathy, cytoprotection, ethylmethylhydroxypyridine succinate, cardiotropic therapy.
For citation: Reznik E.V., Alieva A.M., Ushakova N.A., Krupnova E.S. Metabolic neuroprotection in patient with chronic heart failure: a case report and study results. Russian Medical Inquiry. 2023;7(1):49–55 (in Russ.). DOI: 10.32364/2587-6821-2023-7-1-49-55.
Введение
Сердечно-сосудистые заболевания (ССЗ) остаются ведущей причиной смертности населения как в Российской Федерации (РФ), так и в других странах. Согласно отчету Всемирной организации здравоохранения (ВОЗ) за 2019 г. 17,9 млн человек умерли вследствие ССЗ, что составило 32% от всех смертей в мире. До 85% летальных исходов у больных ССЗ были связаны с инфарктом миокарда (ИМ) и инсультом [1, 2]. По данным Росстата за 2020 г., в РФ диагностировано свыше 4 млн новых случаев ССЗ, из которых 945 тыс. представлено ишемической болезнью сердца (ИБС) [3]. В период с 2015 по 2019 г. отмечали ежегодное снижение смертности от болезней системы кровообращения, однако в 2020 г. этот показатель вырос на 12% и превысил ранее зарегистрированный максимум смертности от ССЗ за 2015 г. [3]. Характерно, что благодаря достигнутым успехам в терапии ССЗ, в частности артериальной гипертензии (АГ) и атеросклероза, в значительной степени изменилась эпидемиологическая структура ССЗ. В то время как относительное бремя ИБС в развитых странах постепенно снижается, распространенность и число госпитализаций по поводу ХСН за последние несколько десятилетий, напротив, имеют тенденцию к росту [4, 5].
Увеличение показателей средней продолжительности жизни населения также влияет на эпидемиологию ССЗ. По данным популяционных исследований, пациенты старше 65 лет имеют самый высокий риск развития ХСН, причем для этой возрастной группы больных показано существенное снижение смертности от ИБС за последние 10 лет [5, 6]. Рост распространенности ХСН неизбежно коррелирует с ростом числа сердечно-сосудистых осложнений, в частности когнитивных нарушений вследствие хронической ишемии головного мозга (ХИГМ) на фоне ХСН. У 43,4% пациентов, госпитализированных по поводу декомпенсации ХСН, развивается кардиогенная энцефалопатия (КЭ), которая приводит к увеличению продолжительности и частоты последующих госпитализаций [7]. Женский пол, коморбидная патология, пожилой возраст ассоциированы с развитием КЭ и увеличением риска неблагоприятного исхода у пациентов с ХСН [7, 8]. По прогнозу ВОЗ, к 2030 г. число лиц в возрасте 65 лет и старше увеличится еще на 44%, что обусловливает необходимость внедрения инновационных и эффективных подходов к профилактике и лечению ССЗ уже сейчас, принимая во внимание значительный рост показателей заболеваемости ХСН и частоты развития ее осложнений [9, 10].
Кардиогенная энцефалопатия при ХСН
По сравнению со здоровыми людьми у пациентов с ХСН чаще выявляется когнитивный дефицит, затрагивающий эмоциональную и интеллектуальную сферы, а также вербальную память. В связи с этим ХИГМ остается значительной проблемой для пациентов с ХСН, при этом истинную распространенность КЭ крайне сложно оценить ввиду отсутствия четких критериев диагностики. Несмотря на значительное количество исследований, описывающих частоту встречаемости КЭ, отмечается значительная неоднородность исследуемых популяций больных [11, 12]. Также отсутствует стандартизация используемых инструментов для оценки когнитивных функций. Наиболее распространенными являются общепризнанные скрининговые тесты: Mini Mental State Examination (MMSE) и Montreal Cognitive Assessment (MoCA). С учетом ограничений для объективной постановки диагноза распространенность КЭ при ХСН довольно высока. Необходимо учитывать возможность присутствия сразу нескольких причин когнитивных нарушений у пациентов старшей возрастной группы с фоновыми заболеваниями, каждое из которых может вносить вклад в развитие ХИГМ.
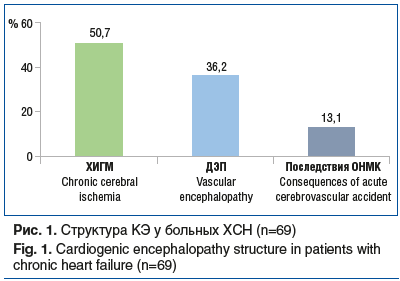
В ретроспективном исследовании была оценена частота встречаемости КЭ у 159 пациентов, госпитализированных в скоропомощной стационар по поводу декомпенсации ХСН [7]. Наличие КЭ констатировалось при указании в клиническом диагнозе / заключении невролога: «ХИГМ», «дисциркуляторная энцефалопатия» (ДЭП), наличии последствий острого нарушения мозгового кровообращения (ОНМК) (рис. 1). При этом были исключены пациенты с сахарным диабетом, онкологическим заболеванием, гемодинамически значимыми пороками сердца, с энцефалопатией несосудистого генеза.
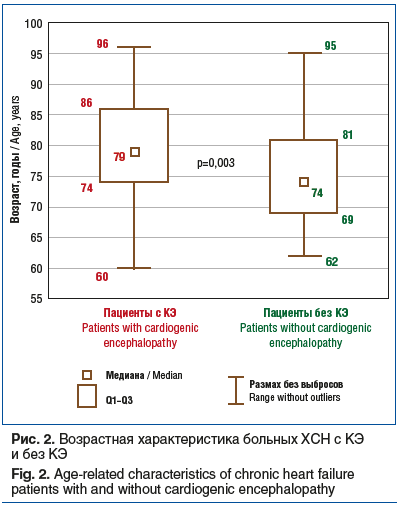
Кардиогенная энцефалопатия была диагностирована у 43,4% (n=69) больных ХСН и чаще встречалась у женщин (60,9%) и более пожилых пациентов — средний возраст пациентов с КЭ составил 77,8 (здесь и далее в скобках представлен интерквартильный размах 73–85) года против 71,9 (64–80) года у пациентов без КЭ, р=0,003 (рис. 2).
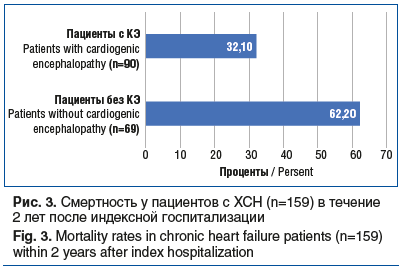
У пациентов с КЭ были выше индекс коморбидности Чарлсон, тяжесть хронической болезни почек, продолжительность индексной госпитализации, частота повторных госпитализаций и смертность в течение 2 лет, чем у пациентов без КЭ (рис. 3) [7].
Все пациенты получали стандартную терапию в соответствии с действовавшими на момент госпитализации национальными клиническими рекомендациями. Специальной нейропротективной терапии независимо от наличия КЭ не проводилось.
Негативное влияние на качество жизни пациентов с ХСН и повышение риска смерти от ССЗ подчеркивают необходимость своевременной диагностики и лечения КЭ. Скрининг КЭ не всегда проводится в рамках реальной клинической практики, а особенности когнитивной дисфункции у пациентов с КЭ остаются малоизученными. Вместе с тем уже доступные терапевтические опции, включая метаболические препараты, показали свою эффективность в лечении пациентов с ИБС и ХСН.
Перспективы метаболической терапии и церебропротекции в лечении ХСН
Принцип действия большинства сердечно-сосудистых препаратов направлен на патофизиологические механизмы, лежащие в основе сердечно-сосудистого континуума. При СН лекарственная терапия направлена на прерывание порочных кругов нейрогормональной активации. Кроме основных терапевтических опций, ряд препаратов, используемых в повседневной кардиологической практике, обладает дополнительными фармакологическими эффектами [13].
Помимо первичных кардиометаболических заболеваний, большинство ССЗ в значительной степени влияют на энергетический баланс миокарда и его адаптацию к ишемии [13]. В этом контексте препараты, влияющие на глобальный и сердечно-сосудистый метаболизм, представляют особый интерес с точки зрения потенцирования эффекта комбинированной кардиотропной терапии. Среди метаболически активных препаратов следует выделить класс миокардиальных цитопротекторов [14].
От классических антиангинальных препаратов группу цитопротекторов отличает механизм, направленный не на непосредственное улучшение коронарного кровообращения, а на устойчивое сохранение функции миокарда при воздействии ишемии. Цитопротекторы улучшают энергетический метаболизм клетки и уменьшают содержание в ней свободных радикалов. В основе оптимизации энергетического метаболизма клетки лежит способность кардиоцитопротекторов стимулировать окисление глюкозы как наиболее выгодный, с точки зрения экономии кислорода, путь генерации энергии в миокарде [15].
С точки зрения терапевтического потенциала, в современной клинической практике перспективны производные 3-оксипиридина, в частности 2-этил-6-метил-3-гидроксипиридина сукцинат, которые помимо антигипоксического эффекта обладают умеренным антиоксидантным действием. В настоящее время из группы метаболических препаратов в плане клинического применения при ССЗ наиболее изучены отечественные кардиоцитопротекторы — препараты линейки Мексикор® (действующее вещество — этилметилгидроксипиридина сукцинат, лекарственные формы — раствор для внутривенного и внутримышечного введения, капсулы)1, которые влияют непосредственно на митохондриальные процессы клеточного метаболизма, активируют сукцинат-зависимый путь окисления глюкозы, что приводит к значительно меньшему использованию кислорода при получении аналогичного количества энергии, выраженного в молекулах аденозинтрифосфата. В доклинических исследованиях in vitro применение этилметилгидроксипиридина сукцината усиливало эндогенный митохондриальный метаболизм практически в 3 раза [16].
Особенность молекулы этилметилгидроксипиридина сукцината заключается в соединении 3-оксипиридина с янтарной кислотой, что позволяет повысить проницаемость сукцината через мембрану клетки и, как следствие, мембрану митохондрии [17]. При этом благодаря антиоксидантным свойствам этилметилгидроксипиридина сукцината снижается образование липопероксидов, что препятствует развитию эндотелиальной дисфункции и способствует улучшению коронарного кровотока. Таким образом, достигается положительный эффект в отношении увеличения энергообмена и снижения оксидативного стресса — одного из ключевых звеньев патогенеза ССЗ [14–16].
Синергия этилметилгидроксипиридина сукцината при применении со стандартной кардиотропной терапией у пациентов с различными ССЗ была доказана в ряде отечественных когортных исследований. Положительный эффект был отмечен как при стабильных формах ИБС, так и при остром коронарном синдроме. Как и все производные 3-оксипиридина, этилметилгидроксипиридина сукцинат водорастворим, что позволяет использовать его в пероральной и инъекционной формах, в том числе и в неотложных ситуациях [18, 19].
Нейропротективный эффект этилметилгидроксипиридина сукцината был изучен при комплексной терапии ишемического инсульта и при хронических нарушениях мозгового кровообращения. В исследовании А.А. Фирсова и соавт. [20] у пациентов с ДЭП 2-й степени с атеросклеротическим поражением сосудов головного мозга или необратимым изменением их архитектоники различного генеза оценивали клинический эффект этилметилгидроксипиридина сукцината по соответствующим неврологическим шкалам и индексам. На фоне парентерального применения этилметилгидроксипиридина сукцината был достигнут достоверный регресс стато-локомоторных расстройств и улучшение координации движений, гностико-мнестических функций и памяти на текущие события, уменьшение выраженности экстрапирамидных расстройств [20].
В рандомизированном когортном исследовании А.П. Бабкина и соавт. [21] изучали динамику показателей суточного мониторирования артериального давления (АД) и когнитивных нарушений у 108 пациентов с АГ 1–2-й степени на фоне антигипертензивной терапии в сочетании с этилметилгидроксипиридина сукцинатом. Добавление этого лекарственного средства к стандартной терапии приводило к достоверному улучшению суточного профиля АД и когнитивных функций у больных АГ старше 60 лет. Эффект в отношении КЭ был клинически значимым уже спустя 2 мес. после начала комбинированной антигипертензивной терапии.
Церебропротекция у пациентов с ХСН
С учетом системного характера цитопротективных свойств этилметилгидроксипиридина сукцината одним из показаний для его назначения является энцефалопатия, в том числе кардиогенного генеза. В нижеприведенном клиническом наблюдении мы описываем историю «хрупкого» коморбидного пациента пожилого возраста с КЭ вследствие ХСН с положительным эффектом после 8 нед. комбинированный терапии с включением этого лекарственного средства.
Клиническое наблюдение
Пациент М., 84 года, амбулаторно консультирован кардиологом в связи с жалобами на одышку при подъеме выше 1-го этажа, периодически беспокоящие сжимающие боли в левой половине грудной клетки продолжительностью до 5 мин при физической нагрузке, проходящие в покое, головокружения, общую слабость, сонливость и эпизоды снижения внимания, частота которых усилилась за последние несколько месяцев и стала беспокоить родственников пациента.
Из анамнеза известно, что пациент перенес ИМ с транслюминальной баллонной ангиопластикой и стентированием передней межжелудочковой ветви левой коронарной артерии в 2012 г., далее повторный ИМ 20.10.2019 со стентированием ветви тупого края. В течение 10 лет гипертоническая болезнь с максимальными значениями АД до 190/100 мм рт. ст. ОНМК и сахарный диабет в анамнезе отрицает. Постоянно принимает тикагрелор 60 мг 2 р/сут, ацетилсалициловую кислоту 75 мг/сут, аторвастатин 20 мг/сут, бисопролол 2,5 мг/сут, периндоприл 2,5 мг 2 р/сут, на фоне чего достигнуто: АД <140/<80 мм рт. ст., частота сердечных сокращений (ЧСС) 55–70 в 1 мин, холестерин липопротеинов низкой плотности 1,88 ммоль/л.
В июле 2022 г. удаление кожного новообразования правой щеки: узловая базалиома pT1N0M0 I ст., III клиническая группа. Без данных за рецидив заболевания.
В августе 2022 г. перенес COVID-19, находился на стационарном лечении: КТ-1 с поражением 10% объема легочной ткани. Проходил лечение и реабилитацию с удовлетворительным результатом, однако после перенесенной инфекции начал отмечать ухудшение толерантности к физическим нагрузкам, выраженную сонливость, частые головокружения и нарушение способности к концентрации внимания.
При осмотре: АД 140/80 мм рт. ст., ЧСС 65 в 1 мин, са-турация 99%, пастозность нижних конечностей. NT-proBNP 608 пг/мл. Фракция выброса левого желудочка (ЛЖ) 56%. При холтеровском мониторировании основной ритм синусовый 36–68–120 в 1 мин, эпизодов диспозиции сегмента ST, пауз не зарегистрировано. Также обращает на себя внимание незначительная деформация обоих коленных суставов и мелких суставов кистей в связи с длительно текущим остеоартритом, множественные себорейные кератомы.
Установлен основной диагноз: «ИБС: Постинфарктный кардиосклероз от 2012 г. и 2019 г. Коронарография, транслюминальная баллонная ангиопластика и стентирование передней межжелудочковой ветви левой коронарной артерии от 2012 г. и ветви тупого края от 2019 г. (2 стента). Стенокардия напряжения II функционального класса (ФК).
Фоновое заболевание: гипертоническая болезнь III стадии, 3-й степени, очень высокий риск. Дислипид-емия. Осложнение: ХСН с сохраненной фракцией выброса, IIА, III ФК.
Сопутствующие заболевания: ХИГМ. Хронический пиелонефрит, стадия ремиссии. Хроническая болезнь почек II стадии (скорость клубочковой фильтрации 65 мл/мин/1,73 м2). Узловая базалиома кожи правой щеки pT1N0M0 I ст., III клиническая группа. Без данных за рецидив. Себорейная экзема. Деформирующий полиостеоартрит с поражением суставов кистей, функциональная недостаточность суставов II».
Учитывая недостаточный контроль за течением ИБС, ухудшение тяжести ХСН после перенесенной коронавирусной инфекции COVID-19, принято решение о коррекции постоянно принимаемой кардиотропной терапии: тикагрелор 60 мг 2 р/сут, бисопролол 5 мг/сут, спиронолактон 25 мг/сут, розувастатин 20 мг/сут, сакубитрил-валсартан 50 мг 2 р/сут, дапаглифлозин 10 мг/сут. Через 8 нед. при повторной консультации одышку не отмечает, сжимающие боли в левой половине грудной клетки при физической нагрузке отрицает, однако сохраняется головокружение, общая слабость, сонливость и эпизоды снижения внимания. К терапии добавлен Мексикор® в лекарственной форме капсулы 100 мг 2 р/сут внутрь в качестве цитопротекторного метаболического агента.
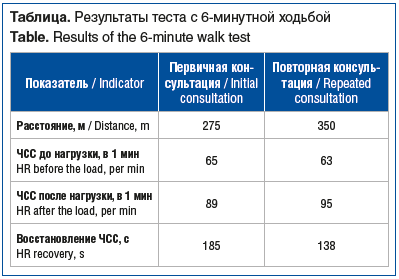
Для объективизации оценки эффективности коррекции терапии был проведен тест с 6-минутной ходьбой до и после назначения препарата (см. таблицу). При повторной консультации через 8 нед. пациент отметил улучшение общего самочувствия, эпизоды ухудшения внимания отмечает реже, повысилась толерантность к физическим нагрузкам (одышка при подъеме выше 3-го этажа, приступы стенокардии отрицает). В связи с улучшением результатов функционального теста, достигнутым контролем симптомов, в том числе когнитивной сферы, рекомендовано продолжение приема назначенной кардиотропной терапии в комбинации с этилметилгидроксипиридина сукцинатом в том же режиме. Нежелательных побочных явлений, связанных с приемом этого препарата, выявлено не было.
Обсуждение
Приведенное нами клиническое наблюдение иллюстрирует терапевтические возможности в лечении ХСН в целом и КЭ в частности, которые могут быть реализованы с помощью дополнения комплексной терапии цитопротекторами.
Улучшение функционального статуса пациента сопровождалось повышением толерантности к физическим нагрузкам, снижением числа эпизодов ухудшения внимания и отсутствием приступов стенокардии, что коррелировало со снижением уровня NT-proBNP, липопротеинов низкой плотности, и улучшением результатов теста c 6-минутной ходьбой через 8 нед. после модификации кардиотропной терапии. Достигнутый терапевтический результат подтверждает кардио- и церебропротективный эффект препарата, установленный в ранее проведенных исследованиях [14, 15, 20, 21]. Позитивная клиническая динамика стала следствием усиления энергетического метаболизма в ишемизированном миокарде, повышения глобальной сократимости миокарда, а также уменьшения проявлений систолической дисфункции ЛЖ, что снизило системную гипоксию тканей, в частности центральной нервной системы, и благоприятно повлияло на когнитивные функции на фоне включения препарата Мексикор® в схему лечения.
Наши наблюдения и анализ ранее проведенных исследований показывают, что добавление этилметилгидроксипиридина сукцината обладает минимальными рисками появления лекарственно-ассоциированных нежелательных явлений или фармакологических взаимодействий. В случае достижения положительной динамики на фоне проводимого лечения возможно продолжение приема указанного препарата по стартовой схеме или, в случае недостаточного эффекта, коррекция кардиотропной терапии с дальнейшей эскалацией его дозы до 800 мг/сут при удовлетворительной переносимости.
Заключение
Как показали проведенные исследования, почти у половины пациентов с ИБС и клинически значимым ухудшением тяжести ХСН выявляется КЭ, которая в значительной степени ухудшает качество жизни и имеет негативное влияние на результаты лечения и прогноз. Пациенты с КЭ представляют наиболее уязвимую группу коморбидных больных пожилого возраста, которым необходимо добавление препаратов с системным и метаболическим характером действия для усиления эффектов стандартной кардиотропной терапии с целью стабилизации течения ХСН и достижения церебропротекции как в лечебном, так и в профилактическом режиме.
Функциональные результаты у пациента в приведенном клиническом наблюдении демонстрируют потенциальную нейропротективную активность этилметилгидроксипиридина сукцината в составе комбинированной терапии КЭ у больных ХСН. Улучшение когнитивно-мнестических функций и толерантности к физической нагрузке достоверно повысило качество повседневной жизни пациента, что является одной из ключевых целей при назначении этилметилгидроксипиридина сукцината в составе комплексного лечения. Для больных с впервые выявленным симптоматическим течением ХСН или ее декомпенсацией рекомендовано добавление препарата Мексикор® (100 мг 2 р/сут внутрь) в рамках многокомпонентной кардиотропной терапии в качестве метаболического агента, оказывающего системное цитопротективное действие, в частности у пациентов с признаками КЭ.
Этилметилгидроксипиридина сукцинат обладает как системным, так и непосредственно влияющим на энергетический метаболизм миокарда действием, что не только повышает эффективность стандартной терапии, но и улучшает качество жизни пациентов. Применение этилметилгидроксипиридина сукцината в комбинации с кардиотропной терапией обладает доказанной синергией в отношении результатов лечения пациентов с ИБС и ХСН.
Целесообразно проведение дальнейших исследований для оценки возможности использования этилметилгидроксипиридина сукцината в качестве метаболического нейропротектора у пациентов с ХСН и другими ССЗ, а также определение лекарственной комбинации, показывающей наилучшую терапевтическую синергию в сочетании с этилметилгидроксипиридина сукцинатом.
1Мексикор® (Электронный ресурс). URL https://grls.rosminzdrav.ru/GRLS.aspx?RegNumber=&MnnR=&lf=&TradeNmR=%d0%9c%d0%b5%d0%ba%d1%81%d0%b8%d... %d0%be%d1%80&OwnerName=&MnfOrg=&MnfOrgCountry=&isfs=0®type=1%2c6&pageSize=10&order=Registered&orderType=desc&pageNum=1 (дата обращения 10.01.2023).
Сведения об авторах:
Резник Елена Владимировна — д.м.н., доцент, заведующая кафедрой пропедевтики внутренних болезней лечебного факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; врач-терапевт, кардиолог, врач функциональной диагностики, ультразвуковой диагностики ГБУЗ «ГКБ № 31 им. академика Г.М. Савельевой ДЗМ»; 119415, Россия, г. Москва, ул. Лобачевского, д. 42; ORCID iD 0000-0001-7479-418X.
Алиева Амина Магомедовна — к.м.н., доцент кафедры госпитальной терапии № 2 лечебного факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0001-5416-8579.
Ушакова Наталья Александровна — аспирант кафедры пропедевтики внутренних болезней лечебного факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-2740-5679.
Крупнова Екатерина Сергеевна — аспирант кафедры пропедевтики внутренних болезней лечебного факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-6088-080Х.
Контактная информация: Елена Владимировна Резник, e-mail: elenaresnik@gmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов: в статье использованы данные постмаркетинговых исследований компании ООО «Экофарминвест».
Статья поступила 10.01.2023.
Поступила после рецензирования 02.02.2023.
Принята в печать 01.03.2023.
About the authors:
Elena V. Reznik — Dr. Sc. (Med.), associate professor, Head of the Department of Propedeutics of Internal Diseases of the Faculty of Medicine, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117997, Russian Federation; therapist, cardiologist, specialist in functional diagnostics and ultrasound diagnostics, Academician G.M. Savel'eva City Clinical Hospital No. 31; 42, Lobachevskiy str., Moscow, 119415, Russian Federation; ORCID iD 0000-0001-7479-418X.
Amina M. Alieva — C. Sc. (Med.), associate professor of the Department of Hospital Therapy No. 2 of the Faculty of Medicine, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117997, Russian Federation; ORCID iD 0000-0001-5416-8579.
Natalya A. Ushakova — postgraduate student of the Department of Propedeutics of Internal Diseases of the Faculty of Medicine, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-2740-5679.
Ekaterina S. Krupnova — postgraduate student of the Department of Propedeutics of Internal Diseases of the Faculty of Medicine, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-6088-080Х.
Contact information: Elena V. Reznik, e-mail: elenaresnik@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
Conflict of interests: the data of post-marketing studies of the company Ecopharminvest LLC are used in the article.
Received 10.01.2023.
Revised 02.02.2023.
Accepted 01.03.2023.
2. Roth G.A., Mensah G.A., Johnson C.O. et al. Global Burden of Cardiovascular Diseases and Risk Factors, 1990-2019: Update From the GBD 2019 Study. J Am Coll Cardiol. 2020;76(25):2982–3021. DOI: 10.1016/j.jacc.2020.11.010.
3. Здравоохранение в России. 2021: стат. сб./Росстат. М., 2021.
4. Virani S.S., Alonso A., Aparicio H.J. et al. Heart Disease and Stroke Statistics-2021 Update: A Report From the American Heart Association. Circulation. 2021;143(8):e254–e743. DOI: 10.1161/CIR.0000000000000950.
5. Roger V.L. Epidemiology of Heart Failure: A Contemporary Perspective. Circ Res. 2021;128(10):1421–1434. DOI: 10.1161/CIRCRESAHA.121.318172.
6. Sidney S., Go A.S., Jaffe M.G. et al. Association Between Aging of the US Population and Heart Disease Mortality From 2011 to 2017. JAMA Cardiol. 2019;4(12):1280–1286. DOI: 10.1001/jamacardio.2019.4187.
7. Ушакова Н.А., Ершов Н.С., Щербакова Е.С. и др. Кардиогенная энцефалопатия у пожилых больных с хронической сердечной недостаточностью. Медицинский Алфавит. 2020;2:59–60.
8. Фонякин А.В., Машин В.В., Гераскина Л.А., Машин В.Л. Кардиогенная энцефалопатия. Факторы риска и подходы к терапии. Consilium Medicum. 2012;14(2):5–9.
9. United Nations, Department of Economic and Social Affairs, Population Division (2019). World Population Ageing 2019: Highlights (ST/ESA/SER.A/430).
10. Polyakov D.S., Fomin I.V., Belenkov Yu.N. et al. Chronic heart failure in the Russian Federation: what has changed over 20 years of follow-up? Results of the EPOCH-CHF study. Kardiologiia. 2021;61(4):4–14. DOI: 10.18087/cardio.2021.4.n1628.
11. Forman D.E., Maurer M.S., Boyd C. et al. Multimorbidity in Older Adults With Cardiovascular Disease. J Am Coll Cardiol. 2018;71(19):2149–2161. DOI: 10.1016/j.jacc.2018.03.022.
12. Andreenko E.Yu., Lukyanov M.M., Yakushin S.S. et al. Early cardiovascular multimorbidity in out- and in-patient care: age characteristics and medication therapy (data from the REKVAZA and REKVAZA-CLINIC registries). Cardiovasc Ther Prev. 2020;19(5):2672. DOI: 10.15829/1728-8800-2020-2672.
13. Honka H., Solis-Herrera C., Triplitt C. et al. Therapeutic Manipulation of Myocardial Metabolism: JACC State-of-the-Art Review. J Am Coll Cardiol. 2021;77(16):2022–2039. DOI: 10.1016/j.jacc.2021.02.057.
14. Зотов Д.Д., Сизов А.В., Дзеранова Н.Я. Миокардиальная цитопротекция в лечении сердечно-сосудистых заболеваний у пациентов старшей возрастной группы. Университетский терапевтический вестник. 2019;1(1):20–29.
15. Акимов А.Г., Полумисков В.Ю. Перспективы применения миокардиальных цитопротекторов в кардиологической практике. Terra medica nova. 2005;4:6–9.
16. Современный подход к цитопротекторной терапии. Методическое пособие для врачей. Под ред. Белоусова Ю.Б. М., 2010.
17. Лукьянова Л.Д. Метаболические эффекты 3-оксипиридина сукцината. Химико-фармацевтический журнал. 1990;8:8–11.
18. Кардиоцитопротектор Мексикор: новое направление в лечении ишемической болезни сердца и артериальной гипертонии. Под ред. Михина В.П. (Электронный ресурс.) URL: https://ephi.ru/upload/iblock/c33/c33b6ad7bcffc9eaf190f27d182546e4.pdf. (дата обращения: 09.01.2023).
19. Михин В.П. Митохондриальные цитопротекторы: сегодняшний день и новые перспективы. М., 2015.
20. Фирсов А.А., Смирнов М.В. Влияние парентерального применения препарата Мексикор на состояние когнитивных функций у больных с хронической ишемией головного мозга. Поликлиника. 2010;2:24–26.
21. Бабкин А.П., Курбатова Т.Л. Эффективность комбинированной антигипертензивной терапии при когнитивных расстройствах у пожилых больных. Российский кардиологический журнал. 2011;13:28–32.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.