Опыт применения азоксимера бромида для профилактики острых респираторных заболеваний и COVID-19 у взрослых из группы повышенного риска инфицирования (медицинских работников «красной зоны»): метаанализ контролируемых клинических исследований
DOI: 10.32364/2587-6821-2022-6-11-635-642
Цель исследования: метаанализ результатов клинических исследований применения азоксимера бромида для профилактики острых респираторных инфекций (ОРИ) и новой коронавирусной инфекции COVID-19 для обобщенной оценки эпидемиологической эффективности азоксимера бромида у взрослых, подверженных повышенному риску инфицирования, — у медицинских работников «красной зоны».
Материал и методы: поиск клинических исследований препарата азоксимера бромид проводился в русскоязычных и международных источниках. Для идентификации контролируемых исследований включали электронные базы данных PubMed, Embase, Cochrane Library, eLIBRARY.RU, научную электронную библиотеку «КиберЛенинка». Поиск осуществлялся с использованием ключевых терминов: «азоксимера бромид», «инфекция дыхательных путей», «COVID-19», «профилактика» и «взрослые» (до мая 2022 г.), «медработники», «медперсонал». Также у компаний-производителей были запрошены отчеты о клинических исследованиях препаратов, содержащих азоксимера бромид в качестве основного действующего вещества. Был проведен отбор статей и отчетов по определенным критериям, оценивался такой параметр, как частота заболеваемости ОРИ и COVID-19. Для проведения метаанализа были найдены точечные оценки эффектов, которые рассчитывались с помощью отношения шансов (ОШ).
Результаты исследования: из общего числа 64 статей и отчетов с участием более 5060 взрослых лиц в результате проведенного поиска исследований и последующего их анализа были отобраны 3 относительно однородных по дизайну клинических исследования, касающиеся азоксимера бромида и соответствующие критериям отбора. Из отобранных исследований с участием 1141 взрослых в возрасте от 18 до 69 лет основную группу составили 718 участников, которым был назначен азоксимера бромид. В группу контроля входили 423 человека. Применение азоксимера бромида повлияло на снижение заболеваемости ОРИ и COVID-19 в группах повышенного риска инфицирования (медицинских работников). У лиц, получавших азоксимера бромид, ОШ не заболеть ОРИ и COVID-19, составило 3,02 (95% доверительный интервал (ДИ) 2,14–3,89), ОШ не заболеть COVID-19 составило 2,65 (95% ДИ 1,53–3,77). Во всех исследованиях авторами был отмечен благоприятный профиль безопасности азоксимера бромида.
Заключение: прием азоксимера бромида показал эпидемиологическую эффективность в группах повышенного риска инфицирования (медицинских работников), значимо снизив заболеваемость ОРИ и COVID-19, что позволяет рекомендовать его в качестве средства профилактики этих инфекций в течение эпидемиологического сезона.
Ключевые слова: острые респираторные инфекции, COVID-19, метаанализ, азоксимера бромид, медицинские работники.
Для цитирования: Омарова Х.Г., Плоскирева А.А., Агаркова И.А., Горелов А.В. Опыт применения азоксимера бромида для профилактики острых респираторных заболеваний и COVID-19 у взрослых из группы повышенного риска инфицирования (медицинских работников «красной зоны»): метаанализ контролируемых клинических исследований. РМЖ. Медицинское обозрение. 2022;6(11):635-643. DOI: 10.32364/2587-6821-2022-6-11-635-642.
Kh.G. Omarova1, A.A. Ploskireva1,2, I.A. Agarkova1, A.V. Gorelov1,3
1Central Research Institute of Epidemiology of the Russian Federal Service for Supervision
of Consumer Rights Protection and Human Well-Being, Moscow, Russian Federation
2Pirogov Russian National Research Medical University, Moscow, Russian Federation
3A.I. Yevdokimov Moscow State University of Medicine and Dentistry, Moscow,
Russian Federation
Aim: meta-analysis of the clinical trials with the use of Azoximer bromide for the prevention of acute respiratory infections (ARI) and the novel coronavirus infection COVID-19 to systematically assess the epidemiological effectiveness of Azoximer bromide in adults at a higher risk of contracting the infection — the "red zone" healthcare workers.
Patients and Methods: the search for clinical trials of Azoximer bromide was performed in the Russian-language and international sources. To identify controlled trials, the authors used such electronic databases as PubMed, Embase, Cochrane Library, eLIBRARY.RU, Scientific Electronic Library, and CyberLeninka. The following keywords were used for conducting the search: Azoximer bromide, respiratory tract infection, COVID-19, prevention, and adults (through May 2022), heathcare workers, medical personnel. Also, clinical trial reports on the use of medications containing Azoximer bromide as the main active ingredient were requested from the manufacturing companies. Publications and reports were selected based on the eligibility criteria. In particular, the assessment included such a parameter as ARI and COVID-19 morbidity. Pointwise estimates of effects were found for conducting meta-analysis which were calculated using odds ratios (OR).
Results: out of the total 64 publications and reports involving over 5060 adults, three clinical trials using Azoximer bromide were selected. These trials had a relatively uniform design and matched the eligibility criteria. The selected trials included 1141 adults 18–69 years old. The treatment group comprised 718 subjects who received Azoximer bromide, and the control group included 423 individuals. The use of Azoximer bromide had the effect of reducing morbidity associated with ARI and COVID-19 in the groups at a higher risk of contracting infection (healthcare workers). For the subjects receiving Azoximer bromide, an OR of not getting sick from ARI and COVID-19 was 3.02 (95% confidence interval (CI) 2.14–3.89); in the control group an OR of not getting sick from COVID-19 was 2.65 (95% CI 1.53–3.77). The authors noted that Azoximer bromide had a good safety profile in all trials.
Conclusion: the epidemiological effectiveness of Azoximer bromide was demonstrated in the groups at a higher risk of contracting the infection (healthcare workers), as proven by the significant reduction of ARI and COVID-19 morbidity. Thus, this drug can be recommended for the prevention of the studied infections during seasonal epidemics.
Keywords: acute respiratory infections, COVID-19, meta-analysis, Azoximer bromide, healthcare workers.
For citation: Omarova Kh.G., Ploskireva A.A., Agarkova I.A., Gorelov A.V. Experience with the use of Azoximer bromide for the prevention of acute respiratory infections and COVID-19 in adults from the group with a higher risk of contracting the infection ("red zone" healthcare workers): meta-analysis of controlled clinical trials. Russian Medical Inquiry. 2022;6(11):635–642 (in Russ.). DOI: 10.32364/2587-6821- 2022-6-11-635-642.
Введение
Острые респираторные инфекции (ОРИ) составляют до 95–97% в структуре инфекционной заболеваемости в России, при этом 10–40% населения нашей страны заболевает ОРИ 1 и более раз в год. В РФ в 2021 г. было зарегистрировано 38,44 млн случаев ОРИ множественной и неуточненной локализации, что составило 75,8% от числа всех выявленных инфекционных и паразитарных болезней. Всего в 2021 г. переболело 26,25% населения страны (в 2020 г. — 22,7%). Раннее начало эпидемического подъема заболеваемости характеризовало эпидемический сезон по гриппу и ОРИ 2021–2022 гг. Отмечается рост заболеваемости на 26% (20 753,87 на 100 тыс. населения) в сравнении со среднемноголетним показателем предыдущего года — на 15,6% (показатель в 2021 г. составил 26 252,14 на 100 тыс. населения). Выявленные различия были статистически значимы (р<0,05). Наибольшую экономическую значимость среди острых и впервые выявленных инфекционных заболеваний в прошедшем году представляли острые инфекции верхних дыхательных путей множественной и неуточненной локализации. По ориентировочным расчетам Роспотребнадзора, экономический ущерб от гриппа и ОРИ в 2018 г. превысил 520 млрд руб. [1], а в 2021 г. он составил уже более 758 млрд руб. и занял первое место в структуре ущерба от всех инфекционных заболеваний [2].
В сезоне 2020–2021 гг. произошла социркуляция возбудителя COVID-19, вирусов сезонных ОРИ и гриппа. В настоящее время новая коронавирусная инфекция COVID-19 остается одной из проблем здравоохранения. В РФ в августе 2022 г. было выявлено уже более 19 млн случаев COVID-19 (в 2021 г. — 9,054 млн.) в 85 регионах, показатель заболеваемости на 100 тыс. населения составил 6181,93. В структуре заболеваемости COVID-19 в 2021 г. наиболее высокие показатели приходились на возрастные группы от 30 до 49 лет (33%), от 50 до 64 лет (24%) и старше 65 лет (20%). Удельный вес возрастной группы от 0 до 17 лет составил около 23%. Среди заболевших основную часть составляли граждане пенсионного возраста (25,5%) [2].
Медицинские работники находятся в непосредственной близости к инфицированным, и вероятность заболеть у них гораздо выше по сравнению с другими, так как они имеют дело с больными, имеющими высокую вирусную нагрузку SARS-CoV-2. Кроме этого, наличие сопутствующих заболеваний и постоянный стрессовый фактор могут способствовать более тяжелому течению инфекции. Более половины летальных исходов регистрируется среди медицинских работников младше 60 лет, а заболеваемость COVID-19 в данной популяции достигала 17% от общего числа заболевших ежемесячно в 2020 г. [3, 4]. Несмотря на принимаемые во всем мире меры по оптимизации работы медицинского персонала в условиях пандемии COVID-19, уровень заболеваемости данной категории населения остается одним из самых высоких
Во время вспышки SARS в 2002–2003 гг. 21% всех подтвержденных случаев заражения в мире пришелся именно на медицинских работников. В период пандемии COVID-19, по обобщенным данным Всемирной организации здравоохранения (ВОЗ), на медицинских работников, составляющих всего 3% населения, приходилось 10% от всех случаев заболевания [5]. По данным проспективного обсервационного когортного исследования, проведенного в Великобритании и США среди населения в целом, включая медицинских работников, работающих с пациентами, зараженными SARS-CoV-2, риск заболеть у них оказался в 11,6 раза выше, чем у людей, не являющихся медицинскими работниками. Причем по сравнению с риском для населения в целом, для медицинских работников, которые первыми контактируют с инфицированными пациентами, он был выше во всех медицинских учреждениях, а для тех, кто работает в стационарных условиях, был самым высоким (скорректированный относительный риск (ОР) 24,30, 95% доверительный интервал (ДИ) 21,83–27) [6].
В связи с этим вопрос поиска возможностей для профилактики инфекций в группах риска в течение последних 2 лет стоит еще более остро. Особенно с учетом того факта, что впервые в истории эпидемиологический процесс характеризуется наслоением сезонных ОРИ и гриппа на фон в виде новой коронавирусной инфекции COVID-19.
В настоящее время существуют обоснованные рекомендации для симптоматической и этиотропной терапии, составленные с учетом убедительной доказательной базы клинических исследований. В научной литературе появились данные об успешном использовании такого препарата, как азоксимера бромид в качестве неспецифической профилактики не только ОРИ, но и COVID-19. Иммуномодулирующий препарат азоксимера бромид, применявшийся в Российской Федерации для профилактики ОРИ, был включен во временные методические рекомендации по лекарственной терапии ОРИ в амбулаторной практике в период COVID-19 в РФ [7].
Благоприятный профиль безопасности азоксимера бромида, разработанного в Институте иммунологии РФ и применяющегося в терапии инфекционно-воспалительных респираторных заболеваний уже более 22 лет, доказан. Комплексный иммуномодулирующий и противовоспалительный эффект продемонстрирован в многочисленных клинических исследованиях. Включение азоксимера бромида в комплексную терапии ОРИ и других респираторных инфекций способствовало сокращению срока до нормализации температуры тела, уменьшению симптомов интоксикации, снижению числа осложнений и частоты ОРИ по сравнению со стандартной терапией [8]. Было показано, что азоксимера бромид повышает фагоцитарную активность макрофагов и нейтрофилов [9, 10], ускоряет созревание дендритных клеток и их миграцию в лимфоидные органы с последующим развитием адаптивного иммунного ответа, сопровождающегося высоким уровнем продукции антител и нормализацией показателей Т-клеточного звена (CD3+, CD4+, CD8+) иммунитета. Он также повышает активность натуральных киллеров, потенцируя их способность к дегрануляции, что является критически важным в противовирусном иммунном ответе. Кроме того, недавно было открыто еще одно важное свойство азоксимера бромида — способность подавлять суицидальные нейтрофильные внеклеточные ловушки (НВЛ), содержащие высокотоксичные для тканей агенты: миелопероксидазу, гистоны, нейтрофильную эластазу, с которыми в первую очередь связывают негативное воздействие НВЛ на организм при инфекционном воспалении [11]. Перечисленные эффекты способствуют ускорению выздоровления и уменьшению общей интоксикации при острых и хронических инфекционно-воспалительных заболеваниях.
В результате проведенных исследований было показано, что азоксимера бромид, усиливая факторы ранней защиты организма от инфекции и повышая бактерицидные свойства слюны и секрета слизистых верхних дыхательных путей, увеличивает резистентность организма в отношении инфекций бактериальной, грибковой и вирусной этиологии. В связи с этим профилактическое применение азоксимера бромида как у часто болеющих детей, так и у взрослых пациентов является обоснованным и может способствовать уменьшению заболеваемости ОРИ [12–15].
Цель исследования: метаанализ результатов клинических исследований применения азоксимера бромида для профилактики ОРИ и новой коронавирусной инфекции COVID-19 для обобщенной оценки эпидемиологической эффективности азоксимера бромида у взрослых, подверженных повышенному риску инфицирования, — у медицинских работников «красной зоны».
Материал и методы
Стратегия поиска исследований
Поиск клинических исследований препарата азоксимера бромид проводился в русскоязычных и международных источниках. Для идентификации контролируемых исследований включали электронные базы данных PubMed, Embase, Cochrane Library, eLIBRARY.RU, научную электронную библиотеку «КиберЛенинка». Поиск осуществлялся с использованием ключевых терминов: «азоксимера бромид», «инфекция дыхательных путей», «COVID-19», «профилактика» и «взрослые» (до мая 2022 г.), «медработники», «медперсонал». Также у компаний-производителей были запрошены отчеты о клинических исследованиях препаратов, содержащих азоксимера бромид в качестве основного действующего вещества. Исследования, включенные в метаанализ, должны были соответствовать следующим критериям отбора:
Сравнительные контролируемые клинические исследования профилактики инфекционно-воспалительных заболеваний дыхательных путей (в том числе разного дизайна: рандомизированные двойные слепые, открытые рандомизированные и нерандомизированные, открытые когортные).
Участники — медработники из группы повышенного риска инфицирования респираторными инфекционно-воспалительными заболеваниями (ОРИ, пневмония).
Возраст участников исследования — от 18 до 69 лет.
Пути введения препарата — пероральный, сублингвальный.
Длительность приема исследуемого препарата — от 30 до 40 дней.
В исследовании изучали применение азоксимера бромида для профилактики инфекционно-воспалительных заболеваний дыхательных путей (в сравнении с плацебо или без него) у медицинских работников.
Критерии оценки эффективности, используемые в исследовании: отсутствие новых случаев заболевания ОРИ и СOVID-19 в период приема азоксимера бромида.
Из анализа были исключены:
Исследования, проведенные в детской популяции.
Исследования, не связанные с профилактикой респираторных инфекций.
Исследования, в которых дополнительно применялись другие виды профилактики, кроме профилактики азоксимера бромидом.
Исследования, в которых длительность приема была меньше 30 дней или превышала 40 дней.
Исследования, в которых доза азоксимера бромида была отличной от 12 мг в сутки и способ введения препарата был не пероральным.
Обзорные статьи, повторяющие данные других исследований.
Конечные точки исследований, используемые в метаанализе
Метаанализ проводился по первичному показателю эффективности — частоте заболеваемости ОРИ и COVID-19 в контрольной и основной группах в период приема препарата. Статистический анализ проводился с использованием пакета программы Stata 16.
В качестве оцениваемого параметра была использована частота заболеваемости ОРИ и COVID-19. Для проведения метаанализа были найдены точечные оценки эффектов, которые рассчитывались с помощью отношения шансов (ОШ). Так, отношение не заболевших к заболевшим в основной группе получавших лечение было поделено на отношение не заболевших к заболевшим в контрольной группе, а затем прологарифмировано. При расчете общего эффекта учитывался вес каждого исследования, включенного в обзор. Выбор модели фиксированных эффектов для анализа показателя эффективности обусловлен тем, что включенные в метаанализ исследования характеризовались высокой степенью однородности, хотя и различались между собой размером выборки. Уровнем статистической значимости теста выбрана вероятность ошибки первого рода, равная 0,05 (p≤0,05).
Результаты и обсуждение
Из общего числа 64 статей и отчетов с участием более 5060 взрослых лиц в результате поиска исследований и последующего их анализа были отобраны 3 относительно однородных по дизайну клинических исследования, касающиеся азоксимера бромида и соответствующие критериям отбора. Из отобранных исследований с участием 1141 взрослого в возрасте от 18 до 69 лет основную группу составили 718 участников, которым был назначен азоксимера бромид. В группу контроля входили 423 человека. В исследование включались медицинские работники в стационарах «красной зоны», имеющие частые контакты с больными COVID-19.
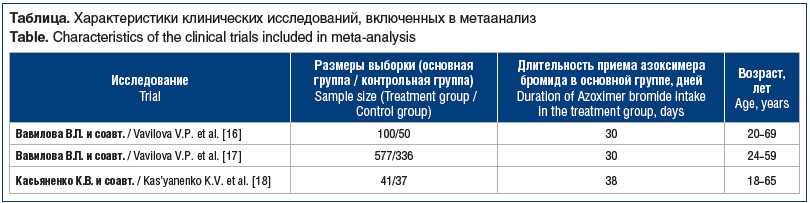
Опытная группа и группа сравнения были определены по списку медицинских работников, имеющих аналогичный риск заражения новой коронавирусной инфекцией согласно временному руководству ВОЗ для оценки рисков контакта с вирусом SARS-CoV-2 для медицинских работников [3]. Наименьшее число участников составляло 78 человек, наибольшее — 913 человек (см. таблицу).
Стояла задача ответить на вопрос, насколько эффективен азоксимера бромид для профилактики не только ОРИ, но и COVID-19. Надо отметить, что среди исследований, включенных в обзор, нет ни одного слепого рандомизированного плацебо-контролируемого, что, вероятно, было продиктовано этическими соображениями в разгар пандемии COVID-19 по отношению к данной категории участников. Тем не менее рассматриваемые исследования уже демонстрируют обнадеживающие результаты.
Авторы этих исследований утверждают, что во время работы в «красной зоне» у участников основных групп, которые принимали азоксимера бромид ежедневно в дозе 12 мг сублингвально, случаи ОРИ, в том числе COVID-19, практически не регистрировались, в отличие от групп контроля.
В аналитический обзор включены две работы В.П. Вавиловой и соавт. [16, 17] и работа К.В. Касьяненко и соавт. [18], исследования проводились в период с 2020 г. по 2022 г. Оценивали влияние профилактического приема азоксимера бромида на заболеваемость ОРИ, вызванными в том числе SARS-CoV-2, среди медицинских работников «красной зоны», находившихся в непосредственном контакте с пациентами, госпитализированными в инфекционный стационар с COVID-19.
Все исследования были открытыми нерандомизированными, с контрольной группой, не получавшей азоксимера бромид. Азоксимера бромид назначали сублингвально в дозе 12 мг 1 р/сут в течение 30 дней в 2 исследованиях [16, 17] (с последующим наблюдением после отмены препарата в течение 3 мес.) и в течение 38 дней с 2-мя 4-дневными перерывами с последующим наблюдением после отмены препарата в течение 38 дней в третьем исследовании [18].
Данные исследования S.V. Efimov [19], в котором медицинские работники получали азоксимера бромид на протяжении 5 мес. пребывания в «красной зоне», не вошли в настоящий метаанализ, так как длительность приема не соответствовала заданным параметрам и отсутствовали данные по контрольной группе.
Результаты, полученные из отчета «Опросник медицинских работников по профилактике COVID-19», в который вошли данные из 15 центров с участием 476 человек, также не вошли в анализ в связи с коротким курсом профилактического применения — преимущественно 10 дней. Такая длительность приема не соответствует заданным критериям отбора.
Все участники 3 исследований, включенных в метаанализ, были распределены в 2 группы, сопоставимые в процентном соотношении по полу и возрасту, а также по наличию хронических заболеваний. Статистически значимых различий между сравниваемыми характеристиками на момент включения в исследование среди медработников не имелось [16–18].
Предварительный анализ показал, что заболеваемость ОРИ в основной группе, получавшей азоксимера бромид, составила 0,7% против 14% в группе сравнения.
В качестве показателя эффективности была рассчитана заболеваемость ОРИ в период приема азоксимера бромида.
В исследовании В.П. Вавиловой и соавт. [16] основная группа включала 100 медработников, контрольная группа составляла 50 медработников, которые не принимали профилактические лекарственные препараты.
Ретроспективно за 1 мес. до начала приема азоксимера бромида была показана сопоставимость контрольной и основной групп по уровню заболеваемости ОРИ и COVID-19 (10% и 12% соответственно; p=0,8559; p=0,6688) [16]. Удельный вес ОРИ любой этиологии, а также COVID-19 на фоне применения азоксимера бромида в основной группе был достоверно ниже, чем в группе сравнения. В ходе исследования было показано, что при сублингвальном применении азоксимера бромида в форме таблеток 12 мг/сут не отмечалось ни одного случая заболевания ОРИ и COVID-19 в течение 1 мес., в это же время в контрольной группе доля заболевших ОРИ составила 16%, а заболевших COVID-19 — 8%.
В исследовании В.П. Вавиловой и соавт. [17] в основную группу было включено 577 человек, получавших азоксимера бромид, и 336 человек, не получавших препарат. При применении азоксимера бромида также зафиксировано значимое уменьшение числа случаев ОРИ и COVID-19 по сравнению с группой контроля. В основной группе ОРИ заболели 0,7% участников, COVID-19 — 0,3%, в группе контроля — 12,2% и 5,1% соответственно.
Применение азоксимера бромида также показало снижение заболеваемости ОРИ, включая COVID-19, по сравнению с контрольной группой в исследовании К.В. Касьяненко и соавт. [18]. Группа терапии с применением азоксимера бромида включала 41 пациента, контрольная группа — 37 пациентов. Число лиц, заболевших COVID-19 в основной группе, было статистически значимо ниже, чем в группе сравнения (2,44% против 16,21%; р<0,05). Статистически значимое различие, свидетельствующее в пользу применения исследуемого препарата, было установлено так же, как и в других исследованиях.
В настоящем исследовании были проанализированы данные 718 человек в основной группе и 423 человек в группе cравнения, которые препарат не получали.
Результаты статистического анализа с применением модели фиксированных эффектов показали значимые различия по заболеваемости при сравнении основной группы с контрольной группой. На это указывает статистическая значимость общего эффекта, а также расположение общего эффекта на форест-графике (см. рисунок). Как видно из рисунка, общий эффект и границы его ДИ находятся справа от нулевого эффекта (обозначается единицей на оси абсцисс графика). Стоит заметить, что наибольшим весом, согласно построенному графику, обладает исследование В.П. Вавиловой 2021 г. (73,5%).
![Рисунок. Профилактическая эффективность азоксимера бромида в отношении ОРИ и COVID-19 [16–18] Figure. Azoximer bromide efficacy for the prevention of ARI and COVID-19 [16–18] Рисунок. Профилактическая эффективность азоксимера бромида в отношении ОРИ и COVID-19 [16–18] Figure. Azoximer bromide efficacy for the prevention of ARI and COVID-19 [16–18]](/upload/medialibrary/10b/635-2.png)
Для анализа однородности включенных в выборку исследований статистический пакет рассчитывает значение I2, которое в процентах выражает степень гетерогенности данных. Расчеты программы показывают, что I2 равно нулю, из чего следует, что выборка является полностью однородной, что указывает на обоснованность использования модели с фиксированными эффектами.
На рисунке показатель расположен справа от нулевого эффекта — единицы на оси абсцисс, что указывает на наличие положительного профилактического эффекта от приема препарата.
Данные по заболеваемости в период последующего наблюдения в течение 3 мес. после прекращения 30-дневного приема азоксимера бромида были представлены только в одном исследовании В.П. Вавиловой и соавт. [17]. Группа профилактики с применением азоксимера бромида включала 245 медработников, в группу сравнения включили 103 медработника, которые не принимали профилактические лекарственные препараты. В течение 3 мес. последующего наблюдения после окончания 30-дневного приема азоксимера бромида также зафиксировано достоверное уменьшение числа случаев ОРИ и COVID-19 по сравнению с контрольной группой (р<0,05): в основной группе ОРИ заболели 32 (13,2%) участника, COVID-19 — 6 (2,4%), в группе контроля — 59 (57,3%) и 27 (26,2%) соответственно. Причем у 12 (35,3%) заболевших ОРИ из группы контроля развилась пневмония.
В основной группе, получавшей этот препарат, никто из участников пневмонией не заболел. Кроме того, авторы отметили, что применение препарата значительно снижает число случаев ОРИ и COVID-19 у медработников, страдающих хроническими патологиями, и способствует более легкому течению заболевания, если оно все же наступало.
У участников исследования, получавших азоксимера бромид, был продемонстрирован выраженный профилактический эффект независимо от наличия хронических заболеваний. Возможно, дополнительные риски заражения ОРИ, обусловленные наличием хронических заболеваний, уменьшаются на фоне приема препарата. Кроме того, было показано, что применение азоксимера бромида приводит к уменьшению случаев ОРИ и COVID-19 у медицинских работников как в период применения препарата, так и в течение 3 мес. после его приема. Это согласуется с полученными ранее данными о том, что использование азоксимера бромида повышает активность лизоцима и продукцию секреторного IgA и может способствовать сохранению этих показателей на высоком уровне даже через 3,5 мес. после окончания приема препарата [16].
Таким образом, в результате проведенного метаанализа данных 3 клинических исследований было установлено, что прием азоксимера бромида в качестве профилактики респираторных инфекций снижает заболеваемость ОРИ, включая COVID-19, в группе высокого риска инфицирования — у медицинских работников «красной зоны» стационаров. Было показано, что данное различие является статистически значимым, что подтверждает ранее сделанные выводы о профилактической эффективности азоксимера бромида у взрослых пациентов из группы высокого риска инфицирования ОРИ, включая COVID-19 [14, 15].
Существует вероятность того, что SARS-CoV-2 может стать постоянно циркулирующим вирусом и вместе с другими респираторными вирусами (вирусами гриппа, риновирусами и др.) вызывать в будущем новые вспышки заболеваемости в России [20]. В связи с этим защита уязвимых для инфицирования групп населения становится особенно актуальной задачей. Поэтому так важны исследования по неспецифической профилактике респираторных инфекций именно в популяции медработников, которые в силу своих профессиональных обязанностей регулярно контактируют с больными ОРИ или COVID-19.
Во всех исследованиях авторами был отмечен благоприятный профиль безопасности азоксимера бромида. Во время курса лечения аллергических реакций или побочных реакций на препарат практически не наблюдалось. Ранее в ходе исследования III фазы у детей [12, 21] также не было выявлено достоверных различий по частоте нежелательных явлений у пациентов, принимавших азоксимера бромид и плацебо. Препарат нетоксичен и хорошо переносится пациентами, в том числе детьми с 6 мес. [8].
Кроме того, получены данные о влиянии азоксимера бромида на мукозальный иммунитет слизистых верхних дыхательных путей, который служит первой линией защиты организма от вторжения респираторных вирусов. Повышенный риск заражения ОРИ связывают именно со снижением функции этой системы, что подтвердило исследование В.П. Вавиловой и соавт. [16]: у медработников «красной зоны» было выявлено значительное снижение показателей мукозального иммунитета — секреторного иммуноглобулина А и лизоцима и высокий уровень тревожности и депрессии. Было показано, что хронический или длительный стресс также оказывает супрессивное влияние на функционирование иммунной системы и продукцию sIgA в слизистой оболочке респираторного тракта. Это согласуется с работами зарубежных авторов, в которых также показано существование отрицательной связи между длительностью стресса и уровнем иммунной защиты — стресс отрицательно коррелировал с уровнем лизоцима в слюне [22]. В работе В.П. Вавиловой и соавт. было продемонстрировано влияние азоксимера бромида на секрецию IgA и лизоцима у медработников в виде повышения их уровней, что имеет важное значение для восстановления мукозального иммунитета.
Представленный в статье метаанализ имеет апостериорный (post-hoc) характер. В анализе применяли подходы без методики восстановления пропущенных значений. Не были включены данные об уровне смертности в исходах заболевания, скорости выздоровления (по причине отсутствия данных о длительности болезни). Кроме того, для проведения более качественной оценки свойств азоксимера бромида требуется проведение дополнительных исследований.
Заключение
В результате метаанализа 3 клинических исследований, в которых изучали эпидемиологическую эффективность азоксимера бромида для профилактики острых и обострения хронических респираторных инфекций, ОРИ, в том числе гриппа и COVID-19, у взрослых из группы риска в возрасте 18–69 лет, было установлено, что применение азоксимера бромида позволяет значимо уменьшить заболеваемость ОРИ согласно модели фиксированных эффектов. С учетом недостаточной эффективности существующих в настоящее время вакцин от коронавирусной инфекции поиск дополнительных средств профилактики ОРИ и COVID-19 остается актуальной задачей. Использование азоксимера бромида в эпидемический сезон имеет большое значение для профилактики ОРИ и COVID-19, так как это дает возможность контролировать заболеваемость даже в когорте лиц, находящихся в группе повышенного риска инфицирования, при этом препарат обладает высоким профилем безопасности.
Сведения об авторах:
Омарова Хадижат Гаджиевна — к.м.н., старший научный сотрудник клинического отдела инфекционной патологии ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0002-9682-2230.
Плоскирева Антонина Александровна — д.м.н., заместитель директора по клинической работе ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; профессор кафедры педиатрии с инфекционными болезнями у детей факультета дополнительного профессионального образования РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-3612-1889.
Агаркова Ирина Александровна — статистик отдела клинических исследований ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0000-0000-0000.
Горелов Александр Васильевич — академик РАН, д.м.н., профессор, заместитель директора по научной работе ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; заведующий кафедрой инфекционных болезней и эпидемиологии ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России; 127473, Россия, Москва, ул. Делегатская, д. 20, стр. 1; ORCID iD 0000-0001-9257-0171.
Контактная информация: Омарова Хадижат Гаджиевна, e-mail: omarova@cmd.su.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 02.09.2022.
Поступила после рецензирования 27.09.2022.
Принята в печать 20.10.2022.
About the authors:
Khadijat G. Omarova — C. Sc. (Med.), Senior Researcher, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being; 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; ORCID iD 0000-0002-9682-2230.
Antonina A. Ploskireva — Dr. Sc. (Med.), Deputy Director for Clinical Practice, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being; 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; Professor of the Department of Pediatrics with Children’s Infectious Diseases, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0002-3612-1889.
Irina A. Agarkova — statistician of the Department of Clinical Research, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being; 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; ORCID iD 0000-0000-0000-0000.
Aleksandr V. Gorelov — Academician of RAS, Dr. Sc. (Med.), Deputy Director for Research, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being; 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; Head of the Department of Infectious Diseases and Epidemiology, A.I. Yevdokimov Moscow State University of Medicine and Dentistry; 20/1, Delegatskaya str., Moscow, 127473, Russian Federation; ORCID iD 0000-0001-9257-0171.
Contact information: Khadijat G. Omarova, e-mail: omarova@cmd.su.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 02.09.2022.
Revised 27.09.2022.
Accepted 20.10.2022.
2. О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2021 году: Государственный доклад. М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека; 2022.
3. WHO. Оценка рисков контакта с вирусом COVID-19 для медицинских работников и ведение контактировавших. Временные рекомендации. 4 марта 2020. (Электронный ресурс.) URL: https://apps.who.int/iris/bitstream/handle/10665/331725/WHO-2019-nCov-HCW_risk_assessment-2020.1-rus.pdf?sequence=1&isAllowed=y.
4. Sant’Ana G., Imoto A.M., Amorim F.F. et al. Infection and death in healthcare workers due to COVID-19: a systematic review. Acta Paul Enferm. 2020;33:eAPE20200107. DOI: 10.37689/acta-ape/2020AO0107.
5. Coronavirus latest: WHO says health workers account for 10% of global infections. (Electronic resource.) URL: https://www.dw.com/en/coronavirus-latest-who-says-health-workers-account-for-10-of-global-infections/a-54208221 (access date: 04.02.2021).
6. Nguyen L.H., Drew D.A., Graham M.S. et al. Risk of COVID-19 among front-line health-care workers and the general community: a prospective cohort study. Lancet Public Health. 2020;5(9):e475–e483. DOI: 10.1016/S2468-2667(20)30164-X.
7. Временные методические рекомендации. Лекарственная терапия острых респираторных вирусных инфекций (ОРВИ) в амбулаторной практике в период эпидемии COVID-19, версия 2 (16.04.2020).
8. Караулов А.В., Горелов А.В. Применение азоксимера бромида в терапии инфекционно-воспалительных заболеваний органов дыхания у детей: метаанализ контролируемых клинических исследований. Журнал инфектологии. 2019;11(4):31–41. DOI: 10.22625/2072-6732-2019-11-4-31-41.
9. Вавилова В.П. Применение отечественного иммуномодулятора Полиоксидония в практике лечения детей с патологией лимфоглоточного кольца. Аллергология и иммунология в педиатрии. 2005;1(4):47–53.
10. Вавилова В.П., Вавилов А.М., Черкаева А.Х. Возможности современной терапии острых респираторных вирусных инфекций у детей. Consilium Medicum. Педиатрия (Прил.). 2015;3:76–81.
11. Пинегин Б.В., Дагиль Ю.А., Воробьева Н.В., Пащенков М.В. Влияние азоксимера бромида на формирование внеклеточных нейтрофильных ловушек. РМЖ. 2019;1(II):42–46.
12. Харит С.М., Галустян А.Н. Азоксимера бромид — безопасный и эффективный препарат при лечении острых респираторных инфекций верхних дыхательных путей у детей: обзор результатов двойных слепых плацебо-контролируемых рандомизированных клинических исследований II и III фазы. Педиатрия (Прил. к журн. Consilium Medicum). 2017;2:55–61.
13. Михайленко А.А., Макаренко О.С., Самошин О.А., Сизякова Р.И. Профилактика гриппа и ОРЗ с помощью сублингвального применения полиоксидония®. Иммунология. 2005;26(4):215–217.
14. Скачков М.В. Безопасность и эффективность Полиоксидония для профилактики ОРЗ у длительно и часто болеющих пациентов. РМЖ. 2008;22:1492.
15. Костинов М.П., Свитич О.А., Маркелова Е.В. Потенциальная иммунопрофилактика COVID-19 у групп высокого риска инфицирования. Временное пособие для врачей. М.: Группа МДВ; 2020.
16. Вавилова В.П., Вавилов А.М., Перевощикова Н.К. и др. Опыт профилактики новой коронавирусной инфекции (COVID-19) у медицинских работников. Терапия. 2020;6:93–102. DOI: 10.18565/therapy.2020.6.93-102.
17. Вавилова В.П., Вавилов А.М., Перевощикова Н.К. и др. Способ профилактики острых респираторных инфекций и COVID-19 у медицинских работников. Терапия. 2021;7(4):114–123. DOI: 10.18565/therapy.2021.4.114-123.
18. Касьяненко К.В., Мальцев О.В., Козлов К.В. и др. Оценка профилактической эффективности и безопасности азоксимера бромида у медицинских работников, находящихся в контакте с пациентами, госпитализированными по поводу COVID-19. Эпидемиология и вакцинопрофилактика. 2022;21(1):67–73. DOI: 10.31631/2073-3046-2022-21-1-67-73.
19. Efimov S.V. Letter to the editor: Experience of medical professionals with Azoximer bromide as prophylactic treatment for COVID-19 patients in Chuvashia Republic, Russia. Infect Dis Trop Med. 2021; 7: e721.
20. Официальный интернет-ресурс для информирования населения о коронавирусе (COVID-19). (Электронный ресурс.) URL: https://стопкоронавирус.рф/ (дата обращения: 04.02.2021).
21. Multicenter double-blind placebo-controlled randomized comparative clinical study to investigate efficacy and safety of use of 12 mg Polyoxidonium® tablets (LLC "NPO Petrovax Pharm") as part of combined therapy of acute upper respiratory infections of children aged 3–14 years: Clinical Study Report. Moscow Region: LLC "NPO Petrovax Pharm". M.; 2008.
22. Yang Y., Koh D., Ng V. et al. Self perceived work related stress and the relation with salivary IgA and lysozyme among emergency department nurses. Occup Environ Med. 2002;59(12):836–841. DOI: 10.1136/oem.59.12.836.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.

