Пандемия новой коронавирусной инфекции в Кабардино-Балкарской Республике. Опыт региона
Цель исследования: провести анализ различных клинических показателей у больных с новой коронавирусной инфекцией и определить основные маркеры заболевания.
Материал и методы: было проанализировано 55 историй болезни пациентов с диагнозом «новая коронавирусная инфекция (COVID-19)». Было выделено 5 групп пациентов: 1-я группа — легкое течение, 2-я группа — среднетяжелое течение со степенью поражения легких на КТ до 25% объема, 3-я группа — среднетяжелое течение со степенью поражения легких на КТ 25–50% объема, 4-я группа — тяжелое течение, 5-я группа — крайне тяжелое течение. Обследование включало проведение клинико-биохимических исследований, коагулограммы, определение РНК SARS-CoV-2 методом полимеразной цепной реакции (ПЦР), а также антител IgM и IgG к нуклеокапсидному белку бета-коронавируса SARS-CoV-2 методом иммуноферментного анализа.
Результаты исследования: установлено, что в клинической картине COVID-19 значимыми являются проявления гастроэнтероколита (13 пациентов, 23,6%) и кожных высыпаний (3 пациентки, 5,5%) наряду с интоксикационным синдромом. У пациентов в зависимости от степени тяжести обнаруживается эритропения (3,51±0,1×1012/л в группе крайне тяжелого течения), лейкопения (2,93±0,1×109/л в группе крайне тяжелого течения) и увеличение скорости оседания эритроцитов (46,14±2,0 мм/ч в группе крайне тяжелого течения), что имеет достоверные отличия от показателей групп со среднетяжелой и тяжелой степенью тяжести заболевания. Уровни С-реактивного белка (СРБ), D-димера, ферритина имеют статистически достоверные отличия (р<0,01) и повышаются в группах в зависимости от тяжести течения COVID-19, например, уровень СРБ повышается более чем в 15 раз. Установлена прямая корреляционная взаимосвязь (r=0,68, p<0,01) между повышением уровня СРБ и тяжестью течения COVID-19. Зарегистрирована прямая корреляционная связь повышения уровня СРБ, интерлейкина-6 (ИЛ-6) и тяжести течения COVID-19 (r=0,56, p<0,05), что позволяет утверждать, что повышение уровня СРБ и ИЛ-6 является маркером тяжести COVID-19.
Заключение: таким образом, в исследовании выделены клинические «маски» COVID-19: кишечная (23,6% больных) и кожная (5,5% больных). В ранние сроки заболевания до формирования пневмонии ПЦР-диагностика COVID-19 является более информативной, что подтверждает наличие 100% положительных результатов мазка ПЦР на РНК SARS-CoV-2 в группе легкого течения COVID-19 и 100% отрицательных результатов мазка ПЦР на РНК SARS-CoV-2 в группе крайне тяжелого течения заболевания.
Ключевые слова: новая коронавирусная инфекция, COVID-19, D-димер, ферритин, сатурация, процент поражения, клинические маски.
Для цитирования: Шогенова М.С., Хутуева С.Х., Тлупова И.Б., Аккиева М.А., Шогенова Л.С. Пандемия новой коронавирусной инфекции в Кабардино-Балкарской Республике. Опыт региона. РМЖ. Медицинское обозрение. 2021;29(6):9-13.
The pandemic of a new coronavirus infection in the Kabardino-Balkarian Republic. Regional experience
M.S. Shogenova1,2, S.Kh. Khutueva1, I.B. Tlupova1, M.A. Akkieva1, L.S. Shogenova2
1Center of Allergology of the Ministry of Health of the KBR, Nalchik
2Kabardino-Balkarian State University named after H.M. Berbekov, Nalchik
Aim: to analyze various clinical indicators in patients with a new coronavirus infection and determine the main disease markers.
Patients and Methods: 55 case histories of patients diagnosed with new coronavirus infection (COVID-19) were analyzed. There were 5 groups: group 1 — mild course; group 2 —moderate course with lung damage up to 25% (according to CT); group 3 — moderate course with lung damage 25–50% (according to CT); group 4 — severe course; group 5 — extremely severe course. The examination included clinical and biochemical studies, coagulogram, determination of SARS-CoV-2 RNA by polymerase chain reaction (PCR), as well as IgM and IgG antibodies to the SARS-CoV-2 betacoronavirus nucleocapsid protein by enzyme immunoassay.
Results: it was found that in the COVID-19 clinical picture, the manifestations of gastroenterocolitis (13 patients, 23.6%) and cutaneous eruption (3 patients, 5.5%), along with intoxication syndrome, were significant. In patients depending on the severity of detected eritropeniya (3,51±0,1×1012/L in group 5), leukopenia (2,93±0,1×109/L in group 5) and elevated ESR (46,14±2.0 mm/h in group 5), which has significant differences versus the groups 3 and 4. Acute-phase proteins — C-reactive protein (CRP), D-dimer, ferritin — had statistically significant differences (p<0.01) and increased in groups depending on the COVID-19 course, for instance, CRP increased more than 15 times. A direct correlation was established (r=0.68, p<0.01) between CRP level and COVID-19 course. A direct correlation was recorded between an increase in the level of CRP, interleukin-6 (IL-6) and COVID-19 course (r=0.56, p<0.05), which suggests that CRP and IL-6 are markers of COVID-19 severity.
Conclusion: thus, the study identified clinical COVID-19 masks —intestinal (23.6% of patients) and cutaneous (5.5% of patients). At the disease onset before the pneumonia occurrence, the PCR diagnosis of COVID-19 is more informative, which confirms the presence of 100% positive results of a PCR smear on SARS-CoV-2 RNA in group 1 and 100% negative results of a PCR smear on SARS-CoV-2 RNA in group 5.
Keywords: new coronavirus infection, COVID-19, D-dimer, ferritin, saturation, lung damage rate, clinical masks.
For citation: Shogenova M.S., Khutueva S.Kh., Tlupova I.B. et al. The pandemic of a new coronavirus infection in the Kabardino-Balkarian Republic. Regional experience. RMJ. 2021;6:9–13 (in Russ.).
Введение
В настоящее время мир переживает пандемию нового вирусного заболевания COVID-19 (от англ. Coronavirus Disease 2019), обусловленного обнаруженным в декабре 2019 г. новым штаммом коронавирусов SARS-CoV-2 (Severe Acute Respiratory Syndrome, Coronavirus-2) [1]. Первые случаи заболевания были зарегистрированы в г. Ухане провинции Хубей в Китае в декабре 2019 г. [2], а уже 11 марта 2020 г. ВОЗ официально классифицировала эпидемическую ситуацию как пандемию.
По состоянию на 7 декабря 2020 г. в 213 странах мира выявлено 67,0 млн случаев COVID-19, 1,54 млн человек скончались в результате этого заболевания [3]. По мнению многих экспертов, фактическое количество случаев COVID-19 во всем мире значительно выше, чем официально подтвержденное. Определенная доля случаев заболевания может оставаться не диагностированной [4]. Как показывает опыт китайского регистра по COVID-19, около 1/3 пациентов с характерной клинической и рентгенологической картиной имеют отрицательный результат тестирования методом полимеразной цепной реакции (ПЦР) на SARS-CoV-2 при заборе материала из верхних дыхательных путей [5–7]. В России на 01.04.2021 было официально подтверждено более 2,49 млн случаев COVID-19, из которых 43 597 закончились летально [8].
По информации оперативного штаба КБР, на 07.12.2020 выявлено 13 392 заболевших, новых за сутки — 98, на лечении — 2555, умерших — 231. В госпиталях получают медицинскую помощь 1446 пациента, в реанимационных отделениях — 88 человек.
По данным Минздрава КБР, для лечения новой коронавирусной инфекции на момент написания статьи в республике развернуто 9 госпиталей особо опасных инфекций (ГООИ) на базе 8 организаций на 1859 коек, в том числе 778 коек с кислородной подводкой, оснащенных в соответствии с нормативом Минздрава России. План Минздрава России по нормативной потребности в койках, разворачивающихся с учетом развития прогнозных сценариев распространения COVID-19, выполнен на 178%. КБР занимает 11-е место среди регионов по обеспеченности койками — 196 коек на 100 000 населения.
Общее количество дыхательной аппаратуры, предусмотренной для оказания помощи больным COVID-19 в развернутых ГООИ, включая резерв аппаратов в иных медицинских организациях, составляет 152 единицы, в том числе 76 аппаратов для инвазивной вентиляции легких (ИВЛ) и 76 — для неинвазивной ИВЛ. Дополнительно в резерве 32 аппарата ИВЛ, переданных Минпромторгом России, поставлено еще 10 аппаратов ИВЛ, закупленных ранее.
В ГБУЗ «Центр аллергологии» Минздрава КБР» в соответствии с приказом Минздрава КБР от 16.03.2020 № 87-П «О плане перепрофилирования медицинских организаций в случае выявления новой коронавирусной инфекции (2019-ncov) в Кабардино-Балкарской Республике» аллерго-иммунологические койки были перепрофилированы в инфекционные [9]. Развернуто инфекционное отделение на 40 коек с 26.03.2020 по 27.08.2020, и с 14.09.2020 по приказу Минздрава КБР от 10.09.2020 № 293-П «Об открытии госпиталя особо опасных инфекций в государственном бюджетном учреждении здравоохранения «Центральная районная больница» г.о. Прохладный и Прохладненского муниципального района» [10] возобновлена работа инфекционного отделения Центра аллергологии, которое функционирует по настоящее время.
В ГБУЗ «Центр аллергологии» Минздрава КБР» осуществляется сортировка больных с дальнейшей маршрутизацией в ГООИ для проведения лечения.
Цель исследования: в условиях инфекционного (нековидного) отделения провести анализ различных клинических показателей у больных с новой коронавирусной инфекцией и изучить основные маркеры заболевания.
Материал и методы
За период с 26.03.2020 по 27.08.2020 в инфекционном отделении ГБУЗ «Центр аллергологии» Минздрава КБР» пролечено 390 больных, из них с установленным диагнозом: новая коронавирусная инфекция — 80, кишечная инфекция — 176, вирусная инфекция (ОРВИ, герпес-вирусная инфекция) — 55, ангина — 23, вирусные гепатиты — 17, цирроз печени — 6, рожистое воспаление — 13, ВИЧ — 11, менингит — 2, сепсис — 2, рак печени — 1, рак толстой кишки — 1. Летальных исходов было 3.
Организация медицинской помощи, обследование и лечение пациентов с COVID-19 проводились в соответствии с временным Порядком организации работы медицинских организаций в целях реализации мер по профилактике и снижению рисков распространения новой коронавирусной инфекции COVID-19, утвержденных приказом Минздрава России от 19.03.2020 № 198н [11].
Нами было проведено ретроспективное исследование. Из 80 историй болезни пациентов с диагнозом COVID-19 были включены в работу 55 историй болезни пациентов, которым были проведены все требуемые дизайном исследования методы. Среди обследованных 55 больных с установленным диагнозом новой коронавирусной инфекции мужчины составили 52,7% (29 больных), женщины — 47,3% (26 больных). Средний возраст составил 52,2±4,6 года. Обследование включало проведение клинико-биохимических исследований (общий анализ крови, глюкоза крови, общий анализ мочи, общий белок, билирубин крови, аланинаминотрансфераза (АЛТ), аспартатаминотрасфераза (АСТ), креатинин крови, мочевина, сывороточное железо, ферритин, С-реактивный белок (СРБ)) с использованием автоматического биохимического анализатора MIURA ONE (I.S.E., Италия), коагулограммы (протромбиновый индекс (ПТИ), международное нормализованное отношение (МНО), D-димер) на автоматическом коагулометре ACL Elite Pro (Instrumentation Laboratory, США), определение РНК SARS-CoV-2 методом ПЦР, а также антител IgM и IgG к нуклеокапсидному белку бета-коронавируса SARS-CoV-2 методом иммуноферментного анализа (ИФА) на микропланшетном ридере Аnthos 2020 (Biochrom, Великобритания). Инструментальные методы диагностики включали рентгенографию органов грудной клетки (рентген цифровой Siemens Luminos Rf Classic, Германия), КТ органов грудной клетки (General Electric Optima CT660, 64-срезовый, США), ЭКГ. Проводилось иммунологическое обследование с определением уровня ИЛ-6 методом ИФА на микропланшетном ридере Аnthos 2020, а также основных субпопуляций лимфоцитов при помощи цитофлуориметра BD FACSCanto II (Becton Diskinson, США).
Для исследования было выделено 5 групп пациентов в зависимости от степени тяжести: 1-я группа — легкое течение, 2-я группа — среднетяжелое течение с процентом поражения (ПП) легких на КТ до 25% объема, 3-я группа — среднетяжелое течение с ПП легких на КТ 25–50% объема, 4-я группа — тяжелое течение, 5-я группа — крайне тяжелое течение.
Статистическая обработка данных проводилась с помощью пакета прикладных программ Statistica Windows 10.0. Оценка распределения и разброса данных проводилась при помощи расчета среднего значения (М±m) для исследуемых величин. Достоверность полученных данных представлена по критерию Стьюдента и Манна — Уитни (для малых выборок). Статистически значимой считалась величина коэффициента p<0,05. Определена корреляционная зависимость показателей по критерию Спирмена (p<0,05).
Результаты исследования
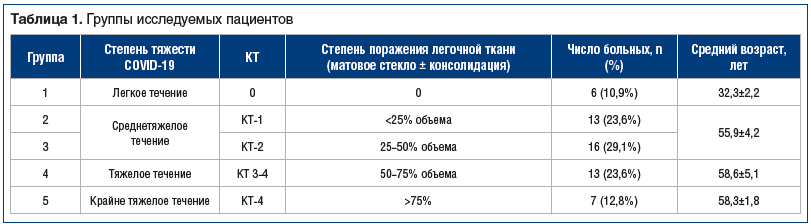
Пациенты классифицированы по степени тяжести заболевания. ПП легочной ткани (матовое стекло ± консолидация) оценивался по результатам КТ по 4 степеням (табл. 1).
В группе легкого течения из 6 пациентов у 5 (83,3%) преобладали проявления гастроэнтероколита, у 1 (16,7%) — кожная сыпь (крапивница), интоксикационный синдром у данной категории больных отсутствовал Эпидемиологический анамнез был положительным у 4 пациентов (66,7%), отрицательный — у 2 (33,3%). Сопутствующие заболевания отсутствовали. Обследованные этой группы имели 100% положительный результат мазка на РНК SARS-CoV-2 методом ПЦР. Сатурация составляла 99,33±0,3%, что исключает дыхательную недостаточность (ДН).
В группе со среднетяжелым течением зарегистрировано 29 больных. У 23 пациентов (79,3%) превалировал интоксикационный синдром, у 4 (13,8%) — проявления гастроэнтероколита. Эпидемиологический анамнез положительный отмечался у 10 пациентов (34,5%), отрицательный — у 19 (65,5%). Положительный результат мазка на РНК SARS-CoV-2 методом ПЦР установлен у 12 пациентов (41,4%), отрицательный — у 17 (58,6%). У 19 пациентов (65,5%) инфекция COVID-19 развилась на фоне сопутствующих заболеваний (сахарный диабет 2 типа, ревматоидный артрит, бронхиальная астма, хроническая обструктивная болезнь легких, гипертоническая болезнь, стенокардия, цереброваскулярная болезнь). У 13 больных (23,6%) среднее значение ПП составило 11,7±1,5%, сатурация — 93,31±0,4% (с достоверными отличиями от показателей пациентов с легким течением, р<0,01), что соответствует ДН 1-й степени. У 16 (29,1%) средний ПП составил 32,4±2,3%, сатурация — 92,63±0,4% (с достоверными отличиями показателей пациентов с легким течением, р<0,01), что характерно для ДН 1-й степени.
В группе тяжелого течения у 9 пациентов (69,2%) в клинической картине интоксикационный синдром был ведущим, 4 больных (30,8%) имели проявления гастроэнтероколита. Все больные этой группы имели сопутствующие заболевания, ведущей патологией было ожирение. У 8 пациентов (61,5%) зарегистрировано совпадение эпидемиологического анамнеза с положительными результатами мазка на РНК SARS-CoV-2 методом ПЦР. Средний ПП легочной ткани у обследованных больных составил 60,4±2,7%, сатурация — 88,62±0,7% (с достоверными отличиями показателей пациентов с легким течением, р<0,01), что является признаком ДН 2-й степени.
У всех больных группы с крайне тяжелым течением основным клиническим синдромом был интоксикационный. Результаты всех мазков на РНК SARS-CoV-2 методом ПЦР были отрицательными, несмотря на положительный эпидемиологический анамнез. Средний ПП легочной ткани в группе составлял 82,4±0,8%, сатурация — 82,43±2,3% (с достоверными отличиями от показателей пациентов с легким течением, р<0,01), с проявлениями ДН 2-й степени.
По результатам исследования установлено, что только 13 (24,6%) пациентов имели положительный результат мазка на РНК (SARS-CoV-2) методом ПЦР и пневмонию по результатам КТ ОГК, в остальных 42 (75,4%) случаях пневмония диагностирована, но результаты мазка на РНК (SARS-CoV-2) методом ПЦР были отрицательными.
Сложности ПЦР-диагностики на РНК SARS-CoV-2 заключаются в том, что отрицательный результат не гарантирует отсутствия SARS-CoV-2 в организме. Для исследования берется мазок из носоротоглотки — места, где новый коронавирус находится ограниченное время на начальном этапе инфицирования. Для вируса слизистая верхних дыхательных путей — это транзитный путь, чтобы проникнуть в организм, что подтверждает масса литературных источников и информация от коллег, в первую очередь азиатских, которые первыми встретили эпидемию COVID-19 [3, 6]. Инкубационный период составляет от 2 до 14 сут, в среднем 5–7 сут [12]. Именно поэтому отмечается такой большой процент отрицательных тестов, когда человек инфицирован, а анализ этого не подтверждает, ведь, как правило, исследуется биоматериал, когда в нем уже нет вируса, — на 7-е (и более) сутки от начала заболевания. По данным иностранных коллег, доля таких тестов составляет от 40% до 60% [3, 5, 6, 12]. Рекомендованный материал для ПЦР-анализа — мокрота из нижних дыхательных путей и бронхоальвеолярный лаваж (лечебная бронхоскопия) [13, 14]. Но технические сложности получения материала лимитируют его использование. Мокроты у пациента может не быть (при новой коронавирусной инфекции кашель чаще сухой и непродуктивный), лаваж можно получить только в условиях стационара, и даже в этих условиях провести процедуру не всегда возможно технически и клинически [7].
У 44,4% пациентов в нашем исследовании был установлен факт наличия антител класса IgM и IgG к SARS-CoV-2 в период нахождения в инфекционном отделении. При определении антител IgM и IgG к нуклеокапсидному белку бета-коронавируса SARS-CoV-2 методом ИФА у обследованных пациентов наличия корреляции со степенью тяжести не получено.
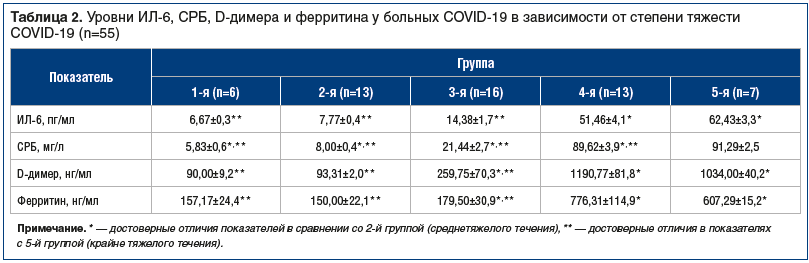
Нами изучены уровни ИЛ-6, СРБ, D-димера и ферритина у больных COVID-19 в зависимости от степени тяжести болезни (табл. 2).
Обсуждение
Проведя анализ уровня кислорода крови пациентов разных групп, можно отметить, что сатурация является маркером тяжести COVID-19 и прямо пропорционально связана с тяжестью течения COVID-19 в группах со среднетяжелым и тяжелым течением (r=0,72, р<0,01).
По результатам проведенного анализа в группах пациентов установлено, что в клинической картине COVID-19 для дифференциации диагноза существенными являются проявления гастроэнтероколита, кожных высыпаний наряду с интоксикационным синдромом. У 13 пациентов (23,6%) зарегистрирован гастроэнтероколит как первое клиническое проявление заболевания. По данным литературы [13, 15], это связано с тем, что эпителиоциты желудка и кишечника, как и эпителий верхних дыхательных путей, являются входными воротами для возбудителя. В соответствии с современными представлениями рецепторы ангиотензинпревращающего фермента II типа (рАПФ2) и клеточная трансмембранная сериновая протеаза типа 2 (ТСП2) экспрессированы на поверхности различных клеток, в том числе кишечника, что связывают с генерализацией коронавирусной инфекции в кишечнике с явлениями гастроэнтероколита [16]. Частота возникновения поражений ЖКТ при COVID-19 варьирует в пределах от 0,4% до 29,3% [17]. Так, у пациентов с впервые возникшими симптомами поражения пищеварительного тракта, особенно после возможного контакта с пациентом с COVID-19, следует подозревать наличие заболевания даже при отсутствии кашля, одышки, боли в горле или лихорадки [18]. У 5,5% (3 пациентки, беременные) дебют заболевания возник с кожных высыпаний — острой крапивницы. Описаны типичные для COVID-19 кожные проявления — от геморрагического синдрома до высыпаний различного вида, патогенез которых неясен [13].
По результатам исследований [12, 19, 20] выделены клинические и морфологические «маски» COVID-19: сердечная, мозговая, кишечная, почечная, печеночная, диабетическая, тромбоэмболическая, септическая, микроангиопатическая, кожная. Наши данные согласуются с мнением экспертов. В группе легкого течения выделены клинические «маски» COVID-19: у 23,6% больных — кишечная, у 5,5% — кожная.
При общеклиническом обследовании зарегистрированы достоверные изменения лабораторных показателей в группах со среднетяжелым и тяжелым течением заболевания. Так, у пациентов в зависимости от степени тяжести обнаруживалась эритропения, лейкопения, тромбоцитопения и увеличение скорости оседания эритроцитов, что имеет достоверные отличия от показателей пациентов из групп со среднетяжелой и тяжелой степенью тяжести заболевания (р<0,01). Исключением была разница показателей лимфоцитов и эозинофилов. По данным авторов [19, 21], у больных COVID-19 с тяжелым течением наблюдается лимфопения, но в нашем исследовании разница в показателях уровня лимфоцитов в группах с легким и крайне тяжелым течением (33,67±5,5% и 26,29±3,3% соответственно) на 22% не имела достоверных различий.
Согласно нашим исследованиям ПЦР-диагностика COVID-19 информативна в ранние сроки заболевания, до формирования пневмонии, что подтверждает наличие 100% положительных результатов мазка ПЦР на РНК SARS-CoV-2 в группе легкого течения и 100% отрицательных результатов мазка ПЦР в группе крайне тяжелого течения.
На основании анализа показателей иммунологического обследования пациентов с COVID-19 (Т-лимфоциты, Т-хелперы, В-лимфоциты) достоверных изменений в группах не зарегистрировано ни в абсолютных, ни в относительных значениях. Можно отметить некоторое снижение уровня В-лимфоцитов (CD19+, CD45+) у пациентов со среднетяжелым (10,9±2,7%) и тяжелым течением (11,8±3,1%) (норма — 21–28%).
При изучении уровня ИЛ-6 отмечено, что в зависимости от степени тяжести болезни во всех обследованных группах уровень этого показателя стремительно возрастал — от 6,67±0,3 пг/мл при легком течении заболевания до 62,43±3,3 пг/мл при тяжелом течении. Зарегистрированы достоверные отличия в показателях при тяжелом течении заболевания (р<0,01). Такая же тенденция отмечается и в работах других авторов [22, 23].
Анализ показателей белков воспаления при COVID-19 показал, что в обследованных группах уровни СРБ, а также D-димера и ферритина имеют статистически достоверные отличия и повышаются в зависимости от тяжести течения COVID-19.
Так, уровень СРБ повышался более чем в 15 раз — с 5,83±0,65 мг/л в группе с легким течением до 91,29±2,5 мг/л в группе крайне тяжелого течения COVID-19 (p<0,01). Уровень D-димера статистически достоверно был повышен в группах тяжелого и крайне тяжелого течения в сравнении с группами с легким и среднетяжелым течением заболевания (р<0,01). Аналогичная ситуация наблюдалась со значениями ферритина — в группах тяжелого и крайне тяжелого течения наблюдалось повышение показателя в 3–4 раза по сравнению со значениями группы с легким течением заболевания (p<0,01). Как видно, уровни D-димера и ферритина возрастают у больных с тяжелым течением COVID-19, у крайне тяжелых пациентов эти показатели немного снижаются, но они достаточно далеки от нормальных значений. Значения СРБ повышены весь период заболевания.
Заключение
У пациентов, включенных в исследование, выявлены клинические «маски» COVID-19: кишечная (у 23,6%) и кожная (у 5,5%). В ранние сроки заболевания, до формирования пневмонии, ПЦР-диагностика COVID-19 является более информативной, что подтверждает наличие 100% положительных результатов мазка ПЦР на РНК SARS-CoV-2 в группе легкого течения COVID-19 и 100% отрицательных результатов мазка ПЦР на РНК SARS-CoV-2 в группе крайне тяжелого течения заболевания. В исследовании подтверждено, что сатурация крови является маркером тяжести COVID-19, имеет прямо пропорциональную зависимость от тяжести течения COVID-19 в группах со среднетяжелым и тяжелым течением (r=0,72, р<0,01).
2. Zhu N., Zhang D., Wang W. et al. A novel coronavirus from patients with pneumonia in China, 2019. N Engl J Med. 2020;382(8):727–733. DOI: 10.1056/NEJMoa2001017.
3. Coronavirus disease (COVID-19) Pandemic. (Electronic resource.) URL: https://www.who.int/emergencies/diseases/novel-coronavirus-2019 (access date: 10.12.2020).
4. Баклаушев В.П., Кулемзин С.В., Горчаков А.А. и др. COVID-19: этиология, патогенез, диагностика и лечение. Клиническая практика. 2020;11(1):7–20. [Baklaushev V.P., Kulemzin S.V., Gorchakov A.A. et al. COVID-19: etiology, pathogenesis, diagnosis and treatment. Clinical practice. 2020;11(1):7–20 (in Russ.)].
5. Qin C., Zhou L., Hu Z. et al. Dysregulation of immune response in patients with COVID-19 in Wuhan, China. Clin Infect Dis. 2020;71(15):762–768. DOI: 10.1093/cid/ciaa248.
6. Yang Y., Yang M.H., Shen C.G. et al. Evaluating the accuracy of different respiratory specimens in the laboratory diagnosis and monitoring the viral shedding of 2019-nCoV infections. medRxiv. 2020; published online Feb 17. DOI: 10.1101/2020.02.11.20021493.
7. Рассохин В.В., Самарина А.В., Беляков Н.А. и др. Эпидемиология, клиника, диагностика, оценка тяжести заболевания COVID-19 с учетом сопутствующей патологии. ВИЧ-инфекция и иммуносупрессии. 2020;12(2):7–30 [Rassokhin V.V., Samarina A., Belyakov N.A. at al. Epidemiology, clinic, diagnosis, assessment of the severity of the COVID-19 disease, taking into account concomitant pathology. HIV infection and immunosuppression. 2020;12(2):7–30 (in Russ.)].
8. Официальный интернет-ресурс для информирования населения по вопросам коронавируса (COVID-19), 2020. Стопкоронавирус.рф (Электронный ресурс.) URL: https://xn—80aesfpebagmfblc0a.xn — p1ai (дата обращения: 7.12.2020) [Official Internet resource for informing the public about coronavirus (COVID-19), 2020. Stopcoronavirus.RF. (Electronic resource.) URL: https://xn—80aesfpebagmfblc0a.xn — p1ai/ (access date: 7.12.2020) (in Russ.)].
9. Приказ Минздрава КБР от 16.03.2020 № 87-П «О плане перепрофилирования медицинских организаций в случае выявления новой коронавирусной инфекции (2019-ncov) в Кабардино-Балкарской Республике». (Электронный ресурс.) URL: https://docs.cntd.ru/document/570715817 (дата обращения: 28.11.2020). [Order of the Ministry of Health of the KBR of 16.03.2020 No. 87-P «On the plan for re-profiling Medical Organizations in case of detection of a new coronavirus infection (2019-ncov) in the Kabardino-Balkar Republic». (Electronic resource.) URL: https://docs.cntd.ru/document/570715817 (access date: 28.11.2020) (in Russ.)].
10. Приказ Минздрава КБР от 10 сентября 2020 г. № 293-П «Об открытии госпиталя особо опасных инфекций в государственном бюджетном учреждении здравоохранения «Центральная районная больница» г.о. Прохладный и Прохладненского муниципального района». (Электронный ресурс.) URL: https://docs.cntd.ru/document/570945137 (дата обращения: 14.11.2020). [Order of the Ministry of Health of the KBR of September 10, 2020 N 293-P «On the opening of a hospital for particularly dangerous infections in the state budgetary health institution «Central District Hospital» of the city of Cool and Cool municipal district». (Electronic resource.) URL: https://docs.cntd.ru/document/570945137 (access date: 14.11.2020) (in Russ.)].
11. Приказ Минздрава России от 19.03.2020 № 198н «О временном порядке организации работы медицинских организаций в целях реализации мер по профилактике и снижению рисков распространения новой коронавирусной инфекции COVID-19». (Электронный ресурс.) URL: https://docs.cntd.ru/document/564482310 (дата обращения: 18.11.2020) [Order of the Ministry of Health of the Russian Federation of 19.03.2020 No. 198n. On the temporary procedure for organizing the work of medical organizations in order to implement measures to prevent and reduce the risks of spreading the new coronavirus infection COVID-19. (Electronic resource.) URL: https://docs.cntd.ru/document/564482310 (access date: 18.11.2020) (in Russ.)].
12. Wong S.H., Lui R.N., Sung J.J. COVID-19 and the Digestive System. J Gastroenterol Hepatol. 2020;35(5):744–748. DOI: 10.1111/jgh.15047.
13. Временные методические рекомендации «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)» и их систематически обновленные версии (версия 9 от 26.10.2020. (Электронный ресурс.) URL: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/052/550/original/%D0%9C%D0%A0_COVID-19_%28v9%29.pdf?1603788097 (дата обращения: 15.12.2020) [Provisional guidelines «Prevention, diagnosis and treatment for novel coronavirus infection (COVID-19)» and their regularly updated versions (version 9 26.10.2020). (Electronic resource.) URL: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/052/550/original/%D0%9C%D0%A0_COVID-19_%28v9%29.pdf?1603788097 (access date: 15.12.2020) (in Russ.)].
14. Митьковская Н.П., Карпов И.А., Арутюнов Г.П. и др. Коронавирусная инфекция COVID-19 (обзор международных научных данных). Неотложная кардиология и кардиоваскулярные риски. 2020;4(1):784–816. [Mitkovckay N.P., Karpov I.A., Arutyunov G.P. et al. COVID-19 coronavirus infection (review of international scientific data). Emergency cardiology and cardiovascular risks. 2020;4(1):784–816 (in Russ.)].
15. Batlle D., Wysocki J., Satchell K. Soluble angiotensin-converting enzyme 2: a potential approach for coronavirus infection therapy? Clin Sci (Lond). 2020;134(5):543–545. DOI: 10.1042/ CS20200163.
16. Wevers B.A., van der Hoek L. Renin-angiotensin system in human coronavirus pathogenesis. Future Virol. 2010;5(2):145–161. DOI: 10.2217/fvl.10.4.
17. Ивашкин В.Т., Шептулин А.А., Зольникова О.Ю. и др. Новая коронавирусная инфекция (COVID-19) и система органов пищеварения. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2020;30(3):7–13. [Ivashkin V.T., Sheptulin A.A., Zolnikova O.Yu. et al. New coronavirus infection (COVID-19) and the digestive system. Russian journal of gastroenterology, hepatology and coloproctology. 2020;30(3):7–13 (in Russ.)].
18. Яковенко Э.П., Яковенко А.В., Иванов А.Н. и др. Патология пищеварительного тракта и печени при COVID-19. Экспериментальная и клиническая гастроэнтерология. 2020;4(176):19–23. [Yakovenko E.P., Yakovenko A.V., Ivanov A.N. et al. Pathology of the digestive tract and liver in COVID-19. Experimental and clinical gastroenterology. 2020;4(176):19–23 (in Russ.)].
19. Satyanath R., Kodidala J., Sorout S. et al. Physiological and clinical aspects in COVID-19. RUDN Journal of Medicine. 2020;24(3):201–206.
20. Шляхто Е.В., Конради А.О., Арутюнов Г.П. и др. Руководство по диагностике и лечению болезней системы кровообращения в контексте пандемии. М., 2020 [Shlyakhto E.V., Konradi A.O., Arutyunov G.P. et al. Guidelines for the diagnosis and treatment of diseases of the circulatory system in the context of a pandemic. Moscow, 2020 (in Russ.)].
21. Щелканов М.Ю., Колобухина Л.В., Бургасова О.А. и др. COVID-19: этиология, клиника, лечение. Инфекция и иммунитет. 2020;10(3):421–445. [Shchelkanov M. Yu., Kolobukhina L.V., Burgasova O.A. et al. COVID-19: etiology, clinic, treatment. Infection and immunity. 2020;10(3):421–445 (in Russ.)].
22. Conti P., Ronconi G., Caraffa A. et al. Induction of proinflammatory cytokines (IL-1 and IL-6) and lung inflammation by Coronavirus-19 (COVID-19 or SARS-CoV-2): anti-inflammatory strategies. J Biol Regul Homeost Agents. 2020;34(2):1.
23. Абатуров А.Е., Агафонова Е.А., Кривуша Е.Л., Никулина А.А. Патогенез COVID-19. Здоровье ребенка. 2020;15(2):133–144 [Abaturov A.E., Agafonova E.A., Krivusha E.L., Nikulina A.A. Pathogenesis of COVID-19. Zdorov’e rebenka. 2020;15(2):133–144 (in Russ.)].

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.