Особенности клиники сочетанных форм гриппа у детей
DOI: 10.32364/2587-6821-2020-4-11-665-669
Цель исследования: установить клинико-лабораторные особенности течения сочетанной инфекции вируса гриппа и других респираторных вирусов у детей.
Материал и методы: проанализированы данные историй болезни 139 детей в возрасте от 2 мес. до 18 лет, госпитализированных в профильный стационар г. Москвы с октября 2017 г. по февраль 2020 г. с клиническими проявлениями острых респираторных инфекций (ОРИ). Пациенты были распределены в 2 группы: 1-я группа — дети с сочетанной инфекцией гриппа и респираторного вируса (n=31); 2-я группа — дети с моноинфекцией гриппа (n=108). Этиологию ОРИ определяли методами: полимеразной цепной реакции (исследование мазков и/или отделяемого слизистой полости рта, носа, мокроты), иммуноферментного анализа (с определением антител к герпесвирусам 1, 2, 6-го типов, цитомегаловирусу, вирусу Эпштейна — Барр, хламидийной и микоплазменной инфекциям).
Результаты исследования: в качестве второго вирусного агента в большинстве случаев выступал респираторно-синцитиальный вирус (8/31), на 2-м месте — риновирус (5/31). Начало респираторной инфекции у детей 1-й группы регистрировалось в среднем за 2,60±1,6 дня до госпитализации, в 2-й группе — за 3,35±1,72 дня (p>0,05). Фебрильная лихорадка продолжалась у детей 1-й группы 4,72±1,25 дня, что почти на 2 дня больше, чем у детей 2-й группы (p<0,05). Частота развития осложнений при гриппе в группах сочетанной и моноинфекции различалась: развитие острого отита (катарального, среднего) отмечено у 35,5% и 8,3% детей (p<0,01), острого синусита — у 12,9% и 8,3%, пневмонии — у 22,6% и 7,4% соответственно.
Заключение: в целом клиническое течение гриппа, сочетанного с другим вирусным агентом, у детей характеризуется большей тяжестью, что определяется высоким уровнем лихорадки, более выраженными симптомами интоксикации, чаще возникающими осложнениями в виде отита, синусита, пневмонии, чаще требуется инфузионная терапия. Дети с сочетанной инфекцией быстрее поступают из поликлинического звена в стационар и госпитализируются на более длительный срок.
Ключевые слова: острые респираторные инфекции, грипп, риновирус, дети, лихорадка, интоксикация, тяжесть течения.
Для цитирования: Николаева С.В., Усенко Д.В., Шабалина С.В., Хлыповка Ю.Н., Медкова А.Ю., Горелов А.В. Особенности клиники сочетанных форм гриппа у детей. РМЖ. Медицинское обозрение. 2020;4(11):665-669. DOI: 10.32364/2587-6821-2020-4-11-665-669.
S.V. Nikolaeva1, D.V. Usenko1, S.V. Shabalina1, Yu.N. Khlypovka1,2,
A.Yu. Medkova2, A.V. Gorelov1,3
1Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being, Moscow, Russian Federation
2Central Clinical Hospital and Polyclinic, Moscow, Russian Federation
3I.M. Sechenov First Moscow State Medical University (Sechenov University), Moscow, Russian Federation
Aim: to identify the clinical laboratory features of coinfection with flu and other respiratory viral infections.
Patients and Methods: case records (inpatient files) of 139 children aged 2 months — 18 years who were admitted to Moscow hospitals from October 2017 to February 2020 with the clinical manifestations of acute respiratory infections (ARI) were analyzed. All children were divided into two groups. Group 1 included children with coexisted flu and other ARI (n=31). Group 2 included children with flu alone (n=108). The etiology of ARI was discovered by polymerase chain reaction (oral or nasal smears and/or discharge, sputum) and enzyme immunoassay (antibodies to herpesvirus type 1, 2, and 6, cytomegalovirus, Epstein-Barr virus, Chlamydia, and Mycoplasma).
Results: respiratory syncytial virus and rhinovirus were the most common viruses coexisted with flu (8/31 and 5/31, respectively). The onset of ARI occurred 2.60±1.6 days before hospital admission in group 1 and 3.35±1.72 days before hospital admission in group 2 (p>0.05). In group 1, febrile temperature lasted for 4.72±1.25 days that is almost 2 days longer than in group 2 (p<0.01). The rate of complications in coinfection with flu and ARI vs. flu alone was different, i.e., acute (catarrhal, medium) otitis was diagnosed in 35.5% and 8.3.% (p<0.01), respectively, acute sinusitis in 12.9% and 8.3%, respectively, and pneumonia in 22.6% and 7.4%, respectively.
Conclusion: in children, coinfection with flu and other respiratory virus is generally more severe as demonstrated by higher temperature, more severe intoxication symptoms, more common complications (e.g., otitis, sinusitis, pneumonia etc.), and a greater need in infusion therapy. Co-infected children are admitted to hospital more rapidly and stay in hospital for a longer period.
Keywords: acute respiratory infections, flu, rhinovirus, children, fever, intoxication, severity.
For citation: Nikolaeva S.V., Usenko D.V., Shabalina S.V. et al. Clinical presentation of flu coinfections in children. Russian Medical Inquiry. 2020;4(11):665–669. DOI: 10.32364/2587-6821-2020-4-11-665-669.
Введение
Острые респираторные инфекции (ОРИ) занимают лидирующее положение в структуре инфекционных болезней у детей и представляют собой серьезную проблему для здравоохранения. Наибольшие опасения традиционно вызывает грипп вследствие высокой заболеваемости, способности вызывать сезонные вспышки, эпидемии и пандемии, большой частоты госпитализаций и осложнений. Первая зарегистрированная в 1918 г. пандемия вируса гриппа H1N1 поразила более 500 млн человек по всему миру и унесла жизни около 100 млн человек (3–5% населения земного шара). Последняя пандемия вируса гриппа H1N1 была зафиксирована в 2009 г. и привела к гибели около 17 тыс. человек по всему миру. Циркуляция пандемического штамма вируса гриппа А (Н1N1) pdm09 сохраняется в настоящее время на всех континентах. Так, в Российской Федерации в 2018 г. его доля в структуре идентифицированных штаммов составила около 50%. Заболеваемость гриппом детей в РФ в 2019 г. составила 95,92 на 100 тыс. населения, заболеваемость детей 1–2 лет — 176,64 на 100 тыс. населения, детей 3–6 лет — 131,28 на 100 тыс. населения. Прямой экономический ущерб от гриппозной инфекции, согласно данным Государственного доклада «О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2019 году», в 2019 г. превысил 1,6 млрд рублей [1].
Вирусы гриппа — это РНК-вирусы, относящиеся к семейству Orthomyxoviridae. Существует три типа вирусов гриппа: A, B и C. Сегментированный вирусный геном заключен в липидсодержащую поверхностную оболочку, с двумя основными поверхностными антигенами — гемагглютинином (ГА) и нейраминидазой (НА). Подтип вируса гриппа определяется этими антигенами — ГА и НА. Вирус типа A имеет много подтипов с различной комбинацией 17 ГА-антигенов и 10 НА-антигенов (H1N1, H3N2, H5N1 и т. п.). Вирусы типа B и типа C не имеют известных подтипов. Вирусы типа А способны инфицировать не только человека, но и животных (птиц, свиней, лошадей и пр.). Они являются антигенно нестабильными, подвергаясь мутациям в вирусном геноме (антигенному сдвигу), вызывая спорадические случаи, сезонные вспышки и эпидемии. Вирусы типа B заражают только людей и не имеют выявленных резервуаров в животном мире. Они имеют менее частые антигенные вариации в геноме, ограничиваясь случаями сезонного гриппа и, редко, эпидемиями. Вирусы типа С заражают людей и свиней и вызывают только легкие заболевания верхних дыхательных путей. Они антигенно стабильны и не вызывают эпидемий.
Клиницисты зачастую диагностируют только вирусы гриппа как ведущий патоген, не учитывая возможного участия в качестве этиологического фактора других инфекционных агентов. Традиционно определенный вклад в общую инфекционную заболеваемость детской популяции вносят наиболее распространенные респираторные вирусы (респираторно-синцитиальный вирус, вирусы парагриппа, риновирус, метапневмовирус, аденовирус, коронавирус), которые могут регистрироваться одновременно с вирусами гриппа у одного пациента, образуя сочетанные формы острой респираторной вирусной инфекции (ОРВИ). Согласно данным литературы, в последние годы отмечено увеличение с 21% до 44,2% доли ОРВИ сочетанной этиологии [2–8], при этом констатируется рост сочетанных негриппозных инфекций. В данной ситуации знание особенностей течения и клинических проявлений ОРИ сочетанной этиологии в комплексе с современными возможностями лабораторной диагностики должны способствовать правильной постановке диагноза, а также оптимизации тактики ведения пациента.
Традиционно для лечения гриппа используют противовирусные этиотропные средства, прежде всего ингибиторы нейраминидазы. Однако, поскольку в последние годы отмечено увеличение доли сочетанных форм ОРИ, в т. ч. гриппа, с другими респираторными вирусами, целесообразно использовать препараты, обладающие высоким терапевтическим эффектом в отношении всех известных респираторных вирусов (ингибиторы слияния, ингибиторы транспорта вирусного нуклеопротеина из цитоплазмы в ядро, препараты интерферонов 1-го типа (например, интерферон альфа-2b с антиоксидантами — Виферон). Адекватное воздействие на определенные звенья инфекционного процесса, вызванного респираторными вирусами, позволяет добиться активации защитных механизмов организма, оптимизировать течение болезни, предотвратить ее осложнения.
Цель исследования: установить клинико-лабораторные особенности течения сочетанной инфекции вируса гриппа и других респираторных вирусов у детей.
Материал и методы
Проведен ретроспективный анализ медицинских карт 139 детей, госпитализированных в профильный стационар г. Москвы в период с октября 2017 г. по февраль 2020 г. с клиническими проявлениями ОРИ. При поступлении ребенка в стационар определяли этиологию ОРИ методами: полимеразной цепной реакции (исследование мазков и/или отделяемого слизистой полости рта, носа, мокроты на наличие РНК/ДНК вируса гриппа, респираторно-синцитиального вируса, риновируса, аденовируса, вируса парагриппа), иммуноферментного анализа (с определением антител к герпесвирусам 1, 2, 6-го типов, цитомегаловирусу, вирусу Эпштейна — Барр, хламидийной и микоплазменной инфекциям).
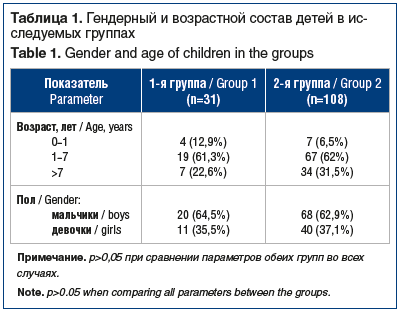
Пациенты были распределены в 2 группы: 1-я группа — дети с сочетанной инфекцией гриппа и респираторного вируса (n=31); 2-я группа — дети с моноинфекцией гриппа (n=108). В качестве второго вирусного агента выступали респираторно-синцитиальный вирус (в большинстве случаев) (8/31) и риновирус (5/31). Все дети не были привиты от гриппа. Гендерный и возрастной состав детей представлен в таблице 1.
При госпитализации всем пациентам проводили исследования, включающие клинический анализ крови с анализом лейкоцитарной формулы и определением СОЭ, общий анализ мочи, микробиологическое исследование биологического материала из зева с определением чувствительности к антибактериальным препаратам. При наличии показаний использовали инструментальные методы диагностики: рентгенографию грудной клетки, электрокардиографию, исследование функции внешнего дыхания, ультразвуковое исследование. Все дети были осмотрены оториноларингологом. Проведен сравнительный анализ частоты и продолжительности основных клинических симптомов и синдромов, частоты развития осложнений гриппа, данных лабораторных общеклинических, биохимических и инструментальных исследований. Анализ характера течения заболевания и лабораторных данных проводили до момента выписки пациентов из стационара.
Статистическая обработка полученных данных осуществлялась с использованием лицензионных программ (Microsoft Excel). Статистический анализ включал в себя анализ количественных и порядковых данных с расчетом значений среднего арифметического (M). Сравнение достоверности различий количественных и порядковых переменных между группами проводили после проверки допущений для применения параметрического многофакторного одномерного дисперсионного анализа с последующим расчетом достигнутых уровней значимости по t-критериям для связанных и несвязанных выборок или непараметрическим критериям. Различия считались достоверными при р<0,05, высокодостоверными — при p<0,01 и p<0,001, недостоверными — при р>0,05 [9].
Результаты исследования
В исследуемых группах распределение детей по полу и возрасту достоверно не различалось. Однако обращает на себя внимание, что госпитализированные в стационар с диагнозом «грипп» дети в подавляющем большинстве случаев были младшего возраста (до 7 лет), что, по-видимому, связано с более тяжелым течением болезни у таких детей, а также с большей настороженностью к состоянию ребенка у родителей.
Начало респираторной инфекции у детей 1-й группы регистрировалось в среднем за 2,60±1,6 дня до госпитализации, у детей 2-й группы отмечено более позднее (почти на 1 день) поступление в стационар — через 3,35±1,72 дня от начала болезни, однако разница недостоверна. Вероятнее всего, на амбулаторном этапе у детей с сочетанной инфекцией болезнь протекала тяжелее и требовала более ранней госпитализации. Средние сроки пребывания в стационаре у детей сравниваемых групп также достоверно не различались: 6,04±1,69 дня в1-й группе и 5,74±2,01 дня в 2-й группе. Длительность госпитализации пациентов с гриппом (моноинфекцией и сочетанными формами) была связана с невозможностью выписки из стационара на долечивание в поликлинику из-за тяжести состояния (табл. 2).
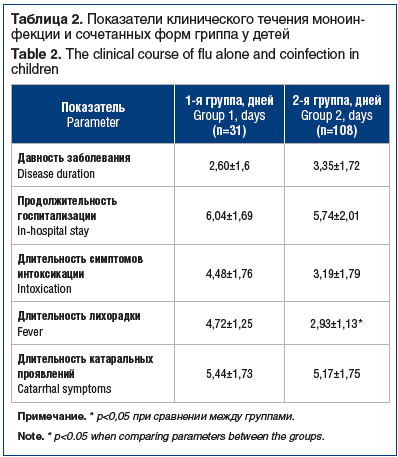
Фебрильная лихорадка — один из ведущих симптомов гриппа — продолжалась у детей с сочетанной инфекцией в среднем 4,72±1,25 дня, что почти на 2 дня больше, чем у детей с моноинфекцией (p<0,05). Средние значения температуры тела детей при поступлении в стационар статистически значимо не различались: в 1-й группе — 37,4 °C (36–39,2 °C), в 2-й группе — 37,5 °C (36–39,1 °C), однако максимальные значения температуры у детей во время болезни были несколько выше в 1-й группе, чем в 2-й группе — 39,2 °C против 38,9 °C (р>0,05).
Тяжесть состояния госпитализированных детей и совокупность клинических симптомов при сочетанном течении «грипп + респираторный вирус» обусловливает более высокую потребность в инфузионной терапии у детей 1-й группы, чем у детей 2-й группы — 25,8% против 14,7% соответственно. Вместе с тем длительность проведения инфузионной терапии в сравниваемых группах статистически не различалась, что можно объяснить одинаковыми терапевтическими подходами к ее проведению.
Течение ОРИ с вовлечением только верхних отделов дыхательных путей (ринофарингит, аденофарингит, ринит, аденоидит, ларингит) выявляли у 22,6% детей 1-й группы и у 50,9% детей 2-й группы (p<0,01). Развитие бронхита отмечено у 35,5% детей 1-й группы и у 13,9% детей 2-й группы (p<0,01). Частота развития осложнений при гриппе в группах сочетанной и моноинфекции различалась: развитие острого отита (катарального, среднего) отмечено у 35,5% и 8,3% детей (p<0,01), острого синусита — у 12,9% и 8,3%, пневмонии — у 22,6% и 7,4% соответственно. Фебрильные судороги развились у 2 детей 1-й группы и у 5 детей 2-й группы.
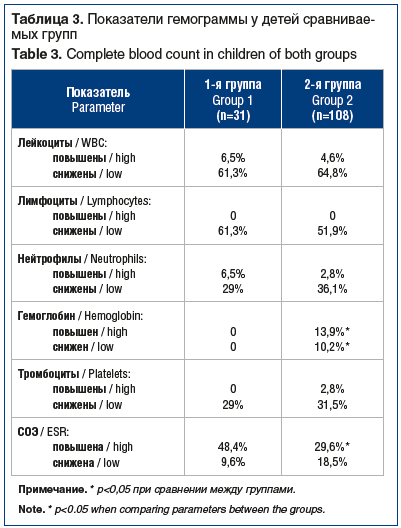
Анализ гематологических показателей представлен в таблице 3. Показатели СОЭ могут отражать более выраженную системную воспалительную реакцию, видимо, за счет сочетанного цитопатического действия двух респираторных вирусов. Отсутствие статистически значимых различий по основным параметрам гемограммы связано, скорее всего, с сочетанием именно вирусных этиологических агентов.
Заключение
В целом клиническое течение гриппа, сочетанного с другим вирусным агентом, у детей характеризуется большей тяжестью, что определяется высоким уровнем лихорадки, более выраженными симптомами интоксикации, более частыми осложнениями в виде отита, синусита, пневмонии (p<0,05), необходимостью инфузионной терапии (p<0,05). Дети с сочетанной инфекцией быстрее поступают из поликлинического звена в стационар и госпитализируются на более длительный срок. Именно поэтому при гриппе, когда репликация наиболее активна и высок риск развития осложнений, связанный с этим, симптоматической терапии может быть недостаточно. Открытие в 1957 г. А. Айзексом и Д. Линденманном интерферонов, которые реализуют врожденную неспецифическую локальную и системную реакции организма в ответ на внедрение и репликацию вирусов [10, 11], позволил решить вопрос терапии. Показано, что интерферон (например, интерферон альфа-2b с антиоксидантами — Виферон) у детей с ОРВИ и гриппом достоверно сокращает продолжительность катаральных явлений в среднем на 1,75 сут, ринореи — на 1,71 сут, интоксикации — на 1,18 сут, лихорадочного синдрома — на 0,8 сут (класс и уровень доказательности IA) [12]. Вышесказанное делает актуальным назначение этой группы препаратов в начальном периоде респираторного заболевания до получения результатов лабораторной диагностики.
Таким образом, выявленная нами взаимосвязь сочетанной этиологии заболевания и риска его тяжелого и осложненного течения определяет необходимость дальнейших исследований по определению предикторов тяжелого течения и факторов, определяющих множественное инфицирование. Требуется дальнейшая оптимизация принципов терапии сочетанной гриппозной и другой вирусной этиологии респираторных заболеваний у детей ввиду высокого риска длительной госпитализации и большой частоты осложнений, что обусловливает привлечение значительных ресурсов.
Благодарность
Редакция благодарит компанию ООО «Ферон» за оказанную помощь в технической редактуре настоящей публикации.
Acknowledgements
Editorial Board are grateful to LLC “Feron” for technical edition.
Сведения об авторах:
Николаева Светлана Викторовна — к.м.н., старший научный сотрудник ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0003-3880-8112.
Усенко Денис Валериевич — д.м.н., ведущий научный сотрудник ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0001-5232-7337.
Шабалина Светлана Васильевна — д.м.н., ведущий научный сотрудник ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0001-7102-5414.
Хлыповка Юлия Николаевна — к.м.н., младший научный сотрудник ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; врач детского инфекционного отделения ФГБУ «ЦКБ с поликлиникой»; 121359, Россия, г. Москва, ул. Маршала Тимошенко, д. 17; ORCID iD 0000-0003-4821-676X.
Медкова Алиса Юрьевна — к.м.н., заведующая детским инфекционным отделением «ЦКБ с поликлиникой»; 121359, Россия, г. Москва, ул. Маршала Тимошенко, д. 17; ORCID iD 0000-0002-1509-0622.
Горелов Александр Васильевич — д.м.н., профессор, член-корр. РАН, заместитель директора по научной работе ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; профессор кафедры детских болезней ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0001-9257-0171.
Контактная информация: Николаева Светлана Викторовна, e-mail: nikolaeva008@list.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 12.08.2020, поступила после рецензирования 07.09.2020, принята в печать 26.09.2020.
About the authors:
Svetlana V. Nikolaeva — Cand. of Sci. (Med.), Senior Researcher, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being, 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; ORCID iD 0000-0003-3880-8112.
Denis V. Usenko — Doct. of Sci. (Med.), Leading Researcher, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being, 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; ORCID iD 0000-0001-5232-7337.
Svetlana V. Shabalina — Doct. of Sci. (Med.), Leading Researcher, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being, 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; ORCID iD 0000-0001-7102-5414.
Yuliya N. Khlypovka — Cand. of Sci. (Med.), Junior Researcher, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being, 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; doctor in Children’s Infectious Department, Central Clinical Hospital and Polyclinic, 17, Marshal Timoshenko str., Moscow, 121359, Russian Federation; ORCID iD 0000-0003-4821-676X.
Alisa Yu. Medkova — Cand. of Sci. (Med.), Head of Children’s Infectious Department, Central Clinical Hospital and Polyclinic, 17, Marshal Timoshenko str., Moscow, 121359, Russian Federation; ORCID iD 0000-0002-1509-0622.
Aleksandr V. Gorelov — Doct. of Sci. (Med.), Professor, Corresponding Member of RAS, Deputy Director for Scientific Work, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being, 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; professor of the Department of Children’s Diseases, I.M. Sechenov First Moscow State Medical University (Sechenov University), 8 Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0001-9257-0171.
Contact information: Svetlana V. Nikolaeva, e-mail: nikolaeva008@list.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 12.08.2020, revised 07.09.2020, accepted 26.09.2020.
2. Шкарин В.В., Сергеева А.В. Эпидемиологические и клинические особенности сочетанных респираторных инфекций у детей. Детские инфекции. 2017;16(1):51–56. DOI: 10.22627/2072-8107-2017-16-1-51-56.
3. Калюжин О.В. Острые респираторные вирусные инфекции: современные вызовы, противовирусный ответ, иммунопрофилактика и иммунотерапия. М.: Медицинское информационное агентство; 2014.
4. Debiaggi M., Canducci F., Ceresola E.R., Clementi M. The role of infections and coinfections with newly identified and emerging respiratory viruses in children. Virol J. 2012;(9):247. DOI: 10.1186/1743-422X-9-247.
5. Hoffmann J., Rabezanahary H., Randriamarotia M. et al. Viral and atypical bacterial etiology of acute respiratory infections in children under 5 years old living in a rural tropical area of Madagascar. PLoS ONE. 2012;7(8): e43666. DOI: 10.1371/journal.pone.0043666.
6. Фадеева Т.В., Верещагина С.А., Габриэль Э.А., Коган А.С. Актуальные проблемы госпитальной инфекции: реинфицирование, суперинфицирование и резистентность возбудителей к антимикробным препаратам. Бюллетень ВСНЦ СО РАМН. 2006;(5):178–182.
7. Mahony J.B. Detection of respiratory viruses by molecular methods. Clin Microbiol Rev. 2008;21(4):716–747.
8. Мазуник Н.Н. Клинические особенности, диагностика и лечение смешанных форм острых респираторных вирусных инфекций у детей. Дис. … канд. мед. наук. М.; 2007.
9. Петри А., Сэбин К. Наглядная медицинская статистика. М.: ГЭОТАР-МЕД; 2019.
10. Калюжин О.В. Острые респираторные вирусные инфекции: современные вызовы, противовирусный ответ, иммунопрофилактика и иммунотерапия. М.: МИА; 2014.
11. Караулов А.В., Калюжин О.В. Иммунотерапия инфекционных болезней: проблемы и перспективы. Терапевтический архив. 2013;85(11):100–108.
12. Руженцова Т.А., Левицкая Д.С. Лечение острых респираторных вирусных инфекций и гриппа у детей: результаты метаанализа. Лечащий врач. 2020;3:52–57.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
