Использование ингаляционного сурфактанта в комплексном лечении тяжелой пневмонии, ассоциированной с COVID-19. Маркеры эффективности
Цель исследования: оценить влияние ингаляционной сурфактант-терапии в комплексном лечении тяжелой внебольничной пневмонии, вызванной вирусом SARS-CoV-2, на течение и исход заболевания и определить возможность использования уровня сурфактантного протеина D (surfactant protein D, SP-D) в сыворотке крови в качестве критерия эффективности лечения.
Материал и методы: выполнено проспективное рандомизированное исследование, в которое вошло 60 пациентов. Критерии включения: подтвержденная инфекция SARS-CoV-2; двусторонняя пневмония с поражением не менее 3-й степени по данным КТ; SpO2 менее 92%. Пациенты были разделены на 2 группы: в 1-й (n=30) получали в дополнение к стандартной терапии сурфактант-терапию, во 2-й (n=30) — только стандартную терапию. Сурфактант вводили ингаляционно в дозе 150–300 мг/сут. Длительность сурфактант-терапии составила 10 сут. Анализировали значения газов крови, клинические параметры и уровень SP-D до и после лечения.
Результаты исследования: через 48 ч от начала терапии у пациентов из 1-й группы зарегистрировали статистически значимый прирост SpO2 по сравнению с приростом у пациентов из 2-й группы (p=0,048). На 10-й день лечения у пациентов из 1-й группы по сравнению с пациентами из 2-й группы отмечали статистически значимое увеличение индекса оксигенации (РаО2/FiO2) (266,82±10,5 мм рт. ст. против 199,67±11,7 мм рт. ст. соответственно, p=0,001), снижение частоты перевода на искусственную вентиляцию легких (ИВЛ) (27% против 67% соответственно, p=0,002), уменьшение длительности госпитализации (21,0 (15;25) сут против 27,0 (15;35) сут соответственно, p=0,05). Летальный исход зарегистрировали у 8 (27%) пациентов из 1-й группы и 18 (60%) пациентов из 2-й группы (p=0,001). Среди пациентов из 1-й группы с благоприятным исходом заболевания в 84% случаев сурфактант-терапия назначалась в более короткие сроки от начала заболевания, чем у больных, лечение которых было неэффективным (3±1,5 дня против 7±2,0 дня). Установлена устойчивая достоверная корреляция между SP-D и РаО2 (r=420, р=0,001), между SP-D и РаО2/FiO2 (r=460, р=0,001).
Заключение: основными эффектами сурфактант-терапии являются более быстрое восстановление газового состава крови, снижение частоты переводов на ИВЛ, сокращение продолжительности пребывания в стационаре, уменьшение летальности. Успех сурфактант-терапии сопряжен с ее ранним назначением. Сурфактант-терапия может быть рассмотрена в качестве дополнительного патогенетически обоснованного компонента в комплексном лечении тяжелой пневмонии, вызванной вирусом SARS-CoV-2. Достоверно более высокий уровень SP-D отмечался у пациентов с тяжелой пневмонией, ассоциированной с COVID-19, при прогрессировании и неблагоприятным исходе заболевания.
Ключевые слова: SARS-CoV-2, COVID-19, пневмония, сурфактант, искусственная вентиляция легких, дыхательная недостаточность, сурфактантный протеин D, SP-D.
Для цитирования: Волчкова Е.В., Александрович Ю.С., Титова О.Н., Кузубова Н.А., Волчков В.А., Пискунов Д.П., Бахолдина М.Н., Битакова Ф.И. Использование ингаляционного сурфактанта в комплексном лечении тяжелой пневмонии, ассоциированной с COVID-19. Маркеры эффективности. РМЖ. Медицинское обозрение. 2022;6(7):352-359. DOI: 10.32364/2587-6821-2022-6-7-352-359.
E.V. Volchkova1, Yu.S. Alexandrovich1, O.N. Titova2, N.A. Kuzubova2, V.A. Volchkov3, D.P. Piskunov4, M.N. Bakholdina5, F.I. Bitakova6
1St. Petersburg State Pediatric Medical University, Saint Petersburg, Russian Federation
2I.P. Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
3St. Petersburg State University, St. Petersburg, Russian Federation
4Multidisciplinary City Hospital No. 2, St. Petersburg, Russian Federation
5St. Petersburg City Pokrovskaya Hospital, St. Petersburg, Russian Federation
6I.I. Mechnikov North-Western State Medical University, St. Petersburg, Russian Federation
Aim: to evaluate the effect of pulmonary surfactant therapy in the complex treatment of severe community-acquired pneumonia caused by the SARS-CoV-2 on the disease course and outcome and to determine the possibility of using the level of surfactant protein D (surfactant protein D, SP-D) in blood serum as a criterion for the treatment efficacy.
Patients and Methods: a prospective randomized study included 60 patients. Inclusion criteria confirmed SARS-CoV-2; bilateral pneumonia with at least grade 3 of lesion according to CT; SpO2 less than 92%. Patients were divided into two groups: group 1 (n=30) received surfactant therapy in addition to standard therapy, group 2 (n=30) received only standard therapy. Surfactant was administered by inhalation at a dose of 150–300 mg/day. The duration of surfactant therapy was 10 days. Arterial blood gas values, clinical parameters and SP-D levels were analyzed before and after treatment.
Results: 48 hours after the therapy start, a statistically significant increase in SpO2 was registered in patients from group 1 versus an increase in patients from group 2 (p=0.048). On the 10th day of treatment, group 1 versus group 2 showed a statistically significant increase in the oxygenation index (PaO2/FiO2) (266.82±10.5 mmHg vs. 199.67±11.7 mmHg, respectively, p=0.001), a decrease in the frequency of artificial lung ventilation (ALV) (27% vs. 67%, respectively, p=0.002), length of hospital stay (21.0 (15;25) days vs. 27.0 (15;35) days, respectively, p=0.05). The fatal outcome was registered in 8 (27%) patients from group 1 and 18 (60%) patients from group 2 (p=0.001). Among patients from group 1 who had a favorable disease outcome, in 84% of cases surfactant therapy was prescribed in a shorter period from the disease onset versus patients whose treatment was ineffective (3±1.5 days vs. 7±2.0 days). A stable, reliable correlation was established between SP-D and PaO2 (r= 420, p=0.001), between SP-D and PaO2/FiO2 (r=460, p=0.001).
Conclusion: the major effects of surfactant therapy are a faster recovery of the arterial blood gas, a decrease in the frequency of ALV, the length of hospital stay, and mortality. The success of surfactant therapy is associated with its early prescription. Surfactant therapy can be considered as an additional pathogenetically justified component in the complex treatment of severe pneumonia caused by the SARS-CoV-2. Significantly higher levels of SP-D were observed in patients with severe pneumonia associated with COVID-19, with the disease progression and adverse outcome.
Keywords: SARS-CoV-2, COVID-19, pneumonia, surfactant, artificial lung ventilation, respiratory failure, surfactant protein D, SP-D.
For citation: Volchkova E.V., Alexandrovich Yu.S., Titova O.N. et al. Pulmonary surfactant in the complex treatment of severe pneumonia associated with COVID-19. Efficacy markers. Russian Medical Inquiry. 2022;6(7):352–359 (in Russ.). DOI: 10.32364/2587-6821-2022-6-7-352-359.
Введение
Высокая смертность при новой коронавирусной инфекции COVID-19, клиническим проявлением которой является двусторонняя пневмония, поставила перед специалистами здравоохранения задачи ранней диагностики, поиска эффективных методов профилактики и лечения осложнений, влияющих на исход заболевания. В период пандемии новой коронавирусной инфекции летальность в отделениях реанимации и интенсивной терапии (ОРИТ) достигала 45–55% [1, 2]. У 3–4% пациентов регистрировалось развитие острого респираторного дистресс-синдрома (ОРДС), который, по результатам метаанализа, включавшего 10 815 пациентов с тяжелой формой COVID-19 и ОРДС, являлся основной причиной смерти в 39% случаев (95% ДИ 23–56%) [1, 3, 4].
Важным звеном патогенеза развития ОРДС при COVID-19-ассоциированной пневмонии является снижение синтеза и функциональной активности легочного сурфактанта вследствие гибели альвеолоцитов 2-го типа, качественные изменения его фосфолипидного состава (увеличение содержания минорных компонентов и ненасыщенных жирных кислот) и протеиновых компонентов [5–7].
В ряде работ отечественных и зарубежных ученых была отмечена возможность использования препаратов экзогенного сурфактанта в комплексном лечении и профилактике развития ОРДС и острого повреждения легких, в том числе вирусной этиологии, в связи с демонстрируемыми им патогенетически обоснованными эффектами: восстановление содержания фосфолипидов, предотвращение коллапса альвеол и микроателектазирования; повышение активности альвеолярных макрофагов; стимуляция синтеза эндогенного сурфактанта альвеолоцитами 2-го типа; элиминация токсических веществ, вирусов, бактерий из альвеолярного пространства [8–12]. Однако результаты влияния сурфактант-терапии на показатели газообмена, тяжесть течения и исходы у взрослых пациентов с тяжелой пневмонией и ОРДС, представленные в научной литературе, неоднозначны [13, 14]. Большинство исследований носило ретроспективный характер, не отвечало на вопрос о преимуществах того или иного способа введения, длительности применения препарата, не включало оценку эффективности терапии сурфактантом на основании маркерного профиля патологического процесса.
В ряде работ в качестве потенциального маркера повреждения альвеолоцитов 2-го типа и структуры аэрогематического барьера предлагалось определять уровень сурфактантного протеина D (SP-D) в крови больных с ОРДС и интерстициальными заболеваниями легких [15–23].
Учитывая, что сурфактантные белки синтезируются в альвеолоцитах 2-го типа, которые экспрессируют рецептор АСЕ-2, являющийся целевым для SARS‑CoV‑2, можно предположить изменение уровня SP-D в зависимости от тяжести и прогноза пневмонии, ассоциированной с COVID-19, и возможности его использования для оценки эффективности сурфактант-терапии. В ряде отечественных и зарубежных работ SP-D рассматривается как потенциальный биомаркер и регулятор локального и системного воспаления при заболеваниях легких. Контроль его уровня в сыворотке при внебольничной пневмонии может отражать не только тяжесть заболевания, но и адекватность комбинированной терапии [1, 15, 24, 25].
Цель исследования: оценить влияние ингаляционной сурфактант-терапии в комплексном лечении тяжелой внебольничной пневмонии, вызванной вирусом SARS-CoV-2, на течение и исход заболевания и определить возможность использования уровня SP-D в сыворотке крови в качестве критерия эффективности лечения.
Материал и методы
Было выполнено проспективное рандомизированное исследование, которое проводилось в условиях палат интенсивной терапии и ОРИТ СПБ ГБУЗ «ГМПБ № 2» и СПб ГБУЗ «Городская Покровская больница», Санкт-Петербург.
В исследование включали пациентов старше 18 лет с тяжелой и крайне тяжелой пневмонией, вызванной SARS-СoV-2 (подтверждено результатами ПЦР-диагностики), вирусным двусторонним полисегментарным поражением легких не менее 3–4-й степени по данным КТ, с нарушениями оксигенации (SpO2 менее 92%), при ингаляции кислорода через лицевую маску с потоком более 6 л/мин. Исследование было одобрено этическим комитетом СПБ ГБУЗ «ГМПБ № 2». Письменное информированное согласие получено от всех пациентов.
Критериями невключения являлись: возраст до 18 лет; нарушения методики ингаляционного введения препарата Сурфактант-БЛ и проведение инвазивной механической вентиляции легких; продолжающиеся на момент скринингового обследования или имеющиеся в анамнезе сопутствующие заболевания, которые повышали риск перевода пациента на искусственную вентиляцию легких (ИВЛ) или могли привести к летальному исходу в течение 3 мес.; наличие в анамнезе состояний, потребовавших проведения ИВЛ; индивидуальная непереносимость компонентов исследуемого препарата; беременность, период грудного вскармливания.
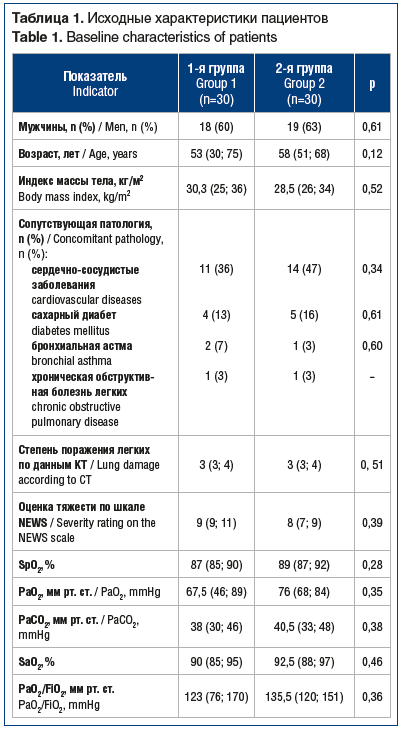
Методом случайной выборки были сформированы 2 группы (n=60), сопоставимые по полу, возрасту, клинически значимым сопутствующим заболеваниям и тяжести их течения, исходным параметрам газообмена, проценту поражения легочной ткани по данным мультиспиральной компьютерной томографии, степени активности воспалительного процесса (по данным лабораторных исследований: лейкоциты, лимфоциты, С-реактивный белок (СРБ)) (табл. 1). Критерием исключения стала необходимость в инвазивной вентиляции легких при поступлении.
Пациенты 1-й группы (n=30) получали ингаляции эмульсии препарата Сурфактант-БЛ («Биосурф», Россия) в дополнение к стандартной терапии и респираторной поддержке. Пациенты 2-й группы (сравнения) (n=30) получали только стандартную терапию.
Пациентам обеих групп проводили лечение в соответствии с временными методическими рекомендациями по диагностике, лечению и профилактике COVID-19, версии 13, 13.1, 2021 г.; методическими рекомендациями Общероссийской общественной организации «Федерация анестезиологов и реаниматологов», версия 2021 г., которое включало противовирусную, патогенетическую, антитромботическую, инфузионную, симптоматическую и антибактериальную терапию [4, 26]. С целью коррекции гипоксии проводилась респираторная поддержка, включающая высокопоточную кислородотерапию через носовые канюли; СРАР-терапию в сочетании с прон-позицией; неинвазивную вентиляцию легких (НИВЛ, опция аппарата Puritan Bennett 980, Covidien/Medtronic, США; «Авента-М», Россия) в режимах c заданным уровнем инспираторного давления (Pressure Support, BIPAP) 14–24 см вод. ст. (минимальный уровень при сохранении комфорта пациента) и минимальной инспираторной фракцией кислорода для поддержания целевого значения SpO2 (60–100%).
Дополнительную терапию пациентам 1-й группы проводили сурфактантом-БЛ, который вводили ингаляционно через компрессорный или mesh-небулайзер Aerogen Solo (Aerogen, Ирландия) по следующей схеме: в дозе 1–1,5 мг/кг (в среднем 75 мг на 1 введение) 2 р/сут. Продолжительность терапии составляла от 3 до 5 сут (n=20) и 7–10 сут (n=10). Пациентам 1-й группы, получавшим сурфактант, в обязательном порядке проводилась персональная подготовка к ингаляции.
У пациентов при поступлении и через 10 дней лечения наряду с клиническими показателями анализировали следующие показатели: лейкоциты и лимфоциты крови (абсолютное число), СРБ (мг/л), D-димер (мг/мл), SpO2 методом пульсоксиметрии, газы артериальной крови с определением SаO2 (%), PaO2, PaCO2, РaO2/FiO2 (мм рт. ст.). Тяжесть состояния исходно оценивали по шкале NEWS. Регистрировали частоту перевода больных на ИВЛ, число пациентов, которым потребовалась НИВЛ, длительность госпитализации (дни), исход заболевания, летальные исходы, наступившие в течение 4 нед. Благоприятным исходом считалось выздоровление пациента.
Контроль уровня SP-D в сыворотке крови осуществлялся дважды в обеих группах: при поступлении и на 10-е сутки с момента госпитализации. Уровень SP-D определяли методом твердофазного ИФА (ELISA). Для его количественного определения в сыворотке крови использовался набор Human SPD (Pulmonary Surfactant Associated Protein D) ELISA Kit, Wuhan Fine Biotech Co., Ltd. Диапазон определения — 1,563–100 нг/мл, чувствительность — 0,938 нг/мл.
Статистический анализ проведен с помощью пакета Statistica 7.0 (StatSoft Inc., США). Данные представлены в абсолютных значениях (%), в виде медианы (25-й; 75-й процентиль), или средней арифметической и ошибки средней (М±SEM) в зависимости от нормальности распределения. Для сравнительного анализа и выявления различий использовали методы непараметрической статистики: дисперсионный анализ методом Краскела — Уоллиса с последующей оценкой U-критерием Манна — Уитни. Анализ категориальных переменных проводили с помощью трансформации Z Фишера с последующим применением двустороннего t-теста. Критическим уровнем значимости считали р=0,05.
Результаты исследования
У всех пациентов, включенных в исследование, имели место начальные проявления ОРДС. Зарегистрированные показатели, отражающие газообменную функцию (параметры оксигенации артериальной крови и их динамика), частоту перевода пациентов на ИВЛ, длительность пребывания в стационаре и исход заболевания, представлены в таблице 2.
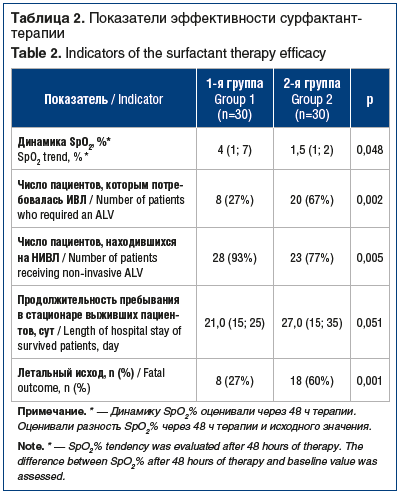
Несмотря на то, что при поступлении большему числу пациентов 1-й группы потребовалось проведение НИВЛ, на фоне лечения сурфактантом отмечалось более быстрое восстановление параметров оксигенации, меньшему числу пациентов потребовалась ИВЛ, летальность в группе сурфактанта была достоверно ниже. Следует отметить, что среди пациентов 1-й группы, имевших благоприятный исход заболевания, в 84% случаев сурфактант-терапия назначалась в более короткие сроки от начала заболевания по сравнению с больными, лечение которых было неэффективным (3±1,5 дня против 7±2,0 дня).
К 10-му дню терапии более чем у 70% пациентов 1-й группы наблюдалось восстановление параметров оксигенации, оцениваемое по газам артериальной крови.
Анализ газового состава крови выживших пациентов в 1-й и 2-й группах через 10 дней лечения показал достоверную положительную динамику показателей: РаO2, SаO2, РаO2 /FiO2 (p<0,005) (табл. 3).
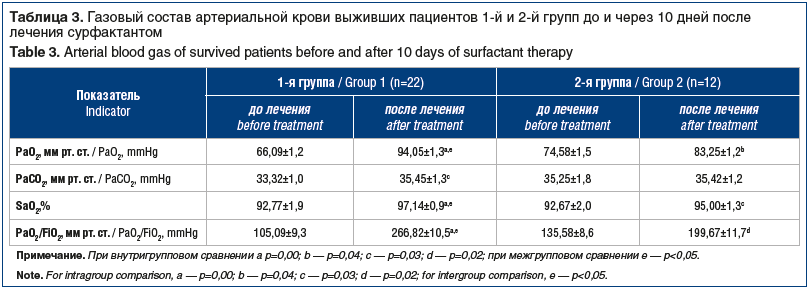
При межгрупповом сравнении с использованием однофакторного дисперсионного анализа у пациентов 1-й группы на 10-й день лечения зарегистрировано статистически достоверное (p<0,005) улучшение показателей газообмена, чему, вероятно, способствовали стабилизация и восстановление аэрогематического барьера, уменьшение нагрузки на респираторную систему вследствие введения сурфактанта.
С динамикой показателей газового состава крови коррелировали положительные изменения маркеров воспаления выживших пациентов 1-й и 2-й групп (табл. 4). Отмечалось достоверное увеличение числа лимфоцитов в крови при исходно выраженной лимфопении. Показатели СРБ, ферритина, D-димера снижались, но не достигали референтных значений.
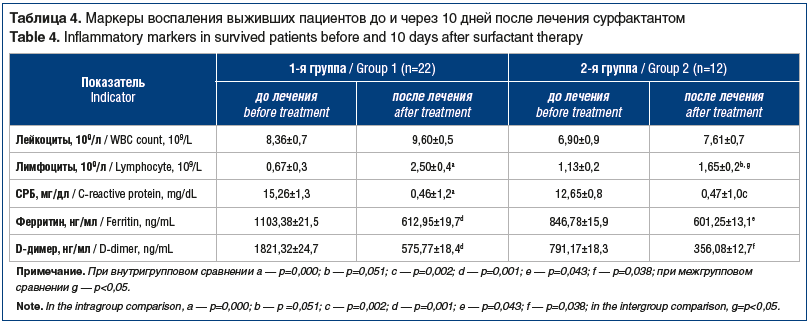
Анализ маркеров воспаления крови в 1-й и 2-й группах через 10 дней лечения с использованием однофакторного дисперсионного анализа демонстрировал достоверные различия по показателю абсолютного числа лимфоцитов (p<0,05), что указывало на активацию лимфопоэза, возможно, за счет комплексной стабилизации иммунного ответа и уменьшения степени выраженности системного воспаления на фоне сурфактант-терапии. По D-димеру межгрупповые различия тоже были достоверны (p=0,04), хотя показатель в 1-й группе был выше, его динамика была более выраженной, чем во 2-й группе. Разность в снижении (улучшении) показателя в 1-й группе составила 1200±60 нг/мл против 410±58 нг/мл.
Исходные значения SP-D в 1-й и 2-й группах не достигали статистически значимых различий. При анализе на 10-й день лечения наиболее высокие значения показателя в сыворотке крови зарегистрированы у пациентов, имевших в последующем тяжелый ОРДС и неблагоприятный исход заболевания (рис. 1).
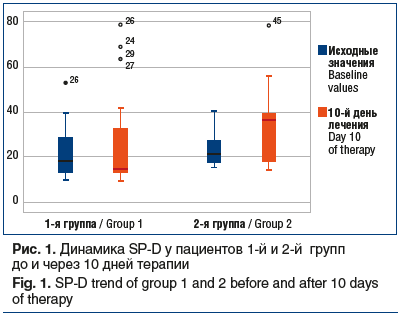
У выживших пациентов 1-й группы в процессе лечения показатель снижался, достигая уровня достоверных различий, во 2-й группе он практически не изменялся (табл. 5).
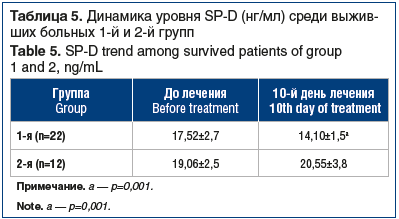
Статистически значимо более выраженное снижение SP-D на 10-й день демонстрировали пациенты 1-й группы по сравнению с показателем у пациентов 2-й группы (3,5±1,8 нг/мл против 1,2±1,3 нг/мл, p=0,04). Однофакторный дисперсионный анализ межгрупповых различий по уровню SP-D подтвердил на 10-й день лечения статистически более низкие значения показателя в группе сурфактант-терапии, р<0,05 (рис. 2).
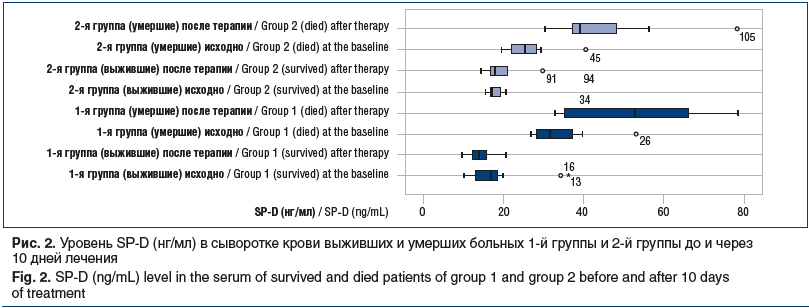
Таким образом, уровень и динамика SP-D в сыворотке крови больных тяжелой COVID-19-ассоциированной пневмонией отражали тяжесть течения заболевания. Показатель повышался при прогрессировании заболевания, развитии ОРДС и неэффективности лечения. Более благоприятный профиль SP-D регистрировали у больных, получавших дополнительную сурфактант-терапию, что подтверждает выполненный корреляционный анализ, где выявлена значимая отрицательная корреляция между уровнем SP-D и количеством лимфоцитов (r=-290, р=0,04), положительная корреляция с СРБ (r=370, р=0,01), РаО2 (r=420, р=0,001), РаО2/FiO2 (r=460, р=0,001). Положительные изменения на КТ грудной клетки в течение рассматриваемого периода отмечали в 65% случаев выживших пациентов 1-й группы, у пациентов 2-й группы — в 48% случаев.
Обсуждение
Результаты, полученные в исследовании, демонстрируют возможность использования сурфактант-терапии в качестве компонента комплексного лечения тяжелой пневмонии, вызванной вирусом SARS-CoV-2. Ингаляционное введение Сурфактанта-БЛ способствовало более быстрому восстановлению параметров оксигенации, улучшению газообмена, снижению числа больных, которым потребовалась ИВЛ, длительности пребывания в стационаре и показателя летальности, что согласуется с выводами ряда отечественных и зарубежных авторов [27–31].
Успехи применения экзогенного сурфактанта в условиях дефицита, связанного с гибелью альвеолоцитов 2-го типа, обусловлены предотвращением микроателектазирования, шунтирования крови и снижения растяжимости легочной ткани [30, 32, 33]. С другой стороны, хорошо известно участие сурфактанта в процессах формирования защитной функции легких в связи с его влиянием на врожденный и адаптивный местный иммунитет [34]. В ряде работ отмечены противовоспалительные и противовирусные свойства сурфактанта при пневмониях, вызванных как SARS-CoV-2, так и другими вирусами [12, 32, 35].
Однако эффективность применения сурфактанта при тяжелых внебольничных пневмониях и ОРДС не всегда оценивается однозначно [5, 13]. В связи с этим актуальными становятся вопросы о маркерах эффективности лечения, начале и длительности применения препарата. В настоящее время обсуждается возможность применения в качестве объективного показателя оценки повреждения структур аэрогематического барьера SP-D в сыворотке крови. В исследовании M. Tong et al. [24] отмечалось значительное повышение уровня SP-D у больных COVID-19 в острой фазе при тяжелом течении заболевания по сравнению с легким. Был сделан вывод о возможности использования этого показателя в качестве потенциального биомаркера тяжести COVID-19 и определения когорты пациентов, состояние которых может ухудшаться на ранней стадии. В выполненном исследовании достоверно более высокий уровень SP-D отмечался у пациентов c тяжелой пневмонией, ассоциированной с COVID-19, при прогрессировании и неблагоприятном исходе заболевания. Он коррелировал со значениями числа лимфоцитов, СРБ, РаО2 и РaO2/FiO2, что соответствует результатам, полученным ранее другими исследователями [15, 25]. Больные с благоприятным исходом заболевания, получавшие сурфактант-терапию, демонстрировали более низкие значения уровня SP-D при поступлении и его статистически достоверное снижение на 10-й день лечения, положительные изменения с тенденцией к нормализации числа лимфоцитов крови, СРБ, D-димера, данных КТ, показателей РаО2 и РaO2/FiO2 по сравнению с выжившими пациентами группы сравнения. Полученные данные позволили сделать вывод о возможности использования уровня SP-D сыворотки крови в качестве дополнительного маркера тяжелого течения пневмонии, вызванной вирусом SARS-CoV-2, полезного для диагностики ранней стадии ОРДС и эффективности лечения. Среди пациентов 1-й группы, имевших благоприятный исход заболевания, в 84% случаев сурфактант-терапия назначалась на более ранних сроках от начала заболевания по сравнению с больными, лечение которых было неэффективным (3±1,5 дня против 7±2,0 дня), что указывает на необходимость включения препарата на ранней стадии развития заболевания и дыхательной недостаточности и согласуется с мнением других исследователей [36].
Заключение
Сурфактант-терапия может быть рассмотрена в качестве дополнительного патогенетически обоснованного компонента в комплексном лечении тяжелой пневмонии, вызванной вирусом SARS-CoV-2. Основными эффектами сурфактант-терапии являются уменьшение риска прогрессирования дыхательной недостаточности, более быстрое восстановление газового состава крови, снижение частоты переводов на ИВЛ, сокращение продолжительности пребывания в стационаре, уменьшение летальности. Успех сурфактант-терапии сопряжен с ранним ее назначением. Определение содержания SP-D может быть использовано в качестве дополнительного маркера диагностики ранней стадии ОРДС у больных с тяжелым течением пневмонии, вызванной вирусом SARS-CoV-2, и эффективности сурфактант-терапии. С целью индивидуализации подхода и повышения эффективности включения сурфактант-терапии в комплексное лечение пациентов с тяжелым течением вирусной пневмонии необходим дальнейший поиск и оценка определяющих факторов, таких как соотношение комплаенса легких и уровня гипоксемии, длительности, дозы и срока начала введения препарата, применение усовершенствованной модели прогнозирования успеха лечения. Особый интерес вызывает влияние сурфактант-терапии, проведенной в острой фазе заболевания, на восстановление респираторной зоны в постковидном периоде.
Сведения об авторах:
Волчкова Елизавета Владимировна — аспирант кафедры анестезиологии, реаниматологии и неотложной педиатрии ФП и ДПО ФГБОУ ВО СПбГПМУ Минздрава России; 194100, Россия, г. Санкт-Петербург, ул. Литовская, д. 2; ORCID iD 0000-0001-6712-5121.
Александрович Юрий Станиславович — д.м.н., профессор, заведующий кафедрой анестезиологии, реаниматологии и неотложной педиатрии ФП и ДПО ФГБОУ ВО СПбГПМУ Минздрава России; 194100, Россия, г. Санкт-Петербург, ул. Литовская, д. 2; ORCID iD 0000-0002-2131-4813.
Титова Ольга Николаевна — д.м.н., профессор, директор НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0003-4678-3904.
Кузубова Наталия Анатольевна — д.м.н., заместитель директора НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0002-1166-9717.
Волчков Владимир Анатольевич — д.м.н., профессор, заслуженный врач РФ, заведующий кафедрой анестезиологии и реаниматологии СПбГУ; 199106, Россия, г. Санкт-Петербург, 21-я лин. В.О., д. 8a; ORCID iD 0000-0002-5664-7386.
Пискунов Дмитрий Павлович — врач СПБ ГБУЗ «ГМПБ № 2»; 194354, Россия, г. Санкт-Петербург, Учебный пер., д. 5; ORCID iD 0000-0002-9752-2539.
Бахолдина Марина Николаевна — главный врач СПб ГБУЗ «Городская Покровская больница»; 199106, Россия, г. Санкт-Петербург, Большой пр-т В.О., д. 85; ORCID iD 0000-0002-6224-6749.
Битакова Фатима Измаиловна — к.м.н., доцент кафедры госпитальной терапии и кардиологии им. М.С. Кушаковского ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России; 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41; ORCID iD 0000-0001-6637-8266.
Контактная информация: Волчкова Елизавета Владимировна, e-mail: elizavetavolch@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 09.07.2022.
Поступила после рецензирования 02.08.2022.
Принята в печать 25.08.2022.
About the authors:
Elizaveta V. Volchkova — post-graduate student of the Department of Anesthesiology, Resuscitation and Emergency Pediatrics, St. Petersburg State Pediatric Medical University; 2, Litovskaya str., St. Petersburg, 194100, Russian Federation; ORCID iD 0000-0001-6712-5121.
Yuri S. Alexandrovich — Dr. Sc. (Med.), Professor, Head of the Department of Anesthesiology, Resuscitation and Emergency Pediatrics, St. Petersburg State Pediatric Medical University; 2, Litovskaya str., St. Petersburg, 194100, Russian Federation; ORCID iD 0000-0002-2131-4813.
Olga N. Titova — Dr. Sc. (Med.), Professor, Director of the Research Institute of Pulmonology, I.P. Pavlov First Saint Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0003-4678-3904.
Natalia A. Kuzubova — Dr. Sc. (Med.), Deputy Director of the Research Institute of Pulmonology, I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0002-1166-9717.
Vladimir A. Volchkov — Dr. Sc. (Med.), Professor, Honored Doctor of the Russian Federation, Head of the Department of Anesthesiology and Resuscitation, St. Petersburg State University; 8a, 21st Line, St. Petersburg, 199106, Russian Federation, ORCID iD 0000-0002-5664-7386.
Dmitry P. Piskunov — doctor, City Multidisciplinary Hospital No. 2; 5, Uchebnii Lane, St. Petersburg, 194354, Russian Federation; ORCID iD 0000-0002-9752-2539.
Marina N. Bakholdina — Chief Medical Officer, City Pokrovskaya Hospital; 85, Bol’shoi Ave, St. Petersburg, 199106, Russian Federation; ORCID iD 0000-0002-6224-6749.
Fatima I. Bitakova — C. Sc. (Med.), Associate Professor of the Department of Hospital Therapy and Cardiology named after M.S. Kushakovsky, I.I. Mechnikov North-Western State Medical University; 41, Kirochnaya str., St. Petersburg, 191015, Russian Federation; ORCID iD 0000-0001-6637-8266.
Contact information: Elizaveta V. Volchkova, e-mail: elizavetavolch@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 09.07.2022.
Revised 02.08.2022.
Accepted 25.08.2022.
2. Suleyman G., Fadel R.A., Malette K.M. et al. Clinical characteristics and morbidity associated with coronavirus disease 2019 in a series of patients in Metropolitan Detroit. JAMA Netw Open. 2020;3(6):e2012270. DOI: 10.1001/jamanetworkopen.2020.12270.
3. Hasan S.S., Capstick T., Ahmed R. et al. Mortality in COVID-19 patients with acute respiratory distress syndrome and corticosteroids use: a systematic review and meta-analysis. Expert Rev Respir Med. 2020;14(11):1149–1163. DOI: 10.1080/17476348.2020.1804365.
4. Временные методические рекомендации по профилактике, диагностике и лечению новой коронавирусной инфекции COVID-19. Версия 13.1, 17.11.2021. [Interim guidelines for the prevention, diagnosis and treatment of a new coronavirus infection COVID-19. Version 13.1, 11.17.2021 (in Russ.)].
5. Bracco L. Covid-19, Type II Alveolar Cells and Surfactant. J Med — Clin Res & Rev. 2020;4(4):1–3.
6. Zhang H., Zhou P., Wei Y. et al. Histopathologic changes and SARS-CoV-2 immunostaining in the lung of a patient with COVID-19. Ann Intern Med. 2020;172(9):629–632. DOI: 10.7326/M20-0533.
7. Günther A., Siebert C., Schmidt R. et al. Surfactant alterations in severe pneumonia, acute respiratory distress syndrome, and cardiogenic lung edema. Am J Respir Crit Care Med. 1996;153(1):176–184. DOI: 10.1164/ajrccm.153.1.8542113.
8. Ahlstrom Z.J., Massaro F., Mikolka P. et al. Synthetic surfactant with a recombinant surfactant protein C analogue improves lung function and attenuates inflammation in a model of acute respiratory distress syndrome in adult rabbits. Respir Res. 2019;25(245):2–13. DOI: 10.1186/s12931-019-1220-x.
9. Pramod K., Kotta S., Jijith U.S. et al. Surfactant-based prophylaxis and therapy against COVID-19: A possibility. Med Hypotheses. 2020;143:110081. DOI: 10.1016/j.mehy.2020.110081.
10. Mirastschijski U., Dembinski R., Maedler K. Lung Surfactant for Pulmonary Barrier Restoration in Patients With COVID-19 Pneumonia. Front Med (Lausanne). 2020;7:254. DOI: 10.3389/fmed.2020.00254.
11. Cattel F., Giordano S., Bertiond C. et al. Use of exogenous pulmonary surfactant in acute respiratory distress syndrome (ARDS): Role in SARS-CoV-2-related lung injury. Respir Physiol Neurobiol. 2021;288:103645. DOI: 10.1016/j.resp.2021.103645.
12. Ghati A., Dam P., Tasdemir D. et al. Exogenous pulmonary surfactant: A review focused on adjunctive therapy for severe acute respiratory syndrome coronavirus 2 including SP-A and SP-D as added clinical marker. Curr Opin Colloid Interface Sci. 2021;51:101413. DOI: 10.1016/j.cocis.2020.101413.
13. Dushianthan A., Cusack R., Goss V. et al. Clinical review: Exogenous surfactant therapy for acute lung injury/acute respiratory distress syndrome-where do we go from here? Crit Care. 2012;16(6):238. DOI: 10.1186/cc11512.
14. Meng H., Sun Y., Lu J. et al. Exogenous surfactant may improve oxygenation but not mortality in adult patients with acute lung injury/acute res-piratory distress syndrome: a meta-analysis of 9 clinical trials. J Cardiothorac Vasc Anesth. 2012;26(5):849–856. DOI: 10.1053/j.jvca.2011.11.006.
15. Мороз В.В., Голубев А.М., Кузовлев А.Н. и др. Сурфактантный протеин-D — биомаркер острого респираторного дистресс-синдрома. Общая реаниматология. 2013;IX(4):11–17. [Moroz B.B., Golubev A.M., Kuzovlev A.N. et al. Surfactant Protein D Is a Biomarker of Acute Respiratory Distress Syndrome. Obshchaya reanimatologiya. 2013;IX(4):11–17 (in Russ.)].
16. Olesen H.V., Holmskov U., Schiøtz P.O., Sørensen G.L. Serum-surfactant SP-D correlates inversely to lung function in cystic fibrosis. J Cyst Fibros. 2010;9(4):257–262. DOI: 10.1016/j.jcf.2010.03.011. 9.
17. National Health Commission of the People’s Republic of China home page. (Electronic resource.) URL: http://en.nhc.gov.cn/ (access datе: 17.06.2022).
18. Tong M., Jiang Y., Xia D. et al. Elevated expression of serum endothelial cell adhesion molecules in COVID-19 patients. J Infect Dis. 2020;222(6):894–898. DOI: 10.1093/infdis/jiaa349.
19. Guo W., Li M., Dong Y. et al. Diabetes is a risk factor for the progression and prognosis of COVID-19. Diabetes Metab Res Rev. 2020;36(7):e3319. DOI: 10.1002/dmrr.3319.
20. Wang D., Hu B., Hu C. et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China. JAMA. 2020;323(11):1061–1069. DOI: 10.1001/jama.2 020.1585.
21. Qin C., Zhou L., Hu Z. et al. Dysregulation of immune response in patients with COVID-19 in Wuhan, China. Clin Infect Dis. 2020;71(15):762–768. DOI: 10.1093/cid/ciaa248.
22. Wang C., Pan R., Wan X. et al. Immediate psychological responses and associated factors during the initial stage of the 2019 coronavirus disease (COVID-19) epidemic among the general population in China. Int J Environ Res Public Health. 2020;17(5):1729. DOI: 10.33 90/ijerph17051729.
23. Johansson J., Curstedt T., Robertson B. The proteins of the surfactant system. Eur Respir J. 1994;7(2):372–391. DOI: 10.1183/09031936.94.07020372.
24. Tong M., Xiong Y., Zhu C. et al. Serum surfactant protein D in COVID-19 is elevated and correlated with disease severity. BMC Infect Dis. 2021;21(1):737. DOI: 10.1186/s12879-021-06447-3.
25. Saito A., Kuronuma K., Moniwa K. et al. Serum surfactant protein A and D may be novel biomarkers of COVID-19 pneumonia severity (preprint). DOI: 10.21203/rs.3.rs-29567/v1. (Electronic resource.) URL: https://www.researchsquare.com/article/rs-29567/v1 (access datе: 17.06.2022).
26. Анестезиолого-реанимационное обеспечение пациентов с новой коронавирусной инфекцией COVID-19. Методические рекомендации Общероссийской общественной организации «Федерация анестезиологов и реаниматологов». Версия 6, 2021 г. [Anesthesiological and resuscitation support for patients with a new coronavirus infection COVID-19. Methodological recommendations of the All-Russian public organization "Federation of anesthesiologists and resuscitators", version 6, 2021 (in Russ.)].
27. Avdeev S.N., Trushenko N.V., Chikina S.Y. et al. Beneficial effects of inhaled surfactant in patients with COVID-19-associated acute respiratory distress syndrome. Respir Med. 2021;185:106489. DOI: 10.1016/j.rmed.2021.106489.
28. Баутин А.Е., Аптекарь В.В., Лапшин К.Б. и др. Экзогенный сурфактант в комплексном лечении тяжелой пневмонии, вызванной вирусом SARS-CoV-2. Трансляционная медицина. 2020;7(6):55–64. DOI: 10.18705/2311-4495-2020-7-6-55-64. [Bautin A.E., Aptekar V.V., Lapshin K.V. et al. Exogenous surfactant in the treatment of severe pneumonia caused by the SARS-CoV-2 virus. Translational Medicine. 2020;7(6):55–64 (in Russ.)]. DOI: 10.18705/2311-4495-2020-7-6-55-64.
29. Heching M., Lev S., Shitenberg D. et al. Surfactant for the Treatment of ARDS in a Patient With COVID-19. Chest. 2021;160(1):e9–e12. DOI: 10.1016/j.chest.2021.01.028.
30. Busani S., Dall’Ara L., Tonelli R. et al. Surfactant replacement might help recovery of low-compliance lung in severe COVID-19 pneumonia. Ther Adv Respir Dis. 2020;14:1753466620951043. DOI: 10.1177/1753466620951043.
31. Dabbagh A., Rajaei S., Ghahremani M. et al. The effect of surfactant on clinical outcome of patients with COVID-19 under mechanical ventilation: A structured summary of a study protocol for a randomised controlled trial. Trials. 2020;21(1):919. DOI: 10.1186/s13063-020-04815-z.
32. Takano H. Pulmonary surfactant itself must be a strong defender against SARS-CoV-2. Med Hypotheses. 2020;144:110020. DOI: 10.1016/j.mehy.2020.110020.
33. Schousboe P., Wiese L., Heiring C. et al. Assessment of pulmonary surfactant in COVID-19 patients. Crit Care. 2020;24(1):552. DOI: 10.1186/s13054-020-03268-9.
34. Davidson W.J., Dorscheid D., Spragg R. et al. Exogenous pulmonary surfactant for the treatment of adult patients with acute respiratory distress syndrome: results of a meta-analysis. Crit Care. 2006;10(2):R41. DOI: 10.1186/cc4851.
35. Numata M., Kandasamy P., Nagashima Y. et al. Phosphatidylglycerol suppresses influenza A virus infection. Am J Respir Cell Mol Biol. 2012;46(4):479–487. DOI: 10.1165/rcmb.2011-0194OC.
36. A Clinical Trial of Nebulized Surfactant for the Treatment of Moderate to Severe COVID-19 (COVSurf). 2020 Clinical Trials.gov identifier NCT04362059. (Electronic resource.) URL: https://clinicaltrials.gov/ct2/show/NCT04362059 (access datе: 17.06.2022).

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Распечатать