Влияние синдрома обструктивного апноэ/гипопноэ сна на экспрессию Е-кадгерина в эпителии пищевода
DOI: 10.32364/2587-6821-2020-4-5-268-273
Цель исследования: оценить влияние синдрома обструктивного апноэ/гипопноэ сна (СОАГС) на экспрессию Е-кадгерина и гистоархитектонику эпителия нижней трети пищевода.
Материал и методы: проведено одномоментное кросс-секционное сравнительное исследование, в которое вошло 108 человек. По результатам сомнологического исследования легкая степень тяжести СОАГС диагностирована у 49 пациентов, средняя степень — у 29, составивших 1-ю и 2-ю группу соответственно. В 3-ю группу (группа сравнения) вошло 30 человек без СОАГС. Всем пациентам выполняли эзофагогастродуоденоскопию с биопсией нижней трети пищевода. Проводили морфометрическую оценку толщины эпителия, высоты соединительнотканных сосочков, межъядерных расстояний во всех слоях эпителия. Для оценки экспрессии Е-кадгерина выполняли иммуногистохимический анализ с использованием моноклональных антител к Е-кадгерину.
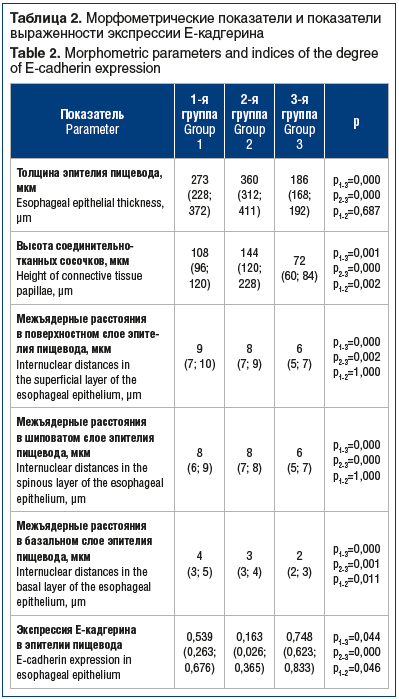
Результаты исследования: пациенты с легкой и средней степенью тяжести СОАГС в отличие от группы сравнения характеризовались более выраженной толщиной эпителия (273 (228; 372), 360 (312; 411), 186 (168; 192) мкм соответственно, р1–3=0,000, р2–3=0,000), более высокими соединительнотканными сосочками (108 (96; 120), 144 (120; 228), 72 (60; 84) мкм соответственно, р1–3=0,001, р2–3=0,000), широкими межъядерными расстояниями в поверхностном (9 (7; 10), 8 (7; 9), 6 (5; 7) мкм соответственно, р1–3=0,000, р2–3=0,002), шиповатом (8 (6; 9), 8 (7; 8), 6 (5; 7) мкм соответственно, р1–3=0,000, р2–3=0,000), базальном (4 (3; 5), 3 (3; 4), 2 (2; 3) мкм соответственно, р1–3=0,000, р2–3=0,001) слоях эпителия. Установлено снижение экспрессии Е-кадгерина в отличие от группы сравнения у пациентов как с легкой степенью тяжести СОАГС (0,748 (0,623; 0,833) и 0,539 (0,263; 0,676) соответственно, р=0,044), так и со средней степенью (0,748 (0,623; 0,833) и 0,163 (0,026; 0,365) соответственно, р=0,000). Выявлены корреляции между показателями респираторного мониторинга и экспрессией Е-кадгерина в эпителии пищевода.
Заключение: СОАГС негативно влияет на состояние слизистой оболочки нижней трети пищевода, способствует потере эпителием Е-кадгерина, в результате чего создаются условия для дезорганизации эпителиальной ткани и увеличиваются риски развития предраковых заболеваний и рака пищевода.
Ключевые слова: синдром обструктивного апноэ/гипопноэ сна, Е-кадгерин, эпителий пищевода, гистоархитектоника, эпителиально-мезенхимальная трансформация, интермиттирующая гипоксия, индекс апноэ/гипопноэ.
Для цитирования: Шелкович Ю.Я. Влияние синдрома обструктивного апноэ/гипопноэ сна на экспрессию Е-кадгерина в эпителии пищевода. РМЖ. Медицинское обозрение. 2020;4(5):268-273. DOI: 10.32364/2587-6821-2020-4-5-268-273.
Yu.Ya. Shelkovich
Grodno State Medical University, Grodno, Republic of Belarus
Aim: to evaluate the effect of obstructive sleep apnea-hypopnea syndrome (OSAHS) on E-cadherin expression and epithelium histoarchitectonics of the lower third of the esophagus.
Patients and Methods: 108 patients were included in a cross-sectional comparative study. According to the results of somnology, a mild severity of OSAHS was diagnosed in 49 patients (group 1), an average severity — in 29 (group 2). Group 3 included 30 people without OSAHS. All patients underwent esophagogastroduodenoscopy with a biopsy of the lower third of the esophagus. Morphometrics of epithelial thickness, height of connective tissue papillae, and internuclear distances in all epithelial layers was performed. To assess the E-cadherin expression, immunohistochemistry was performed using monoclonal antibodies to E-cadherin.
Results: in contrast to the comparison group, patients with mild and moderate OSAHS were characterized by a higher epithelium thickness (273 (228; 372), 360 (312; 411), 186 (168; 192) μm, respectively, р1–3=0.000, р2–3=0.000), higher connective tissue papillae (108 (96; 120), 144 (120; 228), 72 (60; 84) μm, respectively, р1–3=0,001, р2–3=0,000), and larger internuclear distances in superficial layer (9 (7; 10), 8 (7; 9), 6 (5; 7) μm, respectively, р1–3=0.000, р2–3=0.002), spinous layer (8 (6; 9), 8 (7; 8), 6 (5; 7) μm, respectively, р1–3=0.000, р2–3=0.000), basal layer (4 (3; 5), 3 (3; 4), 2 (2; 3) μm, respectively, р1–3=0.000, р2–3=0,001) of epithelium. E-cadherin expression decreased in patients with both mild OSAHS (0.748 (0.623; 0.833) and 0.539 (0.263; 0.676), respectively, p=0.044) and moderate OSAHS (0.748 (0.623; 0.833) and 0.163 (0.026; 0.365), respectively, p=0.000) versus the comparison group. Correlations were found between respiratory monitoring indicators and E-cadherin expression in the esophageal epithelium.
Conclusion: OSAHS negatively affects the lining condition of the lower third of the esophagus, contributes to the loss of E-cadherin, which creates conditions for disorganization of epithelial tissue and increases the risk of precancerous diseases and esophageal cancer.
Keywords: obstructive sleep apnea-hypopnea syndrome, E-cadherin, esophageal epithelium, histoarchitectonics, epithelial-mesenchymal transition, intermittent hypoxia, apnea-hypopnea index.
For citation: Shelkovich Yu.Ya. Effect of obstructive sleep apnea-hypopnea syndrome on E-cadherin expression in esophageal epithelium. Russian Medical Inquiry. 2020;4(5):268–273. DOI: 10.32364/2587-6821-2020-4-5-268-273.
Введение
В настоящее время многие исследователи сосредоточены на изучении синдрома обструктивного апноэ/гипопноэ сна (СОАГС) и его связи с различными заболеваниями. СОАГС представляет собой широко распространенную патологию, которая выявляется у 24% мужчин и 9% женщин в возрасте от 30 до 60 лет и более чем у 60% лиц старше 60 лет [1, 2].
Особый интерес представляет взаимосвязь СОАГС с риском развития онкологических заболеваний. Согласно данным последних эпидемиологических исследований, проведенных среди людей, и экспериментальных исследований на животных, при наличии СОАГС повышается риск развития рака пищевода, колоректального рака, рака легких, почек, молочной железы, меланомы [3–6].
Точные механизмы реализации такого эффекта хронической интермиттирующей гипоксии при СОАГС в настоящее время находятся на стадии изучения. Однако считается, что в основе таких механизмов может лежать активация процессов эпителиально-мезенхимальной трансформации (ЭМТ) [7, 8]. ЭМТ представляет собой переход от эпителиального фенотипа клеток к мезенхимальноподобному. При этом клетки теряют свою форму, апикобазальную ориентированность, разрушаются межклеточные контакты, происходит перестройка цитоскелета, нарушается экспрессия генов, сигнальных молекул, белков, факторов транскрипции и функционирование цепей сигнальных каскадов. В результате клетки становятся более подвижными, способными разрушать базальную мембрану и проникать через нее, противостоять апоптозу [9].
Ключевым звеном в процессах ЭМТ считается потеря клеткой функционирующего Е-кадгерина — трансмембранного белка, ответственного за формирование плотных запирательных контактов между клетками. Снижение экспрессии и ускоренная деградация Е-кадгерина приводят к потере связей между клетками и нарушению их апикобазальной ориентированности [10]. На основании вышесказанного актуальным представляется изучение влияния СОАГС на экспрессию Е-кадгерина в эпителии пищевода.
Цель исследования: оценить влияние СОАГС на экспрессию Е-кадгерина и гистоархитектонику эпителия нижней трети пищевода.
Материал и методы
На базе УЗ «ГКБ № 2 г. Гродно» проведено одномоментное кросс-секционное сравнительное исследование, в которое было включено 108 человек, медиана возраста обследованных составила 49 (43,5; 54) лет. Все пациенты дали письменное согласие на участие в исследовании. Протокол исследования был одобрен этическим комитетом учреждения.
Критерии включения в исследование: возраст от 30 до 60 лет, жалобы на храп и/или остановки дыхания во сне, наличие клинических маркеров СОАГС (абдоминальное ожирение, окружность шеи более 43 см у мужчин и более 37 см у женщин, микро- и/или ретрогнатия), письменное информированное согласие на участие в исследовании.
Критерии невключения: хроническая ишемическая болезнь сердца выше II функционального класса стенокардии; недостаточность кровообращения выше IIА; язва желудка и/или двенадцатиперстной кишки; медикаментозное поражение желудка и двенадцатиперстной кишки; пищевод Баррретта; аденокарцинома пищевода; хронические декомпенсированные заболевания печени, почек, легких; ЛОР-патология, требующая хирургической коррекции; прием препаратов, влияющих на тонус нижнего пищеводного сфинктера и функцию дыхания во сне [10].
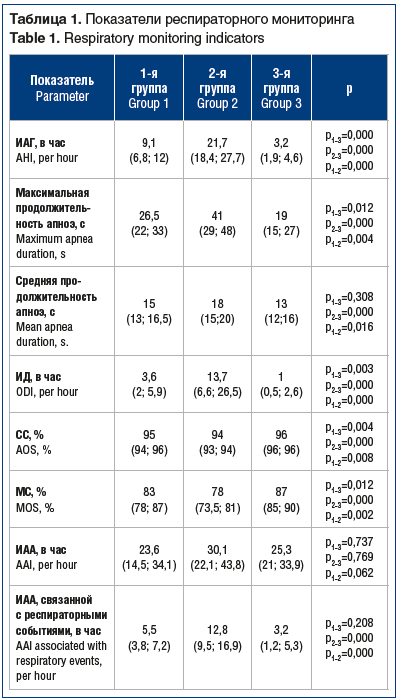
Отбор пациентов с СОАГС был основан на анализе жалоб на храп, остановки дыхания во сне, дневную сонливость. Также использовали опросник Эпворта для оценки степени выраженности дневной сонливости [11]. Отобранным пациентам выполнено сомнологическое исследование с помощью аппарата SOMNOcheck micro (Weinmann); рассчитывались следующие параметры: количество и длительность эпизодов апноэ и гипопноэ, индекс апноэ/гипопноэ (ИАГ), индекс десатурации (ИД), средняя сатурация (СС) кислорода, минимальная сатурация (МС), индекс автономной активации (ИАА), а также ИАА, связанной с респираторными событиями, средняя продолжительность апноэ, максимальная продолжительность апноэ [10].
Степень тяжести СОАГС устанавливали по значению ИАГ: легкая степень тяжести СОАГС — при ИАГ, равном или более 5 в час и менее 15 в час, средняя степень — равном или более 15 в час и менее 30 в час, тяжелая степень — равном или более 30 в час [12]. Пациентов с тяжелой степенью СОАГС из исследования исключали по причине выявленной в процессе детального обследования сопутствующей патологии, относящейся к критериям невключения.
Пациенты были разделены на 3 группы. Первую группу (n=49) составили пациенты с СОАГС легкой степени тяжести, 2-ю группу (n=29) — пациенты с СОАГС средней степени тяжести, 3-ю группу (группа сравнения, n=30) — пациенты без СОАГС. Группы были сопоставимы по возрасту и полу пациентов.
Всем пациентам была выполнена эзофагогастродуоденоскопия с визуальной оценкой состояния слизистой оболочки. Далее выполняли биопсию слизистой пищевода на 3 см выше Z-линии, при наличии измененной слизистой оболочки — из этой области.
Биопсийный материал использовали для изготовления микропрепаратов слизистой оболочки пищевода с окраской гематоксилином и эозином для последующей морфологической оценки изменений в эпителии. Подготовку гистологических срезов проводили по стандартной методике, после чего срезы подвергали световой микроскопии. Затем выполняли морфометрическое исследование с помощью компьютерного анализатора изображения при разных увеличениях микроскопа Axioscop 2 plus (Carl Zeiss, Германия) и цифровой видеокамеры Leica DFC 320 (Германия), используя программу Image Warp (Bit Flow, США). Измеряли толщину эпителия, длину соединительнотканных сосочков, межъядерные расстояния в различных слоях эпителия.
Экспрессию Е-кадгерина оценивали по результатам иммуногистохимического окрашивания препаратов эпителия пищевода моноклональными антителами к Е-кадгерину (Novus Biologicals, США). Для количественной оценки результатов окрашивания были сделаны фотографии микропрепаратов в максимально возможном количестве неперекрывающихся полей зрения с использованием объектива ×10 с разрешением 1600×1200 пикселей при помощи микроскопа Leica и цифровой камеры Leica 425 C. Оценку экспрессии Е-кадгерина проводили с помощью компьютерной программы для обработки цифровых изображений Aperio Image Scope v9.1.19.1567 с вычислением позитивности (в интерфейсе программы positivity), определяемой программой по стандартному алгоритму подсчета позитивных пикселей Positive Pixel Count v9. Показатель позитивности представляет собой отношение числа позитивно окрашенных пикселей к общему числу пикселей на участках, подлежащих оценке [13]. Иммуногистохимический анализ был выполнен у 58 пациентов, из них 26, 15 и 17 из 1-й, 2-й и 3-й группы соответственно.
Данные обрабатывали непараметрическими методами пакета прикладных программ Statistica 10.0 для Windows. Сравнение между тремя группами осуществляли с помощью критерия Краскела — Уоллиса с апостериорным сравнением по методу Данна — Бонферрони. Оценку корреляционных связей проводили с применением коэффициента корреляции Спирмена (r). Различия признавали статистически значимыми при р<0,05. Данные приведены в виде медианы, 25-го и 75-го квартилей [10].
Результаты
В таблице 1 представлены показатели респираторного мониторинга, демонстрирующие различия между группами.
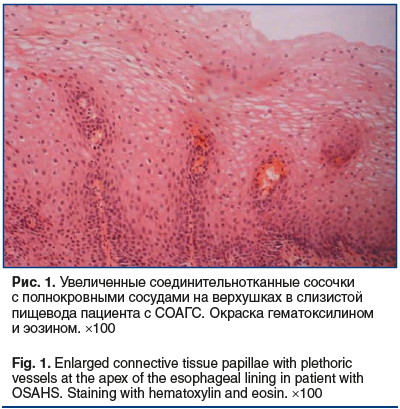
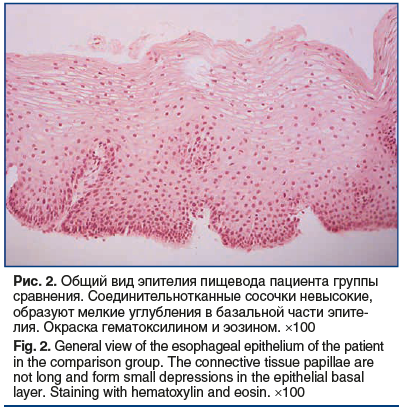
Сравнение морфометрических показателей и экспрессии Е-кадгерина в эпителии пищевода показало, что пациенты с СОАГС в отличие от группы сравнения имели некоторые признаки дезорганизации эпителиальной ткани пищевода, а именно: более выраженную толщину эпителия, более высокие соединительнотканные сосочки, расширенные межъядерные пространства во всех слоях эпителия (табл. 2). В ряде случаев у пациентов с СОАГС определялись признаки микроангиопатии с расширенными капиллярами на верхушках соединительнотканных сосочков (рис. 1), чего не наблюдалось в группе сравнения (рис. 2).
При изучении экспрессии Е-кадгерина было установлено, что пациенты как с легкой, так и со средней степенью тяжести СОАГС характеризовались более низкой экспрессией Е-кадгерина в отличие от пациентов группы сравнения. Кроме того, были обнаружены статистически значимые различия между пациентами с легкой и средней степенью тяжести СОАГС. Анализ данных иммуногистохимического анализа показал, что при возрастании степени тяжести СОАГС экспрессия Е-кадгерина в слизистой оболочке пищевода снижается. На изображениях, полученных при обработке микрофотографий компьютерной программой, можно оценить уровень экспрессии Е-кадгерина (рис. 3).

Корреляционный анализ позволил выявить связь между экспрессией Е-кадгерина в эпителии пищевода и показателями респираторного мониторинга: ИАГ (r=-0,5, p<0,05); ИАА, связанной с респираторными событиями (r=-0,42, p<0,05); максимальной продолжительностью апноэ (r=-0,33, p<0,05); ИД (r=-0,32, p<0,05); СС (r=0,33, p<0,05).
Обсуждение
Установленные различия между группами и обнаруженные корреляционные связи свидетельствуют о негативном влиянии СОАГС на состояние слизистой оболочки пищевода и дополняют ранее опубликованные данные [14]. Снижение в эпителии экспрессии Е-кадгерина, молекулы клеточной адгезии, у пациентов с СОАГС подтверждает выявленные гистологические признаки дезорганизации эпителиального пласта.
Основываясь на данных литературы, можно предположить следующие механизмы реализации негативного влияния хронической интермиттирующей гипоксии при СОАГС на состояние эпителия пищевода. В экспериментальном исследовании при моделировании карциномы пищевода в условиях гипоксии было обнаружено, что снижение экспрессии Е-кадгерина происходит за счет активации гипоксия-индуцибельного фактора 1α (HIF-1α) [15, 16]. Установлено, что при СОАГС в связи с развитием хронической интермиттирующей гипоксии также происходит повышение содержания HIF-1α [17]. HIF-1α участвует в регуляции клеточного метаболизма в условиях гипоксии и стимулирует ангиогенез. Однако при развитии хронической интермиттирующей гипоксии биологический эффект HIF-1α носит дезадаптационный характер, тормозит процессы апоптоза [18]. Увеличение экспрессии данного фактора отмечается при некоторых злокачественных новообразованиях [19–21]. Кроме уже перечисленного, имеются указания на то, что СОАГС может способствовать метастазированию карциномы in situ, поскольку сопровождается гиперпродукцией матриксной металлопротеиназы 2-го типа, способной разрушать базальную мембрану за счет расщепления коллагена IV типа, участвующего в ее формировании [15, 16].
Заключение
Таким образом, по результатам исследования установлено, что у пациентов с СОАГС отмечается снижение экспрессии Е-кадгерина в эпителии пищевода и создаются условия для дезорганизации эпителиальной ткани, что подтверждено гистологически. При воздействии ряда неблагоприятных факторов на эпителий пищевода (например, воспалительных процессов, рецидивирующей нелеченой гастроэзофагеальной рефлюксной болезни, тонкокишечной метаплазии и пищевода Барретта) интермиттирующая гипоксия у пациентов с СОАГС может усугублять нарушения гистоархитектоники эпителия пищевода, затруднять процессы репарации и тормозить процессы апоптоза, повышая риск ЭМТ и аденокарциномы пищевода. Необходимы проведение проспективных исследований с анализом конечных точек для подтверждения выдвинутой гипотезы, а также более углубленное изучение механизмов канцерогенеза при
СОАГС с целью разработки лекарственных препаратов направленного действия.
Сведения об авторе:
Шелкович Юлия Яновна — ассистент 2-й кафедры внутренних болезней, ГрГМУ, 230009, Республика Беларусь, г. Гродно, ул. Горького, д. 80, ORCID 0000-0001-5942-3778.
Контактная информация: Шелкович Юлия Яновна, e-mail: lazarilin@mail.ru. Прозрачность финансовой деятельности: автор не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 28.08.2020, поступила после рецензирования 11.09.2020, принята в печать 25.09.2020.
About the author:
Yulia Ya. Shelkovich — Assistant Professor of the 2nd Department of Internal Medicine, Grodno State Medical University: 80, Gorkogo str., Grodno, 230009, Republic of Belarus, ORCID iD 0000-0001-5942-3778.
Contact information: Yulia Ya. Shelkovich, e-mail: lazarilin@mail.ru. Financial Disclosure: the author has not a financial or property interest in any material or method mentioned. There is no conflict of interest. Received 28.08.2020, revised 11.09.2020, accepted 25.09.2020.
2. Senaratna C.V., Perret J.L., Lodge C.J. et al. Prevalence of obstructive sleep apnea in the general population: A systematic review. Sleep Med Rev. 2017;34:70–81. DOI: 10.1016/j.smrv.2016.07.002.
3. Jara S.M., Phipps A.I., Maynard C. et al. The Association of Sleep Apnea and Cancer in Veterans. Otolaryngol Head Neck Surg. 2020;162(4):581–588. DOI: 10.1177/0194599819900487.
4. Chen C.Y., Hu J.M., Shen C.J. et al. Increased incidence of colorectal cancer with obstructive sleep apnea: a nationwide population-based cohort study. Sleep Med. 2020;66:15–20. DOI: 10.1016/j.sleep.2019.02.016.
5. Gao X.L., Jia Z.M., Zhao F.F. et al. Obstructive sleep apnea syndrome and causal relationship with female breast cancer: a mendelian randomization study. Aging (Albany NY). 2020;12(5):4082–4092. DOI: 10.18632/aging.102725.
6. Sillah A., Watson N.F., Schwartz S.M. et al. Sleep apnea and subsequent cancer incidence. Cancer Causes Control. 2018;29(10):987–994. DOI: 10.1007/s10552-018-1073-5.
7. Geramizadeh B., Salehzadeh A., Taghavi A. et al. Comparison of proliferative (Ki67) and cell adhesion (E-cadherin) markers between gastric intestinal metaplasia and Barrett’s esophagus. Indian J Gastroenterol. 2009;28(3):115–116. DOI: 10.1007/s12664-009-0040-1.
8. Daulagala A.C., Bridges M.C., Kourtidis A. E-cadherin beyond structure: a signaling hub in colon homeostasis and disease. Int J Mol Sci. 2019;20(11):1–17. DOI: 10.3390/ijms20112756.
9. Пучинская М.В. Эпителиально-мезенхимальный переход в норме и патологии. Архив патологии. 2015;77(1):75–83. DOI: 10.17116/patol201577175-.
10. Шелкович Ю.Я. Роль Е-кадгерина в оценке повреждения слизистой оболочки пищевода у пациентов с гастроэзофагеальной рефлюксной болезнью, ассоциированной с синдромом обструктивного апноэ/гипопноэ сна. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2019;29(3):25–32. DOI: 10.25298/2616-5546-2019-3-2-184-189.
11. Касымова О.Д. Диагностика синдрома обструктивного апноэ сна в условиях общесоматического стационара. Клиническая медицина Казахстана. 2011;22,23 (3–4):12–14.
12. Алексеева О.В., Шнайдер Н.А., Демко И.В. и др. Синдром обструктивного апноэ/гипопноэ сна: критерии степени тяжести, патогенез, клинические проявления и методы диагностики. Сибирский медицинский журнал (Иркутск). 2016;1:91–96.
13. Штабинская Т.Т., Басинский В.А., Ляликов С.А. и др. Ангиогенез в аденокарциноме толстой кишки. Гродно: ГрГМУ; 2018.
14. Шелкович Ю.Я., Шишко В.И., Басинский В.А. и др. Экспрессия Е-кадгерина в слизистой оболочке пищевода у пациентов с гастроэзофагеальной рефлюксной болезнью и/или синдромом обструктивного апноэ/гипопноэ сна. Гепатология и гастроэнтерология. 2019;3(2):184–189. DOI: 10.25298/2616-5546-2019-3-2-184-189.
15. Jing S.W., Wang Y.D., Kuroda M. et al. HIF-1α contributes to hypoxia-induced invasion and metastasis of esophageal carcinoma via inhibiting E-cadherin and promoting MMP-2 expression. Acta Med Okayama. 2012;66(5):399–407.
16. Jing S.W., Wang Y.D., Kuroda M. et al. Hypoxia suppresses E-cadherin and enhances matrix metalloproteinase-2 expression favoring esophageal carcinoma migration and invasion via hypoxia inducible factor-1 alpha activation. Dis Esophagus. 2013;26(1):75–83. DOI: 10.1111/j.1442-2050.2011.01321.x.
17. Балабанович Т.И., Шишко В.И., Шулика В.Р. Влияние синдрома обструктивного апноэ/гипопноэ сна на уровни тканевого ингибитора матриксных металлопротеиназ-1 и индуцируемого гипоксией фактора-1α у пациентов с фибрилляцией предсердий. Журнал Гродненского государственного медицинского университета. 2020;18(3):264–270. DOI: 10.25298/2221-8785-2020-18-3-264-270.
18. Маркин А.В., Мартыненко Т.И., Костюченко Г.И. и др. Факторы риска сердечно-сосудистых заболеваний у больных с синдромом обструктивного апноэ сна. Клиницист. 2014;1:15–20.
19. Semenza G.L. Targeting HIF-1 for cancer therapy. Nat Rev Cancer. 2003;3(10):721–732. DOI:10.1038/nrc1187.
20. Zhong H., De Marzo A.M., Laughner E. et al. Overexpression of hypoxia-inducible factor 1alpha in common human cancers and their Metastasis. Cancer Res. 1999;59(22):5830–5835.
21. Talks K.L., Turley H., Gatter K.C. et al. The expression and distribution of the hypoxia-inducible factors HIF-1alpha and HIF-2alpha in normal human tissues, cancers, and tumor-associated macrophages. 2000;157(2):411–421. DOI: 10.1016/S0002-9440 (10) 64554-3.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
