Случай гастроинтестинальной стромальной опухоли желудка
DOI: 10.32364/2587-6821-2021-5-6-433-437
Гастроинтестинальные стромальные опухоли (ГИСО) являются наиболее распространенными злокачественными подслизистыми новообразованиями желудочно-кишечного тракта, с преимущественной локализацией в желудке и тонкой кишке. Особенность заболевания заключается в отсутствии специфических клинических признаков, не менее трети случаев выявляются во время обследований или хирургических вмешательств по поводу других заболеваний или на аутопсии. Алгоритм обследования больных с подозрением на ГИСО включает в себя эндоскопические и лучевые методы диагностики, в том числе ряд дорогостоящих высокотехнологичных, таких как эндоскопическая ультрасонография, компьютерная томография, иммуногистохимические и молекулярно-генетические исследования биопсийного материала. Только проведение полного комплекса обследований позволит своевременно верифицировать диагноз и выбрать оптимальную лечебную стратегию в отношении заболевания, имеющего высокий потенциал озлокачествления. Авторами приведено собственное клиническое наблюдение пациентки с ГИСО с типичной клинико-морфологической картиной, представляющее значительный интерес для клиницистов. Заболевание дебютировало у пациентки в возрасте старше 60 лет, протекало под маской органической диспепсии. В данном случае привлечение дорогостоящих высокотехнологичных методов позволило верифицировать диагноз ГИСО и направить пациентку на оперативное лечение.
Ключевые слова: гастроинтестинальная стромальная опухоль, опухоль желудка, эндоскопическая ультрасонография, иммуногистохимическое исследование, дифференциальная диагностика.
Для цитирования: Скворцова Т.Э., Оганезова И.А., Медведева О.И., Жорина О.М., Беляков И.А., Воробьев С.Л. Случай гастроинтестинальной стромальной опухоли желудка. РМЖ. Медицинское обозрение. 2021;5(6):433-437. DOI: 10.32364/2587-6821-2021-5-6-433-437.
T.E. Skvortsova1, I.A. Oganezova1, O.I. Medvedeva1, O.M. Zhorina1, I.A. Belyakov2, S.L. Vorobiev2
1I.I. Mechnikov North-Western State Medical University, St. Petersburg, Russian Federation
2National Center for Clinical Morphological Diagnostics LLC, St. Petersburg, Russian Federation
Gastrointestinal stromal tumors (GIST) are the most common malignant submucosal neoplasms of the gastrointestinal tract, with predominant localization in the stomach and small intestine. The disease pattern is the absence of specific clinical signs, at least a third of cases are detected during examinations or surgical interventions for other diseases or at an autopsy. The examination algorithm of patients with suspected GIST includes endoscopic and radiation diagnostic methods, including a number of high-tech and expensive techniques, such as endoscopic ultrasonography, computed tomography, immunohistochemical and molecular genetic methods for studying biopsy material. Only conducting a full set of examinations will allow timely diagnosis and choosing the optimal treatment tactics for the disease with a high risk of malignancy. The authors present their own clinical case of a patient, female, with GIST, which is of considerable interest to clinicians. The above clinical case represents a typical clinical and morphological picture of GIST. The disease onset occurred in a patient over the age of 60 years and proceeded under the guise of organic dyspepsia. In this case, the use of expensive high-tech techniques allowed to verify the diagnosis of GIST and refer the patient to surgical treatment.
Keywords: gastrointestinal stromal tumor, stomach tumor, endoscopic ultrasonography, immunohistochemistry, differential diagnosis.
For citation: Skvortsova T.E., Oganezova I.A., Medvedeva O.I. et al. Gastrointestinal stromal tumor of the stomach (clinical case). Russian Medical Inquiry. 2021;5(6):433–437 (in Russ.). DOI: 10.32364/2587-6821-2021-5-6-433-437.
Введение
Гастроинтестинальные стромальные опухоли (ГИСО) считаются редкими мезенхимальными новообразованиями, первичная заболеваемость оценивается от 7 до 20 слу-чаев на 1 млн человек в год. Однако среди злокачественных подслизистых образований желудочно-кишечного тракта именно ГИСО являются наиболее распространенными. Диагностируют заболевание, как правило, у пациентов старше 60 лет, без выраженного полового диморфизма. ГИСО могут обнаруживаться на всем протяжении пищеварительной трубки, чаще всего они локализуются в желудке (50–60%) или в тонкой кишке (25–35%), также могут встречаться в толстой (<7%) или прямой (<5%) кишке, очень редко в пищеводе (1%). Встречаются первичные ГИСО, локализующиеся вне полых органов, например в сальнике или забрюшинном пространстве [1, 2].
Гистологическими вариантами ГИСО являются веретеноклеточный (70%), эпителиоидноклеточный (20%) или смешанный типы (10%). Могут присутствовать клеточноядерный полиморфизм, участки склероза и гиалиноза (склерозирующий тип), миксоидной трансформации стромы. Встречаются палисадоподобные и гиперклеточные субтипы; первый, как правило, выявляется в ГИСО по ходу тонкой кишки, последний нередко сопровождается высокой митотической активностью [3].
Ранее считалось, что ГИСО происходят из гастроинтестинальных стромальных клеток, однако в настоящее время установлено, что ГИСО развиваются из интерстициальных клеток Кахаля, в результате онкогенных мутаций в рецепторе тирозинкиназы (KIT) или в α-рецепторе фактора роста тромбоцитов (Platelet Derived Growth Factor Receptor α, PDGFR-α). Мутации KIT имеют 56–92% больных ГИСО, у 5–10% пациентов обнаруживают мутации PDGFR-α, при этом мутации KIT и PDGFR-α являются взаимоисключающими. Мутации KIT чаще локализуются в 11 (70%) и 9 (10%) экзонах, реже в экзонах 13 (1%) или 17 (1%). Мутации PDGFR-α локализуются в экзонах 18 (5%), 12 (1%), или 14 (<1%). ГИСО с мутациями PDGFR-α чаще всего исходят из желудка (90–93%). Выделяют также дикий тип ГИСО (12–15%), без мутаций в рецепторах KIT и PDGFR-α, который может быть классифицирован на группы в зависимости от наличия или отсутствия дефицита сукцинатдегидрогеназы (СДГ). Группа дефицита СДГ включает триаду Carney и синдром Carney — Stratakis, группа без дефицита СДГ включает нейрофиброматоз 1 типа и ГИСО с BRAF-, KRAS-, PIK3CA-мутациями. Считается, что дикий тип ГИСО обладает более низким потенциалом малигнизации [4–6].
Клиническая картина, диагностика и дифференциальная диагностика ГИСО
Особенностью ГИСО является бессимптомное течение на ранней стадии заболевания и отсутствие специфических клинических признаков. По данным литературы, от 15% до 30% ГИСО протекают бессимптомно и диагностируются случайно — во время обследований или хирургических вмешательств по поводу других заболеваний или на аутопсии (10%). По мере роста опухоли появляются неспе-цифические симптомы, такие как боль в эпигастрии, утомляемость, тошнота, анорексия, потеря массы тела и др. Изъязвление слизистой оболочки может привести к развитию желудочно-кишечного кровотечения с последующей анемией, что требует тщательной дифференциальной диагностики с пептическими язвами желудка и двенадцатиперстной кишки. Также могут наблюдаться симптомы, обусловленные сдавлением/стенозированием просвета определенного участка пищеварительной трубки: описаны случаи билиарной обструкции на фоне ГИСО ампулы фатерова соска, дисфагии при поражении пищевода, констипации, обусловленной ГИСО прямой кишки [7, 8].
Алгоритм обследования больных с подозрением на ГИСО включает в себя эндоскопические и лучевые методы диагностики. Эндоскопическая картина довольно вариабельна: образования могут иметь размеры от 1–2 до 20–30 см. При небольшом размере опухолевого узла эндоскопическая картина может соответствовать, в зависимости от характера роста, неизмененному органу (при экстраорганной форме), сдавлению извне (при смешанной форме) или подслизистому образованию (при эндоорганной форме). Дифференциальная диагностика включает в себя широкий круг нозологических единиц: экзоорганные компрессии, подслизистые варикозные узлы, аберрантную поджелудочную железу, инфильтративный рак, лейомиому, шванному, липому и др. Получить достаточный гистологический материал для диагностики ГИСО при стандартной эндоскопии очень сложно, так как опухоль покрыта нормальной слизистой [9–11].
Ключевым методом дифференциальной диагностики является эндоскопическая ультрасонография (ЭУС), которая позволяет с высокой точностью отличить ГИСО (гипоэхогенные солидные массы) от других подслизистых образований, а при выполнении ЭУС-ассистированной тонкоигольной биопсии возможен забор материала из подслизистого образования для последующего морфологического и иммуногистохимического (ИГХ) исследования [12, 13].
Компьютерная томография (КТ) используется в качестве уточняющего метода диагностики, так как дает более четкое представление о размере, характере роста опухоли, инвазии соседних органов и структур, а также наличии метастазов. На компьютерной томограмме ГИСО выглядят как образования с неоднородной внутренней структурой и четкими контурами, при внутривенном контрастировании отмечается выраженное неравномерное «усиление» опухолевых масс в ранние фазы исследования [14, 15].
Основным методом верификации ГИСО является ИГХ-исследование с определением специфических маркеров. Для ИГХ-картины ГИСО характерна экспрессия CD117 (KIT, экспрессируется до 95% всех ГИСО), аноктамина 1 (DOG1, определяется в 87% случаев), CD34 (обнаруживают в 60–70% опухолей) и ряда других маркеров (гладкомышечный актин, десмин, S-100, общий кератин). Согласно рекомендациям ведущих онкологических сообществ диагноз ГИСО устанавливают на основании морфологического исследования биоптатов с обязательным проведением ИГХ-исследования на выявление вышеуказанных маркеров [7, 11, 16–18].
Лечение и прогноз
Хирургическое вмешательство в настоящее время применяется как основной метод лечения больных с локализованными и местно-распространенными формами ГИСО. При нерезектабельных опухолях, наличии метастазов или при рецидиве ГИСО лечение заключается в назначении ингибиторов тирозинкиназы (иматиниб) [17, 19]. По различным данным, от 10% до 30% ГИСО имеют злокачественный потенциал. ГИСО принято классифицировать по риску малигнизации: очень низкий, низкий, умеренный, высокий. Основными прогностическими факторами для ГИСО, согласно современным международным консенсусам, являются митотический индекс (количество митозов на площади 5 мм2 опухоли при увеличении 400), размер и локализация опухоли. При этом риск метастазирования ГИСО увеличивается в зависимости от размера первичной опухоли, независимо от митотического индекса. Также необходимо отметить значение маркера пролиферативной активности Ki-67, уровень экспрессии которого достоверно повышается с ростом риска агрессивности ГИСО, что используют для оценки степени злокачественности и прогноза. Принято считать, что ГИСО желудка при прочих равных характеристиках имеют более благоприятный прогноз [18, 20, 21].
Определение типов мутаций в различных экзонах KIT и PDGFR-α также является важным прогностическим маркером, который позволяет судить как о клиническом течении заболевания, так и о предполагаемом ответе опухоли на терапию ингибиторами тирозинкиназы [22]. По данным метаанализа L. Yan et al. [23] (20 исследований, 3780 пациентов), выживаемость без прогрессирования ГИСО была значительно хуже у пациентов с мутациями экзона 9 KIT, чем у пациентов с мутациями экзона 11 KIT (отношение шансов [ОШ] 3,60, 95% доверительный интервал [ДИ] 2,17–5,98, z=4,96, p<0,00001, гетерогенность I2=0%). Мутации KIT значительно чаще наблюдались у пациентов с большим размером (≥5 см) ГИСО (ОШ 1,51, 95% ДИ 1,05–2,17, z=2,22, p=0,03, гетерогенность I2=0%, p=0,97), а также у пациентов с более высоким (≥5/50 HPFs) митотическим индексом (ОШ 1,76, 95% ДИ 1,05–2,95, z=2,15, p=0,03, гетерогенность I2=57%, p=0,03).
Собственное клиническое наблюдение ГИСО
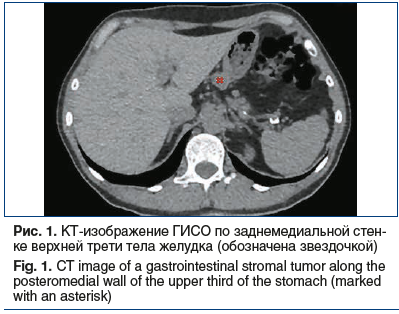
Пациентка Б., 67 лет, в марте 2019 г. обратилась к терапевту по месту жительства с жалобами на боли слабой интенсивности в эпигастрии, эпизоды головокружения на фоне болевого синдрома, тошноту после приема пищи, изжогу, а также боли в гипогастрии, не связанные с актом дефекации и мочеиспусканием. Стул ежедневный, тип 4 по Бристольской шкале, без патологических примесей. Ухудшение самочувствия отмечает в последние 2 мес. В течение длительного времени страдает хроническим гастритом, хроническим некалькулезным холециститом. При физикальном обследовании состояние удовлетворительное; патологических изменений со стороны сердечно-сосудистой и дыхательной систем не выявлено; живот не вздут, мягкий, болезненный при пальпации в эпигастрии, в проекции поперечно-ободочной кишки. Анализы крови в пределах референсных значений. По данным УЗИ органов брюшной полости от 08.04.2019 печень не увеличена, эхогенность ее не изменена, диаметр воротной вены 10 мм, диаметр холедоха 4 мм; желчный пузырь с перегибами, стенки 2 мм, не утолщены, в просвете эхопозитивный подвижный осадок; поджелудочная железа размерами 16×10×14 мм, в области тела лоцируется гипоэхогенное образование 21×20 мм. Для уточнения характера выявленных изменений 23.04.2019 пациентке выполнена КТ органов грудной клетки и брюшной полости с внутривенным контрастированием (йопамидол). На серии снимков легких с двух сторон выявлены очаги с четкими, неровными, бугристыми контурами, накапливающие контрастный препарат с повышением плотности от 13 HU до 93 HU (справа в S3 размерами 8×10 мм, в аксиллярном субсегменте — до 7 мм, слева в S5 — до 3 мм), небольшие участки уплотнения легочной ткани в S6 слева и S9 справа. Увеличенных внутригрудных лимфатических узлов не выявлено. На серии снимков органов брюшной полости по заднемедиальной стенке верхней трети желудка выявлено образование, расположенное кнаружи от желудка, размерами 18×21×13 мм, с четкими контурами, накапливающее контрастный препарат с повышением плотности от 41 HU до 71 HU (рис. 1).
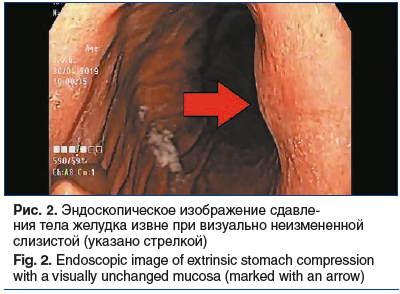
Образование прилежит к стенке желудка на протяжении около 10 мм. Структура паренхимы печени однородная, равномерно накапливает контрастный препарат. Внутри- и внепеченочные желчные протоки не расширены. Желчный пузырь не увеличен, содержимое его однородное, рентгеноконтрастных конкрементов не выявлено, утолщения стенки нет. Воротная и селезеночная вены не расширены, селезенка не увеличена, однородной структуры. Поджелудочная железа не увеличена, однородной структуры, очагов патологического накопления контрастного препарата не выявлено, парапанкреатическая клетчатка не инфильтрирована. Грудной и поясничный отделы позвоночника с дегенеративно-дистрофическими изменениями. Структура тел грудных и поясничных позвонков, а также подвздошных костей неоднородная за счет множественных зон разрежения костной структуры с четкими контурами. Выявляются зоны остеосклероза в теле L4 (4 мм) и в теле левой подвздошной кости (4×6 мм), гемангиома в теле Th9. Для уточнения характера костных изменений выполнена остеосцинтиграфия, убедительных данных за специфическое поражение скелета не получено. С учетом выявленного экзофитного образования, исходящего из желудка, 30.04.2019 пациентке выполнено стандартное эндоскопическое исследование: пищевод свободно проходим, слизистая гиперемирована, на всем протяжении определяется творожистый несмещаемый белесоватый налет. Розетка кардии зияет. Слизистая оболочка желудка пролабирует в пищевод, в области пищеводно-желудочного перехода — кольцо Шацкого с ранимой слизистой в этой области. Форма желудка не изменена. Слизистая диффузно гиперемирована, в антральном отделе 4 острые эрозии под фибрином размерами до 3 мм. По задней стенке желудка визуализируется незначительное сдавление просвета желудка извне на фоне неизмененной слизистой (рис. 2). Для уточнения характера новообразования 17.06.2019 пациентке выполнена ЭУС: в верхней трети тела желудка по малой кривизне, ближе к задней стенке определяется подслизистое образование размером до 15 мм, округлой формы, умеренно выступающее в просвет желудка без его деформации, покрытое неизмененной слизистой. Образование плотное при инструментальной пальпации. При сканировании стенки желудка с частотой 7,5–12 МГц определяется округлой формы, негомогенное, преимущественно гипоэхогенное образование размером до 20 мм, исходящее из мышечной стенки, с преимущественным экстраорганным ростом, с выраженным кровотоком (рис. 3).
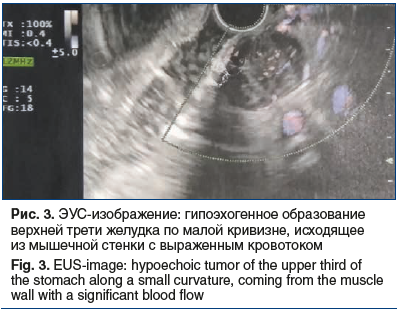
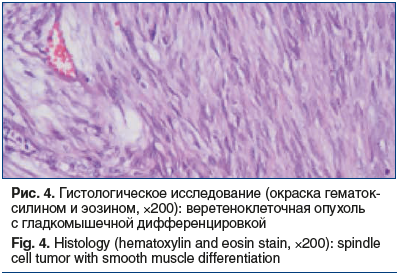
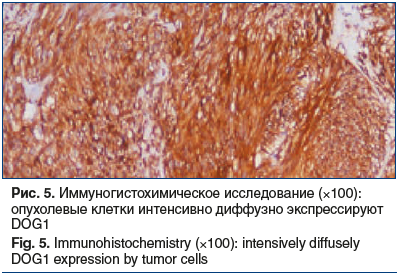
После проведения антимикотической терапии (флуконазол 150 мг/сут 14 дней) 10.07.2019 пациентке выполнена энуклеация экстраорганного образования тела желудка с применением эндоскопической видеоассистенции. Гистологическое исследование удаленного образования: округлое, четко инкапсулированное мезенхимальное, диаметром 2,7 см, представлено веретеновидными клетками без клеточного полиморфизма с обильным коллагеновым матриксом. Картина наиболее характерна для склерозирующего варианта ГИСО. Материал был отправлен на дополнительное исследование в ООО «Национальный центр клинической морфологической диагностики», где 10.07.2019 выполнено патогистологическое исследование удаленного образования. Макроописание: округлый плотный узел диаметром 2,7 см с крупнобугристой поверхностью, на разрезе серый, волокнистый, с множественными точечными кровоизлияниями. Микроописание: четко отграниченное мезенхимальное новообразование диаметром 2,7 см представлено веретеновидными клетками с гладкомышечной дифференцировкой, с минимальным клеточно-ядерным полиморфизмом, участками обильной коллагенизации. Картина наиболее характерна для склерозирующего варианта ГИСО (рис. 4). При ИГХ-исследовании в материале определяются структуры веретеноклеточной опухоли, местами с муаровым паттерном, очаговым фиброзом и гиалинозом. Митотическая активность низкая — менее 5 митозов на 5 мм2 при увеличении 400. Опухолевые клетки интенсивно экспрессируют CD34, DOG1, очагово экспрессируют десмин и не экспрессируют S-100 протеин (рис. 5). Индекс пролиферативной активности Ki-67 в пределах 2–5%. Заключение: гистологическая картина и иммунофенотип опухоли соответствуют гастроинтестинальной стромальной опухоли, GIST, 2-я группа. Пациентка была направлена на оперативное лечение.
Заключение
Гастроинтестинальные стромальные опухоли являются редкими мезенхимальными подслизистыми новообразованиями органов пищеварения, не имеют характерных симптомов, сложны в диагностике, и, как следствие, около 50% образований к моменту постановки диагноза успевают метастазировать. Основная стратегия лечения заключается в радикальном хирургическом лечении локализованных и местно-распространенных форм ГИСО, что позволяет добиться общей 5-летней выживаемости у 54–65% больных [2, 19].
Приведенное клиническое наблюдение представляет типичную клинико-морфологическую картину ГИСО. Заболевание дебютировало у пациентки в возрасте старше 60 лет, протекало под маской органической диспепсии. Только привлечение дорогостоящих высокотехнологичных методов — КТ, ЭУС, ИГХ-исследования позволило верифицировать диагноз ГИСО и направить пациентку на оперативное лечение.
Сведения об авторах:
Скворцова Татьяна Эдуардовна — к.м.н., доцент, доцент кафедры пропедевтики внутренних болезней, гастроэнтерологии и диетологии им. С.М. Рысса ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России; 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41; ORCID iD 0000-0002-9362-9961.
Оганезова Инна Андреевна — д.м.н., профессор, профессор кафедры пропедевтики внутренних болезней, гастроэнтерологии и диетологии им. С.М. Рысса ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России; 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41; ORCID iD 0000-0003-0844-4469.
Медведева Ольга Ивановна — к.м.н., доцент, доцент кафедры пропедевтики внутренних болезней, гастроэнтерологии и диетологии им. С.М. Рысса ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России; 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41; ORCID iD 0000-0002-9730-7361.
Жорина Ольга Михайловна — к.м.н., заведующая отделением компьютерной томографии Клиники имени Петра Великого, доцент кафедры лучевой диагностики и лучевой терапии ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России; 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41; ORCID iD 0000-0002-9116-737X.
Беляков Илья Александрович — заведующий патологоанатомическим отделением ООО «Национальный центр клинической морфологической диагностики»; 192283, Россия, г. Санкт-Петербург, ул. О. Дундича, д. 8, корп. 2, лит. А, пом. 6Н; ORCID iD 0000-0002-9100-7608.
Воробьев Сергей Леонидович — к.м.н., директор ООО «Национальный центр клинической морфологической диагностики»; 192283, Россия, г. Санкт-Петербург, ул. О. Дундича, д. 8, корп. 2, лит. А, пом. 6Н; ORCID iD 000-0002-7817-9069.
Контактная информация: Оганезова Инна Андреевна, e-mail: oganezova@rambler.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах и методах.
Конфликт интересов отсутствует.
Статья поступила 14.07.2021.
Поступила после рецензирования 06.08.2021.
Принята в печать 31.08.2021.
About the authors:
Tatyana E. Skvortsova — C. Sc. (Med.), Associate Professor, Associate Professor of the Department of Propaedeutics of Internal Diseases, Gastroenterology and Nutrition named after S.M. Ryss, I.I. Mechnikov North-Western State Medical University; 41, Kirochnaya str., St. Petersburg, 191015, Russian Federation; ORCID iD 0000-0002-9362-9961.
Inna A. Oganezova — Dr. Sc. (Med.), Professor, Professor of the Department of Propaedeutics of Internal Diseases, Gastroenterology and Nutrition named after S.M. Ryss, I.I. Mechnikov North-Western State Medical University; 41, Kirochnaya str., St. Petersburg, 191015, Russian Federation; ORCID iD 0000-0003-0844-4469.
Olga I. Medvedeva — C. Sc. (Med.), Associate Professor, Associate Professor of the Department of Propaedeutics of Internal Diseases, Gastroenterology and Nutrition named after S.M. Ryss, I.I. Mechnikov North-Western State Medical University; 41, Kirochnaya str., St. Petersburg, 191015, Russian Federation; ORCID iD 0000-0002-9730-7361.
Olga M. Zhorina — C. Sc. (Med.), Head of the Department of Computed Tomography at the Clinic named after Peter the Great, Associate Professor of the Department of Radiation Diagnostics and Therapy, I.I. Mechnikov North-Western State Medical University; 41, Kirochnaya str., St. Petersburg, 191015, Russian Federation; ORCID iD 0000-0002-9116-737X.
Ilya A. Belyakov — Head of the Department of Autopsy, National Center for Clinical Morphological Diagnostics LLC; 8 bld. 2A, O. Dundich str., St. Petersburg, 192283, Russian Federation; ORCID iD 0000-0002-9100-7608.
Sergey L. Vorobiev — C. Sc., Director, National Center for Clinical Morphological Diagnostics LLC; 8 bld. 2A, O. Dundich str., St. Petersburg, 192283, Russian Federation; ORCID iD 000-0002-7817-9069.
Contact information: Inna A. Oganezova, e-mail: oganezova@rambler.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 14.07.2021.
Revised 06.08.2021.
Accepted 31.08.2021.
2. Вашакамадзе Л.А., Колобаев И.В., Беспалов П.Д. и др. Гастроинтестинальные стромальные опухоли: классификация, диагностика и лечение. Онкология. Журнал им. П.А. Герцена. 2013;2(2):66–70. [Vashakamadze L.A., Kolobaev I.V., Bespalov P.D. et al. Gastrointestinal stromal tumors: classification, diagnosis and treatment. Onkologiya Zhurnal im P.A. Gercena. 2013;2(2):66–70 (in Russ.)].
3. Халиков Д.Д., Ахметзянов Ф.Ш., Петров С.В. Клинико-морфологическая характеристика гастроинтестинальных стромальных опухолей. Архив патологии. 2017;79(4):48–55. [Khalikov D.D., Axmetzyanov F.Sh., Petrov S.V. Clinical and morphological characteristics of gastrointestinal stromal tumors. Arhiv patologii. 2017;79(4):48–55 (in Russ.)]. DOI: 10.17116/patol201779448-55.
4. Schaefer I.M., Mariño-Enríquez A., Fletcher J.A. What is New in Gastrointestinal Stromal Tumor? Adv Anat Pathol. 2017;24(5):259–267. DOI: 10.1097/PAP.0000000000000158.
5. Brcic I., Kashofer K., Skone D., Liegl-Atzwanger B. KIT mutation in a naïve succinate dehydrogenase-deficient gastric GIST. Genes Chromosomes Cancer. 2019;58(11):798–803. DOI: 10.1002/gcc.22768.
6. Liu Q.Y., Kong L.F., Xu Z.G. et al. Mutation of the KIT Gene, excluding Exon 11, in Gastrointestinal Stromal Tumors. Biomed Environ Sci. 2020;33(5):369–373. DOI: 10.3967/bes2020.050.
7. Бредихина Е.В., Бредихин Е.М. Диагностика и лечение гастроинтестинальных стромальных опухолей (обзор литературы). Медицинские новости. 2017;2:4–7. [Bredixina E.V., Bredixin E.M. Diagnostics and treatment of gastrointestinal stromal tumors (literature review). Medicinskie novosti. 2017;2:4–7 (in Russ.)].
8. Harris P.S., Romano J., Russ K.B. et al. Gastrointestinal Stromal Tumor: GIST Another Duodenal Ulcer. Ochsner J. 2020;20(2):236–238. DOI: 10.31486/toj.18.0167.
9. Cameron S., Beham A., Schildhaus H.U. Current Standard and Future Perspectives in the Treatment of Gastrointestinal Stromal Tumors. Digestion. 2017;95(4):262–268. DOI: 10.1159/000455835.
10. Nakano A., Nakamura M., Watanabe O. et al. Endoscopic Characteristics, Risk Grade, and Prognostic Prediction in Gastrointestinal Stromal Tumors of the Small Bowel. Digestion. 2017;95(2):122–131. DOI: 10.1159/000454728.
11. Akahoshi K., Oya M., Koga T., Shiratsuchi Y. Current clinical management of gastrointestinal stromal tumor. World J Gastroenterol. 2018;24(26):2806–2817. DOI: 10.3748/wjg.v24.i26.2806.
12. Khan S., Zhang R., Fang W. et al. Reliability of Endoscopic Ultrasound Using Miniprobes and Grayscale Histogram Analysis in Diagnosing Upper Gastrointestinal Subepithelial Lesions. Gastroenterol Res Pract. 2020;2020:6591341. DOI: 10.1155/2020/6591341.
13. Lee M.W., Kim G.H. Diagnosing Gastric Mesenchymal Tumors by Digital Endoscopic Ultrasonography Image Analysis. Clin Endosc. 2020;10.5946/ce.2020.061. DOI: 10.5946/ce.2020.061.
14. Jung H., Lee S.M., Kim Y.C. et al. A pictorial review on clinicopathologic and radiologic features of duodenal gastrointestinal stromal tumors. Diagn Interv Radiol. 2020;10.5152/dir.2019.19432. DOI: 10.5152/dir.2019.19432.
15. Peng F., Liu Y. Gastrointestinal Stromal Tumors of the Small Intestine: Progress in Diagnosis and Treatment Research. Cancer Manag Res. 2020;12:3877–3889. DOI: 10.2147/CMAR.S238227.
16. Nishida T., Blay J.Y., Hirota S. et al. The standard diagnosis, treatment, and follow-up of gastrointestinal stromal tumors based on guidelines. Gastric Cancer. 2016;19(1):3–14. DOI: 10.1007/s10120-015-0526-8.
17. Casali P.G., Abecassis N., Bauer S. et al. Gastrointestinal stromal tumours: ESMO-EURACAN Clinical. Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2018;29:iv68–78. DOI: 10.1093/annonc/mdy095.
18. Wu C.E., Tzen C.Y., Wang S.Y., Yeh C.N. Clinical Diagnosis of Gastrointestinal Stromal Tumor (GIST): From the Molecular Genetic Point of View. Cancers (Basel). 2019;11(5):679. DOI: 10.3390/cancers11050679.
19. Ahmed M. Recent advances in the management of gastrointestinal stromal tumor. World J Clin Cases. 2020;8(15):3142–3155. DOI: 10.12998/wjcc.v8.i15.3142.
20. Никулин М.П., Архири П.П., Владимирова Л.Ю. и др. Практические рекомендации по лекарственному лечению гастроинтестинальных стромальных опухолей. Злокачественные опухоли. 2020;10(3s2–1):510–518. [Nikulin M.P., Arxiri P.P., Vladimirova L.Yu. et al. Practical recommendations for the drug treatment of gastrointestinal stromalene tumors. Zlokachestvenny`e opuholi. 2020;10(3s2–1):510–518 (in Russ.)]. DOI: 10.18027/2224-5057-2020-10-3s2-29.
21. Zhang H., Liu Q. Prognostic Indicators for Gastrointestinal Stromal Tumors: A Review. Transl Oncol. 2020;13(10):100812. DOI: 10.1016/j.tranon.2020.100812.
22. Capelli L., Petracci E., Quagliuolo V. et al. Gastric GISTs: Analysis of c-Kit, PDGFRA and BRAF mutations in relation to prognosis and clinical pathological characteristics of patients — A GIRCG study. Eur J Surg Oncol. 2016;42(8):1206–1214. DOI: 10.1016/j.ejso.2016.05.022.
23. Yan L., Zou L., Zhao W. et al. Clinicopathological significance of c-KIT mutation in gastrointestinal stromal tumors: a systematic review and meta-analysis. Sci Rep. 2015;5:13718. DOI: 10.1038/srep13718.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
