Желчнокаменная болезнь: эпидемиологические данные, ключевые аспекты патогенеза и коморбидности, актуальные терапевтические мишени
DOI: 10.32364/2587–6821–2020–4-5-290-296
Обзор посвящен современным научным данным о патогенезе желчнокаменной болезни и имеющимся на сегодняшний день возможностям для оптимизации литолитической терапии. Показано, что желчнокаменную болезнь следует рассматривать как местное проявление системных нарушений метаболического и воспалительного генеза во всем организме. Продемонстрирована ключевая роль в ее развитии инсулинорезистентности, нарушений обмена холестерина, желчных кислот, дискинезии желчных путей и выработки медиаторов воспаления. Выделены факторы, обусловливающие коморбидность желчнокаменной болезни с сердечно-сосудистыми заболеваниями, цереброваскулярными болезнями, раком желудочно-кишечного тракта различной локализации и заболеваниями печени; обоснована роль холелитиаза как фактора риска и критерия неблагоприятного прогноза. Рассмотрен патогенетически оправданный подход к совершенствованию перорального литолиза, обеспечивающий комплексное воздействие терапии; обоснована рациональность использования фиксированной комбинации урсодезоксихолевой кислоты и глицирризиновой кислоты.
Ключевые слова: желчнокаменная болезнь, холелитиаз, холестериновые камни, пероральный литолиз, урсодезоксихолевая кислота, глицирризиновая кислота, комплексная терапия, метаболические нарушения.
Для цитирования: Никитин И.Г., Волнухин А.В. Желчнокаменная болезнь: эпидемиологические данные, ключевые аспекты патогенеза и коморбидности, актуальные терапевтические мишени. РМЖ. Медицинское обозрение. 2020;4(5):290-296. DOI: 10.32364/2587–6821–2020–4-5-290-296.
I.G. Nikitin1,2, A.V. Volnukhin3,4
1Pirogov Russian National Research Medical University, Moscow, Russian Federation
2National Medical Research Center «Treatment and Rehabilitation Center», Moscow,
Russian Federation
3Sechenov University, Moscow, Russian Federation
4JSC Pharmstandard, Moscow, Russian Federation
The article is devoted to current scientific data on the cholelithiasis pathogenesis and opportunities for optimizing litholytic therapy. It is shown that cholelithiasis should be considered as a topical manifestation of systemic disorders of metabolic and inflammatory genesis throughout the body. The article shows the key role in the development of its insulin resistance, imbalanced cholesterol and bile acid metabolism, biliary dyskinesia, and the production of inflammatory mediators. There are factors that cause cholelithiasis comorbidity with cardiovascular diseases, cerebrovascular diseases, gastrointestinal cancer of various localization, and liver diseases. The role of cholelithiasis as a risk factor and a criterion for an adverse prognosis is justified. Pathogenetically justified method for improving oral litholysis, which provides a complex therapy effect, is considered; the rationality of using a fixed combination of ursodeoxycholic acid and glycyrrhizic acid is justi fied.
Keywords: gallstone disease, cholelithiasis, cholesterol stones, oral litholysis, ursodeoxycholic acid, glycyrrhizic acid, complex therapy, metabolic disorders.
For citation: Nikitin I.G., Volnukhin A.V. Cholelithiasis: epidemiological data, key aspects of the pathogenesis and comorbidity, relevant therapeutic targets. Russian Medical Inquiry. 2020;4(5):290–296. DOI: 10.32364/2587–6821–2020–4-5-290-296.
Введение
Желчнокаменная болезнь (ЖКБ) известна врачам уже на протяжении нескольких веков. Впервые данное заболевание было описано Антонио Бенивьени в 1507 г. [1]. В современной медицине под ЖКБ, или холелитиазом, принято понимать хроническое заболевание с генетической предрасположенностью, при котором наблюдается образование камней в желчных путях [2].
Эпидемиологические данные
По данным статистики, в Европе и США ЖКБ страдают 15–20% жителей [3–6]. Эти цифры можно экстраполировать и на Россию. Вместе с тем справедливо будет заметить, что распространенность холелитиаза в разных странах отличается значительной вариабельностью, что определяется генетическими и внешними факторами [5].
Являясь причиной наибольшего числа госпитализаций среди всех заболеваний желудочно-кишечного тракта, ЖКБ также занимает позицию одной из наиболее затратных для здравоохранения болезней пищеварительной системы [3–7].
К основным факторам риска холелитиаза относятся: пожилой возраст; женский пол; беременность; прием эстрогенов в период постменопаузы; высококалорийная диета, богатая легкоусвояемыми углеводами и бедная клетчаткой; избыточная масса тела или ожирение; наследственная предрасположенность [7, 8].
Несмотря на то, что заболевание встречается преимущественно в возрасте старше 40 лет, отмечается повсеместная тенденция к его омоложению. Все чаще данный диагноз ставится в детском и подростковом возрасте. Данный факт связывают прежде всего с увеличением распространенности у этой категории пациентов ожирения, гиподинамии, сахарного диабета, а также с ранней беременностью [4].
По составу камни делят на холестериновые и пигментные. Локализоваться они могут в желчном пузыре, реже — в общем желчном протоке и внутрипеченочных желчных путях. В 80% случаев заболевание протекает бессимптомно и камни обнаруживаются случайно при ультразвуковом исследовании [9]. Из них 80–90% состоят преимущественно из холестерина [7, 8].
Желчнокаменная болезнь и коморбидная патология
Появляется все больше данных, характеризующих ЖКБ не только как самостоятельное заболевание, но и как коморбидную патологию, имеющую тесную этиологическую и патогенетическую связь с другими болезнями. Она может способствовать их развитию и прогрессированию, влиять на исходы. Возможна и обратная связь: определенные заболевания и состояния могут служить дополнительным фактором риска камнеобразования.
Доказано, что пациенты с холелитиазом, особенно женского пола и молодого возраста, имеют более высокий риск развития сердечно-сосудистых и цереброваскулярных заболеваний [4, 10, 11].
Выявлена прямая связь между ЖКБ и раком желчного пузыря, а также раком желудка, гепатоцеллюлярной карциномой, холангиокарциномой, раком поджелудочной железы, колоректальным раком [12].
Установлено, что при наличии ЖКБ риск смерти от всех причин и от онкологической патологии повышается на 30%, а смерти от сердечно-сосудистых заболеваний — на 40% [13].
Ввиду анатомического и физиологического единства гепатобилиарной системы особого внимания заслуживает сочетание холелитиаза с заболеваниями печени. По имеющимся данным, наличие хронического заболевания печени увеличивает вероятность развития ЖКБ в 1,2–5 раз. При этом распространенность холелитиаза растет пропорционально увеличению класса печеночной недостаточности по Чайлду — Пью [6]. Корреляция была установлена для вирусных гепатитов В и С, что, вероятно, связано с прямым повреждающим действием вируса на клетки стенки желчного пузыря. В отношении алкогольной болезни печени однозначные выводы сделать сложно ввиду противоречивости данных, свидетельствующих либо об отсутствии влияния алкоголя на литогенез, либо о его профилактическом потенциале в умеренных дозах [14–17].
Наиболее сильная взаимосвязь определена для холелитиаза и неалкогольной жировой болезни печени (НАЖБП), особенно у пациентов женского пола. При наличии ЖКБ распространенность НАЖБП в 2 раза выше, чем в общей популяции [18], так же как и выше распространенность воспалительной формы заболевания — неалкогольного стеатогепатита [19]. Примечательно, что холецистэктомия не решает проблему, а является независимым фактором риска НАЖБП [20].
В свою очередь, НАЖБП — это независимый фактор риска ЖКБ, который увеличивает вероятность заболевания более чем на 50% [20]. Дополнительными факторами, способствующими камнеобразованию у этих пациентов, являются старший возраст, высокие значения индекса массы тела и женский пол [21]. При этом распространенность холелитиаза прогрессивно увеличивается по мере возрастания стадии НАЖБП [22] и стадии фиброза: на стадии 0–II составляет 15%, на стадии III — 29%, а на стадии IV (цирроз) — 56% [19].
Ключевые аспекты патогенеза ЖКБ и коморбидной патологии
Образование холестериновых камней в желчном пузыре неразрывно связано с нарушением обмена холестерина. Холестерин в организм поступает извне с пищей, а также синтезируется в печени (эндогенный холестерин). Пищевой холестерин всасывается в тонкой кишке в кровь. Попав в системный кровоток, в составе липопротеидов низкой плотности, хиломикронов и липопротеидов высокой плотности он доставляется в гепатоциты. Абсорбированный и синтезированный холестерин составляет пул внутрипеченочного холестерина. Далее его метаболизм осуществляется тремя путями. Холестерин подвергается этерификации и депонируется в гепатоцитах, включается в состав липопротеидов очень низкой плотности и поступает в системный кровоток, используется для синтеза желчных кислот, в составе которых затем выводится с желчью; секретируется с желчью в неизмененном виде. Регуляция синтеза холестерина, желчных кислот и секреции холестерина с желчью осуществляется через фарнезоидные Х-рецепторы. Попадая вместе с желчью в желчные канальцы, холестерин, желчные кислоты и фосфолипиды формируют простые мицеллы (1–2 нм), смешанные мицеллы (4–8 нм), небольшие однослойные везикулы (40–100 нм) или большие многослойные везикулы (300–500 нм) [23].
В формировании холестериновых камней ключевая роль принадлежитинсулинорезистентности, гипергликемии / сахарному диабету, дислипидемии и ожирению [8]. На фоне инсулинорезистентности повышается синтез эндогенного холестерина в печени и его секреция с желчью, что ведет к перенасыщению последней холестерином; нарушается обратный транспорт холестерина в печень в составе липопротеидов высокой плотности; снижается уровень желчных кислот, препятствующих камнеобразованию; отмечается нарушение моторики и эвакуаторной функции желчного пузыря [4, 19]. Аналогичное негативное влияние на опорожнение желчного пузыря, синтез холестерина и состав желчи оказывают гипертриглицеридемия, сахарный диабет и ожирение [21]. Таким образом эти факторы риска реализуют свой литогенный потенциал.
Перенасыщение холестерином и стаз желчи создают условия для образования кристаллов холестерина в просвете желчного пузыря — нуклеации. Ускоряют этот процесс повышенная секреция муцина в просвет желчного пузыря и воспаление его стенки, развивающееся с участием таких медиаторов, как интерлейкин (ИЛ) 6, ИЛ-10, ИЛ-12 (р70), ИЛ-13, фактор некроза опухоли альфа (ФНО-α) и ряд других [24].
Агрегация кристаллов холестерина и их конгломерация с муцином ведут к образованию микроскопических камней, из которых со временем формируются холестериновые камни.
Дополнительными патогенетическими факторами, способствующими реализации данного патогенетического каскада, могут быть определенные генетические полиморфизмы, повышенное всасывание пищевого холестерина и реабсорбция желчного холестерина, вялая перистальтика кишечника, изменение качественного и количественного состава кишечной микробиоты [4].
Более высокая распространенность ЖКБ у женщин обусловлена влиянием эстрогенов, заключающимся в повышении синтеза холестерина и снижении образования желчных кислот [4].
С точки зрения патогенеза связь холелитиаза с сердечно-сосудистыми и цереброваскулярными заболеваниями объясняется общими патогенетическими факторами инсулинорезистентностью, ожирением, сахарным диабетом / гипергликемией, дислипидемией, воспалением и общими генетическими полиморфизмами. В основе связи с онкологической патологией могут быть воспаление и нарушение оттока желчи [5, 6, 11, 19, 21].
При хронических заболеваниях печени повышенный риск камнеобразования в желчном пузыре связан с поражением гепатоцитов, следствием чего являются снижение синтеза и нарушение транспорта желчных кислот, уменьшение секреции аполипопротеинов АI и AII [6]. Немаловажная роль при этом может принадлежать воспалению, обусловливающему повреждение клеток печени и нарушение моторики желчных путей [25].
В основе коморбидности НАЖБП и холелитиаза прежде всего находятся общие метаболические нарушения — сахарный диабет 2 типа, центральное ожирение и инсулинорезистентность [18, 21]. Весомый вклад во взаимное отягчающее влияние двух заболеваний вносит воспаление, запускающее развитие стеатогепатита и фиброгенез в печени, а также поддерживающее литогенез в желчном пузыре [11, 22]. Кроме того, механизм камнеобразования при НАЖБП может быть запущен нарушением липидного обмена, угнетением окисления жирных кислот и усилением липогенеза [26].
После холецистэктомии меняется метаболизм желчных кислот и их регулирующее влияние на обмен глюкозы и липидов в печени через фарнезоидные Х-рецепторы и TGR5. Кроме того, снижается уровень фактора роста фибробластов 19 (FGF19), регулирующего синтез желчных кислот и липогенез в печени, который секретируется преимущественно слизистой оболочкой желчного пузыря [27–29]. Все это может стать причиной развития НАЖБП.
Таким образом, можно констатировать, что образование холестериновых камней в желчном пузыре является следствием сочетанного влияния целого ряда местных и общих факторов, а саму ЖКБ следует рассматривать как проявление системных нарушений метаболического и воспалительного генеза.
Актуальные терапевтические мишени
В соответствии с последними рекомендациями Российской гастроэнтерологической ассоциации [2] при бессимптомном течении ЖКБ показаны наблюдательная тактика, коррекция питания и образа жизни. Следует придерживаться низкоуглеводной диеты, богатой растительным белком, грубой клетчаткой и растительными маслами. Допускается умеренное потребление алкоголя (при отсутствии других противопоказаний). Также необходима адекватная физическая активность, целью которой являются достижение и поддержание нормальной массы тела.
При появлении клинических симптомов методом выбора становится хирургическое лечение — холецистэктомия, которая выполняется открытым или лапароскопическим доступом. Риски для жизни и здоровья пациента, связанные с выполнением холецистэктомии, невысокие. Смертность после операции составляет менее 1%, постхолецистэктомический синдром развивается примерно у 10% пациентов. Возможные негативные последствия холецистэктомии связаны с потерей желчного пузыря как естественного резервуара и нарушением транскишечного транспорта желчных кислот и их сигнальной функции через фарнезоидные Х-рецепторы [4]. Кроме того, после перенесенной холецистэктомии имеет место риск развития НАЖБП.
У ограниченного числа пациентов возможно применение неинвазивного метода — чрескожной ударно-волновой литотрипсии.
У некоторых пациентов может быть применен пероральный литолиз с использованием урсодезоксихолевой кислоты (УДХК) при соблюдении определенных условий: наличии холестериновых камней диаметром менее 20 мм и при функционирующем желчном пузыре [2].
Вопрос назначения УДХК для первичной профилактики камнеобразования является дискуссионным. Тем не менее в рандомизированном контролируемом исследовании было продемонстрировано достоверное снижение риска камнеобразования на фоне приема в течение 24 мес. УДХК после выполнения хирургической операции по формированию обходного желудочного анастомоза [30]. Ряд специалистов считают возможным назначение УДХК коротким курсом с профилактической целью при высоком риске билиарного сладжа или камнеобразования, например после быстрого значительного похудания или бариатрической операции [7]. Этот тезис находит отражение в клинических рекомендациях Европейской ассоциации по изучению болезней печени [3].
Урсодезоксихолевая кислота
УДХК в настоящее время широко применяется для перорального литолиза у пациентов с холелитиазом. Однако первое документальное подтверждение успешного растворения холестериновых камней связано с применением в 1972 г. другой желчной кислоты — хенодезоксихолевой (ХДХК) [31]. Обладая не меньшей эффективностью и повышенной безопасностью, более гидрофильная УДХК быстро заместила ХДХК в клинической практике и именно на основании ее применения сформирована современная база знаний в области перорального литолиза [8].
История использования УДХК для лечения ЖКБ берет свое начало в Китае, где столетиями применяли желчь взрослых черных медведей для лечения различных гепатобилиарных расстройств [8]. В начале XX в. из желчи белого медведя была выделена ХДХК, которая первоначально получила название «урсохолеиновая кислота». В 1927 г. из желчи медведя была выделена собственно УДХК. Название происходит от латинского «urso» (медведь) и связано с тем, что УДХК является основной желчной кислотой медвежьей желчи [32].
УДХК представляет собой гидрофильную желчную кислоту. Ее основные фармакологические эффекты при холелитиазе связаны со способностью снижать насыщение желчи холестерином за счет подавления его кишечной абсорбции и реабсорбции, угнетения синтеза в печени и уменьшения секреции в желчь. Кроме того, УДХК уменьшает всасывание гидрофобных эндогенных желчных кислот из тонкой кишки, растворяет их соли и оказывает желчегонное действие. Это обеспечивает защиту клеточных мембран от их токсического влияния и предотвращает холестаз [8, 33, 34].
Диапазон доз УДХК, имеющих доказанную эффективность при растворении холестериновых камней, находится в пределах 8–10 мг на 1 кг массы тела. При превышении максимальной дозы эффективность действия не увеличивается [32]. В клинических исследованиях была продемонстрирована возможность растворения холестериновых камней и уменьшения их на 1 мм в месяц в 30–60% случаев [35–37]. Полное растворение мелких камней (<5 мм) через 6 мес. отмечалось в 90% случаев [38]. В исследовании, где УДХК назначалась в дозе 600 мг/сут в течение месяца пациентам с холестериновыми камнями диаметром менее 15 мм, полное растворение было достигнуто в 43,2% случаев, частичное — в 16,2% [39]. В другом исследовании применение УДХК при билиарном сладже в течение 3–6 мес. предотвращало камнеобразование [37]. В многолетнем исследовании было продемонстрировано, что назначение УДХК способствует снижению частоты билиарной боли и холецистита независимо от растворения камней [40].
Урсодезоксихолевая кислота в комбинации с глицирризиновой кислотой
Несмотря на широкую доступность и хорошие результаты хирургического лечения ЖКБ, пероральный литолиз сохраняет свою целевую популяцию пациентов, что обусловливает актуальность оптимизации существующих терапевтических подходов. Современные представления об этиологии и патогенезе ЖКБ, а также коморбидной патологии свидетельствуют о необходимости комплексного подхода к медикаментозному растворению холестериновых камней. Лекарственная терапия должна иметь определенные свойства:
действовать на наиболее значимые с точки зрения развития и прогрессирования холелитиаза терапевтические мишени;
оказывать местное действие на желчеобразование и желчевыделение и системное — на метаболические процессы и развитие воспалительных реакций в организме;
быть тропной к тканям органов желчевыделения, печени, а возможно, и другим тканям.
В качестве наиболее актуальных точек приложения лекарственных препаратов для перорального литолиза в настоящее время рассматриваются:
ингибирование синтеза холестерина в печени;
угнетение всасывания холестерина в кишечнике;
воздействие на фарнезоидные Х-рецепторы;
подавление секреции холестерина с желчью;
модификация кишечной микробиоты;
нормализация моторики желчного пузыря;
подавление продукции медиаторов воспаления [4].
Поиск таких лекарственных препаратов может идти двумя путями: 1) разработка и синтез принципиально новых молекул, обладающих перечисленными фармакологическими эффектами; 2) создание новых комбинаций хорошо изученных действующих веществ с объединением и усилением необходимых свойств.
В качестве одного из возможных решений в области совершенствования перорального литолиза следует рассматривать фиксированную комбинацию УДХК и глицирризиновой кислоты (ГК).
ГК, или глицирризин, является сапонином корня солодки, который используется в медицине уже более 3000 лет. Более того, солодка включена в состав ряда препаратов традиционной китайской медицины, применяемых в терапии ЖКБ с целью купирования воспаления и восстановления функции печени [21, 41].
Химическое строение ГК было установлено в 1930-х гг. [42]. Она является амфифильной молекулой, гидрофильная часть которой представлена двумя остатками глюкуроновой кислоты, а гидрофобная — остатком глицирретовой кислоты [41].
В контексте применения при ЖКБ среди известных эффектов ГК наибольший интерес представляют противовоспалительный, гепатопротекторный, антифибротический и антиканцерогенный.
Противовоспалительное действие связано с ингибированием медиаторов воспаления — ИЛ-1β, ИЛ-6, ФНО-α, простагландина Е2, а также с антиоксидантным эффектом, выражающимся в ингибировании реактивных кислородных частиц. Гепатопротекторное действие реализуется через угнетение некроза и апоптоза клеток печени за счет подавления активности ФНО-α и каспазы-3 соответственно. Также ГК оказывает прямое воздействие на гепатоциты, предотвращая патологические изменения проницаемости клеточных мембран. Замедление прогрессирования фиброза печени при введении ГК объясняется подавлением продукции коллагена звездчатыми клетками, а также разрушением активированных клеток Ито через систему натуральных киллеров. Антиканцерогенный эффект связан с запуском механизмов апоптоза раковых клеток [41, 43, 44].
Иногда обсуждается вопрос о токсичности ГК со ссылками на единичные сообщения в источниках невысокого качества, без доказанной связи таких случаев с применением этого вещества. Убедительным опровержением и свидетельством того, что ГК не является токсичным веществом, может служить тот факт, что в исследовании с участием здоровых добровольцев пероральный прием ГК в дозе 2 мг/кг в сутки в течение 8 нед. не вызывал никаких токсических эффектов [45]. Косвенно это подтверждается и тем, что в США и Евросоюзе ГК в меньших, чем терапевтические, дозах разрешена для повседневного использования как пищевая добавка и в косметологии [46, 47].
Рациональность комбинации УДХК и ГК для перорального литолиза обусловлена возможностью суммирования их фармакологических эффектов. УДХК преимущественно оказывает воздействие на местный обмен холестерина и желчных кислот, а также улучшает функциональное состояние желчных путей. Тем самым она влияет непосредственно на процесс камнеобразования, угнетая его и способствуя растворению камня. Что касается ГК, то она формирует благоприятные условия для реализации литолитического действия УДХК и нейтрализует сопутствующие ЖКБ патологические процессы в печени и других органах. Так, местный противовоспалительный эффект служит дополнительным защитным фактором в отношении литогенеза и триггером для литолиза. Одновременное влияние на патологические процессы в печени предотвращает прогрессирование как заболеваний печени на фоне ЖКБ, так и ЖКБ на фоне болезни печени. Подавляя воспаление на системном уровне, ГК обладает потенциалом для снижения рисков, связанных с развитием коморбидной патологии. Схема комплексного механизма действия УДХК и ГК при холестериновых камнях представлена на рисунке 1.
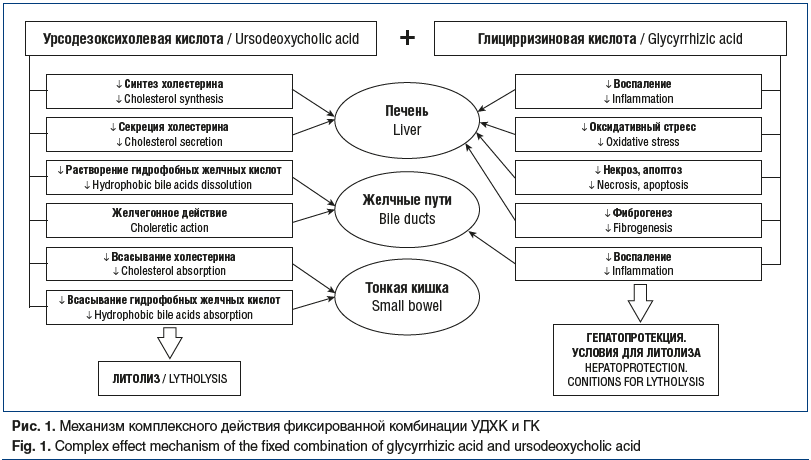
В 2019 г. впервые в России и в мире была зарегистрирована фиксированная комбинация ГК и УДХК в форме капсул, содержащих действующие вещества в количестве 35 мг и 250 мг соответственно [48]. На доклиническом этапе исследований на модели холестаза было установлено, что фиксированная комбинация в сравнении с монопрепаратом УДХК эффективнее влияет на динамику активности аланинаминотрасферазы, аспартатаминотрасферазы, γ-глутамилтранспептидазы, щелочной фосфатазы, уровня прямого и непрямого билирубина, а также на гистологическую картину печени. На основании этого был сделан вывод о синергическом действии ГК и УДХК в составе фиксированной комбинации. Лекарственный препарат прошел клинические исследования в объеме, регламентированном действующим законодательством в сфере обращения лекарственных средств, и в соответствии с правилами надлежащей клинической практики. Комбинация запатентована в качестве средства для лечения и профилактики острого и хронического гепатита и холестаза [49] и согласно официальной инструкции по медицинскому применению может назначаться при ЖКБ в целях перорального литолиза.
Заключение
ЖКБ является местным проявлением системных метаболических нарушений и воспаления в организме. В качестве коморбидной патологии оказывает влияние на развитие, прогрессирование и исходы сердечно-сосудистых, цереброваскулярных заболеваний, болезней печени и рака. Хирургическое лечение, несмотря на доступность и эффективность, не решает всех проблем. Пероральный литолиз сохраняет свою актуальность и нуждается в оптимизации, основным направлением которой является обеспечение комплексного воздействия. Одним из решений может быть недавно зарегистрированная в РФ фиксированная комбинация УДХК и ГК. Препарат может быть использован: у пациентов с билиарным сладжем; пациентов с холестериновыми камнями размером менее 20 мм и функционирующим желчным пузырем — бессимптомных и имеющих клинические симптомы, при невозможности хирургического лечения; в послеоперационном периоде после холецистэктомии для снижения риска камнеобразования в желчных протоках; у пациентов с повышенным риском камнеобразования для первичной профилактики. В настоящее время в условиях реальной клинической практики продолжается изучение долгосрочной эффективности и безопасности препарата, в т. ч. у различных групп пациентов, а также при коморбидных заболеваниях.
Сведения об авторах:
Никитин Игорь Геннадьевич — д.м.н., профессор, заведующий кафедрой госпитальной терапии № 2, ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 117997, Россия, г. Москва, ул. Островитянова, д. 1; директор, ФГАОУ «НМИЦ «ЛРЦ» Минздрава России, 125367, Россия, г. Москва, Иваньковское ш., д. 3, ORCID iD 0000-0003-1699-0881.
Волнухин Артем Витальевич — д.м.н., профессор кафедры общей врачебной практики Института профессионального образования, ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; руководитель группы медицинской аналитики, АО «Фармстандарт», 123112, Россия, г. Москва, ул. Тестовская, д. 10, ORCID iD 0000-0001-5113-2108.
Контактная информация: Волнухин Артем Витальевич, e-mail: volnuhin81@gmail.com. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов: Волнухин А.В. является сотрудником компании АО «Фармстандарт». Статья поступила 27.08.2020, поступила после рецензирования 10.09.2020, принята в печать 24.09.2020.
About the authors:
Igor G. Nikitin — Dr. of Sci. (Med), Professor, Head of the Department of Hospital Therapy No. 2, Pirogov Russian National Research Medical University, 1, Ostrovityanova str., Moscow, 117997, Russian Federation; Director, National Medical Research Center «Treatment and Rehabilitation Center»: 3, Ivankovskoye road, Moscow, 125367, Russian Federation, ORCID iD 0000-0003-1699-0881.
Artem V. Volnukhin — Dr. of Sci. (Med), Professor of the Department of General Practice at the Institute of Professional Education, I.M. Sechenov First Moscow State Medical University (Sechenov University): 8, bld. 2, Trubetskaya str., Moscow, 119991, Russian Federation; Head of the Medical Analytics, Pharmstandard JSC: 10, Testovskaya str., Moscow, 123112, Russian Federation, ORCID iD 0000-0001-5113-2108.
Contact information: Artem V. Volnukhin, e-mail: volnuhin81@gmail.com. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. Conflict of interests: A.V. Volnukhin is an employee of JSC Pharmstandard. Received 27.08.2020, revised 10.09.2020, accepted 24.09.2020.
2. Ивашкин В.Т., Маев И.В., Баранская Е.К. и др. Рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению желчнокаменной болезни. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2016;26(3):64–80.[Ivashkin V.T., Mayev I.V., Baranskaya E.K. et al. Gallstone disease diagnosis and treatment: guidelines of the Russian gastroenterological association. Russian Journal of Gastroenterology, Hepatology, Coloproctology. 2016;26(3):64–80 (in Russ.)]. DOI: 10.22416/1382-4376-2016-26-3-64-80.
3. European Association for the Study of the Liver (EASL). EASL Clinical Practice Guidelines on the prevention, diagnosis and treatment of gallstones. J Hepatol. 2016;65(1):146–181. DOI: 10.1016/j.jhep.2016.03.005.
4. Di Ciaula A., Portincasa P. Recent advances in understanding and managing cholesterol gallstones. F1000Res. 2018;7: F1000 Faculty Rev-1529. DOI: 10.12688/f1000research.15505.1.
5. Tiderington E., Lee S.P., Ko C.W. Gallstones: new insights into an old story. F1000Res. 2016;5: F1000 Faculty Rev-1817. DOI: 10.12688/f1000research.8874.1.
6. Li X., Guo X., Ji H. et al. Gallstones in patients with chronic liver diseases. Bio Med Res Int. 2017;2017:9749802. DOI: 10.1155/2017/9749802.
7. Gutt C., Schläfer S., Lammert F. The treatment of gallstone disease. Dtsch Arztebl Int. 2020;117(9):148–158. DOI: 10.3238/arztebl.2020.0148.
8. Guarino M.P.L., Cocca S., Altomare A. et al. Ursodeoxycholic acid therapy in gallbladder disease, a story not yet completed. World J Gastroenterol. 2013;19(31):5029–5034. DOI: 10.3748/wjg.v19.i31.5029.
9. Gibney E.J. Asymptomatic gallstones. Br J Surg. 1990;77(4):368–372.
10. Lv J., Qi L., Yu C. et al. Gallstone Disease and the Risk of Ischemic Heart Disease. Arterioscler Thromb Vasc Biol. 2015;35(10):2232–2237. DOI: 10.1161/ATVBAHA.115.306043.
11. Shou-Feng Zhao, Ai-Min Wang, Xin-Juan Yul et al. Association between gallstone and cardio-cerebrovascular disease: Systematic review and meta-analysis. Exp Ther Med. 2019;17(4):3092–3100. DOI: 10.3892/etm.2019.7291.
12. Nogueira L., Freedman N.D., Engels E.A. et al. Gallstones, cholecystectomy, and risk of digestive system cancers. Am J Epidemiol. 2014;179(6):731–739. DOI: 10.1093/aje/kwt322.
13. Ruhl C.E., Everhart J.E. Gallstone disease is associated with increased mortality in the United States. Gastroenterology. 2011;140(2):508–516. DOI: 10.1053/j.gastro.2010.10.060.
14. Froutan Y., Alizadeh A., Mansour-Ghanaei F. et al. Gallstone disease founded by ultrasonography in functional dyspepsia: prevalence and associated factors. Int J Clin Exp Med. 2015;8(7):11283–11288. PMID: 26379936
15. Friedman G.D., Kannel W.B., Dawber T.R. The epidemiology of gallbladder disease: observations in the Framingham study. J Chronic Diseases. 1966;19(3):273–292.
16. Scragg R.K., McMichael A.J., Baghurst P.A. Diet, alcohol, and relative weight in gall stone disease: a case-control study. BMJ. 1984;288(6424):1113–1119.
17. Grodstein F., Colditz G.A., Hunter D.J. et al. A prospective study of symptomatic gallstones in women: relation with oral contraceptives and other risk factors. Obstetrics and Gynecology. 1994;84(2):207–214.
18. Ruhl C.E., Everhart J.E. Relationship of non-alcoholic fatty liver disease with cholecystectomy in the US population. Am J Gastroenterol. 2013;108(6):952–958. DOI: 10.1038/ajg.2013.70.
19. Fracanzani A.L., Valenti L., Russello M. et al. Gallstone disease is associated with more severe liver damage in patients with non-alcoholic fatty liver disease. PLoS ONE. 2012;7(7): e41183. DOI: 10.1371/journal.pone.0041183.
20. Koller T., Kollerova J., Hlavaty T. et al. Cholelithiasis and markers of nonalcoholic fatty liver disease in patients with metabolic risk factors. Scand J Gastroenterol. 2012;47(2):197–203. DOI: 10.3109/00365521.2011.643481.
21. Sha-sha Shen, Jiao-jiao Gong, Xi-wei Wang et al. Promotional effect of nonalcoholic fatty liver disease on Gallstone disease: A systematic review and meta-analysis. Turk J Gastroenterol. 2017;28(1):31–39. DOI: 10.5152/tjg.2016.0357.
22. Young-Kyu Kim, Oh-Sung Kwon, Kyu Hee Her. The grade of nonalcoholic fatty liver disease is an independent risk factor for gallstone disease. An observational Study. Medicine (Baltimore). 2019;98(27): e16018. DOI: 10.1097/MD.0000000000016018.
23. Wang D.Q.H., Neuschwander-Tetri B.A., Portincasa P. The Biliary System. 2 ed. Morgan and Claypool Life Sciences; 2017.
24. Liu Z., Kemp T.J., Gao Y.T. et al. Association of circulating inflammation proteins and gallstone disease. J Gastroenterol Hepatol. 2018;33(11):1920–1924. DOI: 10.1111/jgh.14265.
25. Qiliang Chen, Yuanyuan Zhang, Shunan Li et al. Mechanisms underlying the prevention and treatment of cholelithiasis using traditional chinese medicine. Evid Based Complement Alternat Med. 2019;2019:2536452. DOI: 10.1155/2019/2536452.
26. Musso G., Gambino R., Cassader M. Recent insights into hepatic lipid metabolism in non-alcoholic fatty liver disease (NAFLD). Prog Lipid Res. 2009;48(1):1–26. DOI: 10.1016/j.plipres.2008.08.001.
27. Yoosoo Chang, Yoo-Hun Noh, Byung-Seong Suh et al. Bidirectional association between nonalcoholic fatty liver disease and gallstone disease: a cohort study. J Clin Med. 2018;7(11):458. DOI: 10.3390/jcm7110458.
28. Zweers S.J., Booij K.A., Komuta M. et al. The human gallbladder secretes fibroblast growth factor 19 into bile: Towards defining the role of fibroblast growth factor 19 in the enterobiliary tract. Hepatology. 2012;55(2):575–583. DOI: 10.1002/hep.24702.
29. Barrera F., Azocar L., Molina H. et al. Effect of cholecystectomy on bile acid synthesis and circulating levels of fibroblast growth factor 19. Ann Hepatol. 2015;14(5):710–721. PMID: 26256900.
30. Miller K., Hell E., Lang B. et al. Gallstone formation prophylaxis after gastric restrictive procedures for weight loss: a randomized double-blind placebo-controlled trial. Ann Surg. 2003;238(5):697–702. DOI: 10.1097/01.sla.0000094305.77843.cf.
31. Danzinger R.G., Hofmann A.F., Schoenfield L.J., Thistle J.L. Dissolution of cholesterol gallstones by chenodeoxycholic acid. N Engl J Med. 1972;286(1):1–8. DOI: 10.1056/NEJM197201062860101.
32. Makino I., Tanaka H. From a choleretic to an immunomodulator: historical review of ursodeoxycholic acid as a medicament. J Gastroenterol Hepatol. 1998;13(6):659–664. DOI: 10.1111/j.1440-1746.1998.tb00707.x.
33. Di Ciaula A., Wang D.Q., Wang H.H. et al. Targets for current pharmacologic therapy in cholesterol gallstone disease. Gastroenterol Clin North Am. 2010;39(2):245–264, viii-ix. DOI: 10.1016/j.gtc.2010.02.005.
34. Xun Chen, Xiao-Ru Yan, Li-Ping Zhang. Ursodeoxycholic acid after common bile duct stones removal for prevention of recurrence: A systematic review and meta-analysis of randomized controlled trials Medicine (Baltimore). 2018;97(45): e13086. DOI: 10.1097/MD.0000000000013086.
35. Tint G.S., Salen G., Colalillo A. et al. Ursodeoxycholic acid: a safe and effective agent for dissolving cholesterol gallstones. Ann Intern Med. 1982;97(3):351–356. DOI: 10.7326/0003-4819-97-3-351.
36. Lazaridis K.N., Gores G.J., Lindor K.D. Ursodeoxycholic acid ‘mechanisms of action and clinical use in hepatobiliary disorders’. J Hepatol. 2001;35(1):134–146. DOI: 10.1016/s0168-8278 (01) 00092-7.
37. Villanova N., Bazzoli F., Taroni F. et al. Gallstone recurrence after successful oral bile acid treatment. A 12-year follow-up study and evaluation of long-term postdissolution treatment. Gastroenterology. 1989;97(3):726–731. DOI: 10.1016/0016-5085 (89) 90644-6.
38. Portincasa P., Ciaula A.D., Bonfrate L. et al. Therapy of gallstone disease: What it was, what it is, what it will be. World J Gastrointest Pharmacol Ther. 2012;3(2):7–20. DOI: 10.4292/wjgpt.v3.i2.7.
39. Jae Min Lee, Jong Jin Hyun, In Young Choi et al. Comparison on Response and Dissolution Rates Between Ursodeoxycholic Acid Alone or in Combination With Chenodeoxycholic Acid for Gallstone Dissolution According to Stone Density on CT Scan. Medicine (Baltimore). 2015;94(50): e2037. DOI: 10.1097/MD.0000000000002037.
40. Tomida S., Abei M., Yamaguchi T. et al. Long-term ursodeoxycholic acid therapy is associated with reduced risk of biliary pain and acute cholecystitis in patients with gallbladder stones: a cohort analysis. Hepatology. 1999;30(1):6–13. DOI: 10.1002/hep.510300108.
41. Selyutina O.Yu., Polyakov N.E. Glycyrrhizic acid as a multifunctional drug carrier — From physicochemical properties to biomedical applications: A modern insight on the ancient drug. Int J Pharmaceutics. 2019;559:271–279. DOI: 10.1016/j.ijpharm.2019.01.047.
42. Ипатова О.М. Фосфоглив: механизм действия и применение в клинике. М.: Изд-во ГУ НИИ биомедицинской химии РАМН; 2005. [Ipatova O.M. Phosphogliv: mechanism of action and clinical use. Moscow: Ed. GU Research Institute of Biomedical Chemistry, Russian Academy of Medical Sciences; 2005 (in Russ.)].
43. Moro T., Shimoyama Y., Kushida M. et al. Glycyrrhizin and its metabolite inhibit Smad3-mediated type I collagen gene transcription and suppress experimental murine liver fibrosis. Life Sci. 2008;83(15–16):531–539. DOI: 10.1016/j.lfs.2008.07.023.
44. Gao H.-X., Shao S.-H., Wang G.-Q. Research progress of Radix Glycyrrhizae. J Jinggangshan Med Coll. 2004;5(11):8–11.
45. Final report on the safety assessment of Glycyrrhetinic Acid, Potassium Glycyrrhetinate, Disodium Succinoyl Glycyrrhetinate, Glyceryl Glycyrrhetinate, Glycyrrhetinyl Stearate, Stearyl Glycyrrhetinate, Glycyrrhizic Acid, Ammonium Glycyrrhizate, Dipotassium Glycyrrhizate, Disodium Glycyrrhizate, Trisodium Glycyrrhizate, Methyl Glycyrrhizate, and Potassium Glycyrrhizinate. Int J Toxicol. 2007;26(Suppl 2):79–112. DOI: 10.1080/10915810701351228.
46. Omar H.R., Komarova I., El-Ghonemi M. et al. Licorice abuse: time to send a warning message. Ther Adv. Endocrinol. Metab. 2012;3(4):125–138. DOI: 10.1177/2042018812454322.
47. European Food Safety Authority (EFSA). Scientific Opinion on the safety and efficacy of glycyrrhizic acid ammoniated (chemical group 30, miscellaneous substances) when used as a flavouring for all animal species. EFSA J. 2015;13(1):3971. DOI: 10.2903/j.efsa.2015.3971.
48. Регистрационное удостоверение № ЛП-005964 от 03.12.2019 (Электронный ресурс). URL: http://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=1cfd2196-a745–4974–9782–46a5a1368c1fandt= (дата обращения: 20.08.2020). [Registration certificate No ЛП-005964 dated 03.12.2019 (Electronic resource). URL: http://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=1cfd2196-a745–4974–9782–46a5a1368c1fandt= (access date: 08.20.2020) (in Russ.)].
49. Евразийский патент 032457. Композиция для лечения и/или профилактики острого и хронического гепатита и холестаза: заявитель и патентообладатель ЗАО «АФОФАРМ. № 2015000100 (RU); заявл. 30.10.15; опубл. 31.05.19. Бюл. № 5. [Composition for the treatment and / or prevention of acute and chronic hepatitis and cholestasis: Eurasian Pat. 032457: applicant and patentee CJSC AFOFARM. No. 2015000100 (RU); declared 10/30/15; publ. 05/31/19, Bul. No. 5 (in Russ.)].

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.