Эффективность комбинированной терапии больных эрозивной гастроэзофагеальной рефлюксной болезнью
DOI: 10.32364/2587-6821-2021-5-6-366-372
Цель исследования: оценить эффективность и безопасность комбинированной терапии ингибитором протонной помпы (ИПП) и эзофагопротектором для купирования симптомов рефлюкс-эзофагита, повышения качества жизни больных и достижения более быстрой и полной ремиссии заболевания.
Материал и методы: в рандомизированное исследование вошло 60 пациентов, из них 33 мужчины (средний возраст 40,96±13,44 года) и 27 женщин (средний возраст 48,29±12,69 года) с длительностью гастроэзофагеальной рефлюксной болезни (ГЭРБ) 21,85±15,48 мес. и стадией рефлюкс-эзофагита С/D. В зависимости от вида лечения пациенты были разделены на 2 группы по 30 человек. Пациенты основной группы получали комплексную терапию: ИПП пантопразол 40 мг 1 р/сут и эзофагопротектор на основе гиалуроновой кислоты, хондроитина сульфата и полоксамера 407. В группе сравнения назначали только пантопразол в той же дозировке. Продолжительность курса лечения в обеих группах составила 4 нед. До и после лечения оценивали наличие и выраженность жалоб по шкале Лайкерта, качество жизни по опроснику SF-36 и данные эндоскопического исследования.
Результаты исследования: после окончания курса терапии установлено статистически значимое снижение выраженности изжоги, регургитации, боли за грудиной, отрыжки воздухом, одинофагии и дисфагии как в основной группе (во всех случаях p<0,05, критерий Вилкоксона), так и в группе сравнения (во всех случаях p<0,05, критерий Вилкоксона). Применение комбинированной терапии позволило добиться более существенного улучшения качества жизни пациентов по всем показателям в сравнении с монотерапией ИПП. Кроме того, у 3 (10%) пациентов основной группы была достигнута эндоскопическая ремиссия, тогда как в группе сравнения таких пациентов не было. Применение эзофагопротектора в дополнение к ИПП позволило достигать первичной и вторичных конечных точек существенно чаще, чем при использовании монотерапии.
Заключение: полученные данные свидетельствуют о высокой эффективности и безопасности терапии ИПП в комбинации с эзофагопротектором для купирования симптомов заболевания и повышения качества жизни больных, более быстрой и полной ремиссии рефлюкс-эзофагита путем дополнительного восстановления резистентности слизистой оболочки пищевода. Эзофагопротектор как компонент комплексной терапии совместно с ИПП позволяет достичь клинической и эндоскопической ремиссии заболевания у пациентов с эрозивным эзофагитом в более сжатые сроки.
Ключевые слова: гастроэзофагеальная рефлюксная болезнь, резистентность слизистой оболочки пищевода, эзофагопротекция, ингибитор протонной помпы, качество жизни.
Для цитирования: Матошина И.В., Ливзан М.А., Федорин М.М., Лаптева И.В. Эффективность комбинированной терапии больных эрозивной гастроэзофагеальной рефлюксной болезнью. РМЖ. Медицинское обозрение. 2021;5(6):366-372. DOI: 10.32364/2587-6821-2021-5-6-366-372.
I.V. Matoshina1, M.A. Livzan1, M.M. Fedorin1, I.V. Lapteva2
1Omsk State Medical University, Omsk, Russian Federation
2City Hospital No. 3, Omsk, Russian Federation
Aim: to evaluate the efficacy and safety of combined therapy with a proton pump inhibitor (PPI) and an esophagoprotector to relieve the symptoms of reflux esophagitis, improve the life quality of patients and achieve faster and complete disease remission.
Patients and Methods: a randomized study included 60 patients, including 33 men (mean age 40.96±13.44 years) and 27 women (mean age 48.29±12.69 years) with a duration of gastroesophageal reflux disease (GERD) of 21.85±15.48 months and C/D stage of reflux esophagitis. Depending on the prescribed treatment, the patients were divided into 2 groups of 30 subjects. Patients of the main group received complex therapy: PPI pantoprazole 40 mg once per day and esophagoprotector based on hyaluronic acid, chondroitin sulfate and poloxamer 407. In the comparison group, only pantoprazole was prescribed at the same dosage. The duration of the treatment course in both groups was 4 weeks. Before and after treatment, the pr esence and severity of complaints were assessed on the Likert scale, life quality according to the SF-36 questionnaire and endoscopic examination data.
Results: after the end of the therapy course, a statistically significant decrease in the severity of epigastric burning, regurgitation, substernal pain, gaseous eructation, odynophagia and dysphagia was found both in the main group (in all cases p<0.05, Wilcoxon Matched Pairs Test) and the comparison group (in all cases p<0,05, Wilcoxon Matched Pairs Test). The use of combination therapy made it possible to achieve a more significant improvement in the life quality of patients in all indicators versus PPI monotherapy. In addition, 3 (10%) patients of the main group achieved endoscopic remission, while there were no such patients in the comparison group. The use of esophagoprotector in addition to PPI made it possible to reach the primary and secondary endpoints significantly more commonly versus during monotherapy.
Conclusion: the obtained data indicate the high efficiency and safety of PPI therapy in combination with esophagoprotector for relieving the disease symptoms and improving the life quality of patients, faster and complete remission of reflux esophagitis by additional restoration of the esophageal mucosa resistance. Esophagoprotector as a component of complex therapy together with PPI allows achieving clinical and endoscopic disease remission in patients with erosive esophagitis in shorter terms.
Keywords: gastroesophageal reflux disease, esophageal mucosa resistance, esophagoprotection, proton pump inhibitor, quality of life.
For citation: Matoshina I.V., Livzan M.A., Fedorin M.M., Lapteva I.V. Efficacy of combined therapy in patients with erosive gastroesophageal reflux disease. Russian Medical Inquiry. 2021;5(6):366–372 (in Russ.). DOI: 10.32364/2587-6821-2021-5-6-366-372.
Введение
В настоящее время гастроэзофагеальная рефлюксная болезнь (ГЭРБ) определяется как хроническое рецидивирующее заболевание, которое обусловлено нарушением моторно-эвакуаторной функции органов гастроэзофагеальной зоны и характеризуется регулярно повторяющимся забросом в пищевод желудочного содержимого, что приводит к появлению клинических симптомов, ухудшающих качество жизни, и повреждению слизистой оболочки дистального отдела пищевода с развитием в неороговевающем многослойном плоском эпителии дистрофических изменений, катарального или эрозивно-язвенного эзофагита (рефлюкс-эзофагита), а в ряде случаев — цилиндроклеточной метаплазии [1]. ГЭРБ является кислотозависимым заболеванием, которое возникает и прогрессирует при первичном нарушении моторной функции верхних отделов пищеварительного тракта. Основополагающими компонентами в патогенезе ГЭРБ признана частота возникновения, а также продолжительность рефлюкса содержимого желудка, в результате чего рефлюктат, включающий в себя соляную кислоту, пепсин, а в случае сопутствующего дуоденогастрального рефлюкса также желчные кислоты и лизолецитин, забрасывается в вышележащие отделы пищеварительного тракта и оказывает негативное действие на слизистую оболочку пищевода с повреждением межклеточных контактов, воспалительным ответом и нарушением процессов клеточного обновления [2–4]. Следовательно, формирование и тяжесть заболевания будут определяться длительностью и выраженностью моторных нарушений зоны пищеводно-желудочного перехода, агрессивностью рефлюктата и устойчивостью (резистентностью) слизистой оболочки пищевода к его содержимому [2–5].
В соответствии с международными согласительными документами и клиническими рекомендациями, утвержденными Минздравом России, в качестве целей терапии пациентов с ГЭРБ рассматриваются не только купирование симптомов и эпителизация эрозивных дефектов слизистой оболочки пищевода, но и повышение качества жизни больных и профилактика осложнений, в том числе пищевода Барретта и аденокарциномы [1, 6, 7].
Сегодня препаратами первой линии в терапии ГЭРБ являются ингибиторы протонной помпы (ИПП), существенно снижающие агрессивность и объем желудочного содержимого [8, 9]. Препараты данной группы блокируют Н+/К+-АТФазу, участвующую в заключительном этапе секреции желудочной кислоты париетальными клетками, что повышает внутрижелудочный уровень pH за счет снижения секреции соляной кислоты, однако прямо не влияет на частоту спонтанных релаксаций нижнего пищеводного сфинктера [10]. Таким образом, прием ИПП не позволяет компенсировать основную причину рефлюкса — моторные нарушения пищеводно-желудочного перехода, которые являются важнейшим патофизиологическим механизмом ГЭРБ [1, 11, 12]. С другой стороны, соляная кислота сама по себе обладает не самым высоким повреждающим потенциалом. Установлено, что наиболее выраженное повреждающее действие на эпителий оказывает желудочный сок с неконъюгированными желчными кислотами прирН 1–3, в связи с этим присутствие в рефлюктате желчи значимо повышает риск развития пищевода Барретта, дисплазии и неоплазии эпителия пищевода [2, 3]. Экспериментальные модели демонстрируют, что именно синергизм соляной кислоты, пепсина и желчных кислот обладает наибольшим повреждающим потенциалом относительно слизистой оболочки пищевода [13]. В реальной клинической практике, по данным многочисленных систематических обзоров и метаанализов, эффективность монотерапии ИПП не превышает 80%, и для достижения всех целей терапии определенной группе пациентов с ГЭРБ требуется комбинация ИПП с препаратами, обеспечивающими нормализацию моторики и восстановление резистентности слизистой оболочки пищевода [6, 14–16].
К принципиально новому классу препаратов, доступному клиницистам в лечении рефлюкс-эзофагита, относится эзофагопротектор (Альфазокс), состоящий из смеси (в соотношении 1:2,5) низкомолекулярной (80–100 кДа) гиалуроновой кислоты и низкомолекулярного (10–20 кДа) хондроитина сульфата, которые растворены в биоадгезивном носителе (полоксамер 407) и вместе образуют макромолекулярный комплекс, способствующий восстановлению слизистой оболочки пищевода и выступающий в роли механического барьера, равномерно обволакивая стенку пищевода и препятствуя контакту с повреждающими молекулами рефлюктата [11, 17, 18]. Выделение среди когорты лиц, страдающих ГЭРБ, пациентов с низким потенциалом резистентности слизистой оболочки пищевода, комплексная оценка эффективности и безопасности комбинированной терапии ИПП и эзофагопротектором с частотой достижения клинической, эндоскопической и гистологической ремиссии рефлюкс-эзофагита крайне актуальны для повышения эффективности курации больных.
Цель исследования: оценить эффективность и безопасность комбинированной терапии ИПП и эзофагопротектором для купирования симптомов рефлюкс-эзофагита, повышения качества жизни больных и достижения более быстрой и полной ремиссии заболевания.
Материал и методы
Протокол исследования одобрен локальным этическим комитетом ФГБОУ ВО ОмГМУ Минздрава России. В соответствии с критериями включения была сформирована когорта лиц, страдающих эрозивным рефлюкс-эзофагитом стадии С/D по Лос-Анджелесской классификации [19].
Критерии включения в исследование:
возраст от 18 до 75 лет;
диагноз «эрозивный рефлюкс-эзофагит стадии С или D» в соответствии с Лос-Анджелесской классификацией (по результатам эндоскопического исследования, сделанного на визите скрининга либо не позднее чем за 14 дней до визита включения в исследование);
наличие хотя бы одного из представленных симптомов ГЭРБ (рефлюкс-эзофагита) (изжога, регургитация, загрудинная боль, отрыжка) в течение не менее 3 мес. и возникающего не менее 3 раз в неделю за прошедший месяц до начала скринингового визита;
при наличии внепищеводных проявлений ГЭРБ исключены другие причины, которые могут быть связаны с коморбидной патологией;
подписанное информированное согласие на участие в исследовании.
Критерии невключения в исследование:
пищевод Барретта;
язва желудка или двенадцатиперстной кишки;
оперативные вмешательства на желудке или объемные операции на желудочно-кишечном тракте в анамнезе;
реакции гиперчувствительности или непереносимости гиалуроновой кислоты, или хондроитина сульфата, или полоксамера 407 в анамнезе;
наличие противопоказаний к эндоскопическому исследованию;
беременность, период грудного вскармливания или неиспользование методов контрацепции у женщин фертильного возраста;
прием лекарственных препаратов группы альгинатов или H2-гистаминоблокаторов в течение предыдущих
10 дней до визита включения или прием антацидов в течение предыдущих 3 дней до визита включения;
прием цитостатиков, глюкокортикостероидов или
нестероидных противовоспалительных препаратов (НПВП);
рефрактерность к терапии препаратами группы ИПП в анамнезе.
По результатам скрининга и оценки соответствия критериям включения 64 пациентов из выборки было исключено 4 пациента (пищевод Барретта, COVID-19). Таким образом, исследовательскую когорту составили 60 пациентов (средний возраст 43,23±13,06 года) с длительностью течения ГЭРБ 21,85±15,48 мес., из них 33 мужчины (средний возраст 40,96±13,44 года) и 27 женщин (средний возраст 48,29±12,69 года). Длительность заболевания составила 21,16±13,56 мес. и 21,94±15,26 мес. у мужчин и женщин соответственно. При эндоскопическом исследовании рефлюкс-эзофагит стадии С установлен у 43 пациентов, стадии D — у 17 пациентов.
Для оценки эффективности и безопасности комбинированной терапии ИПП и эзофагопротектором участники исследования были рандомизированы методом конвертов на две группы по 30 человек. Основную группу (средний возраст 43,66±10,24 года, длительность заболевания 21,80±17,46 мес.) составили 22 пациента с эрозивным рефлюкс-эзофагитом стадии С и 8 пациентов — стадии D. Группа сравнения (средний возраст 42,98±14,66 года, длительность заболевания 21,80±17,18 мес.) включала 21 пациента с рефлюкс-эзофагитом стадии С и 9 пациентов — стадии D.
Пациенты основной группы в дополнение к ИПП (пантопразол в таблетках 40 мг 1 р/сут) получали эзофагопротектор Альфазокс (гиалуроновая кислота с хондроитина сульфатом и полоксамером 407, ООО «Альфасигма Рус») по схеме: 10 мл 4 р/сут — 3 раза через час после еды и 1 раз перед сном в течение 4 нед. В группе сравнения пациенты получали стандартную терапию пантопразолом в таблетках 40 мг 1 р/сут в течение 4 нед.
В качестве первичных контрольных точек установлены доли (%) пациентов в группах сравнения, у которых отмечалось заживление эрозий после 4 нед. лечения по результатам эндоскопического исследования.
Вторичными конечными точками исследования были:
доли (%) пациентов в каждой группе, у которых отмечалось улучшение эндоскопической картины по результатам лечения как минимум на 1 уровень по Лос-Анджелесской классификации;
средняя разность частоты выявления и оценки (в баллах) тяжести симптомов ГЭРБ по опроснику Лайкерта до и после лечения в группах исследования.
После проведения опроса и физикального обследования пациентам было предложено оценить частоту и тяжесть каждого из симптомов ГЭРБ (изжога, боль за грудиной, рефлюкс, отрыжка воздухом, дисфагия, одинофагия) по опроснику Лайкерта с оценкой интенсивности симптомов от 1 балла до 5: 1 — симптом отсутствует; 2 — симптом можно не замечать, если не думать об этом; 3 — симптом не удается не замечать, но он не нарушает дневную активность и сон; 4 — симптом нарушает сон; 5 — симптом временно делает невозможной дневную активность и сон, выраженно их нарушает.
Пациентам также было предложено заполнить неспецифический опросник качества жизни SF-36. Опросник состоит из 36 вопросов, сгруппированных в 8 шкал: физическое функционирование, ролевая деятельность, телесная боль, общее здоровье, жизнеспособность, социальное функционирование, эмоциональное состояние и психическое здоровье. Показатели каждой шкалы составлены таким образом, что чем выше значение показателя (от 0 до 100), тем выше оценка по избранной шкале.
В течение 4 нед. назначенного лечения состояние участников исследования отслеживалось на предмет развития нежелательных побочных эффектов.
Статистический анализ выполнен в программном пакете Statistica 8 от Statsoft для Windows 10. Уровнем значимости установлена вероятность α менее 0,05. Для определения вида распределения применялись критерии Колмогорова — Смирнова, W-тест Шапиро — Уилка. Поскольку распределение в выборках не удовлетворяло требованиям параметрического анализа, для статистической обработки данных использовали непараметрические методы (критерий χ2 Пирсона, U-тест Манна — Уитни для независимых выборок и критерий Вилкоксона (Wilcoxon Matched Pairs Test) для зависимых выборок). Средние выборочные значения количественных признаков представлены как среднее выборочное (М) и стандартное отклонение (SE) в виде M±SE.
Результаты исследования
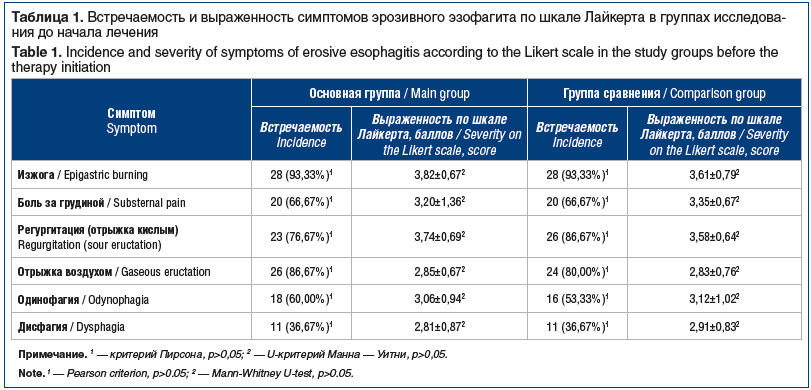
На момент включения в исследование была установлена выраженность симптомов эрозивного эзофагита по шкале Лайкерта. У 56 (93,33%) пациентов отмечена изжога выраженностью 3,71±1,73 балла, в том числе у 12 (20%) больных изжога наблюдалась и в ночные часы. Боль за грудиной выраженностью 3,28±0,82 балла установлена в 40 (66,67%) наблюдениях. Регургитация (отрыжка кислым) выраженностью 3,65±0,66 балла беспокоила 49 (81,67%) пациентов. На отрыжку воздухом пожаловались 50 (83,33%) больных, выраженность симптома составила 2,84±0,71 балла. Жалобы на одинофагию выраженностью 3,09±0,97 балла предъявляли лишь 34 (56,67%) пациента. Дисфагия выраженностью 2,86±0,83 балла беспокоила 22 (36,67%) человек.
Статистически значимых различий в выраженности и встречаемости симптомов, характерных для ГЭРБ, при оценке по шкале Лайкерта в обеих группах до начала лечения не выявлено (табл. 1).
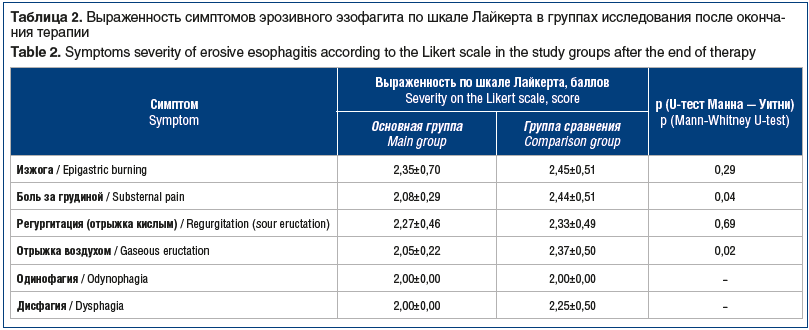
После окончания курса терапии в обеих группах установлено статистически значимое снижение выраженности всех изученных симптомов как в основной группе (во всех случаях p<0,05, критерий Вилкоксона), так и в группе сравнения (во всех случаях p<0,05, критерий Вилкоксона). При этом выраженность боли за грудиной и отрыжки воздухом в основной группе была статистически значимо ниже, чем в группе сравнения. Выраженность изжоги и регургитации также была несколько ниже в основной группе, чем в группе, принимавшей только ИПП, однако различия не достигали уровня статистической значимости. В связи с малым количеством пациентов, имевших симптомы дисфагии (2 участника в основной группе и 4 участника в группе сравнения) и одинофагии (4 участника в основной группе и 10 участников в группе сравнения) после окончания курса лечения, статистическая оценка различий не проводилась (табл. 2).
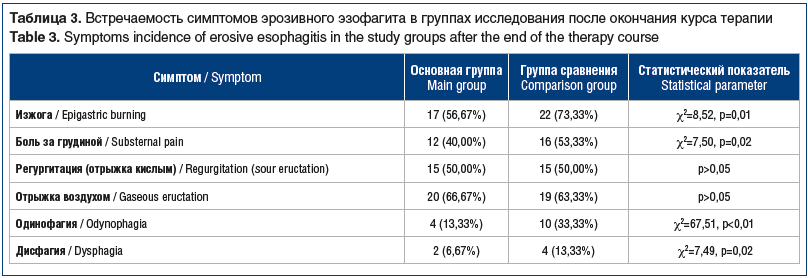
Встречаемость изжоги, боли за грудиной, одинофагии и дисфагии была статистически значимо ниже в группе, принимавшей ИПП и эзофагопротектор, чем в группе сравнения. По встречаемости регургитации и отрыжки воздухом группы существенно не различались (табл. 3).
В основной группе по окончании 4-недельного курса лечения выявлен статистически значимый рост показателей качества жизни по всем шкалам опросника SF-36 (во всех случаях p<0,05, критерий Вилкоксона), за исключением показателя по шкале «Общее состояние здоровья», динамика которого оказалась статистически незначимой (p=0,12, критерий Вилкоксона; табл. 4).
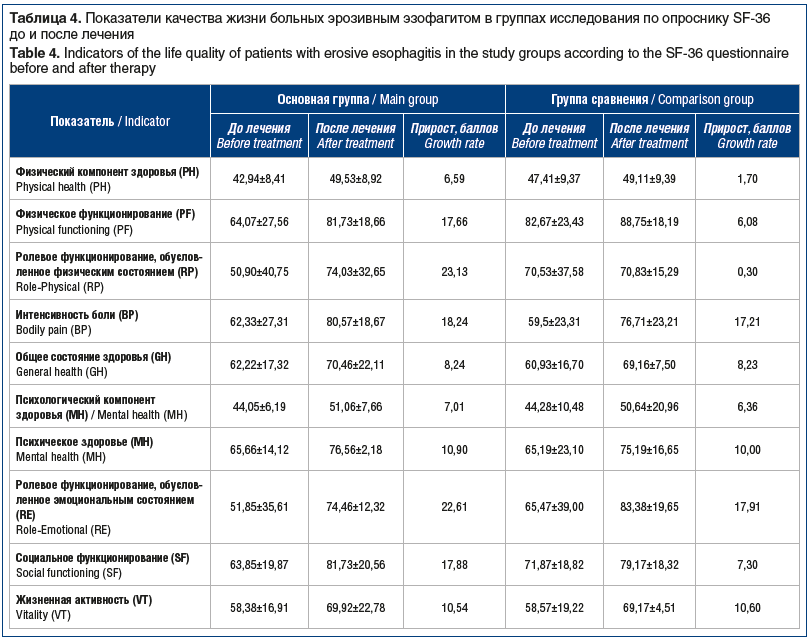
В группе сравнения через 4 нед. после начала терапии ИПП при оценке по опроснику SF-36 выявлено существенное улучшение показателей по шкалам «Интенсивность боли» (p=0,02, критерий Вилкоксона) и «Психологический компонент здоровья» (p=0,02, критерий Вилкоксона). По остальным шкалам значимого улучшения не установлено (p>0,05; см. табл. 4).
При сравнении выраженности повышения качества жизни по опроснику SF-36 выявлена тенденция к более высокому росту показателей в основной группе, чем в группе сравнения, по всем шкалам (см. табл. 4).
По данным эндоскопического исследования было установлено, что через 4 нед. у больных основной группы отмечалась более выраженная редукция макроскопических изменений, оцениваемых эндоскопистом с применением метода «ослепления» (врач-эндоскопист не был информирован о схеме терапии пациентов). Так, в основной группе у 3 (10%) пациентов была достигнута эндоскопическая ремиссия, у 27 (90%) — констатировали уменьшение стадии рефлюкс-эзофагита до стадии А/В, тогда как в группе сравнения случаев эндоскопической ремиссии не зафиксировано, а уменьшение стадии рефлюкс-эзофагита описано лишь у 24 (80%). Таким образом, существенное улучшение эндоскопической картины значимо чаще выявлялось в основной группе, чем в группе сравнения (100% против 80%, p=0,01, критерий Пирсона).
В течение 4 нед. применения назначенной терапии серьезных нежелательных побочных эффектов у участников исследования не выявлено.
Обсуждение
Полученные результаты демонстрируют более эффективное купирование симптомов ГЭРБ при применении комбинированной терапии ИПП и эзофагопротектором, оказывающим заживляющее действие при эрозивных повреждениях эпителия пищевода. Кроме того, применение комбинированной терапии определило тенденцию к более выраженному улучшению качества жизни пациентов в сравнении с монотерапией ИПП. Результаты нашего исследования подтверждаются данными нескольких многоцентровых зарубежных клинических исследований, в которых применение комбинации гиалуроновой кислоты с хондроитина сульфатом и ИПП также позволяло более эффективно купировать клинические проявления заболевания и повышать качество жизни пациентов в сравнении с монотерапией ИПП в течение 4–5 нед. [20, 21]. В нашем исследовании установлена более выраженная редукция макроскопических изменений у больных эрозивным эзофагитом, принимающих ИПП в комбинации с эзофагопротектором. Таким образом, применение эзофагопротектора в дополнение к ИПП позволило достигать первичной и вторичных конечных точек существенно чаще, что позволяет говорить о высокой эффективности применения препарата в комбинации с ИПП при эрозивном эзофагите.
Ограничения исследования. Установленные критерии включения и невключения не позволили оценить эффективность и безопасность комбинированной терапии ИПП и эзофагопротектором у бессимптомных больных, пациентов с неэрозивной формой ГЭРБ, лиц с пищеводом Барретта, сопутствующей язвой желудка и двенадцатиперстной кишки, а также принимающих цитостатики, глюкокортикостероиды или НПВП.
Заключение
Таким образом, наши данные свидетельствуют о высокой эффективности и безопасности комбинированной терапии ИПП и эзофагопротектором на основе гиалуроновой кислоты, хондроитина сульфата и полоксамера 407 для купирования симптомов заболевания и повышения качества жизни больных, более быстрой и полной ремиссии рефлюкс-эзофагита путем дополнительного восстановления резистентности слизистой оболочки пищевода. Эзофагопротектор как компонент комплексной терапии совместно с ИПП способствует достижению клинической и эндоскопической ремиссии заболевания у пациентов с эрозивным эзофагитом в более сжатые сроки.
Сведения об авторах:
Матошина Ирина Вячеславовна — ассистент кафедры факультетской терапии и гастроэнтерологии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0001-6282-8979.
Ливзан Мария Анатольевна — д.м.н., профессор, ректор, заведующая кафедрой факультетской терапии и гастроэнтерологии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-6581-7017.
Федорин Максим Михайлович — ординатор кафедры факультетской терапии и гастроэнтерологии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-0238-4664.
Лаптева Ирина Вячеславовна — заведующая терапевтическим отделением № 1, руководитель гастроэнтерологического центра БУЗОО «Городская больница № 3»; 644029, Россия, г. Омск, ул. Энергетиков, д. 19.
Контактная информация: Федорин Максим Михайлович, e-mail: maxim.f@gmail.com.
Источник финансирования: грант Президента РФ для государственной поддержки ведущих научных школ (НШ-2558.2020.7) (соглашение № 075-15-2020-036 от 17 марта 2020 г.) «Разработка технологии здоровьесбережения коморбидного больного гастроэнтерологического профиля на основе контроля приверженности».
Конфликт интересов отсутствует.
Статья поступила 25.06.2021.
Поступила после рецензирования 20.07.2021.
Принята в печать 12.08.2021.
About the authors:
Irina V. Matoshina — Assistant Professor of the Department of Faculty Therapy and Gastroenterology, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0001-6282-8979.
Maria A. Livzan — Dr. Sc. (Med.), Professor, Head of the Department of Faculty Therapy and Gastroenterology, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0002-6581-7017.
Maxim M. Fedorin — Resident of the Department of Faculty Therapy and Gastroenterology, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0002-0238-4664.
Irina V. Lapteva — Head of the Department of Internal Medicine No. 1, Head of the Center of Gastroenterology, City Hospital No. 3; 19, Energetiki str., Omsk, 644029, Russian Federation.
Contact information: Maxim M. Fedorin, e-mail: maxim.f@gmail.com.
Financial Disclosure: grant of the President of the Russian Federation for state support of leading scientific schools (NSH-2558.2020.7) (Agreement No. 075-15-2020-036 of March 17, 2020) "Development of health-preserving technology for patient with comorbid gastroenterological profile based on adherence control".
There is no conflict of interests.
Received 25.06.2021.
Revised 20.07.2021.
Accepted 12.08.2021.
2. Hopwood D., Bateson M.C., Milne G., Bouchier I.A. Effects of bile acids and hydrogen ion on the fine structure of oesophageal epithelium. Gut. 1981;22(4):306–311. DOI: 10.1136/gut.22.4.306.
3. Dixon M.F., Neville P.M., Mapstone N.P. et al. Bile reflux gastritis and Barrett’s oesophagus: further evidence of a role for duodenogastroesophageal reflux? Gut. 2001;49(3):359–363. DOI: 10.1136/gut.49.3.359.
4. Симаненков В.И., Маев И.В., Ткачева О.Н. и др. Синдром повышенной эпителиальной проницаемости в клинической практике. Мультидисциплинарный национальный консенсус. Кардиоваскулярная терапия и профилактика. 2021;20(1):2758. DOI: 10.15829/1728-8800-2021-2758.
5. Матошина И.В., Федорин М.М., Ливзан М.А., Мозговой C.И. Резистентность слизистой оболочки пищевода у больных ГЭРБ: диалог клинициста и морфолога. Эффективная фармакотерапия. 2021;17(4):34–39. DOI: 10.33978/2307-3586-2021-17-4-34-39.
6. Hunt R., Armstrong D., Katelaris P. et al. Review Team. World Gastroenterology Organisation Global Guidelines: GERD Global Perspective on Gastroesophageal Reflux Disease. J Clin Gastroenterol. 2017;51(6):467–478. DOI: 10.1097/MCG.0000000000000854.
7. Алексеенко С.А., Багдасарян А.А., Бакулин И.Г. и др. Краткие алгоритмы ведения пациентов на этапе оказания первичной медико-санитарной помощи. М.: Видокс; 2019.
8. Akiyama J., Kuribayashi S., Baeg M.K. et al. Current and future perspectives in the management of gastroesophageal reflux disease. Ann N Y Acad Sci. 2018;1434(1):70–83. DOI: 10.1111/nyas.13850.
9. Moayyedi P., Santana J., Khan M. et al. WITHDRAWN: Medical treatments in the short term management of reflux oesophagitis. Cochrane Database Syst Rev. 2011;(2):CD003244. DOI: 10.1002/14651858.CD003244.pub3.
10. Wolfe M.M., Sachs G. Acid suppression: optimizing therapy for gastroduodenal ulcer healing, gastroesophageal reflux disease, and stress-related erosive syndrome. Gastroenterology. 2000;118(2 Suppl 1):S9–31. DOI: 10.1016/s0016-5085(00)70004-7.
11. Маев И.В., Андреев Д.Н., Кучерявый Ю.А. и др. Современные достижения в лечении гастроэзофагеальной рефлюксной болезни: фокус на эзофагопротекцию. Терапевтический архив. 2019;91(8):4–11. DOI: 10.26442/00403660.2019.08.000387.
12. Ливзан М.А., Кононов А.В. Клинические и фармакоэкономические аспекты антисекреторной терапии гастроэзофагеальной рефлюксной болезни. Экспериментальная и клиническая гастроэнтерология. 2004;(4):55–60.
13. Tack J. Review article: role of pepsin and bile in gastro-oesophageal reflux disease. Aliment Pharmacol Ther. 2005;22 Suppl 1:48–54. DOI: 10.1111/j.1365-2036.2005.02609.x.
14. Zhang J.X., Ji M.Y., Song J. et al. Proton pump inhibitor for non-erosive reflux disease: a meta-analysis. World J Gastroenterol. 2013;19(45):8408–8419. DOI: 10.3748/wjg.v19.i45.8408.
15. El-Serag H., Becher A., Jones R. Systematic review: persistent reflux symptoms on proton pump inhibitor therapy in primary care and community studies. Aliment Pharmacol Ther. 2010;32(6):720–737. DOI: 10.1111/j.1365-2036.2010.04406.x.
16. Николаев Н.А., Мартынов А.И., Скирденко Ю.П. и др. Управление лечением на основе приверженности: алгоритмы рекомендаций для пациентов. Междисциплинарные рекомендации. Медицинский вестник Северного Кавказа. 2020;15(4):461–468. DOI: 10.14300/mnnc.2020.15109.
17. Эмбутниекс Ю.В., Валитова Э.Р., Бордин Д.С. Новый подход к лечению гастроэзофагеальной рефлюксной болезни: защита слизистой оболочки пищевода. Эффективная фармакотерапия. 2019;15(18):16–22. DOI: 10.33978/2307-3586-2019-15-18-16-22.
18. Savarino E., Zentilin P., Marabotto E. et al. Drugs for improving esophageal mucosa defense: where are we now and where are we going? Ann Gastroenterol. 2017;30(6):585–591. DOI: 10.20524/aog.2017.0187.
19. Vakil N., van Zanten S.V., Kahrilas P. et al. Global Consensus Group. The Montreal definition and classification of gastroesophageal reflux disease: a global evidence-based consensus. Am J Gastroenterol. 2006;101(8):1900–1920; quiz 1943. DOI: 10.1111/j.1572-0241.2006.00630.x.
20. Savarino V., Pace F., Scarpignato C. Esoxx Study Group. Randomised clinical trial: mucosal protection combined with acid suppression in the treatment of non-erosive reflux disease — efficacy of Esoxx, a hyaluronic acid-chondroitin sulphate based bioadhesive formulation. Aliment Pharmacol Ther. 2017;45(5):631–642. DOI: 10.1111/apt.13914.
21. Palmieri B., Merighi A., Corbascio D. et al. Fixed combination of hyaluronic acid and chondroitin-sulphate oral formulation in a randomized double blind, placebo controlled study for the treatment of symptoms in patients with non-erosive gastroesophageal reflux. Eur Rev Med Pharmacol Sci. 2013;17(24):3272–3278.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Распечатать

