Определение уровня кортизола в слюне, собранной в позднее вечернее время, в скрининге эндогенного гиперкортицизма
Цель исследования: проанализировать результаты оценки уровня кортизола в слюне (КС), собранной в позднее вечернее время, выполненной методом электрохемилюминесцентного анализа (ЭХЛА), у пациентов с различной массой тела, обследованных в связи с подозрением на синдром Иценко — Кушинга, и определение оптимальной точки разделения для этого показателя в скрининге эндогенного гиперкортицизма (ЭГ).
Материал и методы: в исследование включены 100 пациентов, у которых был определен уровень КС, собранной в позднее вечернее время, с целью первичной диагностики ЭГ. Референсным значением считали 6,7 нмоль/л. Для подтверждения результатов исследования использовали как минимум один тест, рекомендованный для диагностики ЭГ. Статистический анализ проведен с помощью пакета IBM SPSS Statistics v. 23. Пороговое значение КС определено с помощью ROC-анализа, в качестве зависимой переменной выбрано наличие ЭГ.
Результаты исследования: из 100 пациентов диагноз ЭГ был установлен в 28 случаях. Пациенты не отличались по индексу массы тела: у пациентов с ЭГ его медиана была 31 [27; 37], а у пациентов без ЭГ — 29,4 [26; 33], р=0,475. По данным ROC-анализа, для диагностики ЭГ оптимальным пороговым значением КС с чувствительностью 93% и специфичностью 87% оказался показатель 6,6 нмоль/л. Площадь под кривой (AUC) составила 0,944, p<0,001. Чувствительность и специфичность для значений 6,7 нмоль/л и 6,85 нмоль/л составили 89,3% / 88% и 89% / 88% соответственно. Чувствительность для показателя 9,4 нмоль/л была 71%, а специфичность — 91,7%.
Заключение: по нашим данным, при использовании ЭХЛА оптимальной точкой разделения для КС, собранной в позднее вечернее время, в скрининге ЭГ является значение 6,6 нмоль/л. Пороговые значения 6,7 нмоль/л и 6,85 нмоль/л мало уступают в чувствительности и специфичности и также могут быть использованы в диагностике ЭГ.
Ключевые слова: электрохемилюминесцентный анализ, кортизол в слюне, эндогенный гиперкортицизм, синдром Иценко — Кушинга, чувствительность, специфичность.
Для цитирования: Тимкина Н.В., Цой У.А., Курицына Н.В., Литвиненко Е.В., Васильева Е.Ю., Гринева Е.Н. Определение уровня кортизола в слюне, собранной в позднее вечернее время, в скрининге эндогенного гиперкортицизма. РМЖ. Медицинское обозрение. 2021;29(2):3-8.
Late-night salivary cortisol as a screening of endogenous hypercortisolism
N.V. Timkina, U.A. Tsoy, N.V. Kuritsyna, E.V. Litvinenko, E.Yu. Vasileva, E.N. Grineva
V.A. Almazov National Medical Research Center, Saint Petersburg
Aim: to analyze the results concerning evaluation of late-night salivary cortisol (LNSC), performed by electrochemiluminescence (ECL) assay in patients with different body weight for the screening of Cushing’s syndrome, and to determine the optimal cut-off value of LNSC for detection of endogenous hypercortisolism (EHC).
Patients and Methods: the study included 100 patients with evaluated LNSC for the purpose of primary diagnosis of EHC. The reference value was 6.7 nmol/L. At least one test for the diagnosis of EHC was used to confirm the study results. The statistical analysis was performed using the IBM SPSS Statistics v. 23 package. LNCS threshold value was determined using receiver-operator characteristic (ROC) analysis, where EHC presence was selected as the dependent variable.
Results: among 100 patients, the diagnosis of EHC was established in 28 cases. The patients’ body m ass index did not differ: in patients with EHC, the median was 31 [27; 37], and in patients without EHC — 29.4 [26; 33], p=0.475. According to the ROC analysis for the diagnosis of EHC, the optimal LNCS cut-off value with a sensitivity of 93% and a specificity of 87% was 6.6 nmol/L. The area under the curve (AUC) was 0.944, р<0.001. The sensitivity/specificity for the values of 6.7 nmol/L and 6.85 nmol/L was 89.3% / 88% and 89% / 88%, respectively. The sensitivity for 9.4 nmol/L was 71%, whereas the specificity was 91.7%.
Conclusion: according to our data during ECL, the optimal cut-off value for LNSC was 6.6 nmol/L in the EHC screening. The threshold values, 6.7 nmol/L and 6.85 nmol/L, were not significantly inferior in sensitivity and specificity, and can also be used in the diagnosis of EHC.
Keywords: electrochemiluminescence assay, salivary cortisol, endogenous hypercortisolism, Cushing’s syndrome, sensitivity, specificity.
For citation: Timkina N.V., Tsoy U.A., Kuritsyna N.V. et al. Late-night salivary cortisol as a screening of endogenous hypercortisolism. RMJ. 2021;2:3–8.
Введение
Эндогенный гиперкортицизм (ЭГ, синдром Иценко — Кушинга) — это заболевание, которое развивается вследствие хронического избытка кортизола [1]. Основными причинами ЭГ являются секретирующая адренокортикотропный гормон (АКТГ) аденома гипофиза, кортизол-продуцирующая аденома надпочечника и нейроэндокринная опухоль с эктопической продукцией АКТГ [1]. Смертность при ЭГ в 4–5 раз выше, чем в общей популяции [2, 3]. Вместе с тем показано, что нормализация уровня кортизола при адекватном лечении ЭГ позволяет улучшить прогноз жизни пациентов [1, 4]. Одним из условий успешного решения этой задачи является ранняя диагностика ЭГ, что может быть обеспечено наличием чувствительных и специфичных диагностических тестов [5]. Согласно международным рекомендациям для скрининга при подозрении на ЭГ следует использовать одно из исследований: определение суточной экскреции свободного кортизола с мочой (СЭСКМ), определение уровня кортизола в слюне (КС), собранной в позднее вечернее время, определение уровня кортизола в сыворотке крови (КСК), взятой утром после приема 1 мг дексаметазона накануне в 23:00 (малая дексаметазоновая проба, МДП), тест с 2 мг дексаметазона. Для подтверждения наличия ЭГ достаточно получить положительные результаты двух из вышеперечисленных тестов [1]. В российских клинических рекомендациях по диагностике и лечению болезни Иценко — Кушинга приоритет отдается двум тестам: определению уровня КС, собранной в 23:00, и МДП [6]. Выбор первых двух тестов в качестве исследований 1-й линии является оправданным, т. к. скрининг при подозрении на ЭГ в большинстве случаев выполняется амбулаторно. Исследование уровня КС, собранной в позднее вечернее время, максимально соответствует требованиям, предъявляемым к скрининговым тестам, и является методом выбора для скрининга ЭГ [1, 6–9]. Тест обладает высокой точностью, он неинвазивный, не требует много времени и является простым в исполнении, может быть легко выполнен пациентом самостоятельно в домашних условиях после получения специального контейнера и инструкции для сбора слюны [1, 6, 8]. Также он лишен ограничений, характерных для исследования СЭСКМ и тестов с дексаметазоном [1, 6]. Однако недостатком этого метода является отсутствие единого стандартизированного метода оценки и, как следствие, отсутствие единых референсных значений для уровня КС, собранной в позднее вечернее время, а также единой точки разделения нормы и ЭГ [10, 11]. В настоящее время в мире используют два основных метода оценки КС: иммунный анализ и метод высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией [10, 12–14]. С учетом разнообразия методов оценки уровня КС рекомендуется в каждой лаборатории разрабатывать свои референсные и пороговые значения [1, 6, 11].
В течение последних лет для определения уровня КС широкое распространение в Российской Федерации получил метод автоматизированного электрохемилюминесцентного анализа (ЭХЛА). В клинических рекомендациях Российской ассоциации эндокринологов по диагностике и лечению болезни Иценко — Кушинга для метода ЭХЛА рекомендована точка разделения 9,4 нмоль/л как пороговая для диагностики ЭГ [6]. Однако, согласно данным исследования, по результатам которого была предложена эта точка разделения, высокие чувствительность (84,4%) и специфичность (92,3%) порогового значения 9,4 нмоль/л были получены для диагностики ЭГ среди пациентов с ожирением [15]. Вместе с тем известно, что не у всех пациентов с синдромом Кушинга имеет место ожирение [16–19]. В связи с этим в ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России при оценке уровня КС, собранной в позднее вечернее время, методом автоматизированного ЭХЛА для диагностики ЭГ в период с 2015 по 2018 г. использовалось пороговое значение 6,7 нмоль/л, которое предложено в качестве референсного согласно инструкции к набору реагентов для количественного определения КС.
Целью настоящего исследования было проанализировать результаты оценки уровня КС, собранной в позднее вечернее время, выполненной методом ЭХЛА в лаборатории ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России, у пациентов с различной массой тела, обследованных в связи с подозрением на ЭГ, и определить оптимальное пороговое значение данного показателя для диагностики синдрома Кушинга у этой категории пациентов.
Материал и методы
Было проведено ретроспективное когортное исследование. Для выявления пациентов, которым с целью скрининга ЭГ выполнялся анализ слюны, собранной в позднее вечернее время, на кортизол, была изучена база данных лаборатории ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России в период с 2015 по 2018 г. Было найдено 420 результатов тестов на КС, собранной в позднее вечернее время у амбулаторных и стационарных пациентов. Затем в системе регистрации медицинских данных Quality Management System были изучены электронные истории болезни с целью выбора пациентов, соответствующих критериям включения.
В исследование включали мужчин и женщин в возрасте от 18 лет и старше, у которых уровень КС, собранной в позднее вечернее время, был определен с целью скрининга на ЭГ. Также у данных пациентов должен был быть известен результат как минимум одного из следующих тестов: СЭСКМ, КСК, забранной в полночь, МДП. Критерии невключения были следующими: беременность, работа в ночную смену, указание на кровоточивость десен, прием глюкокортикоидов и блокаторов стероидогенеза, острые инфекционные заболевания, уровень гликированного гемоглобина более 7,5% при наличии сахарного диабета, тяжелая сопутствующая соматическая патология, терминальные состояния. Всего в исследование было включено 100 пациентов (28 мужчин, 72 женщины), медиана возраста составила 46 лет [34; 61].
Методика исследования уровня кортизола в слюне
Анализ слюны на кортизол назначали врачи-эндокринологи НМИЦ им. В.А. Алмазова при подозрении на ЭГ согласно критериям международных и российских рекомендаций [1, 16]. Все пациенты заполняли информированное добровольное согласие на обработку персональных данных. Специальный контейнер для сбора слюны Salivette Sarstedi (SARSDEDT AG&CO, Германия) и инструкцию по сбору слюны пациенту выдавал врач-эндокринолог, который рекомендовал обследование. Сбор слюны проводился пациентом самостоятельно с 23:00 до 24:00. За сутки до сбора анализа пациентам было рекомендовано воздерживаться от употребления алкоголя; за 30 мин — от курения, употребления каких-либо напитков, кроме простой воды, от чистки зубов. После сбора слюны контейнер помещали в холодильник (не в морозильное отделение). На следующее утро после сбора слюны контейнер доставляли в лабораторию (пациент самостоятельно из дома или медперсонал, если обследование проводилось в стационаре), не допуская его нагрева. Пробирки центрифугировали в течение 2–3 мин на скорости 1000 оборотов в минуту. Определение уровня КС методом автоматизированного ЭХЛА выполнялось с использованием автоматического анализатора Cobas e411 («Хоффманн-Ля Рош», Швейцария). В лаборатории НМИЦ им. В.А. Алмазова референсным значением для КС, собранной в позднее вечернее время, является 6,7 нмоль/л.
Для диагностики ЭГ использовали следующие критерии: уровень КС, собранной в позднее вечернее время, 6,7 нмоль/л и выше и наличие как минимум одного из перечисленных условий: повышение СЭСКМ; отсутствие снижения уровня кортизола в сыворотке менее 50 нмоль/л при проведении МДП; КСК, забранной в полночь, 207 нмоль/л и выше. В случаях, когда уровень КС был ниже 6,7 нмоль/л, выполнялся как минимум один дополнительный диагностический тест. Если его результаты свидетельствовали против ЭГ, дальнейшее обследование не проводили. Если результаты второго теста были в пользу ЭГ, выполняли еще один или два дополнительных теста, если они были положительными, устанавливали диагноз ЭГ. При уровне КС, собранной в позднее вечернее время, 6,7 нмоль/л и выше пациента обследовали в эндокринологическом отделении НМИЦ им. В.А. Алмазова. Диагноз считали подтвержденным при наличии как минимум двух тестов, свидетельствующих в пользу заболевания [6]. Сбор суточной мочи на кортизол проводился согласно клиническим рекомендациям Российской ассоциации эндокринологов по диагностике и лечению болезни Иценко — Кушинга [6].
Исследование проводилось методом ЭХЛА с использованием анализатора Cobas e411. Референсное значение составляет 38–208 нмоль/л/сут. МДП выполняли согласно рекомендованной методике [6]. Исследование КСК проводили методом ЭХЛА, точкой разделения для диагностики ЭГ считали значение 50 нмоль/л и более. Исследование КСК в полночь выполняли пациентам, которые находились в стационаре как минимум через 48 ч после госпитализации. Забор крови осуществлялся у бодрствующих пациентов в 24:00. Для оценки результата использовали точку разделения менее 207 нмоль/л (7,5 мкг/дл), предложенную D. Papanicolaou et al. [20].
Статистический анализ проведен с помощью пакета IBM SPSS Statistics v. 23 (США). Поскольку распределение показателей не было нормальным, данные представлены в виде медианы и квартилей [25 перцентиль;75 перцентиль]. Достоверность различий оценивалась с помощью критерия χ-квадрата Пирсона с поправкой Йетса, а для непрерывных данных сравнение проводилось с помощью критерия Манна — Уитни. Поиск точки разделения значения КС, собранной в позднее вечернее время, для диагностики ЭГ, с расчетом чувствительности и специфичности проводили на основании построения кривых операционных характеристик (ROC-анализ). В качестве зависимой переменной было выбрано наличие ЭГ. Оптимальной точкой разделения считали показатель КС, которому соответствовала максимальная сумма чувствительности и специфичности метода, рассчитанная по результатам ROC-анализа.
Результаты исследования
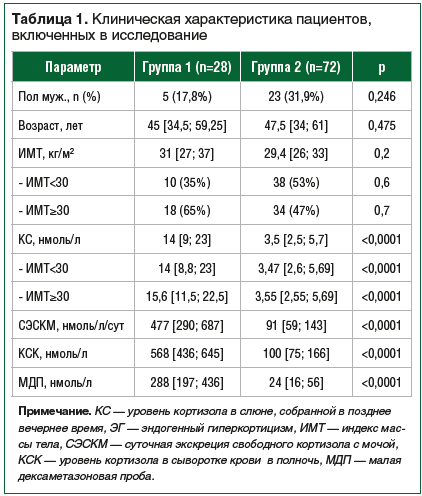
Диагноз ЭГ был подтвержден у 28 пациентов, которые составили группу 1 (у 24 пациентов верифицирована АКТГ-продуцирующая аденома гипофиза, у 3 пациентов был выявлен АКТГ-независимый гиперкортицизм вследствие гиперпродукции кортизола образованиями надпочечников, у 1 пациентки — автономная продукция кортизола двусторонними образованиями надпочечников). В 72 случаях данных за гиперпродукцию кортизола не было получено, эти пациенты составили группу 2. Группы 1 и 2 не отличались по полу, возрасту, индексу массы тела (ИМТ). Клиническая характеристика пациентов представлена в таблице 1. В группе 1 уровень КС был 6,7 нмоль/л и выше в 25 случаях. Из 25 пациентов с повышенным уровнем КС в 5 случаях диагноз ЭГ был подтвержден на основании положительных результатов 3 дополнительных тестов (КСК, МДП и СЭСКМ). В 20 случаях основанием для подтверждения ЭГ были положительные результаты 2 тестов: КСК и МДП — у 7 пациентов, КСК и СЭСКМ — у 10 пациентов, СЭКСМ и МДП — у 3 пациентов.
У 3 пациенток уровень КС оказался ниже 6,7 нмоль/л, однако по данным дополнительного обследования во всех 3 случаях был установлен диагноз ЭГ. Из них у 2 пациенток гиперпродукция кортизола была доказана результатами 2 тестов (СЭСКМ и КСК). Впоследствии у них была диагностирована болезнь Иценко — Кушинга, в т. ч. по данным гистологического и иммуногистохимического исследований удаленной аденомы гипофиза. Обе пациентки имели нормальный ИМТ (23 кг/м2 и 24 кг/м2). У 1 пациентки с ожирением был установлен диагноз автономной продукции кортизола надпочечниками по результатам 2 дополнительных тестов (нормальный уровень КСК в полночь и отсутствие адекватного подавления кортизола в сыворотке при проведении МДП). Все пациенты были оперированы (кроме пациентки с автономной продукцией кортизола, которой было рекомендовано динамическое наблюдение), первоначальный диагноз был подтвержден результатами гистологического и иммуногистохимического исследования (АКТГ-секретирующая аденома гипофиза в 24 случаях, кортизол-секретирующая аденома надпочечника в 3 случаях).
В группе 2 из 72 пациентов уровень КС оказался ниже 6,7 нмоль/л в 65 случаях. Из них 31 пациенту был выполнен 1 дополнительный тест, результаты которого также свидетельствовали об отсутствии ЭГ (СЭСКМ — в 15 случаях, МДП — в 3 случаях, КСК — в 13 случаях). В 30 случаях было проведено 2 дополнительных теста, которые подтвердили отсутствие ЭГ (КСК и МДП — у 6 пациентов, КСК и СЭСКМ — у 19 пациентов, СЭСКМ и МДП — у 5 пациентов). Четырем пациентам были выполнены 3 теста (КСК, СЭСКМ и МДП), их результаты оказались отрицательными, ЭГ был исключен. Следует отметить, что при анализе результатов МДП в группе 2 75 процентиль значения кортизола составила 56 нмоль/л (табл. 1). Это объясняется тем, что у 8 пациентов значения кортизола крови после пробы с дексаметазоном были выше 50 нмоль/л. Однако у данных пациентов ЭГ был исключен на основании других тестов (КС, СЭКСМ, КСК).
У 7 пациентов (4 женщины) из группы 2 уровень КС оказался 6,7 нмоль/л и выше, что свидетельствовало в пользу ЭГ. Однако при последующем обследовании ЭГ был исключен по результатам 2 тестов (СЭКСМ и МДП — в 4 случаях, СЭКСМ и КСК — в 2 случаях, МДП и КСК — в 1 случае). Медиана КС у этих 7 пациентов была 10,19 нмоль/л [8,9; 11,265], максимальное значение КС — 13,1 нмоль/л. У 5 человек было ожирение. При анализе медицинской документации не найдено указаний на кровоточивость десен или нарушение методики сбора КС, однако полностью исключить эти факторы не представлялось возможным. У 2 человек (согласно заключению психолога) причиной ложноположительного результата могли быть расстройство адаптации и депрессия.
Как показано в таблице 1, показатели КС были выше в группе 1 (14 нмоль/л против 3,5 нмоль/л, p<0,0001). Мы проанализировали распределение пациентов с различной массой тела в обеих группах. Оказалось, что количество больных с нормальной и избыточной массой тела и с ожирением не отличалось в обеих группах. Независимо от ИМТ уровень КС в группе 1 был выше, чем в группе 2. Отличий между показателями КС у пациентов с различной массой тела в группе 1 не было выявлено. В группе 2 медиана КС также не отличалась у пациентов с различной массой тела. Распределение пациентов по уровню КС в зависимости от массы тела показано на рисунке 1.
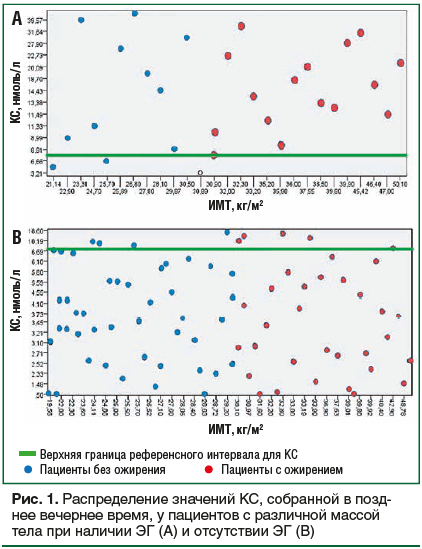
В группе 1 у 5 (18%) пациенток уровень КС оказался выше 6,7 нмоль/л и ниже, чем 9,4 нмоль/л. Из них у 3 было ожирение, у 2 других избыточная масса тела или нормальная масса тела. Во всех случаях был подтвержден диагноз болезни Иценко — Кушинга.
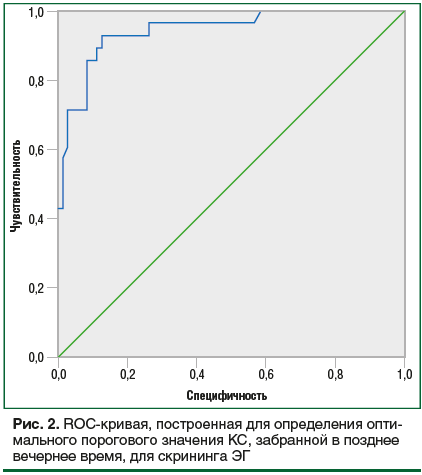
По данным ROC-анализа, оптимальной точкой разделения значения КС, собранной в позднее вечернее время, для диагностики ЭГ с чувствительностью 93% [95% ДИ 74; 97] и специфичностью 87% [95% ДИ 83; 91] оказалось значение 6,6 нмоль/л. Площадь под кривой (AUC) составила 0,944, p<0,001 (рис. 2).
Также с использованием ROC-анализа были оценены чувствительность и специфичность других пороговых значений КС, рекомендованных ранее [15]. Для показателей 9,4 нмоль/л и 6,85 нмоль/л чувствительность оказалась 71% и 89% соответственно, а специфичность — 91,7% и 88% соответственно. Для точки разделения 6,7 нмоль/л чувствительность составила 89,3%, а специфичность — 88%. Результаты оценки специфичности и чувствительности, полученные для других пороговых значений КС, представлены в таблице 2.
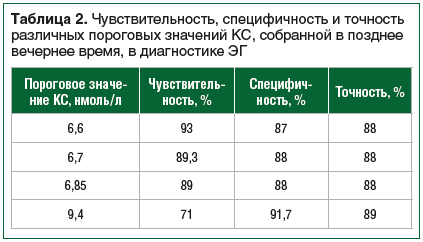
Таким образом, для скрининга ЭГ среди пациентов с различной массой тела оптимальным пороговым значением КС, собранной в позднее вечернее время, оказалось 6,6 нмоль/л, точность — 88%. Чувствительность, специфичность и точность для показателей 6,7 нмоль/л и 6,85 нмоль/л также оказались близкими и достаточно высокими (см. табл. 2).
Обсуждение
В нашем ретроспективном исследовании были проанализированы результаты оценки определения уровня КС в позднее вечернее время, выполненной методом ЭХЛА в лаборатории ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России, у пациентов с различной массой тела, обследованных в связи с подозрением на ЭГ. По данным проведенного ROC-анализа, оказалось, что для диагностики ЭГ оптимальным порогом уровня КС, собранной в позднее вечернее время, является значение 6,6 нмоль/л с чувствительностью 93% и специфичностью 87%. Наши данные совпали с результатами других исследований, в которых была показана высокая информативность данного метода для диагностики синдрома Иценко — Кушинга [18–22]. Так, в исследовании N. Yilmaz et al. был проанализирован 7-летний опыт применения определения уровня КС методом ЭХЛА для диагностики ЭГ. Были получены данные о том, что точка разделения 0,288 мкг/дл обладала чувствительностью 89,6% и специфичностью 81,6% в диагностике синдрома Кушинга [18]. По данным K.D.S. Jarial et al., пороговое значение 10,54 нмоль/л для КС, собранной в позднее вечернее время, обладало чувствительностью 85,7% и специфичностью 88,2% [22]. Несмотря на сопоставимые показатели специфичности и чувствительности, обращает на себя внимание широкий разброс пороговых значений, предлагаемых различными авторами [18, 19, 21–23]. Это может быть обусловлено различиями в используемых анализаторах, а также в методике исследований [10–12].
В Российской Федерации в большом количестве лабораторий определение уровня КС осуществляется методом ЭХЛА с использованием анализаторов Elecsys 1010, Elecsys 2010, MODULAR ANALYTICS E170, Cobas e 411, Cobas e 60. В настоящее время открытым остается вопрос об использовании точки разделения КС для пациентов с ожирением и без ожирения. Известно, что ожирение встречается не у 100% пациентов, которых обследуют в связи с подозрением на ЭГ, включая тех, у кого синдром Иценко — Кушинга оказывается подтвержденным [16–19]. Так, по данным R.A. Alwani et al., среди 73 пациентов, обследованных в связи с подозрением на ЭГ (у 53 была подтверждена болезнь Кушинга, у 20 установлен диагноз «псевдосиндром Кушинга»), ожирение имело место в 60% случаев [19]. Из 249 пациентов, обследованных D. Erickson et al., синдром Кушинга был подтвержден у 47 человек, ожирение имели 28 (60%) из них. А из 202 обследованных, у которых ЭГ не был подтвержден, ожирение было у 135 (66,8%) [17]. По нашим данным, из 28 пациентов с ЭГ 65% имели ожирение, а среди 72 пациентов, у которых синдром Иценко — Кушинга не был подтвержден, ожирение было у 47%, что не противоречит данным других авторов [16–19]. Также в нашем исследовании у 5 (18%) пациентов с ЭГ из 28 уровень КС в позднее вечернее время оказался в диапазоне 6,7–9,4 нмоль/л, у 3 из них имело место ожирение. Таким образом, применение в диагностике ЭГ точки разделения, полученной при обследовании пациентов с ожирением, представляется спорным.
В исследовании Ж.Е. Белой и соавт. для выявления ЭГ также была получена точка разделения 6,85 нмоль/л, которая у лиц с нормальным ИМТ показала чувствительность 91,1% и специфичность 96,9%, а у пациентов с ожирением — чувствительность 91,1% и специфичность 84,6% [15]. Для выявления ЭГ среди лиц с нормальной массой тела чувствительность и специфичность точки разделения 9,4 нмоль/л составили 84,4% и 97,9% соответственно [15]. В нашем исследовании точка разделения 6,85 нмоль/л и точка разделения 6,7 нмоль/л показали очень близкие со значением 6,6 нмоль/л чувствительность и специфичность (89% и 88% соответственно для обоих значений, в сравнении с 93% и 87% соответственно для точки разделения 6,6 нмоль/л). Для этих значений соотношение чувствительности и специфичности оказалось оптимальным в отличие от показателя 9,4 нмоль/л. По данным Ж.Е. Белой и соавт., чувствительность для точки разделения 9,4 нмоль/л оказалась довольно низкой по сравнению с другими пороговыми значениями (а именно 84,4%) как для лиц с ожирением, так и для лиц с нормальным ИМТ [15]. С учетом того, что определение уровня КС, собранной в позднее вечернее время, является скрининговым методом в диагностике ЭГ, высокая чувствительность метода очень важна, т. к. в этом случае количество пациентов, у которых не выявлено заболевание при его наличии, оказывается минимальным. Что касается специфичности, то обязательное дополнительное обследование, предложенное различными клиническими рекомендациями [1, 6], позволяет выявить пациентов с ложноположительным результатом КС, собранной в позднее вечернее время, и исключить диагноз ЭГ.
В нашем исследовании при использовании точки разделения 6,6 нмоль/л было получено 3 ложноотрицательных результата. В 2 случаях ЭГ был верифицирован при помощи исследования уровня кортизола в суточной моче, МДП и исследования КСК в полночь. В обоих случаях это были пациентки с болезнью Иценко — Кушинга с нормальным ИМТ. В 1 случае при обследовании была верифицирована автономная продукция кортизола надпочечниками, что подтверждает данные других исследователей, свидетельствующие о том, что определение уровня КС в позднее вечернее время обладает низкой специфичностью для диагностики автономной продукции кортизола [24]. Так, в работе I. Kuzu et al. было показано, что специфичность этого метода для диагностики субклинического синдрома Кушинга (в настоящее время это состояние называют автономной продукцией кортизола) составляет 60% [24].
Также в нашей работе у 7 пациентов при оценке уровня КС в позднее вечернее время были получены ложноположительные результаты. Причины ложного повышения уровня КС известны и описаны ранее [7–9]. К сожалению, не всегда удается исключить все из них, особенно это касается возможной контаминации микроскопическим количеством крови, что может не определяться визуально, но приводить к ложному повышению показателя КС. Наличие в нашем исследовании ложноотрицательных и ложноположительных результатов анализа уровня КС, собранной в позднее вечернее время, в диагностике ЭГ подтверждает необходимость применения при верификации синдрома Иценко — Кушинга как минимум двух тестов [1, 6].
Заключение
Результаты нашей работы показали, что при обследовании пациентов с подозрением на ЭГ для оценки уровня КС, собранной в позднее вечернее время, более оптимальным является использование точки разделения, определенной для лиц с различной массой тела, включая нормальную массу тела, избыточную массу тела и ожирение. По нашим данным, такой точкой является 6,6 нмоль/л, вместе с тем пороговые значения 6,7 нмоль/л и 6,85 нмоль/л мало уступают в чувствительности и специфичности и также могут быть использованы в диагностике ЭГ.
2. Lindholm J., Juul S., Jorgensen J.O. et al. Incidence and late prognosis of Cushing’s syndrome: a population-based study. J Clin Endocrinol Metab. 2001;86(1):117–123. DOI: 10.1210/jcem.86.1.
3. Etxabe J., Vazquez J.A. Morbidity and mortality in Cushing’s disease: an epidemiological approach. Clin Endocrinol (Oxf). 1994;40(4):479–484. DOI: 10.1111/j.1365-2265.1994.tb02486.x.
4. Swearingen B., Biller B.M., Barker F.G. 2nd et al. Long-term mortality after transsphenoidal surgery for Cushing disease. Ann Intern Med. 1999;130(10):821–824. DOI: 10.7326/0003-4819-130-10-199905180-00015.
5. Kannankeril J., Carroll T., Findling J.W. et al. Prospective Evaluation of Late-Night Salivary Cortisol and Cortisone by EIA and LC–MS/MS in Suspected Cushing Syndrome. J Endocr Soc. 2020;4(10): bvaa107. DOI: 10.1210/jendso/bvaa107.
6. Мельниченко Г.А., Дедов И.И., Белая Ж.E. и др. Болезнь Иценко — Кушинга: клиника, диагностика, дифференциальная диагностика, методы лечения. Проблемы эндокринологии. 2015;61(2):55–77. [Melnichenko G.A., Dedov I.I., Belaya Zh.E. et al. Cushing’s disease: the clinical features, diagnostics, differential diagnostics, and methods of treatment. Problemy endocrinologii. 2015;61(2):55–77 (in Russ.)]. DOI: 10.14341/probl201561255-77.
7. Raff H., Raff J.L., Findling J.W. Late-night salivary cortisol as a screening test for Cushing’s syndrome. J Clin Endocrinol Metab. 1998;83(8):2681–2686. DOI: 10.1210/jcem.83.8.4936. PMID: 9709931.
8. Inder W.J., Dimeski G., Russell A. Measurement of salivary cortisol in 2012 — laboratory techniques and clinical indications. Clin Endocrinol (Oxf). 2012;77(5):645–651. DOI: 10.1111/j.1365-2265.2012.04508.x.
9. Raff H. Utility of salivary cortisol measurements in Cushing’s syndrome and adrenal insufficiency. J Clin Endocrinol Metab. 2009;94(10):3647–3655. DOI: 10.1210/jc.2009-1166.
10. Raff H. Update on late-night salivary cortisol for the diagnosis of Cushing’s syndrome: methodological considerations. Endocr. 2013;44(2):346–349. DOI: 10.1007/s12020-013-0013-0.
11. El-Farhan N., Rees D.A., Evans C. Measuring cortisol in serum, urine and saliva — are our assays good enough? Ann Clin Biochem. 2017;54(3):308–322. DOI: 10.1177/0004563216687335.
12. Sakihara S., Kageyama K., Oki Y. et al. Evaluation of plasma, salivary, and urinary cortisol levels for diagnosis of Cushing’s syndrome. Endocr J. 2010;57(4):331–337. DOI: 10.1507/endocrj.k09e-340.
13. Antonelli G., Ceccato F., Artusi C. et al. Salivary cortisol and cortisone by LC–MS/MS: validation, reference intervals and diagnostic accuracy in Cushing’s syndrome. Clin Chim Acta. 2015;451(Pt B):247–251. DOI: 10.1016/j.cca.2015.10.004.
14. Handelsman D.J., Wartofsky L. Requirement for mass spectrometry sex steroid assays in the Journal of Clinical Endocrinology and Metabolism. J Clin Endocrinol Metab. 2013;98(10):3971–3973. DOI: 10.1210/jc.2013-3375.
15. Belaya Z.E., Iljin A.V., Melnichenko G.A. et al. Diagnostic performance of late-night salivary cortisol measured by automated electrochemiluminescence immunoassay in obese and overweight patients referred to exclude Cushing’s syndrome. Endocrine. 2012;41(3):494–500. DOI: 10.1007/s12020-012-9658-3.
16. Комердус И., Древаль А., Чеканова А., Акулкина Л. Клинические проявления болезни Иценко — Кушинга (результаты анализа базы данных Московской области). Альманах клинической медицины. 2016;44(4):430–438. [Komerdus I., Dreval’ A., Chekanova A., Akulkina L. Clinical manifestations of Cushing’s disease (results of analysis of the clinical database of the Moscow Region). Al’manakh klinicheskoi meditsiny. 2016;44(4):430–438 (in Russ.)]. DOI: 10.18786/2072-0505-2016-44-4-430-438.
17. Erickson D., Ravinder J., Airani S. et al. Late-night salivary cortisol for diagnosis of Cushing’s syndrome by liquid chromatography/tandem mass spectrometry assay. Clin. Endocrinol. 2012;76:467–472. DOI: 10.1111/j.1365-2265.2011.04239.x.
18. Yilmaz N., Tazegul G., Bozoglan H. et al. Diagnostic value of the late-night salivary cortisol in the diagnosis of clinical and subclinical Cushing’s syndrome: results of a single-center 7-year experience. J Investig Med. 2019;67(1):28–33. DOI: 10.1136/jim-2018-000752.
19. Alwani R.A., Schmit Jongbloed L.W., de Jong F.H. et al. Differentiating between Cushing’s disease and pseudo-Cushing’s syndrome: comparison of four tests. Eur J Endocrinol. 2014;170(4):477–486. DOI: 10.1530/EJE-13-0702.
20. Papanicolaou D.A., Yanovski J.A., Cutler G.B. Jr et al. A single midnight serum cortisol measurement distinguishes Cushing’s syndrome from pseudo-Cushing states. J Clin Endocrinol Metab. 1998;83(4):1163–1167. DOI: 10.1210/jcem.83.4.4733.
21. Carrozza C., Corsello S.M., Paragliola R.M. et al. Clinical accuracy of midnight salivary cortisol measured by automated electrochemiluminescence immunoassay method in Cushing’s syndrome. Ann Clin Biochem. 2010;47(Pt 3):228–232. DOI: 10.1258/acb.2010.010020.
22. Jarial K.D.S., Bhansali A., Mukherjee K.K. et al. Utility of a single late-night plasma cortisol and ACTH for the diagnosis of Cushing’s syndrome. Endocr. Pract. 2018;24(2):156–162. DOI: 10.4158/EP171803.OR.
23. Carroll T., Raff H., Findling J.W. Late-night salivary cortisol for the diagnosis of Cushing syndrome: a meta-analysis. Endocr Pract. 2009;15(4):335–342. DOI: 10.4158/EP09023OR.
24. Kuzu I., Zuhur S.S., Demir N. et al. The diagnostic value of late-night salivary cortisol for diagnosis of subclinical Cushing’s syndrome. Endokrynol Pol. 2016;67(5):487–492. DOI: 10.5603/EP.a2016.0028.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.

