Эффективность, безопасность и приверженность лечению внутривенными бисфосфонатами при постменопаузальном остеопорозе
Постменопаузальный остеопороз (ОП) — один из самых частых клинических вариантов остеопороза. В обзоре представлены основные этапы патогенеза ОП, напрямую связанные с формированием дефицита эстрогенов и нарушением процессов костного ремоделирования. Особое внимание уделено вопросам эффективности и безопасности назначения бисфосфонатов (БФ) при постменопаузальном ОП, которые являются препаратами первой линии в лечении этой патологии. Представлена способность БФ подавлять патологическую резорбцию костной ткани и стимулировать костеобразование. Освещены данные международных плацебо-контролируемых и российских наблюдательных исследований, которые свидетельствуют о высокой эффективности ибандроновой кислоты (ИК). Отмечено, что внутривенное введение ИК 3 мг 1 раз в 3 мес. приводит к восстановлению костного обмена, увеличению минеральной плотности костной ткани и прочности кости, снижает риск позвоночных и внепозвоночных переломов в группе больных высокого риска. Анализ результатов динамического наблюдения за пациентами, получавшими ИК, свидетельствует о ее последействии в течение 12-месячного периода после окончания лечения в отношении сохранения минеральной плотности кости позвонков. Преимуществом внутривенного введения ИК является возможность ее назначения пациентам с патологией желудочно-кишечного тракта (язвы пищевода, эзофагит), а также урежение кратности применения (1 раз в 3 мес.), что повышает приверженность терапии.
Ключевые слова: постменопаузальный остеопороз, бисфосфонаты, ибандроновая кислота, комплаентность, сердечно-сосудистый риск.
Для цитирования: Беляева И.Б. Эффективность, безопасность и приверженность лечению внутривенными бисфосфонатами при постменопаузальном остеопорозе. РМЖ. Медицинское обозрение. 2021;29(4):74-77.
Efficacy, safety, and adherence to intravenous bisphosphonate treatment in postmenopausal osteoporosis
I.B. Belyaeva
I.I. Mechnikov North-Western State Medical University, Saint Petersburg
Postmenopausal osteoporosis is one of the most common clinical types of osteoporosis. The article presents the main stages of the osteoporosis pathogenesis, directly related to the formation of estrogen deficiency and bone remodeling disorder. Particular attention is paid to the efficacy and safety of bisphosphonates (BP) administration, which are the first-line drugs in the treatment of this pathology. The article also presents the ability of BP to inhibit pathological bone resorption and stimulate bone formation and highlights the data of international placebo-controlled and Russian follow-up studies, which indicate the high efficacy of ibandronic acid (IA). It was noted that the use of IA with intravenous administration of 3 mg once every 3 months leads to the restoration of bone metabolism, an increase in bone mineral density (BMD) and strength, and reduces the risk of vertebral and extravertebral fractures in high-risk patients. Analysis of the results concerning the dynamic follow-up of patients receiving IA indicates its aftereffect during the 12 months after the end of treatment for the preservation of the spine BMD. The benefit of ibandronate intravenous administration route is the possibility for patients with gastrointestinal pathology (esophageal ulcers, esophagitis), as well as a reduction in the frequency of use (once every 3 months), which increases adherence to therapy.
Keywords: postmenopausal osteoporosis, bisphosphonates, ibandronic acid, compliance, cardiovascul ar risk.
For citation: Belyaeva I.B. Efficacy, safety, and adherence to intravenous bisphosphonate treatment in postmenopausal osteoporosis. RMJ. 2021;4:74–77.
Введение
Остеопороз (ОП) является метаболическим заболеванием скелета, которое характеризуется снижением костной массы, нарушением ее микроархитектоники, а также развитием переломов при минимальной травме (так называемые низкоэнергетические переломы) [1–3]. Установлено, что подавляющее число случаев ОП приходится на постменопаузальный и сенильный его варианты, которые составляют более 85% от всех его клинических вариантов. Так, в течение первых 5 лет после прекращения регулярного менструального цикла дефицит костной массы составляет более 30% от всего дефицита, который формируется в течение всей жизни [4, 5].
Главную роль в патогенезе постменопаузального ОП играет дефицит вырабатываемого яичниками эстрогена, который модулирует костное ремоделирование посредством регулирования процессов продукции цитокинов и факторов роста [6]. Наиболее частыми локализациями переломов в постменопаузе являются позвонки (компрессионные переломы), проксимальные отделы плечевой и бедренной костей, дистальный отдел предплечья. Показано, что при постменопаузальном ОП для женщины в возрасте 50 лет и старше риск перелома позвоночника, шейки бедра, костей запястья, а также любого из трех участков скелета составляет соответственно 15,5, 17,5, 16,0 и 39,7% [7].
Риск переломов при остеопорозе напрямую связан с факторами риска падений, среди которых выделяют эндогенные: возрастные нарушения (функции мышц, когнитивные способности и т. д.), боль, различные заболевания (остеоартрит, эпилепсия и т. д.), особенности образа жизни (алкоголизм, наркомания, прием лекарственных препаратов — морфина, антигипертензивных и т. д.) и экзогенные (неудобная обувь, особенности рельефа) [8]. Следовательно, основополагающими стратегиями ведения пациентов с ОП могут являться: профилактика первичных и повторных переломов костной ткани, стабилизация или увеличение костной массы, улучшение качества жизни. Увеличение комплаентности в лечении таких пациентов можно обеспечить использованием безопасного способа приема препарата, максимальным снижением нежелательных эффектов и стоимости, а также удобством приема препарата.
Механизмы развития постменопаузального ОП
Патогенетические этапы развития постменопаузального ОП напрямую связаны с дефицитом эстрогенов и участием иммунных механизмов в регуляции остеокластогенеза. В многочисленных исследованиях продемонстрирована лидирующая роль в регуляции функции остеокластов макрофагального колониестимулирующего фактора и лиганда — активатора рецептора ядерного фактора κВ (RANKL). Определена прямая взаимосвязь между дефицитом эстрогенов, стимуляцией активности RANKL и гиперпродукцией провоспалительных цитокинов (IL-1, IL-6, TNF-α) [6]. В последние годы установлена патогенетическая роль IL-7 в инициации остеокластогенеза, пусковым фактором в увеличении продукции которого также выступает дефицит эстрогенов. Являясь фактором роста гемопоэтических клеток, этот цитокин стимулирует пролиферацию и дифференцировку Т-лимфоцитов в тимусе и костном мозге. Повышению активности Т-лимфоцитов способствует также снижение синтеза трансформирующего фактора роста фибробластов β, который формируется на фоне дефицита эстрогенов. Следствием цитокинового дисбаланса, активации Т-лимфоцитов является дефицит остеопротегирина. Известно, что последний обеспечивает баланс костеобразования и ее резорбции, а его функциональная недостаточность приводит к пролиферации остеокластов, и, следовательно, к нарушению микроархитектоники кости и к снижению ее прочности [1, 7].
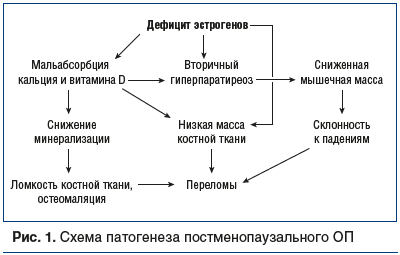
В формировании ОП высока роль дефицита витамина D и недостаточного поступления кальция в костную ткань, что обусловливает развитие вторичного гиперпаратиреоза и запускает медленную потерю костной массы (рис. 1). Кроме того, в период менопаузы дефицит кальция и витамина D связан с секреторной недостаточностью кишечной лактазы и формированием синдрома мальабсорбции, которые приводят к значительному уменьшению поступления кальция с пищей. Немаловажными причинами развития ОП являются: недостаток инсоляции и нарушение синтеза витамина D в коже, нарушения координации, а также формирование дефицита α-гидроксилазы вследствие сниженной синтетической функции почек [9].
Определена роль дефицита некоторых микроэлементов в формировании ОП. Так, недостаток магния тормозит образование фосфата кальция, а дефицит марганца вызывает изменение структуры хряща и соединительной ткани. Дефицит железа связан с расширением костномозговых пространств и деформацией скелета вследствие гиперплазии костного мозга из-за неэффективного эритропоэза. Дефицит меди нарушает ковалентные поперечные связи пептидных цепей в коллагеновых и эластических волокнах соединительной ткани [1].
Таким образом, патогенез ОП носит гетерогенный, многоступенчатый характер, что предполагает комплексный подход к его терапии.
Патогенетическая роль бисфосфонатов в коррекции постменопаузального ОП
Бисфосфонаты (БФ), обладая антирезорбтивными свойствами, являются основными препаратами, используемыми для коррекции метаболических нарушений, ассоциированных с ОП [9]. Основной клеткой-мишенью для БФ выступает остеокласт. Попадая в клетку путем эндоцитоза, БФ сначала находятся во внутриклеточных везикулах, затем поступают в цитозоль и пероксисомы, где реализуют свое биохимическое действие, связываясь с фарнезилпирофосфатсинтазой, которая блокирует синтез фарнезилдифосфата, необходимого для образования геранилгеранилпирофосфата [10]. Этот путь блокирует модификацию сигнальных белков, необходимых для нормального функционирования остеокласта [11, 12]. Кроме того, БФ увеличивают выживаемость остеоцитов, что способствует уменьшению частоты их активации и предупреждению потери костной ткани у женщин в постменопаузе [13]. Анаболические эффекты БФ реализуются за счет торможения апоптоза остеобластов.
В лечении постменопаузального ПО используются следующие азотсодержащие БФ: алендроновая кислота, ризедронат в виде таблеток (кратность приема 1 р/нед.), ибандроновая кислота, доступная в виде таблеток (кратность приема 1 р/мес.) и раствора для внутривенного введения (кратность 1 раз в 3 мес.) и золедроновая кислота для внутривенного введения (кратность 1 р/год).
Эффективность всех доступных в России БФ была доказана результатами многоцентровых двойных слепых рандомизированных плацебо-контролируемых исследований (РКИ) [14–18]. Косвенные сравнения эффективности БФ в различных возрастных группах доказали свое равнозначное влияние на предупреждение повторных переломов позвонков и внепозвоночных переломов в старшей возрастной группе с переломами позвонков и выраженным снижением минеральной плотности кости (МПК) (алендронат, ибандронат, золедронат), в т. ч. у пациентов с уже имеющимся переломом бедра (золедронат). Продемонстрирована эффективность БФ в старшей возрастной группе (старше 65 лет) с переломами в анамнезе и/или со снижением МПК в шейке бедренной кости менее -2,5 (алендронат, золедронат). Интегральный анализ данных РКИ применения БФ (общее количество пациентов — 23 769) показал снижение риска переломов позвонков (-59%; ОШ 0,413, 95% ДИ 0,279–0,612), переломов бедра (-29%; ОШ 0,711, 95% ДИ 0,616–0,820), внепозвоночных переломов (-21%; ОШ 0,796, 95% ДИ 0,739–0,858).
У больных, приверженных лечению, показано снижение риска развития клинически выраженных переломов позвонков (-32%; ОШ 0,680, 95% ДИ 0,592–0,780), переломов бедра (-38%; ОШ 0,622, 95% ДИ 0,462–0,837), внепозвоночных переломов (-19%; ОШ 0,812, 95% ДИ 0,733–0,900) по сравнению с показателями пациентов с низкой комплаентностью [19].
Место ибандроновой кислоты в терапии постменопаузального ОП
Ибандроновая кислота (ИК) является азотсодержащим БФ, который стандартизирован для профилактики и лечения постменопаузального ОП. Установлено, что ИК является одним из наиболее эффективных БФ [20]. Она достоверно увеличивает МПК, снижает риск позвоночных и внепозвоночных переломов в группе больных высокого риска при ее ежемесячном пероральном приеме внутрь или внутривенном введении 3 мг 1 раз в 3 мес. [21]. Эффективность ИК представлена в рамках международного рандомизированного исследования DIVA [21, 22]. В этом исследовании было продемонстрировано отсутствие достоверных различий в динамике МПК и маркеров костной резорбции при следующих способах применения ИК: внутривенно по 2 мг каждые 2 мес., или по 3 мг каждые 3 мес., или перорально по 2,5 мг ежедневно. Через 1 год применения ИК при контрольном исследовании пациентов в группах сравнения (инъекционное внутривенное введение по 2,0 мг каждые 2 мес., или по 3,0 мг каждые 3 мес., или пероральный прием по 2,5 мг ежедневно) показатели МПК при исследовании в поясничном отделе позвоночника увеличились соответственно на 3,8, 5,1 и 4,8%.
Представленные данные четко продемонстрировали преимущество использования ИК в виде внутривенного введения 1 раз в 2 или 3 мес. по сравнению с ежедневным пероральным приемом препарата, т. е. инъекционный путь введения ИК является эффективной альтернативой его пероральному применению.
Следующим этапом оценки результатов РКИ (MOBILE и DIVA) явилось определение годовой кумулятивной дозы ИК [22, 23], которая составила 5,5 мг с учетом абсорбции. Установлено, что эта кумулятивная доза ИК позволяет существенно снизить риск позвоночных и внепозвоночных переломов у пациентов с постменопаузальным ОП.
Следовательно, внутривенное применение ИК 1 раз в 3 мес. в дозе 3 мг для лечения постменопаузального ОП обеспечивает его накопительную годовую дозу 10,8 мг
и прирост МПК в поясничном отделе позвоночника и бедренной кости. С учетом полученных данных ИК в дозе 3 мг внутривенно ежеквартально применяется для терапии постменопаузального ОП в США и Европе.
Как уже упоминалось ранее, успех лечебных стратегий ОП основан на длительной, иногда пятилетней непрерывной лекарственной терапии, а низкая комплаентность больных обусловливает сохраняющийся риск переломов.
Определены важные условия безопасного применения пероральных форм БФ: прием препарата за 60 мин до завтрака и нахождение в вертикальном положении в течение 40 мин после его приема. Пероральные БФ абсолютно противопоказаны пациентам с заболеваниями пищевода (ахалазия или стриктура). Внутривенные БФ, при введении сразу попадающие в системный кровоток, становятся препаратами выбора для пациентов с любыми проблемами ЖКТ или непереносимостью пероральных форм. Назначение этой формы ИК пациентам с ОП повышает приверженность лечению при сохранении эффективности и безопасности. В целом основными преимуществами внутривенного введения ИК и, в частности, нового российского дженерика Резовива, являются длительные (до 3 мес.) интервалы между введениями, отсутствие связи с приемом пищи и особым положением тела после приема препарата, а также безопасность применения при патологии ЖКТ. Кроме того, выбор в пользу внутривенной формы препарата следует делать при ведении пациентов с непереносимостью, тех, кто не может соблюдать требования к приему пероральных форм (рис. 2). Возможность введения препарата 1 раз в 3 мес. обусловлена 100% биодоступностью, обеспечивающей годовую кумулятивную дозу [1, 9].
![Рис. 2. Алгоритм выбора оптимального БФ при постменопаузальном ОП [19] Рис. 2. Алгоритм выбора оптимального БФ при постменопаузальном ОП [19]](/upload/medialibrary/aed/74-2.png)
В клиническом наблюдательном исследовании Г.Н. Романов и соавт. [24] оценивали влияние внутривенной формы введения ИК на показатели МПК у 30 женщин с ОП в возрасте от 50 до 80 лет. Верификация диагноза основывалась на определении Т-критерия в исследуемых зонах согласно рекомендациям ВОЗ. Оценивали абсолютные значения МПК в поясничных позвонках (LIII–LV), в проксимальном отделе бедра и шейке бедренной кости исходно и через 1 год после лечения. После 4 инфузий ИК отмечался достоверный прирост абсолютных показателей МПК в изучаемых зонах. За весь период наблюдения не было зарегистрировано новых переломов, в то время как к началу исследования 30% пациенток имели низкоэнергетические переломы.
В последнее время большое внимание уделяется кардиоваскулярной безопасности лекарственных средств, применяемых пациентами с коморбидными сердечно-сосудистыми заболеваниями, которые выявляются у 70% пациентов с ОП. Более того, потерю МПК в настоящее время ряд авторов рассматривают как фактор риска атеросклеротического поражения коронарных артерий. В связи с доказанным риском нефатальных сердечно-сосудистых осложнений при применении стронция ранелата особое внимание уделяется кардиоваскулярной безопасности БФ. Имеются доказательства безопасности применения БФ у больных с ишемической болезнью сердца. Было показано, что БФ уменьшают кальцификацию стенок артерий, но не влияют на жесткость артерий или вероятность развития сердечно-сосудистого события. Бисфосфонаты, как правило, снижают риск сердечно-сосудистой смерти и смертность от всех причин. Следовательно, их следует рекомендовать для патогенетической терапии ОП у коморбидных пациентов с заболеваниями сердечно-сосудистой системы [25, 26].
Серьезным побочным эффектом длительного применения БФ являются атипичные субтрохантерные переломы бедренной кости [26]. Между тем это осложнение развивается крайне редко и только при длительном (5 лет и более) применении БФ. Этот факт учитывают рекомендации по рациональному применению БФ у пациентов с ОП в течение 5 лет без риска развития атипичных переломов. В дальнейшем рассматривается возможность «лекарственных каникул» у пациентов с низким риском переломов. При высоком риске переломов терапия БФ должна быть продолжена под строгим контролем маркеров костной резорбции [1, 19].
Заключение
Таким образом, применение ИК при постменопаузальном ОП в виде внутривенного введения 1 раз в 3 мес. в дозе 3 мг подтвердило свою высокую эффективность в международных рандомизированных исследованиях и наблюдательных российских исследованиях. Такой вывод основан на доказанности прироста МПК и сохраняющихся низких показателях маркеров костной резорбции в течение 12 мес. после последнего введения препарата. Важным преимуществом внутривенного введения ИК является благоприятный профиль безопасности для пациентов с поражениями ЖКТ и удобство применения, что повышает приверженность лечению. Применение ИК безопасно для коморбидных пациентов с сердечно-сосудистыми заболеваниями.
Благодарность
Редакция благодарит ООО «Фарм-Синтез» за оказанную помощь в технической редактуре настоящей публикации.
2. Лесняк О.М., Баранова И.А., Белова К.Ю. и др. Остеопороз в Российской Федерации: эпидемиология, медико-социальные и экономические аспекты проблемы (обзор литературы). Травматология и ортопедия России. 2018;24(1):155–168. [Lesnyak O.M., Baranova I.A., Belova K. Yu. et al. Osteoporosis in Russian Federation: epidemiology, socio-medical and economical aspects (review). Traumatology and Orthopedics of Russia. 2018;24(1):155–168 (in Russ.)]. DOI: 10.21823/2311-2905-2018-24-1-155-168.
3. Hernlund E., Svedbom A., Ivergård M. et al. Osteoporosis in the European Union: medical management, epidemiology and economic burden: A report prepared in collaboration with the International Osteoporosis Foundation (IOF) and the European Federation of Pharmaceutical Industry Associations (EFPIA). Arch Osteoporos. 2013;8(1–2):136. DOI: 0.1007/s11657-013-0136-1.
4. Фоминых М.П., Попов А.А., Изможерова П.В. и др. Остеопения и остеопороз дистального отдела предплечья у женщин в климактерии. Терапевтический архив. 2007;(4):40–41. [Fominykh M.P., Popov A.A., Izmozherova P.V. et al. Osteopenia and osteoporosis of the distal forearm in women in menopause Terapevticheskii arkhiv. 2007;(4):40–41 (in Russ.)].
5. Лесняк О.М., Торопцова Н.В., Евстигнеева Л.П. Остеопороз. Профилактика и амбулаторное ведение пациентов. Методические рекомендации. М.; 2013. [Lesnyak O.M., Toroptsova N.V., Evstigneeva L.P. Osteoporosis. Prophylaxis and outpatient management of patients. Methodical recommendation. M.; 2013 (in Russ.)].
6. Li L., Wang Z. Ovarian aging and osteoporosis. Adv Exp Med Biol. 2018;1086:199–215. DOI: 10.1007/978-981-13-1117-8_13.
7. Вербовой А.Ф., Пашенцева А.В., Шаронова Л.А. Остеопороз: современное состояние проблемы. Терапевтический архив. 2017;89(5):90–97. [Verbovoy A.F., Pashentseva A.V., Sharonova L.A. Osteoporosis: Current state of the art. Terapevticheskii arkhiv. 2017;89(5):90–97 (in Russ.)].
8. Kerschan-Schindl K. Prevention and rehabilitation of osteoporosis. Wien Med Wochenschr. 2016;166(1–2):22–27. DOI: 10.1007/s10354-015-0417-y.
9. Mountjoy C.R., Shrader S.P., Ragucci K.R. Compliance with osteoporosis treatment guidelines in postmenopausal women. Ann Pharmacother. 2009;43(2):242–250. DOI: 10.1345/aph.1L464.
10. Lewiecki E.M., Babbitt A.M., Piziaket V.K. et al. Adherence to and gastrointestinal tolerability of monthly oral or quarterly intravenous ibandronate therapy in women with previous intolerance to oral bisphosphonates: a 12-month, open-label, prospective evaluation. Clin Therapeutics. 2008;30(4):605–621. DOI: 10.1016/j.clinthera.2008.04.009.
11. Sheehy O., Kindundu C., Barbeau M., LeLorier J. Adherence to weekly oral bisphosphonate therapy: cost of wasted drugs and fractures. Osteoporos Int. 2009;20(9):1583–1594. DOI: 10.1007/s00198-008-0829-2.
12. Lenart B.A., Neviaser A.S., Lyman S. et al. Association of low-energy femoral fractures with prolonged bisphosphonate use: a case control study. Osteoporos Int. 2009;20(8):1353–1362. DOI: 10.1007/s00198-008-0805-x.
13. Coxon F.P., Thompson K., Rogers M.J. Recent advances in understanding the mechanism of action of bisphosphonates. Curr Opin Pharmacol. 2006;6:307–312. DOI: 10.1016/j.coph.2006.03.005.
14. Wilkes M.M., Navickis R.J., Chan W.W., Lewiecki E.M. Bisphosphonates and osteoporotic fractures: a cross-design synthesis of results among compliant/persistent postmenopausal women in clinical practice versus randomized controlled trials. Osteoporosis Int. 2010;21(4):679–688. DOI: 10.1007/s00198-009-0991-1.
15. Durchschlag E., Paschalis E.P., Zoehrer R. et al. Bone material properties in trabecular bone from human iliac crest biopsies after 3 and 5 year treatment with risendronate. J Bone Miner Res. 2006;21(10):1581–1590. DOI: 10.1359/jbmr.060701.
16. Burr D.B. Summary of ASBMR Task Force on NJ. J. Musculoskelet. Neuronal Interact. 2007;7(4):354–355.
17. Cooper A., Drake J., Brankin E. PERSIST investigators. Treatment persistent with once-monthly ibandronate and patient support vs. once-weekly alendronate: results from PERSIST study. Int. J. Clinical Practice. 2006;60:896–905.
18. Camacho P.M., Petak S.M., Binkley N. et al. American association of clinical endocrinologists/american college of endocrinology clinical practice guidelines for the diagnosis and treatment of postmenopausal osteoporosis — 2020 Update. EXECUTIVE SUMMAR. Endocr Pract. 2020;26(5):564–570. DOI: 10.4158/GL-2020-0524.
19. Белая Ж.Е., Рожинская Л.Я. Бисфосфонаты в терапии постменопаузального остеопороза. Доктор.ру. 2010;7(58):29–38. [Belaya Zh.E., Rozhinskaya L.Ya. Bisphosphonates in the treatment of postmenopausal osteoporosis. Doctor.ru. 2010;7(58):29–38 (in Russ.)].
20. Rossini M., Orsolini G., Adami S. et al. Osteoporosis treatment: why ibandronic acid? Expert Opin Pharmacother. 2013;14(10):1371–1381. DOI: 10.1517/14656566.2013.795949.
21. Delmas P.D., Adami S., Strugala C. et al. Intravenous ibandronate injections in postmenopausal women with оsteoporosis one-year results from the dosing intravenous administration study. Arthritis Rheum. 2006;54(6):1838–1846. DOI: 10.1002/art.21918.
22. Eisman J.A., Civitelli R., Adami S. et al. Efficacy and tolerability of intravenous ibandronate injections in postmenopausal osteoporosis: a 2-year results from the DIVA study. J Rheumatol. 2008:35(3):488–497.
23. Miller P.D., Recker R.R., Reginster J.Y. et al. Efficacy of monthly oral ibandronate is sustained over 5 years: the MOBILE long-term extension study. Osteoporos Int. 2012;23:1747–1756.
24. Романов Г.Н., Чернова Н.Ф. Внутривенные бисфосфонаты: роль ибандроновой кислоты в терапии остеопороза. Здравоохранение (Минск). 2014;11:37–40. [Romanov G.N., Chernova N.F. Intravenous bisphosphonates: the role of ibandronic acid in the treatment of osteoporosis. Zdravookhraneniye (Minsk). 2014;11:37–40 (in Russ.)].
25. Kranenburg G., Bartstra J.W., Weijmans M. et al. Bisphosphonates for cardiovascular risk reduction: A systematic review and meta-analysis. Atherosclerosis. 2016;252:106–115. DOI: 10.1016/j.atherosclerosis.2016.06.03.
26. Komm B.S., Morgenstern D., Yamamoto L.A., Jenkins S.N. The safety and tolerability profile of therapies for the prevention and treatment of osteoporosis in postmenopausal women. Expert Rev Clin Pharmacol. 2015;8(6):769–784. DOI: 10.1586/17512433.2015.1099432.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
