Легочно-сердечная гемодинамика у больных ХОБЛ и муковисцидозом по данным эходопплеркардиографии
DOI: 10.32364/2587-6821-2021-5-7-456-461
Цель исследования: оценка функционального состояния правых отделов сердца у больных хронической обструктивной болезнью легких (ХОБЛ) и больных со смешанной и легочной формами муковисцидоза (МВ) с помощью эходопплеркардиографии.
Материал и методы: у 30 взрослых больных МВ и 82 больных ХОБЛ с помощью ультразвуковых методов исследования оценивали функциональное состояние легочно-сердечной гемодинамики. Все обследуемые были разделены на 4 группы в зависимости от наличия или отсутствия клинических признаков правожелудочковой недостаточности и легочной гипертензии.
Результаты исследования: установлено, что у больных ХОБЛ нарушения диастолической функции правых отделов сердца могут носить доклинический характер и зачастую предшествуют систолическим расстройствам. Развитие гипертрофии и недостаточности правого желудочка (ПЖ) у больных МВ может наблюдаться при относительно невысоких величинах давления в легочной артерии, когда систолическое давление в ней не превышает 40–50 мм рт. ст., гипертрофия и дилатация нередко отмечались одновременно. По мере нарастания расстройств диастолической функции ПЖ у больных МВ отмечался рост сократительной активности правого предсердия одновременно с понижением соотношения скоростей наполнения левого желудочка в раннюю диастолу и в систолу предсердий.
Заключение: при тяжелом течении ХОБЛ определялись существенные нарушения структуры и функции ПЖ. Компенсаторные возможности обоих желудочков сердца истощались, изменялось межжелудочковое взаимодействие, что создавало условия для прогрессирования сердечной недостаточности и развития хронического легочного сердца. У больных МВ нарушения диастолической функции правых отделов сердца зачастую предшествуют расстройствам систолической функции, что проявляется в изменении соотношения различных фаз наполнения ПЖ. В условиях нарушения диастолической функции ПЖ происходит усиление сократительной способности правого предсердия, которая снижается лишь в фазе выраженной декомпенсации хронического легочного сердца.
Ключевые слова: хроническая обструктивная болезнь легких, муковисцидоз, эхокардиография, допплеркардиография, легочная гипертензия, правожелудочковая недостаточность, диастолическая функция.
Для цитирования: Титова О.Н., Кузубова Н.А., Александров А.Л., Перлей В.Е., Гичкин А.Ю. Легочно-сердечная гемодинамика у больных ХОБЛ и муковисцидозом по данным эходопплеркардиографии. РМЖ. Медицинское обозрение. 2021;5(7):456-461. DOI: 10.32364/2587-6821-2021-5-7-456-461.
O.N. Titova, N.A. Kuzubova, A.L. Aleksandrov, V.E. Perley, A.Yu. Gichkin
I.P. Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
Aim: to assess the functionality of the right heart in patients with chronic obstructive pulmonary disease (COPD), mixed cystic fibrosis (CF), and cystic fibrosis lung disease by Doppler echocardiography.
Patients and Methods: 30 adults with CF and 82 adults with COPD underwent ultrasonography to evaluate pulmonary and cardiac hemodynamics. All patients were divided into four groups based on the presence/absence of clinical signs of right ventricular failure and pulmonary hypertension.
Results: in COPD, diastolic dysfunction of the right heart can be subclinical preceding systolic impairment. Right ventricular hypertrophy and failure in CF occur in relatively low pulmonary artery pressure. Thus, in systolic pulmonary pressure less than 40–50 mm Hg, hypertrophy and dilation were concomitant. As the diastolic function of the right ventricle worsens, right atrial contractility increases while the ratio of left ventricular filling velocities during the early atrial diastole and systole reduces in patients with CF.
Conclusion: in severe COPD, significant structural and functional impairments of the right ventricle occur. Compensatory potentialities of the right and left ventricles exhaust, thereby providing the conditions for the progression of heart failure and the development of the chronic pulmonary heart. In CF, diastolic dysfunction of the right heart often precedes systolic dysfunction, as illustrated by changes in the proportion of various filling phases of the right ventricle. In right ventricular diastolic dysfunction, an increase in right atrial contractility occurs that reduces only in severe decompensation of the chronic pulmonary heart.
Keywords: chronic obstructive pulmonary disease, cystic fibros is, echocardiography, Doppler cardiography, pulmonary hypertension, right ventricular failure, diastolic function.
For citation: Titova O.N., Kuzubova N.A., Aleksandrov A.L. et al. Pulmonary and cardiac hemodynamics in COPD and cystic fibrosis by Doppler echocardiography. Russian Medical Inquiry. 2021;5(7):456–461 (in Russ.). DOI: 10.32364/2587-6821-2021-5-7-456-461.
Введение
По данным Всемирной организации здравоохранения, на 2019 г. хроническая обструктивная болезнь легких (ХОБЛ) стала причиной смерти 2,32 млн человек [1]. Хроническое воспаление, прогрессирующая эмфизема, легочная гиперинфляция приводят у больных ХОБЛ к повышению постнагрузки на правый желудочек (ПЖ) за счет увеличения легочного сосудистого сопротивления и к умеренному росту систолического давления в легочной артерии (ЛА), что с течением времени вызывает структурные изменения правых отделов сердца и правожелудочковую недостаточность [2–4]. Болезнь постепенно и неуклонно прогрессирует, что приводит к инвалидизации больных [1]. Основными причинами смерти при ХОБЛ являются прогрессирующая дыхательная и сердечная (правожелудочковая) недостаточность.
Муковисцидоз (МВ) является системным наследственным заболеванием, которое регистрируется с частотой 1:3000–1:6000 новорожденных. Прогрессирование дыхательной недостаточности и сопутствующая гипоксия у больных МВ в 70% случаев сочетаются с нарушениями легочно-сердечной гемодинамики, вплоть до развития хронического легочного сердца [5–7]. Одной из основных причин развития недостаточности ПЖ у больных МВ некоторые считают легочную гипертензию (ЛГ), приводящую к перегрузке правых отделов сердца, однако механизмы декомпенсации сердечной деятельности остаются предметом дискуссий, особенно в случае незначительного повышения давления в ЛА или отсутствия ЛГ [8, 9].
Следует заметить, что диагностика ранних признаков недостаточности кровообращения у больных с хронической легочной патологией непроста, особенно на ранних этапах заболевания, т. к. гемодинамические нарушения маскируются сопутствующей дыхательной недостаточностью.
Цель исследования — эходопплеркардиографическая оценка функционального состояния правых отделов сердца у ХОБЛ и больных со смешанной и легочной формами МВ.
Материал и методы
Всего обследовано 112 больных. Из них 82 были пациенты с ХОБЛ (все мужчины, средний возраст — 54±1,6 года) III стадии по GOLD (The Global Initiative for Chronic Obstructive Lung Disease – Глобальная инициатива по хронической обструктивной болезни легких), смешанный эмфизематозно-бронхитический фенотип, в период ремиссии заболевания. Все пациенты в качестве базисной терапии получали олодатерол + тиотропия бромид 2,5 мкг + 2,5 мкг (Спиолто® Респимат®) по 2 ингаляции 1 р/сут. Остальные 30 пациентов страдали МВ, смешанной формой, преимущественно среднетяжелого течения (19 мужчин и 29 женщин, средний возраст — 28±1,1 года). Контрольную группу составили 40 здоровых добровольцев в возрасте от 18 до 59 лет (средний возраст — 41±3,1 года). В зависимости от наличия ЛГ и признаков недостаточности правых отделов сердца пациентов разделили на 4 группы: в 1-ю группу включили 11 больных МВ с ЛГ в покое (систолическое давление в легочной артерии [СДЛА] выше 30 мм рт. ст.) без признаков недостаточности правых отделов сердца; во 2-ю группу включили 47 больных ХОБЛ с ЛГ в покое (СДЛА выше 30 мм рт. ст.) без признаков недостаточности правых отделов сердца; 3-ю группу составили 19 больных МВ с ЛГ и признаками недостаточности ПЖ; в 4-ю группу вошли 35 мужчин с тяжелым течением ХОБЛ, сопровождающимся ЛГ и правожелудочковой недостаточностью.
Эходопплеркардиографическое (ЭхоДКГ) исследование легочно-сердечной гемодинамики проводили на ультразвуковой диагностической системе VIVID 7 Dimension (GE, США) по стандартной методике [10]. Рассчитывали показатели, характеризующие функциональное состояние правых отделов сердца: конечно-систолический размер (КСР) и конечно-диастолический размер (КДР) ПЖ, толщину миокарда передней стенки ПЖ в систолу и толщину миокарда передней стенки ПЖ в диастолу (ТМ ПСПЖд), скорость сокращения миокарда и скорость расслабления миокарда ПЖ, фракцию систолического утолщения миокарда передней стенки ПЖ (ФСУт ПСПЖ), фракцию систолического уменьшения площади правого предсердия (ФСУ ПП), СДЛА по градиенту трикуспидальной регургитации с учетом диаметра нижней полой вены и ее коллабирования при дыхании для оценки правопредсердного давления. Систолическую функцию ПЖ оценивали по амплитуде движения кольца трикуспидального клапана, а диастолическую функцию ПЖ — по спектрограммам транстрикуспидального кровотока. При проведении ЭхоДКГ оценивали Е/А — соотношение скоростей раннего и предсердного диастолического потока и E/e’ – соотношение максимальной скорости трансмитрального кровотока и пиковой скорости расслабления миокарда в фазу раннего наполнения желудочков. Использование тканевой допплерографии позволяло определить соответствующие скорости сокращения базального сегмента передней стенки ПЖ.
Для исследования механики дыхания выполняли спирометрию и бодиплетизмографию по стандартным методикам на установке Master Screen (E. Jaeger, Германия). Выполнили оценку следующих показателей легочной вентиляции: форсированная жизненная емкость легких (ФЖЕЛ), объем форсированного выдоха за 1 секунду (ОФВ1), индекс Генслера (ОФВ1/ФЖЕЛ), общая емкость легких и остаточный объем легких. Статистическая обработка материала выполнялась стандартными методами с помощью пакета Statistica for Windows 6.0. Различия считали статистически значимыми при р<0,05.
Результаты и обсуждение
Сердечно-сосудистые заболевания считаются одной из самых важных сопутствующих патологий при ХОБЛ, поскольку риск их развития в 2–3 раза превышает таковой у пациентов без ХОБЛ, с поправками на курение и возраст [11]. Нарушения гемодинамики малого круга кровообращения у больных с хронической патологией легких проявляются в виде повышения легочного сосудистого сопротивления и ЛГ 1-й степени, что впоследствии может привести к структурным изменениям правых камер и правожелудочковой недостаточности.
Как следует из таблицы 1, у больных ХОБЛ отмечалась тенденция к более выраженным изменениям эхокардиографических показателей правых отделов сердца по сравнению с показателями у больных МВ. Так, расчетное СДЛА у больных ХОБЛ во 2-й группе было достоверно выше, а КДР ПЖ — больше, чем у пациентов из 1-й группы, составив 44,9±3,4 мм рт. ст. и 3,26±0,26 см против 36,3±1,73 мм рт. ст. и 2,96±0,09 см соответственно (р<0,01). Наметившиеся проявления диастолической дисфункции миокарда также оказались более выраженными у больных ХОБЛ, чем у пациентов с МВ. Так, показатели Е/А ПЖ и Е/е’ ПЖ, составили 0,70±0,09 и 6,9±1,13 у пациентов из 2-й группы против 0,95±0,05 и 5,7±1,11 у пациентов из 1-й группы соответственно (р<0,01). Следует отметить, что ФСУ ПП у пациентов с ХОБЛ по сравнению с показателем у здоровых добровольцев проявляла тенденцию к статистически недостоверному снижению, а у больных МВ, напротив, к повышению. Амплитуда движения кольца трикуспидального клапана у больных МВ мало отличалась от контрольного значения, а у пациентов с ХОБЛ была существенно ниже.
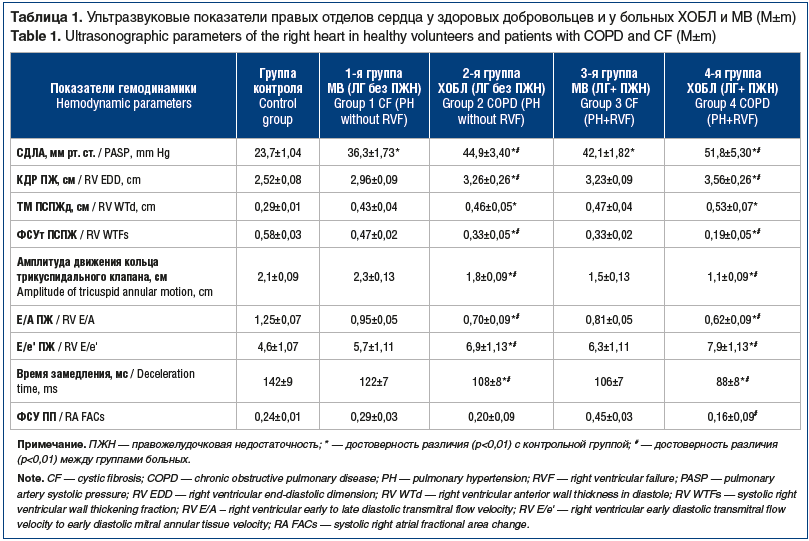
Как следует из таблицы 1, у больных ХОБЛ с сочетанием ЛГ и недостаточности ПЖ отмечались выраженные нарушения правожелудочковой гемодинамики, у пациентов с МВ эти нарушения выявлялись в меньшей степени. Так, расчетное СДЛА у больных ХОБЛ в 4-й группе было существенно повышено относительно нормальных значений, составив 51,8±5,3 мм рт. ст., у пациентов в 3-й группе СДЛА повышалось достоверно менее выраженно — до 42,1±1,82 мм рт. ст. (р<0,01 по сравнению с показателем у пациентов из 4-й группы). Сходные закономерности выявлены и относительно размеров ПЖ.
Наметившиеся у пациентов в первых двух группах проявления диастолической дисфункции миокарда были более выраженными у пациентов с признаками правожелудочковой недостаточности — в 3-й и 4-й группах, причем большая выраженность отмечалась у больных ХОБЛ, чем у пациентов с МВ. Так, у больных из 4-й и 3-й групп показатели Е/А ПЖ и Е/е’ ПЖ составили 0,62±0,09 и 7,9±1,13 против 0,81±0,05 и 6,3±1,11 соответственно (р<0,01).
ФСУ ПП у пациентов из 4-й группы по сравнению с контрольной группой оказалась существенно снижена (0,16±0,09 и 0,24±0,01 соответственно), а у больных из 3-й группы, напротив, повышена до 0,45±0,03. Амплитуда движения кольца ТК у больных из 4-й группы также снизилась в существенно большей степени, чем у пациентов из 3-й группы.
Таким образом, если у больных без существенной гипоксемии, гиперкапнии и хронической интоксикации резервные возможности миокарда ПЖ вполне достаточны, то у лиц с ЛГ, нарушенным газовым составом крови и хроническим воспалительным процессом в легочной ткани ПЖ испытывает повышенную нагрузку, а после исчерпания функциональных резервов происходит формирование хронического легочного сердца [12, 13]. Наблюдались и нарушения функции левого желудочка (ЛЖ) за счет десинхронии межпредсердной перегородки, которая может при этом становиться функционально как бы частью гипертрофированного и дилатированного ПЖ, что, в свою очередь, снижает фракцию выброса ЛЖ и также приводит к формированию левожелудочковой недостаточности [14].
Представленные данные свидетельствуют о том, что диастолическая функция ПЖ обладает меньшими компенсаторными возможностями, в отличие от систолической функции, и при неблагоприятных условиях нарушается в первую очередь [15, 16]. Такое нарушение процессов расслабления ПЖ, проявляющееся в виде более медленного снижения давления в нем, приводит к уменьшению максимальной скорости раннего диастолического наполнения и вызывает не только увеличение длительности, но и уменьшение скорости замедления кровотока в раннюю диастолу у пациентов с хронической патологией легких.
Динамика максимальных скоростей кровотока в фазу раннего и позднего диастолического наполнения E/A ПЖ свидетельствует о состоянии пред- и постнагрузки и позволяет судить об эластичности миокарда, т. е. о его жесткости и растяжимости, от которых зависит величина пассивного наполнения желудочка. Кроме того, изменение временных показателей в фазу быстрого наполнения желудочков позволяет определить скорость сокращения наружной косой и внутренней прямой мышц желудочка, что обеспечивает дальнейшее изменение формы и объема его полости, истончение стенки и степени развития присасывающей силы [17, 18]. К неблагоприятным факторам, вызывающим нарушение диастолической функции в виде замедления релаксации, увеличения жесткости стенок ПЖ, следует отнести хроническую гипоксемию, гиперкапнию, ацидоз, в анамнезе — длительную хроническую интоксикацию у больных ХОБЛ.
По-видимому, можно согласиться с авторами, считающими, что функциональное состояние ПЖ связано в большей степени с выраженностью артериальной гипоксемии и гиперкапнии, характером и длительностью инфекционно-токсических и аутоиммунных воздействий на миокард, а не непосредственно с уровнем давления в МКК [19, 20]. Нормальной компенсаторной реакцией на возрастание постнагрузки на ПЖ являлась тенденция к увеличению некоторых фракционных и скоростных показателей миокарда, сохранности амплитуды движения кольца трикуспидального клапана.
При хронической сердечной недостаточности выделяют два классических типа: систолический диагностируют при фракции выброса ЛЖ менее 45%, диастолический – при фракции выброса ЛЖ более 45%, наличии диастолической дисфункции ЛЖ и клинических признаков хронической сердечной недостаточности. Вероятно, у больных ХОБЛ может первоначально наблюдаться субклиническое снижение сократимости сердца с развитием диастолической дисфункции и относительно сохраненной фракцией изгнания, что следует учитывать при их терапевтическом ведении.
Результаты проведенного исследования показывают, что развитие гипертрофии и недостаточности ПЖ может наблюдаться при относительно невысоких величинах давления в ЛА, когда СДЛА не превышает 40–50 мм рт. ст., гипертрофия и дилатация нередко отмечались одновременно.
Еще одним актуальным вопросом для пациентов с ХОБЛ и сердечно-сосудистой патологией являются эффективность и безопасность использования комбинаций длительно действующих бронхолитиков. Объединенный анализ нескольких крупных исследований показал, что добавление олодатерола к тиотропию не связано с повышением риска сердечно-сосудистых нежелательных явлений, таким образом, комбинация тиотропия/олодатерола является подходящим вариантом терапии даже при наличии сердечно-сосудистых факторов риска [21]. Также в ретроспективном анализе применения комбинации тиотропия/олодатерола по сравнению с монотерапией в долгосрочной перспективе не наблюдалось увеличения ЧСС и систолического и диастолического АД [22]. Таким образом, терапия комбинацией тиотропия/олодатерола является эффективным и безопасным вариантом терапии для пациентов с ХОБЛ и сопутствующей сердечно-сосудистой патологией.
Заключение
Таким образом, правое предсердие у больных МВ способно компенсировать нарушения функции ПЖ. В условиях нарушения диастолической функции ПЖ происходит усиление сократительной способности правого предсердия, которое снижается лишь в фазе выраженной декомпенсации хронического легочного сердца. У больных МВ нарушения диастолической функции правых отделов сердца предшествуют расстройствам систолической функции. У пациентов с ХОБЛ в обеих группах определялись более существенные нарушения структуры и функции ПЖ. Компенсаторные возможности ПЖ и ЛЖ истощались, изменялось межжелудочковое взаимодействие, что создавало условия для прогрессирования сердечной недостаточности и развития хронического легочного сердца.
Благодарность
Редакция благодарит компанию «Берингер Ингельхайм» за оказанную помощь в технической редактуре настоящей публикации.
Acknowledgements
The technical edition is supported by Boehringer Ingelheim.
Сведения об авторах:
Титова Ольга Николаевна — д.м.н., профессор, директор НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0003-4678-3904.
Кузубова Наталия Анатольевна — д.м.н., заместитель директора НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0002-1166-9717.
Александров Альберт Леонидович — д.м.н., профессор, руководитель отдела НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0002-9246-5256.
Перлей Виталий Евгеньевич — д.м.н., профессор, ведущий научный сотрудник НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0001-6292-3888.
Гичкин Алексей Юрьевич — к.м.н., врач функциональной диагностики НИИ хирургии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0003-1127-0041.
Контактная информация: Кузубова Наталия Анатольевна, e-mail: kuzubova@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах и методах.
Конфликт интересов отсутствует.
Статья поступила 05.07.2021.
Поступила после рецензирования 28.07.2021.
Принята в печать 20.08.2021.
About the authors:
Olga N. Titova — Dr. Sc. (Med.), Professor, Director of the Research Institute of Pulmonology, I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0003-4678-3904.
Nataliya A. Kuzubova — Dr. Sc. (Med.), Deputy Director of the Research Institute of Pulmonology, I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0002-1166-9717.
Albert L. Aleksandrov — Dr. Sc. (Med.), Professor, Head of Division of the Research Institute of Pulmonology, I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0002-9246-5256.
Vitaliy E. Perlei — Dr. Sc. (Med.), Professor, leading researcher of the Research Institute of Pulmonology, I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0001-6292-3888.
Aleksey Yu. Gichkin — C. Sc. (Med.), functional diagnostician of the Research Institute of Pulmonology, I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0003-1127-0041.
Contact information: Nataliya A. Kuzubova, e-mail: kuzubova@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 05.07.2021.
Revised 28.07.2021.
Accepted 20.08.2021.
2. Горелик И.Л., Калманова Е.Н., Айсанов З.Р., Чучалин А.Г. Диагностика ранних признаков ремоделирования сердца у пациентов с ХОБЛ. Практическая медицина. 2011;3(51):72–77.
3. Кузубова Н.А. Патофизиологические механизмы формирования хронической обструктивной болезни легких (клинико-экспериментальное исследование). Дис. … докт. мед. наук. СПб.; 2009.
4. Меньшикова И.Г., Лоскутова Н.В., Сундукова Е.А., Квасникова Ю.В. Предикторы прогрессирования недостаточности кровообращения у больных хронической обструктивной болезнью легких, осложненной хроническим легочным сердцем. Дальневосточный медицинский журнал. 2012;2:21–24.
5. Ziegler B., Perin C., Casarotto F.C. et al. Pulmonary hypertension as estimated by Doppler echocardiography in adolescent and adult patients with cystic fibrosis and their relationship with clinical, lung function and sleep findings. Clin Respir J. 2018;12(2):754–761. DOI: 10.1111/crj.12590.
6. Tonelli A.R., Fernandez-Bussy S., Lodhi S. et al. Prevalence of pulmonary hypertension in end-stage cystic fibrosis and correlation with survival. J Heart Lung Transplant. 2010;29(8):865–872. DOI: 10.1016/j.healun.2010.04.006.
7. Podolska E., Pogorzelski A., Woś H. Echokardiograficzna ocena wystepowania serca płucnego u chorych z mukowiscydoza [Echocardiographic assessment of cor pulmonale in patients with cystic fibrosis]. Wiad Lek. 2006;59(3–4):208–213.
8. Burghuber O.C., Salzer-Muhar U., Bergmann H., Götz M. Right ventricular performance and pulmonary haemodynamics in adolescent and adult patients with cystic fibrosis. Eur J Pediatr. 1988;148(3):187–192. DOI: 10.1007/BF00441398.
9. Belle-van Meerkerk G., Cramer M.J., Kwakkel-van Erp J.M. et al. Pulmonary hypertension is a mild comorbidity in end-stage cystic fibrosis patients. J Heart Lung Transplant. 2013;32(6):609–614. DOI: 10.1016/j.healun.2013.03.006.
10. Lang R.M., Badano L.P., Mor-Avi V. et al. Recommendations for cardiac chamber quantification by echocardiography in adults: an update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. Eur Heart J Cardiovasc Imaging. 2015;16(3):233–270. DOI: 10.1093/ehjci/jev014.
11. Chen W., Thomas J., Sadatsafavi M., FitzGerald J.M. Risk of cardiovascular comorbidity in patients with chronic obstructive pulmonary disease: a systematic review and meta-analysis. Lancet Respir Med. 2015;3(8):631–639. DOI: 10.1016/S2213-2600(15)00241-6.
12. Хроническая обструктивная болезнь легких: монография. Под ред. проф. А. Г. Чучалина. М.: Атмосфера; 2011.
13. Alter P., Watz H., Kahnert K. et al. Airway obstruction and lung hyperinflation in COPD are linked to an impaired left ventricular diastolic filling. Respir Med. 2018;137:14–22. DOI: 10.1016/j.rmed.2018.02.011.
14. Badano L.P., Ginghina C., Easaw J. et al. Right ventricle in pulmonary arterial hypertension: haemodynamics, structural changes, imaging, and proposal of a study protocol aimed to assess remodelling and treatment effects. Eur J Echocardiogr. 2010;11(1):27–37. DOI: 10.1093/ejechocard/jep152.
15. Fenster B.E., Holm K.E., Weinberger H.D. et al. Right ventricular diastolic function and exercise capacity in COPD. Respir Med. 2015;109(10):1287–1292. DOI: 10.1016/j.rmed.2015.09.003.
16. Güder G, Störk S. COPD and heart failure: differential diagnosis and comorbidity. Herz. 2019;44(6):502–508. DOI: 10.1007/s00059-019-4814-7.
17. Howard L.S., Grapsa J., Dawson D. et al. Echocardiographic assessment of pulmonary hypertension: standard operating procedure. Eur Respir Rev. 2012;21(125):239–248. DOI: 10.1183/09059180.00003912.
18. Meluzín J., Spinarová L., Bakala J. et al. Pulsed Doppler tissue imaging of the velocity of tricuspid annular systolic motion; a new, rapid, and non-invasive method of evaluating right ventricular systolic function. Eur Heart J. 2001;22(4):340–348. DOI: 10.1053/euhj.2000.2296.
19. Mocan M., Mocan Hognogi L.D., Anton F.P. et al. Biomarkers of Inflammation in Left Ventricular Diastolic Dysfunction. Dis Markers. 2019;2019:7583690. DOI: 10.1155/2019/7583690.
20. Vonk Noordegraaf A., Galiè N. The role of the right ventricle in pulmonary arterial hypertension. Eur Respir Rev. 2011;20(122):243–253. DOI: 10.1183/09059180.00006511.
21. Ferguson G.T., Buhl R., Bothner U. et al. Safety of tiotropium/olodaterol in chronic obstructive pulmonary disease: pooled analysis of three large, 52-week, randomized clinical trials. Respir Med. 2018;143:67–73. DOI: 10.1016/j.rmed.2018.08.012.
22. Andreas S., McGarvey L., Bothner U. et al. Absence of Adverse Effects of Tiotropium/Olodaterol Compared with the Monocomponents on Long-Term Heart Rate and Blood Pressure in Patients with Moderate-to-Very-Severe COPD. Int J Chron Obstruct Pulmon Dis. 2020;15:1935–1944. DOI: 10.2147/COPD.S246348.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
