Формирование крупных «белых тромбов» в нижней полой вене и правом предсердии у пилота ближнемагистральных самолетов
В статье представлен первый документально зафиксированный случай остро сформировавшегося большого подвижного «белого тромба» в системе нижней полой вены (НПВ), с подвижными элементами в правом предсердии (ПП) у пилота турбовинтового самолета. После проведенного тромболизиса при ЭхоКГ и МРТ-исследованиях регистрировался «лизис» подвижных структур в ПП
(в действительности — его дефрагментация с массивной тромбоэмболией легочной артерии) и внезапной гибелью пациента на 4-й день с момента выполнения тромболизиса. В данном случае нельзя исключить наследственный (либо приобретенный) тромбофилический компонент процесса тромбообразования, в т. ч. как следствие антифосфолипидного синдрома, гипергомоцистеинемии (ГГЦ). Последние следует рассматривать как предрасполагающие факторы, которые чаще реализуются под влиянием внешних факторов (вибрация, гиподинамия, гипотермия, гиповолемия) в виде гиперкоагуляционного синдрома. Не исключая вероятность тромбофилии, возможно предположить, что, с учетом информации о механизмах образования «белых тромбов», длительная гирудотерапия, имевшая место у пациента, могла спровоцировать появление рыхлых «белых тромбов» в системе НПВ и в ПП (так называемая гирудин-индуцированная тромбоцитопатия) и повлиять на исход заболевания.
Ключевые слова: тромбоэмболия легочной артерии, гирудин, авиаперелет, эхокардиография, гепарин-индуцированная тромбоцитопатия, гиперкоагуляционный синдром, факторы риска, белые тромбы, тромболизис, тромбоз.
Для цитирования: Цоколов А.В., Ильин И.Б., Крылов В.А., Трофимец А.И., Колесова И.А., Каленицкая А.О. Формирование крупных «белых тромбов» в нижней полой вене и правом предсердии у пилота ближнемагистральных самолетов. РМЖ. Медицинское обозрение. 2019;27(8(II)):108-112.
Large white thrombi formation in the inferior vena cava and right atrium in a pilot of short-haul aircraft
A.B. Tsokolov, I.B. Ilyin, V.A. Krylov, A.I. Trofimets, I.A. Kolesova, A.O. Kalenitskaya
Naval Clinical Hospital 1409, Kaliningrad
The article presents the first documented case of an acutely formed large mobile white thrombus in the vena cava inferior (VCI) system, with moving elements in the right atrium (RA) in a pilot of turboprop aircraft. After conducted thrombolysis with EchoCG and MRI studies, lysis of mobile structures was recorded (in fact, it was defragmentation with massive thromboembolism of pulmonary artery), and the sudden patient lethal outcome on the 4th day after thrombolysis. In this case, the hereditary (or — acquired) thrombophilic component of the thrombosis process cannot be excluded, including as a result of the antiphospholipid syndrome, hyperhomocysteinemia. The latter should be considered as predisposing factors that are commonly realized under the external factors influence (vibration, hypodynamia, hypothermia, hypovolemia) in the hypercoagulative syndrome form. Without excluding the thrombophili a likelihood, it is possible to assume that long-term hirudotherapy, which occurred in the patient, could provoke the appearance of loose white thrombi in the VCI system and RA (so-called hirudin-induced thrombocytopathy), and influence the outcome of the disease, taking into account information about their formation mechanisms.
Keywords: thromboembolism of pulmonary artery, hirudin, flight, echocardiography, heparin-induced thrombocytopathy, hypercoagulable syndrome, risk factors, white thrombi, thrombolysis, thrombosis.
For citation: Tsokolov A.B., Ilyin I.B., Krylov V.A. et al. Large white thrombi formation in the inferior vena cava and right atrium in a pilot of short-haul aircraft. RMJ. 2019;8(II):108–112.
В статье представлен первый документально зафиксированный случай остро сформировавшегося большого подвижного «белого тромба» в системе нижней полой вены, с подвижными элементами в правом предсердии у пилота самолета.
Актуальность
О случаях тромбообразования в системе глубоких вен нижних конечностей у пассажиров при длительных авиаперелетах к настоящему времени накоплен большой объем информации. Можно предположить, что схожие патофизиологические процессы могут происходить и у самих пилотов самолетов, возможно, даже с большей долей вероятности, однако никаких данных по этой теме нам найти не удалось.
В этой связи достаточно интересен случай остро сформировавшегося большого подвижного «белого тромба» (как это было установлено в дальнейшем при аутопсии) в системе нижней полой вены (НПВ) — в проксимальном отделе вены и на уровне бифуркации, с заполнением большей части объема правого предсердия (ПП) подвижными элементами данного тромба.
Клиническое наблюдение
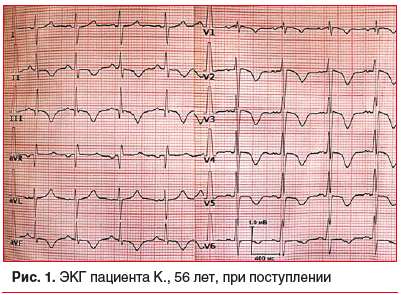
Пациент К., пилот ближнемагистрального турбовинтового самолета (возраст — 56 лет), с общим налетом более 6000 ч и налетом за месяц, предшествовавший госпитализации, порядка 100 ч (дневной налет достигал 5–7 ч), обратился в клинику с жалобами на ощущение тяжести в грудной клетке, нехватку воздуха, умеренную слабость. В течение месяца беспокоили боли в поясничном отделе позвоночника и отечность/пастозность нижних конечностей, по поводу чего самостоятельно занимался гирудотерапией. В силу определенных характерологических и профессиональных особенностей (пилоты не должны иметь серьезной патологии внутренних органов) к врачам не обращался. При поступлении на ЭКГ (рис. 1) были зарегистрированы диффузные изменения по типу «трансмуральной ишемии миокарда левого желудочка». Глубокие остроконечные зубцы «-Т» в отведениях V1–V6, III, II, aVF. ЭКГ-признак Мак-Джин — Уайта QIIISITIII — положительный. Однако, по данным Г.А. Макарова (2018), этот признак является малоспецифичным для легочной эмболии, его ценность составляет не более 10–50%. Отсутствие тахикардии как одного из наиболее важных ЭКГ-критериев тромбоэмболии легочной артерии (ТЭЛА), вероятно, обусловлено в данном случае хронической природой тромбоэмболии [1]. Предварительный диагноз: острый коронарный синдром.
При флюорографическом обследовании патологии легких выявлено не было, несмотря на жалобы на одышку, тяжесть в груди и изменения на ЭКГ.
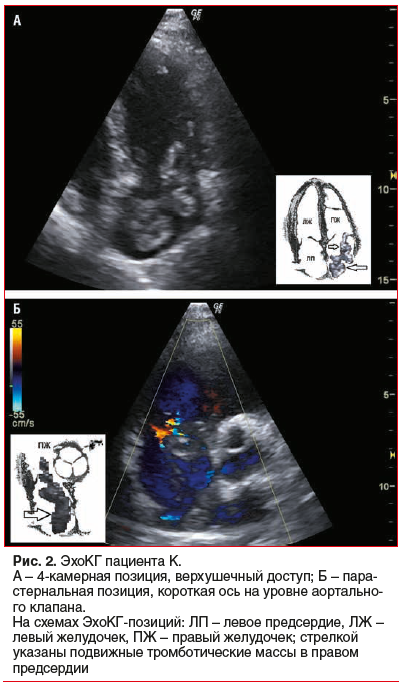
При трансторакальной ЭхоКГ было выявлено расширение полости ПП и правого желудочка (ПЖ), легочная гипертензия оказалась близкой к умеренной. В полости ПП — подвижная структура диаметром до 10 мм, плотная, пролабирующая через трехстворчатый клапан (ТК) в полость ПЖ до 2–3 см, берущая свое начало на уровне проксимального отдела НПВ. Тромб заполнял полость ПП до 50%. На рисунке 2А отмечается расширение полости ПП и ПЖ. В полости ПП — средней плотности неоднородные тромботические массы, высокоподвижные, пролабирующие через плоскость ТК в камеру ПЖ до 3 см; на рисунке 2Б в ПП в режиме цветового допплеровского картирования визуализируются тромботические массы, заполняющие полость предсердия более чем на 50%. Тромботические тяжи берут начало в проксимальном отделе НПВ. Схожая с настоящей ситуация приводится Ю.Л. Шевченко (2013) [2]. При этом при ЭхоКГ, выполненной за 6 мес. до настоящего эпизода, патологии не выявлялось.
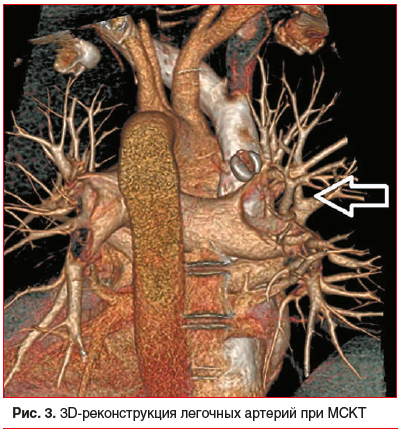
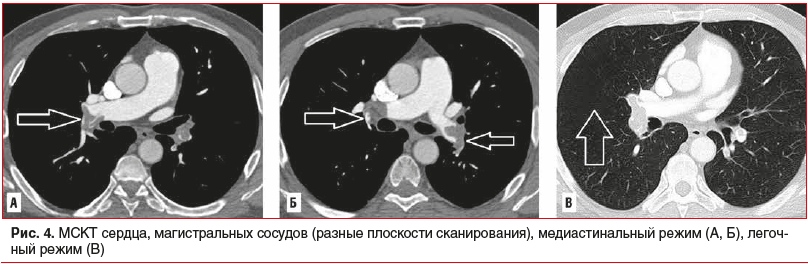
Ввиду особенностей расположения подвижных тромботических масс (НПВ-ПП) и неэффективности установки кава-фильтра (при таком расположении тромбов) было принято решение о проведении тромболизиса. В динамике при ЭхоКГ и мультиспиральной компьютерной томографии (МСКТ) регистрировался «лизис» (псевдолизис) подвижных структур в ПП, с некоторым улучшением общего состояния пациента. На рисунке 3 показана 3D-реконструкция легочных артерий при МСКТ. Отмечаются субтотальные дефекты наполнения обеих ветвей легочной артерии, левая и правая легочные артерии — с тромбами, с обеднением периферического легочного рисунка, более выраженным в правом легком (указано стрелкой). На рисунке 4 представлены поперечные срезы с массивной двусторонней эмболией. Дефектов заполнения в НПВ и верхней полой вене не выявлено; виден неоднородный (петлеобразный) внутрисосудистый тромб в дистальном сегменте правой ветви легочной артерии (рис. 4А, указано стрелкой), субтотальный дефект заполнения в дистальных сегментах обеих легочных артерий (рис. 4Б), обеднение легочного рисунка в правом легком (рис. 4В, указано стрелкой).
На 4-й день с момента выполнения тромболизиса наступила внезапная смерть больного.
При аутопсии — массивная тромбоэмболия мелких и средних ветвей легочной артерии обоих легких. Подкожные и глубокие вены нижних конечностей — без патологии, проходимы. В НПВ и ПП тромботических масс и атеросклеротических бляшек также выявлено не было.
Обсуждение
Состояние «тромбоз глубоких вен» (ТГВ) само по себе не опасно, но его осложнение в виде ТЭЛА может оказаться жизнеугрожающим. Термин «синдром экономкласса» впервые был использован Symington и Stack в 1977 г., затем Cruickshank et al. в 1988 г. [3]. В то время авторами было сделано ошибочное предположение о том, что ТГВ не наблюдается у пассажиров бизнес- и первого класса, а также у путешествующих другими видами транспорта на большие расстояния. Термин «тромбоз путешественника» в данном случае все же оказывается наиболее подходящим. К 2001 г. по всему миру было зафиксировано порядка 200 случаев тромбоза путешественника [4]. В настоящее время есть информация о том, что порядка 20% популяции населения планеты могут иметь повышенную свертываемость крови. Следовательно, в любой группе путешествующих с имеющимися факторами риска могут быть лица с риском развития ТГВ во время полета или через некоторое время после такого путешествия. Однако следует заметить, что до настоящего времени не было проведено никаких эпидемиологических исследований, которые показали бы статистически значимое увеличение числа случаев ТГВ у путешественников при отсутствии у них предшествующих факторов риска [5, 6].
Факторы, увеличивающие вероятность ТГВ, включают следующие механизмы:
замедление скорости кровотока;
изменение вязкости крови;
повреждение или патологию сосудистой стенки.
Эти факторы впервые были описаны профессором Вирховым и в настоящее время известны как «Вирховская триада». При отсутствии каких-либо проспективных исследований доказательство связи ТГВ с полетом оказывается случайным. Является ли ТГВ или ТЭЛА, которая связана по времени с авиаперелетом, результатом длительной иммобилизации у лиц с предрасположенностью к факторам риска, либо имеется причинно-следственная связь с нахождением в кабине самолета, пока неизвестно.
Представленный случай, конечно, не до конца ясен и однозначен, много информации осталось за кадром. Однако можно предположить несколько возможных вариантов формирования тромбов у данного больного. Формирование тромбов вследствие самого авиаперелета и влияния неблагоприятных факторов окружающей среды в кабине самолета с большой долей вероятности можно исключить, поскольку в настоящее время нет доказанных фактов их влияния на формирование тромбов. Но поскольку в настоящее время не представляется возможным провести точную этиологическую диагностику причины возникновения тромбоза НПВ-ПП с последующей массивной ТЭЛА «белыми тромбами», остается только делать предположения относительно механизмов формирования последних. И возможных вариантов здесь не так уж много.
В первую очередь нельзя исключить наследственный (либо приобретенный) тромбофилический компонент процесса тромбообразования, в т. ч. антифосфолипидный синдром (АФЛС), гипергомоцистеинемию (ГГЦ), как предрасполагающие факторы, которые могут реализоваться под влиянием внешних факторов в виде гиперкоагуляционного синдрома [7].
Признаки тромбофилии могут появиться у любого человека, но степень их проявления будет различной в зависимости от наличия совокупности факторов риска данной патологии. Приобретенные факторы редко становятся первопричиной тромбофилии, но при их совокупности создаются условия для формирования тромбоэмболических осложнений. К ним относятся в т. ч. обезвоживание, сопровождающееся полицитемией, заболевания аутоиммунного характера. АФЛС часто рассматривается как основной фактор риска тромбообразования, а формирование тромбов — уже как следствие длительных авиаперелетов и влияния множества неблагоприятных факторов полета, тем более на турбовинтовом самолете (вибрация, гиподинамия, гипотермия, стресс, гиповолемия). Определенное сходство с АФЛС имеет и ГГЦ как основной фактор риска артериального тромбогенеза (в артериях чаще формируются «белые тромбы»), являющаяся в т. ч. и одним из основных наследственных факторов риска [8]. Повышенный уровень гомоцистеина в крови при ГГЦ напрямую связан с состоянием свертывающей системы крови. Наряду с АФЛС ГГЦ способствует усилению агрегации тромбоцитов, непосредственно создавая условия для образования тромбов. В случае ГГЦ патологический процесс запускается накопленным в излишних количествах гомоцистеином, а в случае с АФЛС главную отрицательную роль играют антифосфолипидные антитела. Ожидаемое повышение уровня гомоцистеина в крови наблюдается у лиц с нарушением толерантности к глюкозе, при уменьшении уровня витаминов В6, В12 в пище, уровня фолиевой кислоты, при избыточном употреблении мяса (за счет повышения метионина), а также кофе, у лиц с соединительнотканной дисплазией и при остеопорозе.
И, наконец, не вполне ясна роль гирудотерапии в процессе формирования «белых тромбов» в данном случае. Здесь стоит вспомнить о таком редком состоянии, как гирудин-индуцированная тромбоцитопатия. Дело в том, что пациент достаточно долгое время (на протяжении как минимум 6 мес.) занимался самолечением пиявками и на момент поступления в стационар имел следы на местах присасывания пиявок на коже живота в виде множественных обширных подкожных гематом.
Таким образом, не исключая вероятность тромбофилии, необходимо отметить, что, с учетом информации о механизмах образования «белых тромбов», длительная гирудотерапия могла спровоцировать появление рыхлых «белых тромбов» в системе НПВ и в ПП. Есть доказанные данные о том, что антитела в организме могут образовываться и на гирудин [9, 10], и в этом случае ситуация может оказаться аналогичной той, которая наблюдается у лиц с гепарин-индуцированной тромбоцитопатией, активацией тромбоцитов, изменением свойств их мембран и последующей гиперкоагуляцией [11].
В настоящее время нет четких данных в отношении связи уровня антител к гирудину с тромботическими или геморрагическими эпизодами [9]. Однако есть указания на то, что антигирудин-иммунные комплексы (АГИК) влияют на метаболизм рекомбинантного гирудина, что предполагает необходимость контроля коагуляционных процессов у таких пациентов с выявленными АГИК. Их клиническая значимость в отношении тромбообразования и геморрагий подлежит дальнейшему изучению [10].
При этом отдаленные последствия самостоятельного использования гирудина в форме гирудотерапии, несмотря на его ожидаемые положительные эффекты (за счет предотвращения образования плотных красных тромбов), при предположительной скрытой патологии эндотелия и/или тромбоцитов, а также влияние ряда неблагоприятных факторов полета могли оказаться решающими.
И, наконец, последний вопрос, на который требуется ответить: каково место тромболизиса в исходе заболевания? 11% пациентов с фатальной ТЭЛА умирают в течение 1-го ч, 43–80% — в течение 2 ч, 85% — в течение 6 ч. В настоящее время у большинства пациентов с массивной ТЭЛА в качестве терапии выбора широко применяют тромболизис. Поскольку тромботические массы, визуализированные при ЭхоКГ и МРТ, имели достаточно плотную структуру, давность образования тромбов должна была составлять порядка 10 сут. В таком случае тромболизис ожидаемо должен быть неэффективным, тем более для подобного объема тромботических масс. По мнению R. Kieny et al. [12], величина окклюзии, равная 50%, как правило, неплохо переносится больными и поддается лечению тромболитиками, а выключение 70% легочного кровотока ведет к высокой летальности при проведении консервативного лечения.
Наличие противопоказаний также снижает значимость этого метода. В этом случае актуальным становится вопрос об оперативном лечении таких больных. Показанием к тромбэктомии являются неэффективный тромболизис или противопоказания к нему, тромбоз полостей сердца (ПЖ, ПП), наличие выраженной хронической постэмболической легочной гипертензии до последнего эпизода эмболии, тяжелые гемодинамические нарушения, требующие хирургического вмешательства. Применение хирургической тактики обосновано в ранние сроки [13–15]. Однако у 43% больных даже при правильном лечении и благополучно перенесенной ТЭЛА существует вероятность ее повторения [13]. Вероятность выздоровления больных при проведении консервативной терапии, включая активаторы фибринолиза, не превышает 12%. Выживаемость после экстренной легочной тромбоэмболэктомии варьирует в пределах от 40% до 92% [16]. Противопоказаниями к легочной эмболэктомии считаются тяжелые сопутствующие заболевания с неблагоприятным прогнозом: злокачественные новообразования при наличии отдаленных метастазов, выраженная недостаточность кровообращения, вызванная сопутствующими сердечно-сосудистыми заболеваниями, при которых успех операции сомнителен, а риск ее не оправдан.
Ретроспективный анализ возможностей эмболэктомии у больных, умерших от массивной эмболии, показал, что на успех можно рассчитывать лишь в 10–11% случаев и даже при удачно выполненной эмболэктомии не исключена возможность повторной эмболии [14, 15].
Мы считаем, что в общих чертах, с учетом клиники и лабораторно-инструментальных данных, патогенетическая картина представленного случая тромбообразования у пилота ближнемагистральных самолетов может быть представлена в следующем виде. При исходно имеющейся тромбоцитопатии (вероятно, приобретенного характера) и на фоне неблагоприятных условий работы, факторов внешней среды, а также самостоятельного использования гирудина (в форме длительной (!) гирудотерапии) в острой стадии процесса произошел блок образования фибрина и свертывания крови; ингибирование активности тромбина (с блоком свертывания фибриногена); замедление реакции активации тромбином факторов V, VIII, XIII. Позже, к 30–40-му дню от момента начала поступления гирудина в организм, мог значительно повыситься уровень антигирудиновых антител (которые, по данным литературы, остаются на высоком уровне до 90–100 сут и сохраняются в крови до 490 сут), с последующим повышением образования тромбина (что наблюдается при гепарин-индуцированной тромбоцитопении и может наблюдаться у таких пациентов с последующим увеличением содержания антигирудиновых антител) [17], в конечном итоге приведшим к гиперкоагуляции.
Диагностика в таких случаях предполагает, в первую очередь, уточнение возможной патологии свертывающей системы крови (коагулограмма, протромбиновое время, активированное частичное тромбопластиновое время, фибриноген, антитромбин III, протеин С, протеин S, фактор V и др.), с оценкой Лейденской мутации, выявление мутации гена MTHFR (метилентетрагидрофолатредуктазы), гена протромбина, волчаночного антикоагулянта, антител к кардиолипину и т. д. [7]. Помощь в диагностике может оказать и анализ крови на гомоцистеин, однако основная проблема такой диагностики — ее стоимость.
В качестве перспективной методики своевременной диагностики тромбоэмболии мелких ветвей легочной артерии у таких больных должна рассматриваться методика перфузионной сцинтиграфии легких [18, 19], в том случае, если для этого есть возможности. Особенно это актуально при поражении 4–5 и 8–9 бронхолегочных сегментов легких, анатомически являющихся «прямым продолжением» основной сосудистой магистрали. Определение клинической вероятности ТЭЛА служит основанием для дальнейшей инструментальной диагностики тромбоэмболии с целью ее подтверждения или исключения. При неопределенной (промежуточной) вероятности ТЭЛА по радиологическим критериям и для исключения данного вида осложнений может потребоваться повторное сцинтиграфическое исследование перфузии легких после курса гепаринотерапии. По данным литературы, увеличение перфузии легких на 10% и более свидетельствует в пользу тромбоэмболии мелких ветвей легочной артерии. Обязательным также остается выполнение ЭхоКГ, рентгенографии органов грудной клетки и лабораторных анализов. Таким образом, в случае появления подозрений на ТЭЛА для точной топической диагностики предпочтение следует отдавать МСКТ [20], а также, в случае необходимости, — сцинтиграфии легких. Лечение диагностированной тромбофилии на начальных стадиях патологического процесса включает использование дезагрегантов, антикоагулянтов, препаратов, способствующих укреплению сосудистой стенки, препаратов фолиевой кислоты.
Что касается методов профилактики, то соблюдение санитарно-гигиенических норм и рекомендаций по авиаперелетам остается неизменным и главным требованием на протяжении последних десятилетий.
Предложенный клинический случай — первое описание тяжелого тромбоза НПВ-ПП с последующей ТЭЛА у пилота самолета. Случай требует более детального анализа, что в дальнейшем будет способствовать осуществлению быстрой и эффективной диагностики таких состояний, а также оптимальному подбору терапии.
Следует понимать, что исход подобных состояний чаще оказывается печальным и вопросов все равно остается больше, чем ответов. Однако знание патофизиологических механизмов, в т. ч. механизмов формирования осложнений, может позволить спасти некоторых из таких пациентов. Поиск новых способов борьбы с тромбофилией, а также с осложнениями, возникающими в ходе ее лечения, равно как и с повторными эпизодами тромбоза, тромбоэмболии [12, 13], остается первостепенной задачей врачей терапевтического стационара.
Выводы
Подводя итог и обобщая имеющуюся информацию по данной проблематике, следует заключить:
Необходимо иметь настороженность в отношении вероятной тромбофилии и наиболее частой в таких случаях патологии V и II факторов свертывания крови.
Следует помнить о возможности развития парадоксальных тромбозов на 4–5-й день с момента начала гепаринотерапии, а в ряде случаев — и гирудотерапии.
Консервативная терапия ТЭЛА в большинстве случаев заканчивается гибелью пациентов; только неотложное оперативное лечение дает шанс на спасение жизни таких больных, хотя у них и сохраняется большая вероятность повторных тромбозов и тромбоэмболий.
2. Шевченко Ю.Л., Стойко Ю.М., Лыткин М.И. Основы клинической флебологии. 2-е изд. М.: Шико; 2013. [Shevchenko Yu.L., Stoyko Yu.M., Lytkin M.I. Basics of clinical phlebology. 2nd ed. M.: Shiko; 2013 (in Russ.)].
3. Cruikshank J.M., Gorlin J., Jennett B. Air travel and thrombotic episodes: the economy class syndrome. Lancet. 1988;2:497–498.
4. Bagshaw M. Air Transport Medicine Committee of the Aerospace Medical Association. Traveler`s thrombosis: a review of deep vein thrombosis associated with travel. Aviat Space Environ Med. 2001;72:848–851.
5. Hughes R.J., Hopkins R.J., Hill S. et al. Frequency of venous thromboembolism in low to moderate risk long distance air travellers: the New Zealand Air Traveller’s Thrombosis (NZATT) study. Lancet. 2003;362:2039–2044.
6. Gavish I., Brenner B. Air travel and risk of thromboembolism. Intern Emerg Med. 2011;6:113–116. DOI: 10.1007/s11739-010-0474-6.
7. Патрушев Л.И. Тромбофилические состояния и современные методы их диагностики. Русский медицинский журнал. 1998;3:7. [Patrushev L.I. Thrombophilic conditions and modern methods for their diagnosis. RMJ. 1998;3:7 (in Russ.)].
8. Шиффман Ф.Д. Патофизиология крови. М. — СПб.: БИНОМ — Невский Диалект; 2000. [Shiffman F.D. Pathophysiology of blood. M. — SPb .: “BINOM Publishing House” — “Nevsky Dialect”; 2000 (in Russ.)].
9. Song X., Huhle G., Wang L. et al. Generation of anti-hirudin antibodies in heparin-induced thrombocytopenic patients treated with r-hirudin. Circulation. 1999;100:1528–1532.
10. Eichler P., Friesen H., Lubenow N. et al. Antihirudin antibodies in patients with heparin-induced thrombocytopenia treated with lepirudin: incidence, effects on aPTT, and clinical relevance. Blood. 2000;96:2373–2378.
11. Warkentin T.E., Kelton J.G. Delayed-onset heparin-induced thrombocytopenia and thrombosis. Ann Intern Med. 2001;135:502–506.
12. Kieny R., Charpentier A., Kieny M.T. What is the place of pulmonary embolectomy today? J Cardiovasc Surg (Torino). 1991;32:549–554.
13. Бураковский В.И., Бокерия Л.А. Сердечно-сосудистая хирургия: руководство. М.: Медицина; 1989. [Burakovskiy V.I., Bockeria L.A. Cardiovascular Surgery: A Handbook. M.: Medicine; 1989 (in Russ.)].
14. Медведев А.П., Немирова С.В., Пичугин В.В. и др. Открытая эмболэктомия в лечении массивной тромбоэмболии легочной артерии. Медицинский альманах. 2013;28(4):58–60. [Medvedev A.P., Nemirova S.V., Pichugin V.V. et al. Open emblektomy in the treatment of massive thromboembolia of the pulmonary arteries. Medical Almanac. 2013;28(4):58–60 (in Russ.)].
15. Абдульянов И.В., Вагизов И.И., Омеляненко А.С. Современная стратегия лечения острой тромбоэмболии легочной артерии. Практическая медицина. 2015;88(3):35–40. [Abdulyanov I.V., Vaghizov I.I., Omelyanenko A.S. Modern treatment strategy for acute pulmonary thromboembolism. Practical medicine; 2015;88(3):35–40 (in Russ.)].
16. Небылицин Ю.С., Назарук А.А. Флебология: настоящее и будущее. Российский медико-биологический вестник имени академика И.П. Павлова. 2017;25(1):133–148. [Nebylytsin Yu.S., Nazaruk A.A. Phlebology: present and future. Russian Medical and Biological Bulletin named after academician I.P. Pavlov. 2017;25(1):133–148 (in Russ.)].
17. Warkentin T.E., Greinacher A. Heparin-induced thrombocytopenia: recognition, treatment, and prevention: the Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy. Chest. 2004;126(3 suppl):311S–337S. DOI: 10.1378/chest.126.3_suppl.311S.
18. Bajc M., Neilly J.B., Miniati M. et al. EANM guidelines for ventilation/perfusion scintigraphy: Part 1. Pulmonary imaging with ventilation/perfusion single photon emission tomography. Eur J Nucl Med Mol Imaging. 2009;36(8):1356–1370.
19. Тюкалова Л.И., Посохов И.Н., Попов С.В. Немассивная тромбоэмболия легочной артерии при постоянной электрокардиостимуляции в клинике внутренних болезней. Томск: STT, 2006:44–46. [Tyukalova L.I., Posokhov I.N., Popov S.V. Nonmassive pulmonary embolism with constant pacing in the clinic of internal diseases. Tomsk: STT. 2006:44–46 (in Russ.)].
20. Клауссен К.Д., Миллер Ш., Риссен Р. и др. Лучевая диагностика. Сердце / Пер. с англ. М.: МЕДпресс-информ; 2011. [Klaussen K.D., Miller S., Rissen R. et al. Radiodiagnosis. Heart. M.: MEDpress-inform; 2011 (in Russ.)].

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.