Интерфероновый профиль мукозального иммунитета у женщин с папилломавирусной инфекцией
Введение: папилломавирусы представляют собой группу ДНК-содержащих вирусов, относящихся к семейству Papillomaviridaе, которые вызывают патологические состояния, проявляющиеся воспалением, экзофитными образованиями, онкогенезом, репродуктивными и перинатальными нарушениями. Состояние иммунной системы является значимым фактором, которое определяет тяжесть и продолжительность воспалительных заболеваний, особенности течения латентных вирусных и eнфекций, в том числе и папилломавирусной инфекции (ПВИ). Действие иммунной системы организма направлено на предотвращение персистирования, реактивации и развития клинической симптоматики ПВИ. Клеточный иммунный ответ реализуется под контролем системы интерферонов (ИФН). На сегодняшний день отсутствуют комплексные исследования системы ИФН I, II, III типов в цервикальной слизи у пациенток с ПВИ в ассоциациях с герпетической и хламидийной инфекциями.
Цель исследования: провести сравнительный анализ интерферонового профиля мукозального иммунитета у пациенток с ПВИ в ассоциациях с герпетической и хламидийной инфекциями.
Материал и методы: в исследование было включено 149 пациенток в возрасте от 25 до 44 лет. Пациентки были разделены на 4 группы: I группа — пациентки только с ПВИ (n=21), II группа — с ПВИ и герпетической вирусной инфекцией (ГВИ) (n=47), III группа — с ПВИ и хламидийной инфекцией (n=39) и IV группа — контрольная (n=30). Комплексное клинико-лабораторное исследование проводили в амбулаторных условиях по единой программе, включающей клинико-функциональное, биохимическое и иммунологическое обследование с целью детализации патофизиологических механизмов ПВИ в урогенитальном тракте. Определение в цервикальной слизи уровня ИФН: ИНФ-β, ИФН-γ, ИФН-λ1 (ИЛ-29), ИФН-λ3 (ИЛ-28B) — проведено методом твердофазного иммуноферментного анализа.
Результаты исследования: во всех исследуемых группах установлены закономерности в виде дефицита ИФН-λ3 и ИФН-γ. При ПВИ ведущим нарушением был дефицит ИФН-γ. Во II группе при ассоциации ПВИ и ГВИ — дефицит ИФН-λ3. В III группе у пациенток с ассоциацией вирусной и бактериальной инфекций установлен выраженный дефицит ИФН-β.
Заключение: выявленные закономерности демонстрируют значимую роль дефицита интерферонового звена иммунного ответа в патогенезе ПВИ как в моноварианте, так и в ассоциациях с ГПИ и хламидийной инфекцией. Выявленные нарушения на уровне мукозального иммунитета могут слуЦ 6ить обоснованием для назначения иммунотропной терапии при данных инфекциях.
Ключевые слова: вирус папилломы человека, герпетическая инфекция, хламидийная инфекция, интерфероны, иммунная система, цервикальная слизь, мукозальный иммунитет.
Для цитирования: Маркелова Е.В., Тулупова М.С., Невежкина Т.А., Матюшкина Л.С., Черникова М.А., Кныш С.В. Интерфероновый профиль мукозального иммунитета у женщин с папилломавирусной инфекцией. РМЖ. Медицинское обозрение. 2022;6(2):67-71. DOI: 10.32364/2587-6821-2022-6-2-67-71.
E.V. Markelova1, M.S. Tulupova2, T.A. Nevezhkina1, L.S. Matyushkina1, M.A. Chernikova1,3, S.V. Knysh1
1Pacific State Medical University, Vladivostok, Russian Federation
2LLC "Paracelsus", Vladivostok, Russian Federation
3LLC "Asklepiy", Vladivostok, Russian Federation
Papillomaviruses are a group of DNA viruses belonging to the Papillomavirida family. These viruses provoke pathological conditions manifesting with inflammation, exophytic masses, carcinogenesis, reproductive and perinatal disorders. Immune status is an essential factor de-termining the severity and duration of inflammatory diseases, the course of latent viral infections, including papillomavirus infection (PVI). The human immune system prevents the persistence, reactivation, and development of PVI clinical presentations. The cellular immune response is realized under the control of interferons (IFNs). Today, no complex studies on type 1, 2, or 3 IFNs in the cervical mucus of women with PVI associated with herpesvirus and chlamydia infec-tions are available.
Aim: to compare IFN profile of mucosal immunity in women with PVI associated with herpesvirus and chlamydia infections.
Patients and Methods: this study enrolled 149 women aged 25–44. Women were divided into four groups. Group 1 included women with PVI only (n=21). Group 2 included women with PVI and herpesvirus infection (n=47). Group 3 included women with PVI and chlamydia infec-tions (n=39). Group 4 included controls (n=30). Complex outpatient clinical laboratory examina-tion included clinical functional, biochemical, and immunological tests to detail pathophysiolog-ical mechanisms of urogenital PVIs. IFN (IFN-β, IFN-γ, IFN-λ1/IL-29, IFN-λ3/IL-28B) levels in the cervical mucus were measured by ELISA.
Results: in all groups, IFN-λ3 and IFN-γ deficiencies were detected. In PVI, IFN-γ deficiency prevailed. In PVI associated with herpesvirus infection, IFN-λ3 deficiency prevailed. In PVI associated with chlamydia infection, a severe IFN-β deficiency was revealed.
Conclusion: these patterns demonstrate a relevant role of the interferon arm of the im-mune response in the pathogenesis of isolated PVI and PVI associated with herpesvirus and chlamydia infections. These alterations in mucosal immunity support the prescription of immu-notherapy for these infections.
Keywords: human papillomavirus, herpesvirus infection, chlamydia infection, interferons, immune system, cervical mucus, mucosal immunity.
For citation: Markelova E.V., Tulupova M.S., Nevezhkina T.A. et al. Interferon profile of the mucosal immunity in women with papillomavirus infection. Russian Medical Inquiry. 2022;6(2):67–71 (in Russ.). DOI: 10.32364/2587-6821-2022-6-2-67-71.
Введение
Папилломавирусная инфекция (ПВИ) — инфекционное заболевание человека, вызываемое вирусами папилломы человека (ВПЧ). ВПЧ — большая и гетерогенная группа вирусов, являющихся инициирующим фактором для формирования ряда патологических процессов шейки матки и кожи — цервикальных интраэпителиальных неоплазий, рака шейки матки, кондиломатоза; кроме этого, персистенция ВПЧ способствует длительному, вялотекущему воспалительному процессу в органах малого таза с дальнейшим развитием репродуктивных и перинатальных нарушений — бесплодия, невынашивания беременности, фетоплацентарной недостаточности, преэклампии и многих других [1]. До настоящего времени остается неясным, почему в одних случаях происходит спонтанная элиминация ВПЧ, а в других наблюдается длительная персистенция вируса и его реактивация.
Особенностью ВПЧ является то, что, находясь внутриэпителиально, он не распознается антигенпрезентирующими клетками. Интеграция и репликация вируса происходят в клетках, которые будут вскоре отторгнуты. В связи с этим при попадании в организм человека нет специфических признаков виремии, цитолиза и воспаления [2]. Одним из первых механизмов защиты репродуктивного тракта женщины является врожденный мукозальный иммунитет, который, в свою очередь, включает патогенетические механизмы против ВПЧ, усиливая в первую очередь выработку важных цитокинов — интерферонов (ИФН) [2–4].
Нами было выдвинуто предположение, что существенная роль в патогенезе инфекций и нарушений фертильности (синдрома потери плода) при вирусных процессах принадлежит дисфункции в системе ИФН, при этом все их 3 типа остаются малоизученными у пациенток в прегравидарном периоде. Поэтому нами принято решение определить ИФН локально, в цервикальной слизи, так как именно их присутствие отражает состояние мукозального иммунного ответа.
Цель исследования: провести сравнительный анализ интерферонового профиля мукозального иммунитета у пациенток с ПВИ в ассоциациях с герпетической и хламидийной инфекциями.
Материал и методы
В исследование было включено 149 пациенток в возрасте 25–44 лет (средний возраст 27±2,7 года). Пациентки были разделены на 4 группы в зависимости от наличия инфекций: I группа — с ПВИ (n=21), II группа — с ПВИ и герпесвирусной инфекцией (ГВИ) (n=47), III группа — с ПВИ и хламидийной инфекцией (n=39) и IV группа — контрольная (30 практически здоровых женщин, сопоставимых по возрасту).
Комплексное клинико-лабораторное исследование проводили в амбулаторных условиях по единой программе, включающей клинико-функциональное, биохимическое и иммунологическое обследование с целью детализации патофизиологических механизмов ПВИ в урогенитальном тракте. Определение в цервикальной слизи уровня ИФН: ИФН-β, ИФН-γ, ИФН-λ1 (ИЛ-29), ИФНλ3 (ИЛ-28B) — проведено методом твердофазного иммуноферментного анализа с использованием специфических реактивов фирмы R&D Diagnostic Inc. (США).
Статистическая обработка данных выполнена с использованием программы IBM SPSS® v.22. Внутри- и межгрупповые различия оценивали с помощью критерия Манна — Уитни с поправкой Бонферрони. При ненормальном распределении и малом числе наблюдений показатели представляли в виде медианы (Ме), нижнего и верхнего квартилей (Q21; Q3). Для проверки взаимосвязи или независимости между величинами определяли коэффициент корреляции Спирмена. Статистически значимыми считали различия при p<0,05.
Результаты исследования
При исследовании уровня ИФН I, II и III типов в цервикальной слизи были выявлены общие закономерности и ряд различий в группах (см. таблицу).
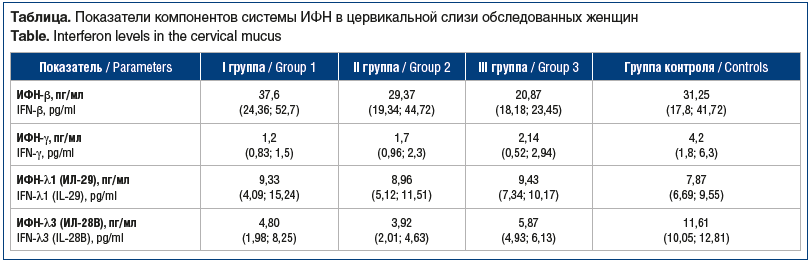
Уровень ИФН-β в I и II группах находился в пределах референсных величин, в то время как в III группе его уровень был статистически значимо снижен как по сравнению с группой контроля (p<0,05), так и по сравнению с I (p=0,022) и II (p=0,037) группами.
Уровень ИФН-γ был снижен в 2–4 раза у пациенток всех 3 групп по сравнению с группой контроля (p<0,05). Однако значения в группах изменялись в разной степени. Так, в I группе было зарегистрировано наиболее выраженное понижение в сравнении с II и III группами (p=0,043 и p=0,032 соответственно).
Уровень ИФН-λ1 не имел статистически значимой разницы между основными группами и в сравнении с группой контроля (p>0,05). В то же время уровень ИФН-λ3 был снижен в 2–3 раза во всех исследуемых группах по сравнению с референсными величинами (p<0,01). Межгрупповые различия также были статистически значимыми. Так, в группе с ассоциациями вирусных инфекций показатель был более низким в сравнении с I (p=0,04) и III (p=0,026) группами.
Анализ полученных результатов показал, что у пациенток всех основных групп выявлен дефицит ИФН-γ и ИФН-λ3. Анализируя особенности в этих группах, можно констатировать, что при ПВИ ведущим нарушением был дефицит ИФН-γ. Во II группе, с ассоциациями вирусных инфекций, задокументирован максимально низкий уровень ИФН-λ3. В группе с ассоциацией вирусной и бактериальной инфекций выявлен дефицит продукции ИФН-β.
Обсуждение
Система ИФН эволюционно представляет собой один из наиболее значимых механизмов контроля и клиренса вирусных возбудителей в организме человека, особенно на локальном уровне. Ввиду этого истощение данной защитной системы становится очевидным при развитии клинически значимого инфекционного процесса. Вызывает интерес тот факт, что вирусная эвазия способна подавлять как продукцию ИФН, так и их взаимодействие между собой и другими цитокинами путем модификации и ингибирования сигнальных путей, а также влияния на возможность процессинга антигенов [5, 6].
ИФН I типа не только обладают выраженным противовирусным действием, но и важны для правильной регуляции всей системы в период инфекционного процесса. Снижение концентрации ИФН-β в группе с хламидийной инфекцией может свидетельствовать о нарушении взаимодействия с мембранными рецепторами, что клинически может проявляться образованием фиброзной ткани [7]. В отличие от лейкоцитарного ИФН-α, ИФН-β образуется в стимулированных фибробластах, что предполагает наибольшее его снижение при ассоциации вирусной и бактериальной инфекций, это приводит к нарушению пролиферации фибробластов и дальнейшему формированию соединительной ткани в просвете маточной трубы, способствуя спаечному процессу и репродуктивным нарушениям в виде бесплодия [8]. Регуляторную функцию ИФН-β способен реализовывать через модуляцию TLR-зависимого иммунного ответа, запуская каскад противовирусных реакций. Это послужило формированию мнения, что изолированный дефицит данного звена интерфероновой системы не играет клинически значимой роли при инфекционном поражении [9]. Основываясь на результатах нашего исследования, можно сделать вывод, что, несмотря на большее изменение уровня ИФН-β в группе с ПВИ и хламидийной инфекцией, уровень ИФН-γ в данной группе изменялся в меньшей степени, что, безусловно, требует дальнейшего изучения с позиции перекрестных взаимодействий ИФН.
ИФН II типа наиболее изучены с позиции иммунорегуляции, а не прямого противовирусного эффекта. Индукция синтеза ИФН-γ крайне зависима от активации ИФН-зависимых сигнальных путей (ИНФ I типа), однако в то же время существует возможность нарушения и ИФН-γ-сигнальной активности, которая может приводить к рецидивирующему течению ГВИ при нормализации уровня ИФН-γ [10]. Подобная картина характерна и для пациенток с ПВИ при наличии определенной формы мутации в гене ИФН-γ: полиморфизм +874T/A характеризуется большей восприимчивостью к ПВИ, чем +874А/A, однако именно у носителей АА-варианта уровень ИФН-γ был ниже [10]. Оценивая полученные нами результаты с позиции современных знаний о роли ИФН-γ, мы можем предположить, что его дефицит является характерным проявлением вирусной эвазии, однако существующих данных недостаточно, чтобы однозначно судить о влиянии степени дефицита на клиническую картину заболевания, это подводит нас к рассмотрению возможности рутинго генотипирования пациенток с вирусными инфекциями для решения вопроса об индивидуализации терапии.
ИФН III типа представляют в настоящее время особый интерес для исследователей вирусных заболеваний. Обладая всеми положительными сторонами ИФН I типа, они лишены ряда их негативных сторон, когда мы оцениваем их как потенциальные мишени или инструменты терапевтического взаимодействия. Учитывая меньшую эффекторную широту экспрессии рецепторов, активация ИФН-λ способна обеспечивать как противовирусную защиту на ранних стадиях инфекции, так и контроль реактивации вирусов [6, 11]. При ПВИ и ГВИ ИФН III типа имели разнонаправленные изменения: определено снижение уровня ИФН-λ3, в то время как уровень ИФН-λ1 оставался без изменений. Существует мнение о том, что инфицирование высокоонкогенными типами ВПЧ ассоциировано со сниженным уровнем ИФН-λ1, а сочетанная вирусная инфекция, вероятно, провоцирует интерферонодефицит, таким образом, снижая противоопухолевую функцию данного ИФН [12, 13]. Уровень ИФН-λ3 демонстрирует картину, которую сложно оценить однозначно. Известно о возможности вирус-зависимой индукции экспрессии генов ИФН III типа, при этом ее уровень и скорость различаются при разной локализации вирусного поражения. Вероятно, подобные результаты ассоциированы с генетическим полиморфизмом, однако это требует дополнительного изучения [7, 14]. Дисбаланс ИФН в цервикальной слизи у женщин свидетельствует о нарушении противовирусной защиты еще на локальном уровне в результате процессов активного потребления и, вероятно, нарушения их продукции [15, 16].
Заключение
В результате проведенного нами исследования выявлено развитие разноуровневого интерферонодефицита у всех пациенток как с моновариантной ПВИ, так и в сочетании с ГВИ или хламидийной инфекцией. Патогенетическое значение имеет не только выявленный дефицит преимущественно ИФН II и III типов, но и их дисрегуляция, которая является как проявлением стратегии иммунной эвазии возбудителей, так и, вероятно, генетической особенностью макроорганизма, повышающей восприимчивость к патогенам. Дальнейшее комплексное изучение уровня ИФН, их рецепторов и генов, а также функционирования ИФН-зависимых сигнальных путей является объективной необходимостью и обязательным шагом для разработки новых терапевтических и профилактических подходов у пациенток с вирусными и бактериальными инфекциями.
Сведения об авторах:
Маркелова Елена Владимировна — д.м.н., профессор, заведующая кафедрой нормальной и патологической физиологии ФГБОУ ВО ТГМУ Минздрава России; 690002, Россия, г. Владивосток, пр-т Острякова, д. 2; ORCID iD 0000-0001-5846-851X.
Тулупова Марина Сергеевна — к.м.н., главный врач ООО «Парацельс»; 690005, Россия, г. Владивосток, ул. Новоивановская, д. 4А; ORCID iD 0000-0003-1017-6299.
Невежкина Татьяна Андреевна — ассистент кафедры акушерства и гинекологии, ассистент кафедры нормальной и патологической физиологии ФГБОУ ВО ТГМУ Минздрава России; 690002, Россия, г. Владивосток, пр-т Острякова, д. 2; ORCID iD 0000-0002-9165-3511.
Матюшкина Людмила Семеновна — к.м.н., доцент, заведующая кафедрой акушерства и гинекологии ФГБОУ ВО ТГМУ Минздрава России; 690002, Россия, г. Владивосток, пр-т Острякова, д. 2; ORCID iD 0000-0002-5404-4215.
Черникова Мария Анатольевна — аспирант кафедры нормальной и патологической физиологии ФГБОУ ВО ТГМУ Минздрава России; 690002, Россия, г. Владивосток, пр-т Острякова, д. 2; заведующая отделением лабораторной диагностики ООО «Асклепий»; 690033, Россия, г. Владивосток, ул. Гамарника, д. 3-Б; ORCID iD 0000-0002-6556-7118.
Кныш Сергей Васильевич — к.м.н., доцент кафедры нормальной и патологической физиологии ФГБОУ ВО ТГМУ Минздрава России; 690002, Россия, г. Владивосток, пр-т Острякова, д. 2; ORCID iD 0000-0003-4571-1749.
Контактная информация: Невежкина Татьяна Андреевна, e-mail: www.tanya.ru9292@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 01.02.2022.
Поступила после рецензирования 25.02.2022.
Принята в печать 24.03.2022.
About the authors:
Elena V. Markelova — Dr. Sc. (Med.), Professor, Head of the Department of Normal and Pathological Physiology, Pacific State Medical University; 2, Ostryakov av., Vladivostok, 690002, Russian Federation; ORCID iD 0000-0001-5846-851X.
Marina S. Tulupova — C. Sc. (Med.), Head Doctor, JSC "Paratsels"; 4A, Novoivanovskaya str., Vladivostok, 690005, Russian Federation; ORCID iD 0000-0003-1017-6299.
Tatyana A. Nevezhkina — assistant of the Department of Obstetrics and Gynecology, assistant of the Department of Normal and Pathological Physiology, Pacific State Medical University; 2, Ostryakov av., Vladivostok, 690002, Russian Federation; ORCID iD 0000-0002-9165-3511.
Lyudmila S. Matyushkina — C. Sc. (Med)., Associate Professor, Head of the Department of Obstetrics and Gynecology, Pacific State Medical University; 2, Ostryakov av., Vladivostok, 690002, Russian Federation; ORCID iD 0000-0002-5404-4215.
Maria A. Chernikova — postgraduate student of the Department of Normal and Pathological Physiology, Pacific State Medical University; 2, Ostryakov av., Vladivostok, 690002, Russian Federation; Head of the Department of Lab Diagnostics, JSC "Asklepiy", 3B, Gamarnik str., Vladivostok, 690033, Russian Federation; ORCID iD 0000-0002-6556-7118.
Sergey V. Knysh — C. Sc. (Med.), associate professor of the Department of Normal and Pathological Physiology, Pacific State Medical University; 2, Ostryakov av., Vladivostok, 690002, Russian Federation; ORCID iD 0000-0003-4571-1749.
Contact information: Tatyana A. Nevezhkina, e-mail: www.tanya.ru9292@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 01.02.2022.
Revised 25.02.2022.
Accepted 24.03.2022.
2. Андосова Л.Д., Конторщикова К.Н., Качалина О.В. Роль факторов местного иммунитета в манифестации ВПЧ-ассоциированных поражений шейки матки. Медицинский альманах. 2011;6:95–97. DOI: 10.12737/22636.
3. Викулов Г.Х., Вознесенский С.Л., Фролкин Д.И. ВПЧ- и герпесвирусные инфекции: эпидемиологические, патогенетические и клинико-иммунологические аспекты, принципы диагностики и терапии. Акушерство, гинекология и репродуктология. 2019;13(4):102–111. DOI: 10.17749/2313-7347.2020.14.1.102-111.
4. Ершов Ф.И., Неровлянский А.Н. Теоретические и прикладные аспекты системы интерферонов: к 60-летию открытия интерферонов. Вопросы вирусологии. 2018;63(1):10–18. DOI: 10.18821/0507-4088-2018-63-1-10-18.
5. Луцкий А.А., Жирков А.А., Лобзин Д.Ю. и др. Интерферон-γ: биологическая функция и значение для диагностики клеточного иммунного ответа. Инфектология. 2015;7(4):10–22.
6. Feng E., Balint E., Vahedi F. et al. Immunoregulatory functions of interferons during genital HSV-2. Infection Front Immunol. 2021;12:724618. DOI: 10.3389/fimmu.2021.724618.
7. Moghimi M., Tavakoli F., Doosti M. et al. Correlation between interleukin-28 gene polymorphism with interleukin-28 cytokine levels and viral genotypes among HCV patients in Yazd, Iran. BMC Res Notes. 2019;12(1): 46–51. DOI: 10.1186/s13104-019-4651-z.
8. Назарова Н.М., Некрасова М.Е., Довлетханова Э.Р., Абакарова П.Р. Вагиниты и цервициты: выбор эффективного метода терапии (обзор литературы). Медицинский совет. 2020;3:17–23. DOI: 10.21518/2079-701X-2020-3-17-23.
9. Slade J.A., Hall J.V., Kintner J., Schoborg R.V. The type I interferon receptor is not required for protection in the Chlamydia muridarum and HSV-2 murine super-infection model. Pathogens and Disease. 2021;76(8):5–7. DOI: 10.1093/femspd/fty075.
10. Zhang Q., Song J., Yu J. et al. Polymorphism of IFN-γ +874T/A associated with production of IFN-γ affects human papillomavirus susceptibility in rural women from Luohe, Henan, China. Onco Targets Therapy. 2018;11:4339–4344.
11. Davidson S., Crotta S., McCabe T. et al. Pathogenic potential of interferon αβ in acute influenza infection. Nat Commun. 2014;5:48–52. DOI: 10.1038/ncomms4864.
12. Fernandes J., De Medeiros Fernandes T., De Azevedo J. et al. Link between chronic inflammation and human papillomavirus-induced carcinogenesis (Review). Oncol Lett. 2015;9(3):1015–1026. DOI: 10.3892/ol.2015.2884.
13. A. Stiff. Investigations of Interferon-Lambda for the Treatment of Cancer. J Innate Immunity. 2015;7(3):243–250. DOI: 10.1159/000370113.
14. Yin Y., Herman W. Herpesviruses and the type III interferon system. Virol Sin. 2021;36(4):577–587. DOI: 10.1007/s12250-020-00330-2.
15. Кихтенко П.Н., Олейник Л.А., Макаров В.К. и др. Интерфероны лямбда — возможности терапевтического применения. Сибирский научный медицинский журнал. 2020;40(2):15–23. DOI: 10.15372/SSMJ20200202.
16. Саляев Р.К., Рекославская Н.И., Столбиков А.С. Индукция синтеза интерферона, CD4 и СD8 Т лимфоцитов в крови и селезенке мышей, перорально вакцинированных «ранним белком» ВПЧ16 Е2. Доклады Академии наук. 2019;488(3):333–337. DOI: 10.31857/S0869-56524883333-337.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
